Uorganisk kemi. HF HCl HBr HI Hydrogenchlorid 10/27/2009. Halogener. H F Cl Br I. Forekomst.87%.07% 1.4% 2.5ppm.3ppm
|
|
|
- Kaare Eskildsen
- 8 år siden
- Visninger:
Transkript
1 Halogener Noter 7 H F Cl Br I Forekomst.87%.07% 1.% 2.5ppm.3ppm Ionisationsenergi /kjmol 1 (cf.) 517(Li) 93(Na) 16(K) 01(Rb) 373(Cs) Elektronaffinitet /kjmol 1 Elektronega tivitet Atomradius/Å E 0 /V (X 2 + 2e > 2X ) Ionradius X r/å Kp/ o CX Smp/ o CX Navn noter 8 HF HCl HBr HI Hydrogenfluorid Hydrogenchlorid Hydrogenbromid Hydrogeniodid Kp/ 0 C HX Dipolmoment/ D Bindingsstyrke HX (kj/mol) Afstand HX /Å Vandig opløsning Flussyre Saltsyre Opløselighed af HX liter HX(1atm)pr liter vand 25 0 C Azeotrop/1 atm g/100 g opløsning Densitet(25 0 C) concentration/m Kp/oC af azeotrop
2 Halo genos salt dannere Reaktion med metaller Stor elektronegativitetsforskel ladningsseperation Salte: Ionisk opbygning, faste stoffer NaCl AgCl CaCl 2 CoCl 2 PbCl 2 CrCl 3 6H 2 O CrCl 3 AlCl 3 CrCl Chlorforbindelser i pblokken BCl 3 (12.5) CCl (76.7) B(OH) 3 AlCl 3 * (s) Al(H 2 O) 3+ 6 NCl 3 (71) ClO 2 (11) HNO 2 HClO 2 +ClO 3 FCl (100) Cl 2 (3) SiCl (57.6) Si(OH) PCl 5 (160) POCl 3 H 3 PO S 2 Cl 2 (1) H 2 S SCl 2 (59) PCl 3 (76) H 2 S x O y H 3 PO 3 GeCl (83) AsCl 3 (130) Se 2 Cl 2 (130 d ) ClBr (5) Ge(OH) H 3 AsO 3 SnCl (11) SnCl x (OH) 6x 2 PbCl 2 (953, s ) PbCl 3 SbCl 3 (223) SbCl SbCl 5 (10 d ) SbCl 6 BiCl 3 (1, s) BiCl 5 2 Te Cl 6 (s ) I 2 Cl 6 (s ) Noter fx Højere oxidationstrin Cl 2 + 2OH ClO + Cl + H 2 O 3I 2 + 6OH IO 3 + 5I + 3H 2 O ClO 3 + SO 2 2ClO 2 + SO 2 2I 2 + 5O 2 2I 2 O
3 HXO n HOF (mægtig ustabil HF +½O 2 ) HClO hypochlorsyrling ClO hypochlorit HClO 2 chlorsyrling ClO 2 chlorit HClO 3 chlorsyre ClO 3 chlorat HClO perchlorsyre ClO perchlorat HBrO HIO HBrO 3 HIO 3 HBrO HIO (meta)periodsyre H 5 IO 6 orthoperiodsyre Oxosyrers styrke pk~85n (n: antal =O) Meget svage (n=0) Svage (n=1) Stærke (n=2) Meget stærke (n=3) ClOH 7.2 NOOH 3.3 NO 2 OH 1. ClO 3 OH (10) BrOH 8.7 ClOOH 2.0 ClO 2 OH 1 MnO 3 OH (meget) IOH 10.0 CO(OH) IO 2 OH 0.8 As(OH) SO(OH) SO 2 (OH) 2 <0 Sb(OH) SeO(OH) SeO 2 (OH) 2 <0 B(OH) TeO(OH) Si(OH) 10.0 PO(OH) Ge(OH) 8.6 AsO(OH) Te(OH) 8.8 IO(OH) HPO(OH) H 2 PO(OH) 2.0 noter side Noter 8 Halogener 1 Følgende negative ioner kan komme på tale: Cl, Br, I, ClO, ClO 2, ClO 3, og tilsvarende BrO n og IO n incl. perbromat og periodat. Hvor der er behov for en fælles betegnelse skriver vi X eller XO n 1.Bringes på reduceret form XO n + nso 2 + nh 2 O X +nso 2 + 2nH + 9 3
4 Halogener 2 Halogener i oxtrin 1 : X 2. X + Ag + AgX(s) (kridhvidt, offwhite, gulligt) (de eneste tungtopl. sølv salte i sur væske) Opløselighed li dfalder i rækken Cl, Br, I 3. AgCl + 2NH 3 Ag(NH 3 ) 2+ +Cl mens AgBr og AgI er for tungtopløselige Ag(NH 3 ) Br AgBr påviser Cl AgBr 10 Halogener 3 AgBr og AgI tilbage: Ag(I) reduceres med Zn. 2AgX + Zn 2Ag + Zn X Br og I har forskellig reducerende evne (eller: lader sig ikke lige nemt oxidere) 5. 2I + 2Fe 3+ I 2 + 2Fe 2+ Iod i opløsning I 2 (aq) I 2 (tol); K er stor Farve brun violet Br oxideres kun med stærkere ox midler 11 Oversættelse (her: prøve for I ) Fe Oversæt den udførte operation (her: tilsæt et par dråber jern(iii)sulfat og et par dråber toluen) vha. viden om partiklernes egenskaber i stoffet og vha. formålet med operationen til formler (her: jern(iii) ioner og deres farve) 2. Huske stoffernes (her toluens) relevante egenskaber (her lavere densitet end vands og upolært opløsningsmiddel) 3. Kende til forskellige udfald af operationen formuleret i kemiske termer (formler og reaktionsligninger). Oversætte forskellige udfald til hvordan de manifesterer sig i reagensglasset så de kan iagttages 5. Iagttage udfaldet korrekt og afgøre hvilket af de mulige det er (violet i øverste fase) 6. Slutte tilbage om hvad det iagttagede udfald betyder for tilstedeværelsen af en bestemt komponent i prøven (her:iodid) 7. Benytte denne og andre operationer til at afgøre hvilke komponenter prøven indeholder 12
5 Halogener 10Br + 2MnO + 16H + 5Br 2 + 2Mn 2+ +8H 2 O Brom i opløsning Br 2 (aq) Br 2 (tol); K er stor Farve brun brun Br påvist 13 Noter 8 Kvantitativt 1 1.Titrering efter Mohr : Chlorid Procedure: Der titreres med AgNO 3 opløsning med kendt koncentration indtil rødfarvning. Indikator: natriumchromat Princip: Ag + + Cl AgCl (shvidt) ; 2Ag + + CrO 2 Ag 2 CrO (srødt) Opløselighed 10 5 mol/liter ~3x10 mol/liter Støkiometri: V(AgNO 3 ) C(Ag + ) = n(ag + ) = n(cl ) = m(xcl)/m(xcl) Noter 8 Kvantitativt 2 2. Titrering efter Volhardt: Bromid eller iodid. Procedure: Der tilsættes overskud af AgNO 3 opløsning med kendt koncentration. Overskuddet af Ag + titreres med KSCNopløsning med kendt koncentration indtil rødfarvning. Indikator: jern(iii)sulfat Princip: Ag + + X AgX (shvidt/gult); SCN + Ag + AgSCN (s) xscn + Fe 3+ Fe(SCN) x (3x)+ (intens rød) Støkiometri V(AgNO 3 ) C(Ag + ) V(KSCN) C(SCN ) = n(x )
6 Noter 8 Kvantitativt 3 3. Potentiometrisk titrering : Chlorid, bromid og /eller iodid Procedure: Der titreres med AgNO 3 opløsning med kendt koncentration, idet potentialeforskellen mellem en sølvelektrode og en standardelektrode registreres løbende. Ækvivalenspunkter (aflæs volumen) ved potentialespring. Princip: AgI, AgBr og AgCl fældes rækkefølge i tre fraktioner fordi opløseligheden er forskellig Støkiometri: V(AgNO 3 ) C(Ag + ) = n(x ) Eksempel Br fundet. Til 5.00 ml opløsning sættes 25 ml M sølvnitrat. Der tilsættes lidt jern(iii) sulfat og der titreres med 9.5 ml M kaliumthiocyanat. Hvad er [Br ]? 0.311M
Test din viden B-forløb
 Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Opgaver til: 6. Syrer og baser
 Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Test din viden E-forløb
 OPGAVE E8 Test din viden E-forløb Har du styr på E-forløbets kernestof? Nu har du lært en masse om spændingsrækken og redoxreaktioner. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle områder,
OPGAVE E8 Test din viden E-forløb Har du styr på E-forløbets kernestof? Nu har du lært en masse om spændingsrækken og redoxreaktioner. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle områder,
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Der tilsættes 50,0 ml 1,00 M saltsyre. Hvor stor en masse af jern opløses, hvis reaktionen forløber fuldstændigt, og der er overskud af Fe(s)?
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
Syrer, baser og salte
 Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Eksamensspørgsmål 2c ke, juni Fag: Kemi C-niveau. Censor: Andreas Andersen, Skanderborg Gymnasium
 Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Aurum KEMI FOR GYMNASIET 2 KIM RONGSTED KRISTIANSEN GUNNAR CEDERBERG
 Aurum KEMI FOR GYMNASIET 2 KIM RONGSTED KRISTIANSEN GUNNAR CEDERBERG Opgave 4.8 Brug tabellen over styrkeeksponenter til at finde pk S og pk B for følgende amfolytter, og afgør i hvert tilfælde, om amfolytten
Aurum KEMI FOR GYMNASIET 2 KIM RONGSTED KRISTIANSEN GUNNAR CEDERBERG Opgave 4.8 Brug tabellen over styrkeeksponenter til at finde pk S og pk B for følgende amfolytter, og afgør i hvert tilfælde, om amfolytten
Spørgsmål 1 Carbonhydrider
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Højere Teknisk Eksamen maj Kemi A. - løse opgaverne korrekt. - tegne og aflæse grafer. Ved bedømmelsen vægtes alle opgaver ens.
 054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
Formål Ud fra en række udvalgte salte, skal man finde ud af om de er let- eller tungtopløselige i vand. Ved at blande saltene sammen med hinanden en f
 Saltes opløselighed i vand. Af: Ulrich Olsen 1e Tirsdag 11/9-2001 Formål Ud fra en række udvalgte salte, skal man finde ud af om de er let- eller tungtopløselige i vand. Ved at blande saltene sammen med
Saltes opløselighed i vand. Af: Ulrich Olsen 1e Tirsdag 11/9-2001 Formål Ud fra en række udvalgte salte, skal man finde ud af om de er let- eller tungtopløselige i vand. Ved at blande saltene sammen med
Test din viden D-forløb
 Test din viden D-forløb Har du styr på D-forløbets kernestof? Nu har du lært en masse om syrer og baser, ph-beregning og syre-basetitrering. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle
Test din viden D-forløb Har du styr på D-forløbets kernestof? Nu har du lært en masse om syrer og baser, ph-beregning og syre-basetitrering. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
OPGAVER OM DANNELSE AF IONER. OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal.
 OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
TI-B 9 (85) Prøvningsmetode Hærdnet betons chloridindhold
 Hærdnet betons chloridindhold Teknologisk Institut, Byggeri Hærdnet betons chloridindhold Deskriptorer: - Udgave: 1 Dato: 1985-05-7 Sideantal: / Bilag: 1 Udarbejdet af: BF/JKU Hærdnet betons chloridindhold
Hærdnet betons chloridindhold Teknologisk Institut, Byggeri Hærdnet betons chloridindhold Deskriptorer: - Udgave: 1 Dato: 1985-05-7 Sideantal: / Bilag: 1 Udarbejdet af: BF/JKU Hærdnet betons chloridindhold
O-affald O-AFFALD. Dangerous goods specialists and training
 O-AFFALD ADR-FAREKLASSER Klasse 1 Eksplosive stoffer og genstande Klasse 2 Gasser Klasse 3 Brandfarlige væsker Klasse 4.1 Brandfarlige faste stoffer, selvnedbrydende stoffer og faste desensibiliserede
O-AFFALD ADR-FAREKLASSER Klasse 1 Eksplosive stoffer og genstande Klasse 2 Gasser Klasse 3 Brandfarlige væsker Klasse 4.1 Brandfarlige faste stoffer, selvnedbrydende stoffer og faste desensibiliserede
Syre-base titreringer
 Syre-base titreringer Titrering: Er en analytisk metode til bestemmelse af mængden af et stof (A) i et kendt volumen af en opløsning. Metode: Et kendt volumen af opløsningen der indeholder A udtages. En
Syre-base titreringer Titrering: Er en analytisk metode til bestemmelse af mængden af et stof (A) i et kendt volumen af en opløsning. Metode: Et kendt volumen af opløsningen der indeholder A udtages. En
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014
 Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT
 1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
Eksamensspørgsmål 2z ke (ikke godkendte) Fag: Kemi C Dato: 7. juni 2013 Lærer: Peter R Nielsen (PN) Censor: Tanja Krüger, VUC Aarhus
 1. Kemisk Binding Gør rede for øvelsen Kovalent- eller Ionbinding? Beskriv ionbinding og kovalent binding og forklar hvordan forskellene på de to typer af kemisk binding udnyttes i for66søget. Stikord
1. Kemisk Binding Gør rede for øvelsen Kovalent- eller Ionbinding? Beskriv ionbinding og kovalent binding og forklar hvordan forskellene på de to typer af kemisk binding udnyttes i for66søget. Stikord
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Kemirapport 5. Henning hvp@inano.dk 20031325. 13. december 2004
 Kemirapport 5 Henning hvp@inano.dk 20031325 13. december 2004 Vi får fem ukendte stoffer udleveret, og vi skal identificere hvert af dem ved hjælp af metoderne fra øvelserne 1-4. Vi har en liste med mulige
Kemirapport 5 Henning hvp@inano.dk 20031325 13. december 2004 Vi får fem ukendte stoffer udleveret, og vi skal identificere hvert af dem ved hjælp af metoderne fra øvelserne 1-4. Vi har en liste med mulige
Kemiaflevering uge 37
 Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
%2fAfleveringsportal%2fopgaveaflevering.aspx%3felementId%3d461315
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 UORGANISK KEMI Tirsdag den 18. december 2012
 Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
KORT SUMMARISK GENNEMGANG AF KEMIEN 2013.
 COPYRIGHT NIELS NORDHOLT 2000-2013 S. 1 KORT SUMMARISK GENNEMGANG AF KEMIEN 2013. Sætning, reaktion eller kort forsøgsbeskrivelse Ved en fysisk forandring omdannes stoffer ikke til andre stoffer. Ved en
COPYRIGHT NIELS NORDHOLT 2000-2013 S. 1 KORT SUMMARISK GENNEMGANG AF KEMIEN 2013. Sætning, reaktion eller kort forsøgsbeskrivelse Ved en fysisk forandring omdannes stoffer ikke til andre stoffer. Ved en
Hæld 25 ml NaOH(aq) op i et bægerglas. Observer væsken. Er den gennemsigtig? Hvilke ioner er der i ionsuppen?
 Fældningsreaktion (som erstatning for titrering af saltvand) Opløs 5 g CuSO 4 i 50 ml vand Opløses saltet? Følger det teorien? Hvilke ioner er der i ionsuppen? Hæld 25 ml NaOH(aq) op i et bægerglas. Observer
Fældningsreaktion (som erstatning for titrering af saltvand) Opløs 5 g CuSO 4 i 50 ml vand Opløses saltet? Følger det teorien? Hvilke ioner er der i ionsuppen? Hæld 25 ml NaOH(aq) op i et bægerglas. Observer
Kemiøvelser (til eleverne)
 Fra ressourceforbandelse til grøn omstilling Kemiøvelser (til eleverne) Udviklet af Kjeld Lundgaard, kemilærer på Ingrid Jespersens Gymasieskole 1. Eksperiment: Opløselighed af lithiumchlorid Formål: Bestemme
Fra ressourceforbandelse til grøn omstilling Kemiøvelser (til eleverne) Udviklet af Kjeld Lundgaard, kemilærer på Ingrid Jespersens Gymasieskole 1. Eksperiment: Opløselighed af lithiumchlorid Formål: Bestemme
Gruppe 2 Læsestof : Kap. 11.
 ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
Udvalgte grundstoffers kemi i vandig opløsning
 Udvalgte grundstoffers kemi i vandig opløsning Fældning Opløsning Syre-baseligevægte Kompleksdannelse Oxidation Reduktion Peter Andersen og Ole Mønsted Kemisk Institut Københavns Universitet 2004 Denne
Udvalgte grundstoffers kemi i vandig opløsning Fældning Opløsning Syre-baseligevægte Kompleksdannelse Oxidation Reduktion Peter Andersen og Ole Mønsted Kemisk Institut Københavns Universitet 2004 Denne
Torben Rosenørn. Aalborg Universitet. Campus Esbjerg
 Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
[H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2
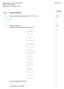
![[H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2 [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2](/thumbs/48/24964855.jpg) ph = -log [H 3 O + ] poh = -log [OH ] pk s = -log K s pk b = -log K b [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b m ph + poh = 1 [H 3 O + ][OH ] = 10 1 m 2 pk s + pk b = 1 K s K
ph = -log [H 3 O + ] poh = -log [OH ] pk s = -log K s pk b = -log K b [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b m ph + poh = 1 [H 3 O + ][OH ] = 10 1 m 2 pk s + pk b = 1 K s K
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA
 1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA Formålet med denne øvelse er at bestemme indholdet af krystalvand i krystalsoda, som har den kemiske formel Na 2 CO 3 xh 2 O. Teori: En del ionforbindelser (salte)
1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA Formålet med denne øvelse er at bestemme indholdet af krystalvand i krystalsoda, som har den kemiske formel Na 2 CO 3 xh 2 O. Teori: En del ionforbindelser (salte)
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017
 EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
Oversigt med forklaring over forskellige begreber
 Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
%2fAfleveringsportal%2fopgaveaflevering.aspx%3felementId%3d476671
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi F15 / Opgaver Eksamen F15 Side 1 Navngivning Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Vægtning 1 % Opskriv den kemiske formel for kobber(i)oxid
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi F15 / Opgaver Eksamen F15 Side 1 Navngivning Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Vægtning 1 % Opskriv den kemiske formel for kobber(i)oxid
KVANTITATIV ANALYSE Peter Andersen og Ole Mønsted Kemisk Institut Københavns Universitet 2004
 KVANTITATIV ANALYSE Peter Andersen og Ole Mønsted Kemisk Institut Københavns Universitet 2004 Denne udgivelse er en introduktion til elementær kvantitativ analyse som beskrevet i bogen "Grundlæggende
KVANTITATIV ANALYSE Peter Andersen og Ole Mønsted Kemisk Institut Københavns Universitet 2004 Denne udgivelse er en introduktion til elementær kvantitativ analyse som beskrevet i bogen "Grundlæggende
Danmarks Tekniske Universitet
 Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 UORGANISK KEMI Torsdag den 22. maj 2014
 Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest.
 Jordbundsanalyse ph Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest 31 21 - Vejledning til Rapitest Læs vejledningen fra Rapitesten: Nu er det let at forbedre sin have med den nye Rapitest
Jordbundsanalyse ph Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest 31 21 - Vejledning til Rapitest Læs vejledningen fra Rapitesten: Nu er det let at forbedre sin have med den nye Rapitest
Skriftlig eksamen i Almen Kemi I
 Skriftlig eksamen i Almen Kemi I Molekylær Biomedicin November 2005 Hjælpemidler tilladt: Lærebøger, undervisningsmateriale, opgavebesvarelser, noter, molekylbyggesæt, lommeregner og sædvanlige skrive-
Skriftlig eksamen i Almen Kemi I Molekylær Biomedicin November 2005 Hjælpemidler tilladt: Lærebøger, undervisningsmateriale, opgavebesvarelser, noter, molekylbyggesæt, lommeregner og sædvanlige skrive-
Øvelse 4.2 1/5 KemiForlaget
 KST G ERNÆRING Benthe Schou ØVELSE 4. Øvelse: Iodtal for fedtstoffer Indledning Et fedtstofs ernæringsmæssige sundhed bestemmes af hvilke fedtsyrer, der indgår i fedtstoffet. Fedtstoffets sundhed er stærkt
KST G ERNÆRING Benthe Schou ØVELSE 4. Øvelse: Iodtal for fedtstoffer Indledning Et fedtstofs ernæringsmæssige sundhed bestemmes af hvilke fedtsyrer, der indgår i fedtstoffet. Fedtstoffets sundhed er stærkt
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
Mundtlige eksamensopgaver
 Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Skriftlig prøve i kursus 26173/E15 Side 1 af 13 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 13 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. C: [He]2s 2 2p 2 P: [Ne]3s 2 3p 3 Zn 2+ : [Ar]3d 10 I : [Xe] 1.2 Molekylorbitalteori.
Skriftlig prøve i kursus 26173/E15 Side 1 af 13 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. C: [He]2s 2 2p 2 P: [Ne]3s 2 3p 3 Zn 2+ : [Ar]3d 10 I : [Xe] 1.2 Molekylorbitalteori.
1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.
 Indhold 1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.... 2 2. Fældningsreaktioner herunder eksperimentet Saltes opløselighed i vand.... 3 3. Stofmængdekoncentration
Indhold 1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.... 2 2. Fældningsreaktioner herunder eksperimentet Saltes opløselighed i vand.... 3 3. Stofmængdekoncentration
Preview from Notesale.co.uk Page 11 of 51
 Centrifugalpumpe: Den kan flytte større mængder vand. Den kan ikke selv suge vandet til sig. (ikke selvansugende). Den skal spædes med vand for, at kunne køre. Hvis man får en større løftehøjde kan man
Centrifugalpumpe: Den kan flytte større mængder vand. Den kan ikke selv suge vandet til sig. (ikke selvansugende). Den skal spædes med vand for, at kunne køre. Hvis man får en større løftehøjde kan man
Jernindhold i fødevarer bestemt ved spektrofotometri
 Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Øvelse: Ligevægt. Aflever de udfyldte journalark på Fronter individuelt
 KEMI kl.2.1 Øvelse Oprettet 2007-05-20 hjsn@rts.dk videreforarbejdet af 2008-09 bos@rts.dk Øvelse: Ligevægt Læremål at kunne anvende Le Chateliers princip til bestemmelse af forskydningen af en ligevægt
KEMI kl.2.1 Øvelse Oprettet 2007-05-20 hjsn@rts.dk videreforarbejdet af 2008-09 bos@rts.dk Øvelse: Ligevægt Læremål at kunne anvende Le Chateliers princip til bestemmelse af forskydningen af en ligevægt
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD).
 Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
VUC Århus Laboratoriekursus for selvstuderende i kemi højniveau
 Øvelse 1: Bestemmelse af reaktionshastighed Apparatur: 100 ml bægerglas, pipetter 10 ml og 20 ml, sugebold, reagensglas, spatel, stopur. Kemikalier: 0.200 M Na 2 S 2 O 8 ; 0.100 M Na 2 S 2 O 8 (opløsningen
Øvelse 1: Bestemmelse af reaktionshastighed Apparatur: 100 ml bægerglas, pipetter 10 ml og 20 ml, sugebold, reagensglas, spatel, stopur. Kemikalier: 0.200 M Na 2 S 2 O 8 ; 0.100 M Na 2 S 2 O 8 (opløsningen
Syrer, baser og salte
 Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Facitliste. Grundstoffer og molekyler
 Facitliste. Grundstoffer og molekyler 2 En kemisk reaktion 2.1 d) Hydrogen + oxygen vand eller d) Brint + ilt vand 2.2 Jern + svovl jern(ii)sulfid 2.3-2.4 a) carbon + oxygen carbondioxid b) carbon + oxygen
Facitliste. Grundstoffer og molekyler 2 En kemisk reaktion 2.1 d) Hydrogen + oxygen vand eller d) Brint + ilt vand 2.2 Jern + svovl jern(ii)sulfid 2.3-2.4 a) carbon + oxygen carbondioxid b) carbon + oxygen
Eksaminationsgrundlag for selvstuderende
 Eksaminationsgrundlag for selvstuderende Skolens eksaminationsgrundlag: Jeg ønsker at gå til eksamen i nedennævnte eksaminationsgrundlag (pensum), som skolen har lavet. Du skal ikke foretage dig yderligere
Eksaminationsgrundlag for selvstuderende Skolens eksaminationsgrundlag: Jeg ønsker at gå til eksamen i nedennævnte eksaminationsgrundlag (pensum), som skolen har lavet. Du skal ikke foretage dig yderligere
Eksamensspørgsmål. Spørgsmål : Atomer og bindinger (Hvilken type stof?) Spørgsmål : Ionforbindelser (Saltes opløselighed i vand
 Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
BASISKEMI C. Facit HELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN HAASE & SØNS FORLAG
 BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
Kemi B 2a3ax 2012. Der er 14 elever, som skal til eksamen: Nogle fra 2a, nogle fra 3a og nogle fra 3x
 Kemi B 2a3ax 2012 Der er 14 elever, som skal til eksamen: Nogle fra 2a, nogle fra 3a og nogle fra 3x De har læst kemi C efter forskellige lærebogssystemer På Kemi B har vi brugt H Mygind Basiskemi B, 1.
Kemi B 2a3ax 2012 Der er 14 elever, som skal til eksamen: Nogle fra 2a, nogle fra 3a og nogle fra 3x De har læst kemi C efter forskellige lærebogssystemer På Kemi B har vi brugt H Mygind Basiskemi B, 1.
Uorganisk kemi - Kemisk ligevægt
 Vejledning til laboratorieøvelser Uorganisk kemi - Kemisk ligevægt Navn: Revision 2011 Kemisk Institut Århus Universitet Rita Hazell & J.-E. Jørgensen 2 Uorganisk kemi - kemisk ligevægt Formålet med dette
Vejledning til laboratorieøvelser Uorganisk kemi - Kemisk ligevægt Navn: Revision 2011 Kemisk Institut Århus Universitet Rita Hazell & J.-E. Jørgensen 2 Uorganisk kemi - kemisk ligevægt Formålet med dette
Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen. Notatark
 BASISKEMI C Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen Notatark HAAse & Søns forlag Helge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Notatark forfatterne og Haase & Søns Forlag
BASISKEMI C Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen Notatark HAAse & Søns forlag Helge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Notatark forfatterne og Haase & Søns Forlag
Opgaver til: 5. Mængdeberegninger
 Opgaver til: 5. Mængdeberegninger 1. Beregn molarmassen for følgende forbindelser: a) SO 3 b) N 2 O 3 c) Na 2 CO 3 d) Fe 3 (PO 4 ) 2 e) Cl 2 O 7 f) (N 4 ) 2 CO 3 g) C 3 C 2 O 2. Beregn stofmængden, n,
Opgaver til: 5. Mængdeberegninger 1. Beregn molarmassen for følgende forbindelser: a) SO 3 b) N 2 O 3 c) Na 2 CO 3 d) Fe 3 (PO 4 ) 2 e) Cl 2 O 7 f) (N 4 ) 2 CO 3 g) C 3 C 2 O 2. Beregn stofmængden, n,
Kemi A. Studentereksamen
 Kemi A Studentereksamen 2stx111-KEM/A-30052011 Mandag den 30. maj 2011 kl. 9.00-14.00 pgavesættet består af 4 opgaver med i alt 18 spørgsmål samt 2 bilag i 2 eksemplarer. Svarene på de stillede spørgsmål
Kemi A Studentereksamen 2stx111-KEM/A-30052011 Mandag den 30. maj 2011 kl. 9.00-14.00 pgavesættet består af 4 opgaver med i alt 18 spørgsmål samt 2 bilag i 2 eksemplarer. Svarene på de stillede spørgsmål
-1- Niels Thorup OPGAVER I KEMI
 -1- Niels Thorup OPGAVER I KEMI Netversion 2005 -2- Forord. Denne samling af opgaver i almen og fysisk kemi er udarbejdet til undervisning af ikke-kemistuderende på Danmarks Tekniske Universitet (DTU).
-1- Niels Thorup OPGAVER I KEMI Netversion 2005 -2- Forord. Denne samling af opgaver i almen og fysisk kemi er udarbejdet til undervisning af ikke-kemistuderende på Danmarks Tekniske Universitet (DTU).
Lokalenhed Midtjylland (MJL). Bilagsoversigt.
 Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Storstrøm (STO). Bilagsoversigt.
 Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Eksamensopgaverne offentliggøres selvfølgelig med det forbehold, at censor kan komme med ændringsforslag.
 VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi enkeltfag
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi enkeltfag
Lokalenhed Fyn (FYN). Bilagsoversigt.
 Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Sjælland (SJL). Bilagsoversigt.
 Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
reduktion oxidation Reduktion optagelse af elektroner Oxidation afgivelse af elektroner
 8. Redoxreaktioner reduktion oxidation Reduktion optagelse af elektroner Oxidation afgivelse af elektroner (Hel eller delvis) Der er grundlæggende 4 væsentlige kemiske reaktioner: 1. Udfældning af tungtopløselige
8. Redoxreaktioner reduktion oxidation Reduktion optagelse af elektroner Oxidation afgivelse af elektroner (Hel eller delvis) Der er grundlæggende 4 væsentlige kemiske reaktioner: 1. Udfældning af tungtopløselige
Eksamensspørgsmål til 2b kemi C 2017
 Eksamensspørgsmål til 2b kemi C 2017 Eksamensdato: fredag d. 2/6 2017 8 eksaminander skal eksamineres, og der er derfor 11 eksamensopgaver, sådan at den sidste har 4 muligheder. Opgaverne skal tilsammen
Eksamensspørgsmål til 2b kemi C 2017 Eksamensdato: fredag d. 2/6 2017 8 eksaminander skal eksamineres, og der er derfor 11 eksamensopgaver, sådan at den sidste har 4 muligheder. Opgaverne skal tilsammen
Rapport over Fældningsreaktioner
 Rapport over Fældningsreaktioner Formål: at undersøge, hvilke salte der dannes ud fra forskellige fældningsreaktioner, og efterfølgende at undersøge hvilke af disse salte, der er tungtopløselige og hvilke,
Rapport over Fældningsreaktioner Formål: at undersøge, hvilke salte der dannes ud fra forskellige fældningsreaktioner, og efterfølgende at undersøge hvilke af disse salte, der er tungtopløselige og hvilke,
Et fedtstofs iodtal. Problemstilling. Kapitel 2: Uorganisk kemi (iodometri) R 1 CH 2 O C R 2 O R 3. H + Br Br C C Br Br
 Et fedtstofs iodtal Kapitel 2: Uorganisk kemi (iodometri) Problemstilling Additionsreaktionen til dobbeltbindinger mellem -atomer, 8?7, kan vises ved addition af dibrom til et fedtstof. Reaktionen benyttes
Et fedtstofs iodtal Kapitel 2: Uorganisk kemi (iodometri) Problemstilling Additionsreaktionen til dobbeltbindinger mellem -atomer, 8?7, kan vises ved addition af dibrom til et fedtstof. Reaktionen benyttes
Kemi A. Højere teknisk eksamen
 Kemi A Højere teknisk eksamen htx111-kem/a-2-19052011 Torsdag den 19. maj 2011 kl. 9.40-14.40 Side 1 af 6 sider Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt
Kemi A Højere teknisk eksamen htx111-kem/a-2-19052011 Torsdag den 19. maj 2011 kl. 9.40-14.40 Side 1 af 6 sider Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt
Øvelsesvejledninger til laboratoriekursus for selvstuderende i kemi C. Københavns VUC
 Øvelsesvejledninger til laboratoriekursus for selvstuderende i kemi C Københavns VUC Marts 2015 Kemi C laboratoriekursus oktober/november 2014 Københavns VUC Sankt Petri Passage 1, 1165 København K April
Øvelsesvejledninger til laboratoriekursus for selvstuderende i kemi C Københavns VUC Marts 2015 Kemi C laboratoriekursus oktober/november 2014 Københavns VUC Sankt Petri Passage 1, 1165 København K April
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
ph-beregning September 2003 Revideret november 2010 Niels Frederiksen November 2010, Niels Frederiksen
 ph-beregning September 2003 Revideret november 2010 Niels Frederiksen ph-beregning side 1 af 6 I lærebogen er der angivet formler til beregning af ph i opløsninger af en stærk syre, en middelstærk syre
ph-beregning September 2003 Revideret november 2010 Niels Frederiksen ph-beregning side 1 af 6 I lærebogen er der angivet formler til beregning af ph i opløsninger af en stærk syre, en middelstærk syre
Reaktionsmekanisme: 3Br 2 + 3H 2 O. 5Br - + BrO 3 - + 6H + Usandsynligt at alle 12 reaktantpartikler støder sammen samtidig. ca.
 Reaktionsmekanisme: 5Br - + BrO 3 - + 6H + 3Br 2 + 3H 2 O Usandsynligt at alle 12 reaktantpartikler støder sammen samtidig ca. 10 23 partikler Reaktionen foregår i flere trin Eksperimentel erfaring: Max.
Reaktionsmekanisme: 5Br - + BrO 3 - + 6H + 3Br 2 + 3H 2 O Usandsynligt at alle 12 reaktantpartikler støder sammen samtidig ca. 10 23 partikler Reaktionen foregår i flere trin Eksperimentel erfaring: Max.
Exoterme og endoterme reaktioner (termometri)
 AKTIVITET 10 (FAG: KEMI) NB! Det er i denne øvelse ikke nødvendigt at udføre alle forsøgene. Vælg selv hvilke du/i vil udføre er du i tvivl så spørg. Hvis du er interesseret i at måle varmen i et af de
AKTIVITET 10 (FAG: KEMI) NB! Det er i denne øvelse ikke nødvendigt at udføre alle forsøgene. Vælg selv hvilke du/i vil udføre er du i tvivl så spørg. Hvis du er interesseret i at måle varmen i et af de
Anvendt kemi 2 - ekstraopgaver
 1 Anvendt kemi - ekstraopgaver Enthalpiberegninger Stoffet ethan (H6) kan afbrændes. a) Opskriv og afstem reaktionsskemaet for forbrændingen. b) Beregn H for reaktionen. Opgave Betragt følgende redoxreaktionsskema:
1 Anvendt kemi - ekstraopgaver Enthalpiberegninger Stoffet ethan (H6) kan afbrændes. a) Opskriv og afstem reaktionsskemaet for forbrændingen. b) Beregn H for reaktionen. Opgave Betragt følgende redoxreaktionsskema:
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
