Indhold. Forord. 11 Forfattere og reviewere Kemi Proteiner Kulhydrater Cellen. 39. Cytoplasma Resume...
|
|
|
- Lotte Iversen
- 8 år siden
- Visninger:
Transkript
1 Oversigt Forord. Forfattere og reviewere. 3 Kemi. 5 Cellen Proteiner Kulhydrater. 6 5 Lipider Membranstruktur og membrantransport Osmose og væskeelektrolytbalancen. 07 Enzymer. 9 Fordøjelse og absorption af føde Vitaminer. 5 Stofskiftet I: Generelt. 65 Stofskiftet II: Forskellige tilstande. 7 3 Leveren æmostase DNA og gener. Appendiks. 37 Stikordsregister. 40
2
3 Indhold Forord. Forfattere og reviewere. 3 Kemi. 5 Atomet Kemiske bindinger Kovalente bindinger Ionbindinger Polære og upolære molekyler.... Nonkovalente bindinger Funktionelle grupper i molekyler.. 6 Brug af det periodiske system Masse og mol Molekylvægt Mol og molvægt Koncentration og molær koncentration Syrer, baser, p og buffere Syrer Baser p Buffere Resume Cellen. 39 Cellens opbygning Cellemembranen Cytoplasma Resume Proteiner. 47 Proteiner er opbygget af aminosyrer. 47 Aminosyrernes struktur Proteiners struktur Peptider og proteiner vert protein har en bestemt struktur Foldning af proteiner Proteiners funktion Binding af regulatoriske molekyler kan ændre et proteins struktur Denaturering kan ændre et proteins struktur Ændringer af aminosyrer efter proteinets dannelse Proteiner i kosten Essentielle aminosyrer Resume Kulhydrater. 6 Kulhydrater er opbygget af monosakkarider Monosakkarider Monosakkaridernes struktur
4 Eksempler på vigtige monosakkarider Glukose Galaktose Fruktose Disakkarider Sukrose Laktose Maltose Polysakkarider Stivelse og glykogen er oplagringsformer for glukose Cellulose Resume Lipider. 75 Fedtsyrer Essentielle fedtsyrer Triglycerid (triacylglycerol) Fosfolipider Steroider Kolesterol Steroidhormoner Galdesyrer Transport af lipider i blodet med lipoproteinpartikler... 5 Resume Membranstruktur og membrantransport. 93 Membranstruktur Lipider i membraner Proteiner i membraner Kulhydratkæder på oversiden af cellemembranen Membrantransport Typer af transport Passiv transport Aktiv transport Endocytose og eksocytose Endocytose Eksocytose Resume Osmose og væskeelektrolytbalancen. 07 Fordeling af vand og ioner i kroppen Osmose Osmotisk tryk ypotone, isotone og hypertone væsker samt cellernes respons derpå Kroppens væskebalance Væskeindgift Væsketab Kroppens elektrolytbalance (ionbalance) Elektrolytubalance Resume Enzymer. Enzymernes virkemåde Enzymernes opbygning Reaktionshastighed og regulering af enzymaktivitet Substratmængde Enzymmængde Temperatur pværdi Enzymhæmmere (inhibitorer). 9 Andre metoder til regulering af enzymaktivitet Resume Fordøjelse og absorption af føde. 35 Oversigt over fødens vej gennem mavetarmkanalen
5 Mundhule og svælg (cavitas oris og pharynx) Mavesækken (ventriklen) Tolvfingertarmen (duodenum). 3 Øvre og nedre tyndtarm (jejunum og ileum) Tyktarmen (colon) Fordøjelse og absorption af fødens makromolekyler Fordøjelse og absorption af kulhydrater Fordøjelse og absorption af fedt. 44 Fordøjelse og absorption af protein Fra tarmcellerne til blodet Resume Vitaminer. 5 Fedtopløselige og vandopløselige vitaminer Fedtopløselige vitaminer Vandopløselige vitaminer Vitaminer i kosten Personer i risikogruppen for vitaminmangel Fokus på særlige vitaminer Dvitamin Kvitamin Thiamin/B vitamin Folsyre/folat Cobalamin/B vitamin Resume Stofskiftet I: Generelt. 65 Basalstofskiftet og arbejdsstofskiftet Basalstofskiftet Arbejdsstofskiftet Energiudbytte fra energimolekylerne Nedbrydning af næringsstoffer til energi de kemiske processer overordnet set ATP er cellens penge Fra energimolekyle til ATP Omsætning af kroppens energimolekyler Energidannelse i fravær af ilt.. 75 Resume Stofskiftet II: Forskellige tilstande. 7 Tilstanden efter et måltid postprandialt Tilstanden ved kortvarig faste postabsorptivt Stofskiftet ved langvarig faste (over tre dage) Stofskiftet ved sygdom (stressmetabolismen) Resume Leveren. 90 Leverens rolle i stofskiftet Efter et måltid Mellem måltider Leverens rolle i nedbrydning og afgiftning Afgiftningsreaktionerne Forskelle i afgiftningsenzymernes aktivitet Afgiftningsreaktionerne kan give molekyler nye funktioner.. 95 Omsætning af ethanol (alkohol).95 Nedbrydning af hæmoglobin Leverens rolle i syntesereaktioner. 99 Plasmaproteiner Resume
6 4 æmostase. 06 Sammentrækning af blodkar Dannelse af en prop af blodplader primær hæmostase Koagulation sekundær hæmostase Koagulationsfaktorer Aktivering af koagulation..... Dannelse af fibrinnetværket... 3 Inhibering af koagulation Fibrinolyse Forstyrrelser i hæmostasen Øget blødningstendens Trombedannelse (trombose)... 5 Kliniske målinger af koagulationsevnen INR (International Normalised Ratio) APTT (aktiveret partiel tromboplastintid) Resume DNA og gener. DNA DNAmolekylets struktur..... Baseparringen er komplementær Kromosomer Gener Proteinsyntese Genetiske sygdomme Mutationer Celledeling Replikation Deling af celler Resume Appendiks. 37 Stikordsregister. 40
7 Forord Basal biokemi med klinisk perspektiv er en grundbog i biokemi. Bogen har fokus på dagligdagen i klinikken, både med hensyn til beskrivelsen af emnerne og brug af sproget. Det er intentionen, at bogen vil gøre biokemien relevant, interessant, håndgribelig og nærværende for læseren. Bogens emner og opbygning Bogen er opbygget, så læseren først får gennemgået de grundlæggende kemiske og biokemiske processer: lidt om kemi og cellens opbygning. Derefter, hvordan kroppens tre store molekylgrupper, protein, kulhydrat og fedt, er opbygget, og hvad deres vigtigste roller i kroppen er. Denne gennemgang danner fundamentet for forståelsen af kroppens mere komplicerede processer: fordøjelsen, metabolismen og leverens funktion. erudover gennemgås kliniske relevante og mere tunge emner som væske og elektrolytbalancen, vitaminernes rolle i kroppen og hæmostasen. Fokus er igennem hele bogen det kliniske perspektiv sundhed og sygdom. Derfor vil der i bogen være: Beskrivelser af den biokemiske baggrund for en række analyser, der udføres i dagligdagen i klinikken. erunder beskrivelse af blodprøvesvar og grundlaget for ernæringsscreeninger og væsketerapi. Beskrivelser af den biokemiske baggrund for en række sygdomsbilleder og sygdomme, der ofte mødes i dagligdagen i klinikken. eriblandt diabetes mellitus (sukkersyge), aterosklerose (åreforkalkning) og cancer (kræft). Inddragelse af relevante forebyggende tiltag, herunder de officielle kostråd og behandling med vitamintilskud. Gennemgang af forskellige behandlingsmetoder, medicintyper og anden relevant farmakologi. På denne måde gøres biokemien håndgribelig, samtidig med at kliniske emner gennemgås grundigt og pædagogisk. Bogen er opbygget med en grundtekst, der systematisk gennemgår den biokemiske baggrund for kroppens funktioner. ertil kommer en række bokse. Der er kliniske bokse ( Klinik ), hvor relevante sygdomme, symptombilleder og behand forord
8 linger beskrives i lyset af den biokemiske grundviden. De mange kliniske eksempler er med til at gøre biokemien klinisk relevant og vil samtidig introducere andre fag som sygdomslære og farmakologi ud fra et biokemisk synspunkt. erudover findes uddybende bokse ( Fordybelse ) med supplerende viden for den særligt interesserede. Ved at holde sig til grundteksten får man et overblik over det ønskede emne, mens boksene kan betragtes som ekstramateriale, der giver mulighed for fordybelse i enkelte emner. Bogen kan derfor bruges af fagpersoner med forskellig interesse og forskellige faglige niveauer. Sprogbrug Bogens kliniske perspektiv afspejles i sprogbrugen. Derfor vil der være en blanding af latinske og danske udtryk for bl.a. organer og sygdomme, alt efter hvilke termer der dominerer i den kliniske jargon. Målgruppe Bogen er især målrettet biokemiundervisningen ved sygeplejeuddannelsen i Danmark. Teksten er blevet reviewet af undervisere på Metropol i København og grundigt gennemlæst af en række sygeplejersker på Aarhus Universitetshospital og på Sygehus ThyMors. Derudover er Basal biokemi med sit kliniske fokus og mange kliniske bokse relevant for de sundhedsprofessionelle, der er i berøring med medicinsk behandling. Først og fremmest sygeplejersker, ergoterapeuter og fysioterapeuter, både under uddannelse og i livet på klinikken derefter. Desuden kan bogen med fordel benyttes af jordemødre og medicinstuderende. Tak Vi skylder en stor tak til de mange, der har hjulpet til undervejs i bogens tilblivelse. Ikke mindst vores familier, men også de mange reviewere, der har deltaget med stor entusiasme i projektet og været medvirkende til at give bogen sin endelige form. En særlig tak til Line Becher Johannesen, Gitte Ravn Billeschou, Lisa Visbye Bendtsen, Karina Jakobsen og Bendt Gufler for deres kliniske og pædagogiske bidrag til bogens udformning. November 0 Vibeke Diness Borup og Jakob Dal Basal biokemi
9 Forfattere og reviewere Forfatterne Fra Metropol, København Vibeke Diness Borup Født 975. Molekylærbiolog, ph.d. fra Aarhus Universitet. Forfatter til lærebogen Biokemi for medicinstuderende (FADL s Forlag, 00). Undervisningserfaring: Molekylærbiologi på molekylærbiologistudiet samt cellebiologi og medicinsk biokemi på medicinstudiet, Aarhus Universitet. Lene erly Lektor, cand.scient. Gudrun Spure ansen Lektor, cand.scient. i humanbiologi. Suzanne Flemingübertz Underviser, cand.scient. Jakob Dal Født 90. Reservelæge på Medicinsk Endokrinologisk Afdeling MEA, Nørrebrogade, Aarhus Universitetshospital. Undervisningserfaring: Medicinsk biokemi på medicinstudiet ved Aarhus Universitet og Medicinsk biokemi og endokrinologi på Sygeplejerskeuddannelsen i Thisted, VIA University College. Sygeplejersker Fra Medicinsk Endokrinologisk afdeling MEA, Nørrebrogade, Aarhus Universitetshospital Line Becher Johannesen Specialeansvarlig. Reviewerne Undervisere Bendt Gufler Tidligere ekstern underviser ved sygeplejeuddannelsen i Næstved og Ringsted. Gitte Ravn Billeschou Klinisk vejleder. Lisa Visbye Bendtsen Klinisk vejleder. forfattere og reviewere 3
10 Fra Sygehus ThyMors, Thisted Karina Jakobsen Sygeplejerske. enrik olm Thomsen. reservelæge. Medicinsk Endokrinologisk Afdeling MEA, Nørrebrogade, Aarhus Universitetshospital. Forsker Maciej Bogdan Maniecki Msc, ph.d. Klinisk Biokemisk Afdeling. Aarhus Universitetshospital. Læger Lisbet Ambrosius Christensen Overlæge, klinisk lektor, dr.med. Medicinsk epatogastroenterologisk Afdeling V. Aarhus Universitetshospital. Christian Lodberg vas. reservelæge, ph.d. Medicinsk epatogastroenterologisk Afdeling V. Aarhus Universitetshospital. Niels Møller Professor, dr.med. Medicinsk Endokrinologisk Afdeling MEA, Nørrebrogade, Aarhus Universitetshospital. Gerda Elisabeth Villadsen Overlæge, klinisk lektor, ph.d. Medicinsk epatogastroenterologisk Afdeling V. Aar hus Universitetshospital. Søren Kragh Moestrup Professor, dr.med. Institut for Biomedicin Medicinsk Biokemi. Aarhus universitet. 4 Basal biokemi
11 Kemi Kemien beskriver, hvordan stoffer er opbygget, og hvordan de virker på hinanden. Kemi er det fundament, som hele livet bygger på. Alle kroppens processer foregår ved hjælp af kemi. Det er kemi, der får hjertet til at slå, og det er kemi, der får hjernen til at tænke tanker. De kemiske processer påvirker alle typer stoffer i kroppen atomer, ioner, salte og molekyler og for at forstå alle disse processer er det nødvendigt at kende en række kemiske grundbegreber. Atomet Alt omkring os er opbygget af atomer, både alt dødt som jord, luft, ild og vand og alt levende, dvs. planter og dyr. For at forstå, hvordan atomerne påvirker hinanden og samarbejder i kroppen, er det vigtigt at vide lidt om atomets opbygning. Alle atomer består af: Positivt ladede protoner Neutralt ladede neutroner Negativt ladede elektroner Atomets kerne består af protoner og neutroner (figur.). Indholdet af protoner giver kernen en positiv ladning. De neutralt ladede (dvs. ikkeladede) neutroner sørger for at skabe afstand mellem de positivt ladede protoner, så den elektriske frastødning mellem dem mindskes. Ellers ville kernen ikke kunne holdes sammen som en enhed. Protoner og neutroner er omtrent lige store, og det er disse partikler, der udgør størstedelen af atomets vægt, for elektronerne er meget mindre (.000 gange mindre) end disse. Når man beregner atomets vægt, hvilket også kaldes atomets masse, kan man derfor se bort fra elektronerne og kun tælle protoner og neutroner i kernen. Elektronerne bevæger sig med stor fart omkring kernen. Elektronerne bevæger sig i særlige baner, der også kaldes elektronskaller (figur.). I den inderste elektronskal, dvs. den skal, der er nærmest kernen, er der maksimalt plads til to elektroner. vis der var flere elektroner i den inderste elektronskal, ville frastødningen mellem de negativt ladede elektroner blive for stor. I de andre skaller, der ligger længere væk fra kernen, og som derfor er stør kemi 5
12 re, er der plads til flere elektroner. De negativt ladede elektroner holdes fast i deres baner omkring kernen, fordi de tiltrækkes af den positivt ladede kerne. Det er antallet af protoner i kernen, der definerer et atom. De atomer, der har samme antal protoner i kernen, har samme kemiske egenskaber og kaldes samlet for et grundstof. vert grundstof har et kemisk navn, et bogstavsymbol og et atomnummer. Atomnummeret angiver, hvor mange protoner der er i kernen. Eksempelvis har brint det kemiske navn hydrogen, atomtegnet og atomnummer, fordi det er det mindste atom med kun én proton i kernen (figur.a). elium har atomtegnet e og atomnummer, fordi der er to protoner i kernen. Kulstof har det kemiske navn carbon, atomtegnet C og atomnummer 6, fordi det har seks protoner i kernen, osv. Grundstofferne opstilles efter deres atomnummer og kemiske egenskaber i det, man kalder det periodiske system (figur.7 og side 7). Et atom indeholder lige så mange elektroner som protoner og er derfor totalt set uladet. F.eks. vil kulstofatomet indeholde seks elektroner og seks protoner (figur.b). Inden for det samme grundstof kan atomerne have et forskelligt antal neutroner i kernen. Normalt svarer antallet af neutroner i kernen til antallet af protoner, men nogle gange kan der være flere eller færre neutroner end protoner. Atomer med samme antal protoner i kernen, men med forskellige antal neutroner, kaldes isotoper af et grundstof. Isotoper vil have samme atom nummer, dvs. de tilhører samme grund stof, men vil have forskellig vægt (forskel lig atommasse). Nogle isotoper er ustabile og vil med tiden henfalde til mere stabile former. F.eks. kan en overskydende neutron blive nedbrudt. I henfaldsprocessen udskilles radioaktiv stråling, der kan måles. Disse ustabile isotoper kal des radioaktive isotoper og bruges i kli nikken til bl.a. at bestemme mængden af et bestemt stof i kroppen eller til at under søge, hvordan et stof bevæger sig rundt i kropa) b) + Brintatomet Kulstofatomet elektron elektronskal proton neutron Figur.. Atomers opbygning a) Brintatomet (hydrogenatomet) er det mindste atom. Kernen består af én proton. Omkring kernen bevæger sig én elektron. b) Kulstofatomet (carbonatomet) er et større atom. Kernen består af seks positivt ladede protoner og seks neutralt ladede neutroner. Seks elektroner bevæger sig omkring kernen. Elektronernes bane er her tegnet i ét plan. I virkeligheden vil elektronerne bevæge sig rundt om kernen på en tredimensionel måde. 6 Basal biokemi
13 pen. Radioaktive partikler benyttes også i kræftbehandlingen til bekæmpelse af kræftceller. Et atom kan afgive eller optage elektroner fra omgivelserne. erved dannes en ion. En ion vil have en ubalance mellem antallet af negativt ladede elektroner og positivt ladede protoner og vil derfor totalt set være ladet. vis ionen mangler en eller flere elektroner, vil det have en overskydende positiv ladning, fordi der nu er flere protoner end elektroner. En positiv ladet ion kaldes en kation, fordi den vil vandre mod en negativt ladet pol, der kaldes katoden, når den anbringes i et elektrisk felt. Eksempler på kationer er Na +, der har afgivet én elektron og Ca +, der har afgivet to elektroner. vis ionen har en eller flere elektroner, end der er protoner i kernen, vil den have en negativ ladning. En negativt ladet ion kaldes en anion, fordi den i et elektrisk felt vil vandre mod en positivt ladet pol, der kaldes anoden. Et eksempel på en anion er Cl, der har optaget én elektron. I klinikken betegnes ioner ofte som elektrolytter, se kapitel 7. Kemiske bindinger Atomernes elektroner er kemisk vigtige, fordi det er dem, der gør det muligt for atomer at danne bindinger med hinanden. Vigtigst er elektronerne i atomets yderste elektronskal. Et atom er mest stabilt, når det har den yderste elektronskal fyldt op med elektroner. De små atomer hydrogen og helium er således mest stabile, når de har to elektroner i deres eneste og derfor yderste skal. Andre og større atomer med flere elektronskaller er mest stabile med otte elektroner i deres yderste skal. Atomer vil derfor stræbe efter at få deres yderste skal fyldt op med elektroner. Denne stræben efter at få to eller otte elektroner i den yderste elektronskal kaldes oktetreglen (octo = otte). Atomerne kan få deres yderste elektronskal fyldt op ved at gå sammen med andre atomer enten så atomerne deles om elektroner, eller ved at det ene atom afgiver en eller flere elektroner til et andet atom, så der dannes to ioner. erved kan der dannes to typer bindinger, der kaldes henholdsvis kovalente bindinger og ionbindinger. Kovalente bindinger En kovalent binding dannes, hvor to atomer hver bidrager med en elektron til et fællesskab. Dvs. to atomer deles om et elektronpar (figur.a). Kovalente bindinger kaldes derfor også for elektronparbindinger. De to elektroner, som deles af de to atomer i bindingen, kaldes for bindingselektroner. Begge atomer i den kovalente binding kan tælle de to fælles elektroner som deres egne. Begge atomer i bindingen vil herved have en mere stabil struktur, end hvis atomerne var hver for sig. Kovalente bindinger er de stærkeste af alle bindinger. Det er de kovalente bindinger, der binder atomer sammen til molekyler. Molekyler kan bestå af to til flere tusinde atomer, der alle er bundet sammen med kovalente bindinger. Når man tegner et molekyle, vil man angive de kovalente bindinger med solide streger mellem atomerne (figur.). Enkeltbindinger, dvs. en kovalent binding, hvor der deles om ét kemi 7
14 a) Et molekyle Deles om elektroner Kovalent binding b) C C C C 4 Methan c) O C O O C O O C O CO Kuldioxid d) O O O O O O O Iltmolekylet e) O O O O Vand f) N N N N N N N Nitrogengas Basal biokemi elin@gigraf.dk tlf Illustration fig. Bognavn Biokemi i sygeplejen
15 Figur.. Kovalente bindinger og molekyler a) En kovalent binding dannes mellem to atomer, der deles om et elektronpar. bf) Eksempler på molekyler, der dannes ved sammenbinding af atomer med kovalente bindinger. vert atom i den kovalente binding leverer en elektron til den kovalente binding. Elektronerne fra de forskellige atomer er angivet med lyseblå og mørkeblå farve (molekylformlerne til venstre og i midten til venstre). I enkeltbindinger deles to atomer om et elektronpar. Enkeltbindinger vises med enkeltstreger (stregformlerne i midten til højre). I dobbeltbindinger deles om to elektronpar, hvilket vises med dobbeltstreger. I tripelbindinger deles om tre elektronpar, hvilket vises med tripelstreger. elektronpar, angives med en enkelt streg (figur.b og e). Dobbelte kovalente bindinger, der kaldes dobbeltbindinger, dannes, når to atomer deles om fire elektroner, dvs. om to elektronpar. Dobbeltbindinger angives med to streger mellem atomerne (figur.c og d). vis de to atomer deles om tre elektronpar, kaldes det en tripelbinding. Tripelbindinger angives med tre streger mellem atomerne (figur.f). Antallet af kovalente bindinger, som et atom kan danne, afhænger af antallet af elektroner i atomets yderste elektronskal. Dette antal kan ses i det periodiske system (figur.7). Eksempelvis har brintatomet (hydrogen, ) én elektron i sin yderste (og eneste) skal og vil gerne have en elektron mere for at få skallen fyldt op. Brintatomet kan derfor få parret sin enlige elektron ved at danne én kovalent binding (figur.b og e). Kulstofatomet (carbon, C) har fire elektroner i sin yderste skal og vil gerne have fire mere for at opnå otte elektroner i sin yderste skal. Kulstofatomet kan derfor få parret sine fire enlige elektroner ved at indgå i fire kovalente bindinger (figur.b og c). Kvælstofatomet (nitrogen, N) har fem elektroner i sin yderste elektronskal og ønsker tre mere. Kvælstofatomet kan derfor danne tre kovalente bindinger (figur.f). Iltatomet (oxygen, O) har seks elektroner i sin yderste skal og vil gerne have to mere. Iltatomet kan derfor danne to kovalente bindinger (figur.c, d og e). Kulstofatomet benyttes som byggesten i mange molekyler, fordi det kan danne fire mulige kovalente bindinger (se Fordybelse.). Eksempelvis kan kulstofatomet vælge at placere sig helt tæt op ad fire brintatomer (), der hver har én elektron at tilbyde fællesskabet. erved dannes methanmolekylet, C 4, der indeholder fire kovalente bindinger (figur.b). Kulstofatomet kan også lægge sig tæt op ad to iltatomer (O), så der dannes kuldioxid, CO, der indeholder to dobbelte kovalente bindinger (figur.c). I figur. vises også opbygningen af iltmolekylet (O ), vandmolekylet ( O) og nitrogenmolekylet (N ), der indeholder en tripelbinding. Kovalente bindinger dannes mellem atomer, der ikke er metaller (se figur.7, Det periodiske system). Kroppens molekyler vil primært være opbygget af grundstofferne kulstof (C), brint (), ilt (O), kvæl stof (N), fosfor (P), og svovl (S). Se også Fordybelse.. kemi 9
16 Fordybelse.: Organiske molekyler Kulstofatomet kan danne hele fire kovalente bindinger med andre atomer. Dette gør det muligt at opbygge store og komplicerede molekyler med en kerne af kulstofatomer, hvorpå der sidder mange forskellige sidegrupper. F.eks. består sukkermolekylet glukose af seks kulstofatomer med sidegrupper (figur 4.). Ligeledes består aminosyrer og lipider (fedtstoffer) af en kulstofkerne med sidegrupper (figur 3., 5., 5.4 og 5.6). Alle molekyler (undtagen CO ), der indeholder kulstofatomet, kaldes for organiske molekyler. Tidligere mente man, at så komplicerede molekyler kun kunne dannes i levende organismer, heraf navnet organisk. Ionbindinger En Ionbinding dannes mellem to ioner. Ioner dannes ved, at et atom overfører en eller flere elektroner til et andet atom. Der dannes herved to ioner, en positivt ladet kation og en negativt ladet anion (figur.3a). De to ioner kan holdes sammen i en ionbinding, fordi deres to modsatrettede ladninger (plus og minus) tiltrækker hinanden. Alle salte består af ioner, der holdes sammen med ionbindinger. Et klassisk eksempel på en ionbinding er sammenbinding af natriumionen (Na + ) og klorionen (Cl ) til saltet natriumklorid (NaCl), der er almindeligt køkkensalt. De to ioner dannes, fordi der sker en elektronoverførsel (figur.3b). Natrium har én elektron i sin yderste elektronskal og otte elektroner i sin næstyderste skal. Natrium vil derfor gerne af med den ene elektron i sin yderste skal, så den opnår otte elektroner yderst. Modsat har klor syv elektroner i sin yderste skal og vil gerne have en mere for at fylde skallen op. Natrium kan derfor med fordel overføre en elektron til klor, hvorved der dannes Na + og Cl. Disse to ioner kan herefter interagere elektrisk (ved plusminustiltrækning) med en ionbinding, hvorved der dannes NaCl. Andre salte dannes på lignende vis. Et salt er derfor ikke et molekyle, men en generel betegnelse for en ionforbindelse mellem en positivt ladet ion, typisk en metalion, og en negativt ladet ikkemetalion (om metaller og ikkemetaller, se figur.7, Det periodiske system). F.eks. kan der dannes salte mellem metalionerne Na +, Ca +, K + og Mg + og ikkemetalionerne Cl 3, PO 4 (fosfat) og CO 3 (carbonat). Ikkemetalionerne er typisk syrerester, hvilket er den negative ion, der er tilbage, når en syre har afgivet sin + (se side 3 og figur.). En klump salt vil indeholde mange ionforbindelser. F.eks. består en klump bordsalt af mange NaClionforbindelser. Antallet af positive og negative ladninger i ionbindingen skal være ens, dvs. der skal være lige så mange positive ladninger som negative ladninger. Eksempelvis vil Na + og Cl danne NaCl (natriumklorid), mens Ca + må finde to negative ladninger at binde med, f.eks. CO 3, så der dannes CaCO 3 (calciumcarbonat, almindeligt kalk), eller Cl, så der dannes CaCl (calciumklorid). I molekyler, dvs. atomer bundet sammen med kovalente bindinger, kan nogle af atomerne i molekylet også afgive eller optage elektroner og blive til ioner. En molekylgruppe, som er en ion, kaldes en ioni 0 Basal biokemi
17 Figur.3. Ionbinding og ioner a) Ioner dannes ved overførsel af en elektron fra et atom til et andet. erved dannes en positivt ladet ion og en negativt ladet ion. Ioner med modsat ladning tiltrækkes og kan fastholdes ved elektrostatiske kræfter i en ionbinding. b) Natriumatomet kan overføre en elektron til kloratomet, hvorved der dannes en natriumion (Na + ) og en klorion (Cl ). De to ioner kan fastholdes i en ionbinding og danne saltet NaCl. seret gruppe, og en sådan gruppe vil have en negativ eller en positiv ladning. Eksempler på molekylgrupper, der ofte er ioniserede i kroppen, er aminogrupper (N ), der er positivt ladede i kroppen (N 3+ ), og carboxylgrupper (COO) og fosforsyregrupper ( PO 4 ), der er negativt ladede (COO og PO 4 ). Disse ladede grupper kan danne ionbindinger med hinanden, + f.eks. kan N 3 danne en ionbinding med COO. Ioner og ioniserede grupper er nemme at genkende på illustrationer, fordi ladningen altid angives med et + eller på atomet eller molekylet. Polære og upolære molekyler Atomerne i et molekyle holdes sammen af kovalente bindinger. I en kovalent binding vil de to atomer deles om to elektroner. kemi
18 Men de to atomer, som deler elektroner, kan være uens eller ens i styrke, mht. hvor meget de trækker bindingselektronerne til sig. erved kan der dannes polære og upolære molekyler. Polære molekyler dannes, hvis de indeholder en kovalent binding, hvor de to atomer i bindingen har forskellig evne til at trække de negativt ladede elektroner til sig. er bliver bindingselektronerne ulige fordelt mellem de to atomer. Omkring det atom, der suger elektronerne til sig, vil der blive en smule negativt ladet. Modsat vil der omkring det andet atom i bindingen blive en smule positivt ladet, fordi elektronerne er suget væk. Der vil således blive dannet et molekyle, hvor der inden for molekylet optræder områder med svage negative og svage positive ladninger. Der bliver ikke dannet en decideret ion, for elektronerne er ikke helt afgivet eller optaget. Elektronerne er stadig i den kovalente binding, de er bare forskudt mod det ene atom i bindingen. Et sådant molekyle kaldes et polært molekyle, fordi det har svagt ladede ender, dvs. svagt ladede poler. Vandmolekylet er et sådan polært molekyle, se Fordybelse. og figur.4. Molekylgrupperne O, =O, CO eller S er polære, og molekyler med disse grupper vil være polære molekyler (tabel. og kapitel 3). Upolære molekyler dannes, når molekylet udelukkende indeholder kovalente bindinger, hvor de to atomer i bindingen har samme evne til at trække elektroner til sig. er vil bindingselektronerne være ligeligt fordelt mellem de to atomer i bindingen. Der vil derfor ikke dannes små ladningsforskydninger i molekylet, og molekylet vil ikke have nogen ladning udadtil. Et sådan neutralt ladet molekyle siges at være upolært. Alle CC og Cbindinger er upolære. Lipider (fedtstoffer) består fortrinsvis af disse typer bindinger, og alle lipider er upolære molekyler (kapitel 5). Om et molekyle er polært eller upolært, spiller en stor rolle for dets mulighed for at interagere med andre molekyler i omgivelserne, heriblandt om det er opløseligt i vand eller ej. Alle interaktioner mellem molekyler foregår ved nonkovalente bindinger, der beskrives i næste afsnit. Fordybelse.: Vandmolekylet er et polært molekyle Vandmolekylet består af et iltatom (O) og to brintatomer (). Iltatomet danner en kovalent binding med hvert brintatom (figur.4). Ilt er bedre til at trække elektroner til sig end brint. Evnen til at trække elektroner til sig kaldes elektronegativitet. Et meget elektronegativt atom har en høj evne til at trække elektroner til sig. Dvs. ilt er mere elektronegativt end brint. Derfor vil der opstå en svag negativ ladning omkring iltatomet og en svag positiv ladning omkring hvert brintatom i vandmolekylet (figur.4). Da vandmolekylet er lidt asymmetrisk opbygget med brintatomerne siddende sammen lidt mod den ene side, er resultatet, at vandmolekylet har to poler: en negativ pol, hvor iltatomet sidder, og en positiv pol, hvor brintatomerne sidder. Vandmolekylet er derfor generelt et polært molekyle og mere specifikt en dipol (di = to) (figur.4). Basal biokemi
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Intra- og intermolekylære bindinger.
 Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Atomets bestanddele. Indledning. Atomer. Atomets bestanddele
 Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Torben Rosenørn. Aalborg Universitet. Campus Esbjerg
 Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
DET PERIODISKE SYSTEM
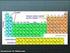 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Lim mellem atomerne Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Proteiner. Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde
 Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Opgave: Du skal udfylde de manglende felter ud fra den information der er givet
 pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Molekyler & Mere Godt Kemi
 Molekyler & Mere Godt Kemi Elektronparbindinger Molekylgeometri Elektronegativitet Ethanol Buchminster Fulleren Carbondioid Asbest influenza vaccine Diamant Indhold. 1. Molekyler og Kovalente Bindinger....
Molekyler & Mere Godt Kemi Elektronparbindinger Molekylgeometri Elektronegativitet Ethanol Buchminster Fulleren Carbondioid Asbest influenza vaccine Diamant Indhold. 1. Molekyler og Kovalente Bindinger....
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Kemiske bindinger. Præsentation: Niveau: 8. klasse. Varighed: 7 lektioner
 Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Proteiners byggesten er aminosyrer
 PTEIE G EZYME Proteiners byggesten er aminosyrer Lad os se på den kemiske opbygning af et protein. Proteiner er store molekyler der er opbygget af mindre molekyler, som man kalder aminosyrer. Der findes
PTEIE G EZYME Proteiners byggesten er aminosyrer Lad os se på den kemiske opbygning af et protein. Proteiner er store molekyler der er opbygget af mindre molekyler, som man kalder aminosyrer. Der findes
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017
 EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
Eksamensopgaver. NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL
 Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Ernæring, fordøjelse og kroppen
 Ernæring, fordøjelse og kroppen Modul 4 Kernestof a) Kost & fordøjelse b) Kroppens opbygning & motion Mål med modulet Ernæring og fordøjelse At give kursisten vished om næringsstoffers energiindhold, herunder
Ernæring, fordøjelse og kroppen Modul 4 Kernestof a) Kost & fordøjelse b) Kroppens opbygning & motion Mål med modulet Ernæring og fordøjelse At give kursisten vished om næringsstoffers energiindhold, herunder
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi enkeltfag
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi enkeltfag
1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation
 Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
KEMI C. Videooversigt
 KEMI C Videooversigt Afstemning og mængdeberegning... 2 Atomer og det periodiske system... 2 Forsøgsfilm... 2 Ioner og salte... 3 Molekyler... 3 Opløsninger og tilstandsformer... 3 Organisk kemi... 3 Redoxreaktioner...
KEMI C Videooversigt Afstemning og mængdeberegning... 2 Atomer og det periodiske system... 2 Forsøgsfilm... 2 Ioner og salte... 3 Molekyler... 3 Opløsninger og tilstandsformer... 3 Organisk kemi... 3 Redoxreaktioner...
Litteratur: Naturfag Niveau D og C, H. Andersen og O. B. Pedersen, Munksgaard, 2016 Grundlæggende kemi intro (kap 2)
 Læringsmål Naturfag C niveau Litteratur: Naturfag Niveau D og C, H. Andersen og O. B. Pedersen, Munksgaard, 2016 Grundlæggende kemi intro (kap 2) Du forklarer, hvad et atoms opbygning er ved hjælp af det
Læringsmål Naturfag C niveau Litteratur: Naturfag Niveau D og C, H. Andersen og O. B. Pedersen, Munksgaard, 2016 Grundlæggende kemi intro (kap 2) Du forklarer, hvad et atoms opbygning er ved hjælp af det
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Læringsmål i fysik - 9. Klasse
 Læringsmål i fysik - 9. Klasse Salte, syrer og baser Jeg ved salt er et stof der er opbygget af ioner. Jeg ved at Ioner i salt sidder i et fast mønster, et iongitter Jeg kan vise og forklare at salt, der
Læringsmål i fysik - 9. Klasse Salte, syrer og baser Jeg ved salt er et stof der er opbygget af ioner. Jeg ved at Ioner i salt sidder i et fast mønster, et iongitter Jeg kan vise og forklare at salt, der
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Mundtlige eksamensopgaver
 Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
Forord. Undervisere kan bruge arket ved først at kontakte pierre@naae.dk og få et skriftligt tilsagn.
 Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Syrer, baser og salte
 Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
1 Atomets opbygning. Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom.
 1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2012 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2012 Københavns
Oversigt med forklaring over forskellige begreber
 Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Kulhydrater består af grundstofferne C, H og O. Der findes tre former for kulhydrater. Monosakkarider, disakkarider og polysakkarider
 Madkemi Mad giver os de dele vi skal bruge til at opbygge vores krop. Maden består af de kemiske stoffer vi skal bruge, når nye celler skal dannes. Hvis vi ikke spiser en varieret kost kan vi komme til
Madkemi Mad giver os de dele vi skal bruge til at opbygge vores krop. Maden består af de kemiske stoffer vi skal bruge, når nye celler skal dannes. Hvis vi ikke spiser en varieret kost kan vi komme til
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Eksamensopgaverne offentliggøres selvfølgelig med det forbehold, at censor kan komme med ændringsforslag.
 VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
Eksamensspørgsma l kemi C, 2015, kec324 (CHT)
 Oversigt Sp. 1 og 2 Ioner og Ionforbindelser Sp. 3, 4 og 5 Molekylforbindelser Sp. 6 Kemisk mængdeberegning Sp. 7 Koncentration i en opløsning Sp. 8 og 9 Organisk kemi Sp. 10 og 11 Syrer og baser Sp. 12
Oversigt Sp. 1 og 2 Ioner og Ionforbindelser Sp. 3, 4 og 5 Molekylforbindelser Sp. 6 Kemisk mængdeberegning Sp. 7 Koncentration i en opløsning Sp. 8 og 9 Organisk kemi Sp. 10 og 11 Syrer og baser Sp. 12
BASISKEMI C. Facit HELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN HAASE & SØNS FORLAG
 BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
1 Ioner og ionforbindelser
 1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men
 På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
Fagmål. Naturfag. C niveau
 Fagmål Naturfag C niveau 1. Selvstændigt kan vælge og anvende naturfaglige begreber og modeller på udvalgte naturog erhvervsfaglige problemstillinger 2. selvstændigt kan vælge og anvende matematik til
Fagmål Naturfag C niveau 1. Selvstændigt kan vælge og anvende naturfaglige begreber og modeller på udvalgte naturog erhvervsfaglige problemstillinger 2. selvstændigt kan vælge og anvende matematik til
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj/ Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF Kemi enkeltfag
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj/ Juni 2016 Institution HF & VUC Nordsjælland Uddannelse Fag og niveau Lærer(e) Hold HF Kemi enkeltfag
ZCD Anatomi og Fysiologi
 ZCD Anatomi og Fysiologi Modul 1 Indtroduktion til anatomi, fysiologi og sundhedsvidenskab Lektion 2 Sundhedsvidenskab for anatomi og fysiologi studerende 1.0 Tekniske måleenheder: I fysiologi anvendes
ZCD Anatomi og Fysiologi Modul 1 Indtroduktion til anatomi, fysiologi og sundhedsvidenskab Lektion 2 Sundhedsvidenskab for anatomi og fysiologi studerende 1.0 Tekniske måleenheder: I fysiologi anvendes
Fedt -det gode, det onde og det virkelig grusomme. Mette Riis, kostvejleder, fitnessdk Slagelse 2. okt. 2008
 Fedt -det gode, det onde og det virkelig grusomme Fedme er den vigtigste kendte årsag til type 2- diabetes forårsager øget risiko for - kar sygdomme øger risikoen for visse former for kræft kan være årsag
Fedt -det gode, det onde og det virkelig grusomme Fedme er den vigtigste kendte årsag til type 2- diabetes forårsager øget risiko for - kar sygdomme øger risikoen for visse former for kræft kan være årsag
Madkemi Kulhydrater: er en gruppe af organiske stoffer der består af kul, hydrogen og oxygen (de sidste to i forholdet 2:1, ligesom H 2
 Madkemi Kulhydrater: er en gruppe af organiske stoffer der består af kul, hydrogen og oxygen (de sidste to i forholdet 2:1, ligesom H 2 O); derfor navnet kulhydrat (hydro: vand (græsk)). fælles for sukkermolekylerne
Madkemi Kulhydrater: er en gruppe af organiske stoffer der består af kul, hydrogen og oxygen (de sidste to i forholdet 2:1, ligesom H 2 O); derfor navnet kulhydrat (hydro: vand (græsk)). fælles for sukkermolekylerne
Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold
 Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Ernæring, fordøjelse og kroppen
 Ernæring, fordøjelse og kroppen Modul 4 Kernestof a) Kost & fordøjelse b) Kroppens opbygning & motion Mål med modulet Ernæring og fordøjelse At give kursisten vished om næringsstoffers energiindhold, herunder
Ernæring, fordøjelse og kroppen Modul 4 Kernestof a) Kost & fordøjelse b) Kroppens opbygning & motion Mål med modulet Ernæring og fordøjelse At give kursisten vished om næringsstoffers energiindhold, herunder
Fysikforløb nr. 6. Atomfysik
 Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2012-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2012-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Opgave 2a.01 Cellers opbygning. Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten
 Opgave 2a.01 Cellers opbygning Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten Vakuole - Lager-rum med energi Grønkorn Cellekerne (DNA) Cellemembran Cellevæg Mitokondrier 1. Hvad
Opgave 2a.01 Cellers opbygning Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten Vakuole - Lager-rum med energi Grønkorn Cellekerne (DNA) Cellemembran Cellevæg Mitokondrier 1. Hvad
Oxidationstal og elektronparbindinger December 2015
 idationstal og elektronparbindinger December 2015 idationstal og elektronparbindinger I redokemi findes en række simple regler, som gør det muligt at bestemme oidationstal for et atom i en kemisk forbindelse,
idationstal og elektronparbindinger December 2015 idationstal og elektronparbindinger I redokemi findes en række simple regler, som gør det muligt at bestemme oidationstal for et atom i en kemisk forbindelse,
Spørgsmål 1. Øvelse: Kobber plus dibrom. Teori: Atomers opbygning.
 Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af salte og
Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af salte og
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men
 På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Spørgsmål 1 Den kemiske reaktion
 Spørgsmål 1 Den kemiske reaktion Du skal gennemgå eksperimentet Fyrfadslys inddrag gerne dine forsøgsresultater og vurder om de understøtter modellen reaktionskemaet. Du skal endvidere give eksempler på
Spørgsmål 1 Den kemiske reaktion Du skal gennemgå eksperimentet Fyrfadslys inddrag gerne dine forsøgsresultater og vurder om de understøtter modellen reaktionskemaet. Du skal endvidere give eksempler på
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Københavns
Spørgsmål 1. Øvelse: Kobber plus dibrom. Teori: Atomers opbygning.
 Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af ioner og
Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af ioner og
KEMI Vigtig baggrundsviden for biologer
 KEMI Vigtig baggrundsviden for biologer af Niels Roholt Århus Akademi 1994 For at forstå, hvordan en levende organisme fungerer, må man vide noget om sammensætningen af stofferne i protoplasma og de ændringer,
KEMI Vigtig baggrundsviden for biologer af Niels Roholt Århus Akademi 1994 For at forstå, hvordan en levende organisme fungerer, må man vide noget om sammensætningen af stofferne i protoplasma og de ændringer,
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Du skal også komme ind på øvelsen Saltes opløselighed i vand.
 1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
Fysik og kemi i 8. klasse
 Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Eksamensspørgsmål. Spørgsmål : Atomer og bindinger (Hvilken type stof?) Spørgsmål : Ionforbindelser (Saltes opløselighed i vand
 Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
Er der flere farver i sort?
 Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj, 2019 (denne
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj, 2019 (denne
Folkeskolens afgangsprøve Maj-juni 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Vikar-Guide. Den elektriske ladning af en elektron er -1 elementarladning, og den elektriske ladning af protonen er +1 elementarladning.
 Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014
 Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Grundlæggende egenskaber for vand og fedt
 Side: 1/9 Grundlæggende egenskaber for vand og fedt Forfattere: Morten Christensen Redaktør: Thomas Brahe Faglige temaer: Vand, Olie, Hydrofil, Hydrofob Kompetenceområder: Undersøgelse, Perspektivering,
Side: 1/9 Grundlæggende egenskaber for vand og fedt Forfattere: Morten Christensen Redaktør: Thomas Brahe Faglige temaer: Vand, Olie, Hydrofil, Hydrofob Kompetenceområder: Undersøgelse, Perspektivering,
Syrer, baser og salte:
 Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Alkohol Ingrid Jespersens Gymnasieskole 2007
 Alkohol Ingrid Jespersens Gymnasieskole 007 Ethanols fysiske egenskaber Kogepunkt 78,5 o C På side 8 i Alkohol også vises Frysepunkt -114, o C opskriften på et forsøg til bestemmelse af Massefylde 0,789
Alkohol Ingrid Jespersens Gymnasieskole 007 Ethanols fysiske egenskaber Kogepunkt 78,5 o C På side 8 i Alkohol også vises Frysepunkt -114, o C opskriften på et forsøg til bestemmelse af Massefylde 0,789
Platin komplekser i kampen mod kræft. Koordinationskemi i aktion. cis-ptcl 2 (NH 3 ) 2. Essentiel, nyttig eller toxisk. Hvad der faktisk skete
 Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Spørgsmål 1 Den kemiske reaktion
 Spørgsmål 1 Den kemiske reaktion Med udgangspunkt i eksperimentet Fyrfadslys ønskes der en gennemgang af modellen reaktionskemaet. Du skal endvidere inddrage forskellige typer af kemiske reaktioner i din
Spørgsmål 1 Den kemiske reaktion Med udgangspunkt i eksperimentet Fyrfadslys ønskes der en gennemgang af modellen reaktionskemaet. Du skal endvidere inddrage forskellige typer af kemiske reaktioner i din
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Forløb: 9/7-2010 9/8-2012, Eksamen: 15/8-2012 Institution VUC Vest Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Forløb: 9/7-2010 9/8-2012, Eksamen: 15/8-2012 Institution VUC Vest Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Termin hvori undervisningen afsluttes: Maj/juni 2021 (denne UVB dækker kun 1.g) Institution Uddannelse Fag
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Termin hvori undervisningen afsluttes: Maj/juni 2021 (denne UVB dækker kun 1.g) Institution Uddannelse Fag
Brugsvejledning for 7827.10 dialyseslange
 Brugsvejledning for 7827.10 dialyseslange 14.06.07 Aa 7827.10 1. Præsentation Dialyseslangen er 10 m lang og skal klippes i passende stykker og blødgøres med vand for at udføre forsøgene med osmose og
Brugsvejledning for 7827.10 dialyseslange 14.06.07 Aa 7827.10 1. Præsentation Dialyseslangen er 10 m lang og skal klippes i passende stykker og blødgøres med vand for at udføre forsøgene med osmose og
Teoretiske mål: Praktiske mål:
 Teoretiske mål: at kunne redegøre for simpel organisk kemi, herunder kulbrinter. at kunne redegøre for kulhydrater, herunder monosakkarider, disakkarider og polysakkarider samt deres indvirkning på kroppen.
Teoretiske mål: at kunne redegøre for simpel organisk kemi, herunder kulbrinter. at kunne redegøre for kulhydrater, herunder monosakkarider, disakkarider og polysakkarider samt deres indvirkning på kroppen.
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas
 Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen. Notatark
 BASISKEMI C Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen Notatark HAAse & Søns forlag Helge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Notatark forfatterne og Haase & Søns Forlag
BASISKEMI C Helge Mygind Ole Vesterlund Niel sen Vibeke A xelsen Notatark HAAse & Søns forlag Helge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Notatark forfatterne og Haase & Søns Forlag
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Termin hvori undervisningen afsluttes: Maj/juni 2020 (denne UVB dækker kun 1.g) Institution Uddannelse Fag
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Termin hvori undervisningen afsluttes: Maj/juni 2020 (denne UVB dækker kun 1.g) Institution Uddannelse Fag
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Vinter 2016 Institution VUC Lyngby Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C COL 16kemc21 Oversigt
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Vinter 2016 Institution VUC Lyngby Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C COL 16kemc21 Oversigt
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2013 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2013 Københavns
