Medicintilskudsnævnet
|
|
|
- Sara Krog
- 7 år siden
- Visninger:
Transkript
1 Lægemiddelstyrelsen Den 29. juni 2011 Axel Heides Gade København S Revurdering af tilskudsstatus for lægemidler i ATC-gruppe C01 (Hjerteterapi) Baggrund og indhold Lægemiddelstyrelsen har som led i revurderingsprocessen anmodet om at revurdere tilskudsstatus for lægemidler i ATC-gruppe C01, hjerteterapi. Flere af lægemidlerne er udelukkende eller i vidt omfang sygehusbehandling. ne til hjerteterapi i C01 fordeler sig i 5 undergrupper: Hjerteglykosider (C01A) Digoxin Antiarytmika, klasse I og III (C01B) Lidocain, propafenon, flecainid, amiodaron og dronedaron Hjertestimulerende midler ekskl. hjerteglycosider (C01C) Dopamin, dobutamin og adrenalin Vasodilatorer anvendt ved hjertesygdomme (C01D) Glycerylnitrat, isosorbiddinitrat, isosorbidmononitrat og nicorandil Andre midler til hjerteterapi (C01E) Adenosin og ivabradin Bilag A er en grafisk oversigt over lægemiddelstofferne i C01. Indstillingen omfatter alle 1 lægemidler i ATC-gruppe C01, der er godkendt til markedsføring i Danmark og som er eller har været markedsført per den 16. maj Vernakalant koncentrat til infusionsvæske, opløsning (C01BG11), alprostadil koncentrat til infusionsvæske, opløsning (C01EA01), ibuprofen injektionsvæske, opløsning (C01EB16) og icatibant injektionsvæske, opløsning (C01EB19) er alle begrænset til udlevering til sygehus og er derfor ikke medtaget i indstillingen. Indstillingen omfatter heller ikke lægemidler med indhold af trimetazidin (C01EB15), 1 s revurdering og denne indstilling omfatter dog ikke lægemidler godkendt med begrænset udlevering ( BEGR og AP4BG ) og naturlægemidler. 1
2 filmovertrukne tabletter, da disse lægemidlers tilskudsstatus vil blive revurderet senere sammen med andre lægemidler mod sygdomme i øret (ATC-gruppe S02). Nedenfor følger s indstilling til lægemidlernes fremtidige tilskudsstatus, en kort gennemgang af revurderingsforløbet og nævnets bemærkninger og begrundelser i relation til lægemidlerne og indstillingen. Bilag B er en oversigt over lægemiddelstofferne med angivelse af hvilke indikationer, lægemidler med indhold af det pågældende lægemiddelstof er godkendt til 2, lægemiddelnavne, lægemiddelformer, udleveringsgruppe, gældende tilskudsstatus, behandllingspris, årligt forbrug og oplysninger om enkelttilskud. s indstilling indstiller følgende til Lægemiddelstyrelsen: 1. i ATC-gruppe C01A (hjerteglykosider) med indhold af lægemiddelstoffet: Digoxin (C01AA05) bevarer gældende tilskudsstatus: generelt tilskud. 2. Perorale lægemidler i ATC-gruppe C01B (antiarytmika, klasse I og III) med indhold af lægemiddelstofferne: Propafenon (C01BC03) Flecainid (C01BC04) Amiodaron (C01BD01) bevarer gældende tilskudsstatus: generelt tilskud. 3. i ATC-gruppe C01B (antiarytmika, klasse I og III) med indhold af lægemiddelstoffet: Dronedaron (C01BD07) bevarer gældende tilskudsstatus: ikke generelt tilskud. Parenterale lægemidler i ATC-gruppe C01B (antiarytmika, klasse I og III) med indhold af lægemiddelstofferne: Lidocain (C01BB01) 3 2 Der er tale om en sammenskrivning af den eller de godkendte indikationer for lægemidler med indhold af det pågældende lægemiddelstof og lægemiddelform/administrationsvej. 3 med indhold af lidocain med ATC-koder inden for gruppe N (nervesystemet) og D (dermatologiske midler) er ikke omfattet af denne indstilling. 2
3 Flecainid (C01BC04) Amiodaron (C01BD01) bevarer gældende tilskudsstatus: ikke generelt tilskud 4. i ATC-gruppe C01C (hjertestimulerende midler ekskl. hjerteglycosid) med indhold af lægemiddelstofferne: Dopamin (C01CA04) Dobutamin (C01CA07) bevarer gældende tilskudsstatus: ikke generelt tilskud. 5. Parenterale lægemidler i ATC-gruppe C01C (hjertestimulerende midler ekskl. hjerteglycosider) med indhold af lægemiddelstoffet: Adrenalin (C01CA24) til autoinjektion, 0,15 mg/dosis og 0,3 mg/dosis bevarer gældende tilskudsstatus: generelt tilskud. 6. Parenterale lægemidler i ATC-gruppe C01C (hjertestimulerende midler ekskl. hjerteglycosider) med indhold af lægemiddelstoffet: Adrenalin (C01CA24) ampuller, 1 mg/ml ændrer tilskudsstatus fra generelt tilskud til ikke generelt tilskud. 7. i ATC-gruppe C01D (vasodilatorer anvendt ved hjertesygdomme) med indhold af lægemiddelstofferne: Glycerylnitrat (C01DA02) sublinguale resoribletter, sublingualspray og depotplastre Isosorbiddinitrat (C01DA08) depottabletter Isosorbidmononitrat (C01DA14) bevarer gældende tilskudsstatus: generelt klausuleret tilskud med klausulen: Angina pectoris. 8. i ATC-gruppe C01D (vasodilatorer anvendt ved hjertesygdomme) med indhold af lægemiddelstofferne: Glycerylnitrat (C01DA02) depotresoribletter Isosorbiddinitrat (C01DA08) tabletter ændrer tilskudsstatus fra generelt klausuleret tilskud med klausulen Angina pectoris til ikke generelt tilskud. 3
4 9. i ATC-gruppe C01D (vasodilatorer anvendt ved hjertesygdomme) med indhold af lægemiddelstoffet: Nicorandil (C01DX16) bevarer gældende tilskudsstatus: generelt tilskud. 10. i ATC-gruppe C01E (andre midler til hjerteterapi) med indhold af lægemiddelstofferne: Adenosin (C01EB10) Ivabradin (C01EB17) bevarer gældende tilskudsstatus: ikke generelt tilskud. Revurderingsforløb Lægemiddelstyrelsen orienterede i brev af 13. juni 2005 samtlige virksomheder med markedsføringstilladelse til humane lægemidler 4 om, at man ville indlede revurderingsprocessen med at revurdere tilskudsstatus for lægemidler i ATC-gruppe A, C og J. En række videnskabelige selskaber og patientforeninger modtog samme orientering i brev af 20. juni I meddelelse af 4. juli 2006 på Lægemiddelstyrelsens netsted orienterede Lægemiddelstyrelsen om, at vi forventede i løbet af efteråret 2006 at starte på at revurdere tilskudsstatus for 4 terapeutiske grupper i ATC-gruppe C, heriblandt C01. drøftede tilskudsstatus for lægemidler i ATC-gruppe C01 første gang på møde den 19. september har efterfølgende drøftet tilskudsstatus for lægemidler i ATC-gruppe C01 på sine møder den 7. november 2006, den 28. august 2007 og den 24. maj s bemærkninger og begrundelser s drøftelser har taget udgangspunkt i de anbefalinger om lægemidlernes anvendelse, som kommer til udtryk i Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning, maj Kapitel 3, Stabil iskæmisk hjertesygdom. Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning, maj Kapitel 5. Kronisk venstresidig hjertesvigt. Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning maj Kapitel 15, Atrieflimren og atrieflagren. Institut for Rationel Farmakoterapi. National rekommandationsliste for C01D af den 24. februar Med undtagelse af virksomheder med markedsføringstilladelse til lægemidler med begrænset udlevering, naturlægemidler, stærke vitamin- og mineralpræparater og radioaktive lægemidler. 4
5 Nævnet har endvidere fået forelagt følgende publikationer: Lægemiddelstyrelsen. Nyt Om Bivirkninger. 21. februar Malling H-J et al. Anafylaksi. Ugeskr. Læger 2005;167: Til grund for nævnets anbefalinger ligger endvidere oplysninger fra Lægemiddelstyrelsens Lægemiddelstatistikregister om forbruget af lægemidlerne i den primære sundhedssektor for årene samt oplysninger om lægemidlernes priser, der fremgår af Bilag B. Ad 1. med indhold af digoxin (C01AA05) Digoxin er det eneste lægemiddelstof i C01A, hjerteglykosider. Digoxin anvendes til kontrol af supraventrikulære arytmier, hovedsageligt atrieflimren samt i behandlingen af hjerteinsufficiens og har den godkendte indikation Hjerteinsufficiens. Atrieflimren og atrieflagren med hurtig ventrikelaktion samt andre supraventrikulære takykardier (1). Digoxin kombineres ofte med andre stoffer i behandlingen af atrieflimren, da den frekvensregulerende virkning hovedsagelig er til stede ved hvile, men hos ældre relativt immobile patienter kan der ofte behandles alene med digoxin (2). Ved behandling af hjerteinsufficiens kan digoxin anvendes ved uacceptable symptomer på trods af anden behandling (3). Digoxin har et smalt terapeutisk indeks og dermed en risiko for overdosering (4). Antallet af patienter i behandling med digoxin har været svagt faldende gennem flere år i 2008 til i Prisen er lav - 0,82 kr. per tablet. finder, at digoxin har en veldefineret plads i terapien, trods det snævre terapeutiske indeks, og at lægemidler med indhold af digoxin opfylder kriterierne for fortsat at oppebære generelt tilskud. På denne baggrund indstiller, at lægemidler med indhold af digoxin bevarer generelt tilskud. Ad 2 og 3. med indhold af lidocain (C01BB01), propafenon (C01BC03), flecainid (C01BC04), amiodaron (C01BD01) og dronedaron (C01BD07) ne tilhører alle gruppen af antiarytmika, klasse I og III. Lidocain (C01BB01) er et klasse Ib antiarytmikum med indikationen Forebyggelse og behandling af ventrikulære takyarytmier. Ventrikulære ekstrasystoler og ventrikulær takykardi understøttende ved ventrikelflimren med øget pacemakeraktivitet. (1). Lidocain (med ATC-koden C01BB01) findes kun som infusionsvæske og har ikke været markedsført siden Lægemidlet anvendes i sygehusbehandling og har ikke været solgt i primærsektoren. I gruppen af klasse Ic antiarytmika findes lægemiddelstofferne propafenon (C01BC03) og flecainid (C01BC04). Propafenon har den godkendte indikation Forebyggelse og behandling af supraventrikulære og ventrikulære arytmier og findes som tabletter. Flecainid findes både som tabletter og injektionsvæske og har fx den godkendte indikation Symptomgivende supraventrikulære arytmier, hvor anden behandling har været ineffektiv. Livstruende ventrikulære arytmier (1). ne anvendes til konvertering af 5
6 atrieflimren af kort varighed samt til anfaldsforebyggende behandling, og Dansk Cardiologisk Selskab skelner i sine anbefalinger ikke mellem de 2 lægemiddelstoffer (2). Påbegyndelse af behandling med propafenon og flecainid kræver indlæggelse, men lægemidlerne kan ordineres i almen praksis. Injektionsformen af flecainid anvendes udelukkende til sygehusbehandling. Amiodaron (C01BD01) og dronedaron (C01BD07) er klasse III antiarytmika. Amiodaron har den godkendte indikation Forebyggelse og behandling af supraventrikulære og ventrikulære takyarytmier, hvor andre antiarytmika har utilstrækkelig effekt (1) og findes både som tabletter og til injektion. Amiodaron anvendes bl.a. til konverterende behandling af atrieflimren og som anfaldsforebyggende det er førstevalgspræparat ved samtidig hjertesvigt (2). Tabletterne har udleveringsbestemmelse NBS 5, og ordinationen er forbeholdt sygehuse og kardiologer. Amiodaron injektionsvæske har udleveringsbestemmelse A men anvendes i praksis udelukkende på sygehuse. Dronedaron har den godkendte indikation Voksne, klinisk stabile patienter med nuværende eller tidligere ikke-permanent atrieflimren (AF) for at forebygge tilbagefald af AF eller at nedsætte ventrikelaktionen (1). Dronedaron anvendes anfaldsforebyggende ved atrieflimren (2). Behandling med både propafenon, flecainid, amiodaron og dronedaron er behæftet med risiko for alvorlige bivirkninger. Risikoen for proarytmier er størst for propafenon og flecainid, hvilket er baggrunden for opstart under indlæggelse. Behandling med amiodaron giver bl.a. risiko for partikelaflejringer i øjne og påvirkning af thyroidea (4). For dronedaron er der rapporteret tilfælde af alvorlig leverskade (5). Forbruget i primærsektoren ligger udelukkende på de perorale former. Forbruget af propafenon i primærsektoren har været svagt faldende gennem de senere år, og i 2010 var personer i behandling. Antallet af patienter, som har indløst recept på flecainid har gennem årene været svagt stigende fra i 2008 til i De tilsvarende tal for antallet af patienter, som har indløst recept på amiodaron var og Dronedaron blev først markedsført i starten af 2010, og i 2010 indløste 810 personer recept på lægemidlet (6). Behandlingsprisen per døgn for de perorale former er 1,91-3,82 kr. for amiodaron, 3,10-4,96 kr. for propafenon, 5,66 kr. for flecainid og 26,68 kr. for dronedaron. Anvendelsen af propafenon og flecainid udenfor sygehusregi er begrænset, hvorimod amiodaron anvendes væsentligt mere. Anvendelsen af lægemidler med disse tre indholdsstoffer må antages at være rationel. finder, at lægemidler med indhold af propafenon, flecainid og amiodaron fortsat opfylder kriterierne for at oppebære generelt tilskud, og at de perorale lægemiddelformer af disse lægemidler fortsat bør have generelt tilskud. Dansk Cardiologisk Selskab ligestiller behandling med dronedaron og klasse Ic antiarytmika (propafenon og flecainid) til patienter med ingen eller minimal samtidig hjertesygdom (2). På denne baggrund samt på baggrund af den betydeligt højere behandlingspris for dronedaron sammenlignet med propafenon og flecainid finder ikke, at den behandlingsmæssige værdi af dronedaron står i et rimeligt forhold til prisen og indstiller, at dronedaron fortsat ikke bør have generelt, herunder generelt klausuleret, tilskud. For patienter der ikke kan behandles med klasse Ic antiarytmika fx pga. kontraindikationer, kan der som hidtil søges om enkelttilskud. 5 Må kun udleveres til sygehuse eller efter ordination af nærmere bestemte speciallæger. 6
7 Lidocain, flecainid og amiodaron til injektion eller infusion anvendes udelukkende i sygehusregi og bør efter s opfattelse af denne grund fortsat ikke have generelt tilskud. Ad 4. med indhold af dopamin (C01CA04) og dobutamin (C01CA07) Dopamin (C01CA04) og dobutamin (C01CA07) tilhører sammen med adrenalin gruppen af hjertestimulerende midler. Dopamin og dobutamin findes begge som koncentrat til infusionsvæske og er godkendt til henholdsvis kardiogent shock (dopamin) og hjertepumpesvigt og akut ophævelse eller mindskning af betablokkeres effekt (dobutamin) (1) og er derfor sygehusbehandling. På denne baggrund finder fortsat ikke, at lægemidler med indhold af disse lægemiddelstoffer bør have generelt tilskud. Ad 5 og 6. med indhold af adrenalin (C01CA24) Adrenalin injektionsvæske (C01CA24) findes i to former. Injektionsvæske 1 mg/ml findes som almindelige ampuller og er godkendt til Asthma bronchiale og anden bronkospasme. Anafylaktisk shock. Hjertestimulering (1). Det anvendes primært til sygehusbehandling eller til brug i praksis, hvor det anvendes akut. Adrenalin injektionsvæske er optaget på regionernes positivlister og kan uden betaling rekvireres af læger til brug i praksis. Adrenalin injektionsvæske i styrkerne 0,3 mg/dosis og 0,15 mg/dosis til autoinjektion er indiceret til akut behandling af alvorligt anafylaktisk shock eller allergisk reaktion overfor allergener fx insektstik eller -bid, fødevarer eller lægemidler (1). Autoinjektoren er designet til nemt at kunne anvendes af patienten selv og skal betragtes som førstehjælp. Patienter med anafylaksi udløst af fødevarer, ubehandlet insektallergi, fysisk anstrengelse eller idiopatisk udløst bør udstyres med adrenalin til selvinjektion (7). Tal fra Lægemiddelstatistikregistret viser, at der i primærsektoren i 2009 var 6506 personer i behandling med adrenalin som autoinjektor og 384 personer med injektionsvæsken som ampuller. For 2010 var tallene 7009 personer og 423 personer (6). Prisen for autoinjektoren er 442,98 kr. for en dosis. finder, at lægemidler med adrenalin til autoinjektion opfylder kriterierne for fortsat at oppebære generelt tilskud. Der er tale om livsvigtig behandling, som der ikke findes noget alternativ til. Adrenalin, injektionsvæske i lægemiddelformen ampuller anvendes i sygehusbehandling og til brug i praksis, herunder i vagtlægetjeneste. Nævnet finder ikke denne lægemiddelform velegnet til at blive administreret af patienten selv og har ingen eksempler på anvendelse ved salg til enkeltpersoner. På denne baggrund finder nævnet ikke, at lægemidlet opfylder kriterierne for at oppebære generelt tilskud og indstiller derfor, at det generelle tilskud bortfalder. Ad 7, 8 og 9. med indhold af glycerylnitrat (C01DA02), isosorbiddinitrat (C01DA08), isosorbidmononitrat (C01DA14) og nicorandil (C01DX16) Midler mod angina pectoris (hjertekrampe) (C01D) består af nitraterne glycerylnitrat, isosorbiddinitrat og isosorbidmononitrat samt af nicorandil. 7
8 Nitraterne anvendes overvejende til akut og anfaldsprofylaktisk behandling af angina pectoris. De opdeles i de akut virkende og de profylaktisk virkende. Der udvikles hurtigt tolerance overfor nitraterne (efter ca. 24 timer). Derfor bør der være en nitratfri periode på minimum 10 timer indenfor et døgn. Konsekvenser heraf er, at der ikke opnås en døgndækkende behandling, og nitraterne kan derfor ikke anvendes som monoterapi til forebyggelse af anfald af angina pectoris (4,8). Glycerylnitrat (C01DA02) er det eneste nitrat, der kan anvendes til akut behandling. Det findes i de hurtigtvirkende former sublinguale resoribletter og sublingualspray med indikationen Angina pectoris, men også i depotformuleringer som depotresoribletter med indikationen Forebyggelse af angina pectoris. Hjerteinsufficiens, der ikke kan behandles med anden terapi og som depotplastre med indikationen Forebyggelse af angina pectoris. For depotplastre i styrken 5mg/24 timer endvidere med tilføjelsen Forebyggelse af flebit og ekstravasal infusion ved i.v. infusion (1). De hurtigvirkende former har en hurtig indsættende effekt og anvendes ved akut angina pectoris (4). Depotresoribletterne skal opbevares i mundhulen i 3-5 timer. Depotplastrene virker potentielt i 24 timer og skal derfor fjernes efter timer for at undgå toleranceudvikling (8). Isosorbiddinitrat (C01DA08) findes som tabletter og depottabletter og er godkendt til Forebyggelse af angina pectoris og for tabletternes vedkommende også til Hjerteinsufficiens, hvor digoxin og diuretika ikke har tilstrækkelig effekt. Depottabletterne doseres 1, evt. 2, gange dagligt og tabletterne 3 gange dagligt med 12 timer mellem sidste dosis og næste dags første dosis (1,4). Isosorbidmononitrat (C01DA14) findes som depottabletter og depotkapsler og er godkendt til Forebyggelse af angina pectoris. ne kan doseres en gang dagligt (1). Nicorandil (C01DX16) findes som tabletter og er godkendt til forebyggelse af angina pectoris (1). I modsætning til nitraterne er der ikke problemer med toleranceudvikling, og det kan derfor anvendes både som monoterapi og i kombination med andre lægemidler (4). Dansk Cardiologisk Selskab anfører at virkningen er omdiskuteret og omtaler nicorandil som en alternativ mulighed (9). I 2010 var personer i behandling med de hurtigvirkende former af glycerylnitrat og 136 personer med depotplastrene. Forbruget har for begge former været let faldende de seneste år. Depotresoribletterne har ikke været markedsført siden Ca personer var i 2010 i behandling med isosorbidmononitrat. For isosorbiddinitrat fordeler forbruget sig med godt i behandling med depottabletter og ca med tabletter. Forbruget af isosorbiddinitrat er faldet over en årrække. I 2010 var ca personer i behandling med nicorandil (6). Behandlingspriserne for de langtidsvirkende nitrater/depotformuleringer ligger på 1,18 8,32 kr. per døgn. Isosorbidmononitrat depottabletter er billigst, mens glycerylnitrat depotplaster og isosorbiddinitrat tabletter er de dyreste. Behandlingsprisen for nicorandil er 4,90-10,52 kr. For de hurtigvirkende former af glycerylnitrat er der tale om veldokumenterede lægemidler med en hurtigt indsættende effekt, hvilket er vigtigt ved behandling af akut angina pectoris. Nævnet vurderer, at lægemidlernes pris står i et rimeligt forhold til den behandlingsmæssige værdi ved behandling af angina pectoris. Glycerylnitrat i form af depotresoribletter skal opbevares i mundhulen i 3-5 timer og rekommanderes ikke af IRF (8). finder ikke, at dette er en hensigtsmæssig formulering, og når glycerylnitrat i form af depotresoribletter stilles over for andre depotformuleringer af nitrater finder nævnet, at pri- 8
9 sen ikke står i et rimeligt forhold til den behandlingsmæssige værdi. indstiller derfor, at det generelt klausulerede tilskud til disse lægemidler bortfalder. Glycerylnitrat i form af depotplaster er ikke en hensigtsmæssig formulering til forebyggelse af angina pectoris, da der er risiko for at glemme de minimum 8 timers nitroglycerinpause dagligt. Plastrene virker i 24 timer, og det er derfor vigtigt at huske at skifte dem. Denne formulering er heller ikke rekommanderet af IRF (8). Nævnet finder, at der kan være enkelte patienter, fx patienter der ikke kan synke depottabletter, hvor depotplastrene kan være den bedste behandlingsmulighed og indstiller med henvisning hertil samt til det meget begrænsede forbrug, at disse lægemidler bevarer det generelt klausulerede tilskud. Isosorbidmononitrat og isosorbiddinitrat i depotformulering skal doseres en (evt. to for isosorbiddinitrat) gang daglig, og ved denne dosering er der ikke problemer med toleranceudvikling. Nævnet finder derfor, at disse lægemidler bør være førstevalg ved behov for forebyggende behandling af angina pectoris med nitrater, og at lægemidlerne opfylder kriterierne for at oppebære generelt tilskud. Isosorbiddinitrat tabletter skal doseres 3 gange dagligt, hvilket ikke er hensigtsmæssigt for en profylaktisk behandling. Samtidig er der risiko for toleranceudvikling, hvis pausen på 12 timer ikke overholdes. Når behandling med tabletter således stilles overfor behandling med depottabletter finder nævnet ikke, at lægemidlerne opfylder kriterierne for at oppebære generelt tilskud og indstiller på denne baggrund, at det generelt klausulerede tilskud bortfalder. Nicorandil har en anden virkningsmekanisme end nitraterne og nævnet bemærker, at Dansk Cardiologisk Selskab anfører, at virkningen er omdiskuteret. Nævnet finder dog, at lægemidlerne har sin egen plads i behandlingen af enkelte patienter og indstiller med henvisning til det begrænsede forbrug, at lægemidler med indhold af nicorandil bevarer generelt tilskud. Ad 10. Samtlige lægemidler med indhold af adenosin (C01EB10) og ivabradin (C01EB17) Ovennævnte er de eneste lægemiddelstoffer i gruppen af Andre midler til hjerteterapi (C01E), som kan sælges i primærsektoren. Adenosin (C01EB10) findes som injektions- og infusionsvæske og er godkendt til afbrydelse af paroksystisk supraventrikulær takykardi, hvori atrio-ventrikulærknuden er en integreret del af impulskarrusellen (nodal takykardi og WPW-takykardi med accessorisk ledningsbane) (1). Lægemidlet anvendes til sygehusbehandling og bør derfor efter s opfattelse fortsat ikke have generelt tilskud. Ivabradin (C01EB17) har den godkendte indikation Symptomatisk behandling af kronisk stabil angina pectoris hos voksne med koronararteriesygdom og normal sinusrytme. Ivabradin er indiceret dels til voksne, som ikke tåler betablokkere eller for hvem betablokkere er kontraindiceret, dels i kombination med betablokkere til patienter, som ikke opnår tilstrækkelig kontrol med optimal dosering af en betablokker, og hvis hjertefrekvens er > 60 slag i minuttet. (1). Betablokkere er førstevalg til anfaldsprofylakse ved angina pectoris. Ved kontraindikation, intolerans eller utilstrækkelig effekt kan primært anvendes nitrater, calciumantagonister eller ivabradin. Ivabradin kan anvendes ved sinusrytme og frekvens > 60 slag i minuttet (9). 9
10 Antallet af personer, der har indløst recept på ivabradin er steget fra 211 i 2008 til 413 i 2010 (6). Behandlingsprisen per døgn er 22,16 kr. Behandlingsprisen for calciumantagonister ligger i intervallet 0,48-16,56 kr. per døgn. finder ikke, at den behandlingsmæssige værdi af ivabradin står i et rimeligt forhold til den behandlingsmæssige værdi, når ivabradin stilles overfor anden 2. valgsbehandling af angina pectoris, fx calciumantagonister. Behandlingsprisen for calciumantagonister er væsentlig lavere end behandlingsprisen for ivabradin, og der er ikke dokumentation for en bedre effekt af ivabradin. indstiller derfor fortsat, at ivabradin ikke bør have generelt, herunder generelt klausuleret, tilskud. For patienter, der ikke kan behandles med billigere 2. valgsbehandling af angina pectoris fx calciumantagonister, kan der som hidtil søges om enkelttilskud. På nævnets vegne Mogens Laue Friis Formand Referencer: 1. Lægemiddelstyrelsen. Produktresumeer for de enkelte lægemidler Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning maj Kapitel 15, Atrieflimren og atrieflagren. atrieflimren-og-atrieflagren&catid=5# Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning, maj Kapitel 5. Kronisk venstresidig hjertesvigt. kronisk-systolisk-ve-hjertesvigt&catid=5 4. Dansk Lægemiddel Information A/S. pro.medicin.dk Lægemiddelstyrelsen. Nyt Om Bivirkninger. 21. februar Lægemiddelstyrelsens Lægemiddelstatistikregister Malling H-J et al. Anafylaksi. Ugeskr. Læger 2005;167: Institut for Rationel Farmakoterapi. National rekomandationsliste for C01D af den 24. februar api.htm 9. Dansk Cardiologisk Selskab. NBV11 - Den Nationale Kardiologiske Behandlingsvejledning, maj Kapitel 3, Stabil iskæmisk hjertesygdom. stabil-angina-pectoris&catid=5. 10
11 Bilag: A. Grafisk oversigt over ATC-gruppe C01, hjerteterapi. B. Oversigt over lægemiddelstofferne med angivelse af hvilke indikationer, lægemidler med indhold af det pågældende lægemiddelstof er godkendt til, lægemiddelnavne, lægemiddelformer, udleveringsgruppe, gældende tilskudsstatus, behandllingspris, årligt forbrug og oplysninger om enkelttilskud. 11
12 C01 Hjerteterapi Bilag A 29. juni 2011 C01A Hjerteglykosider C01B Anti-arytmika, klasse I og III C01C Hjertestim. midler excl. hjerteglycosid. C01D Vasodil. anvendt ved hjertesygdomme C01E Andre midler til hjerteterapi C01AA C01BB Anti-arytmika, klasse I b C01BC Antiarytmika, klasse I c C01BD Anti-arhytmika, klasse III C01BG Andre antiarhytmika, klasse I og III C01CA Adrenerge og dopaminerge midler C01DA Organiske nitrater C01DX Andre vasodil. anvendt ved hjertesygdom C01EA Digitalisglykosider Prostaglandiner C01EB Andre hjertemidler C01AA05 Digoxin C01BB01 Lidocain C01BG11 Vernakalant C01DA02 Glycerylnitrat C01DA08 Isosorbiddinitrat C01DA14 Isosorbidmononitrat C01EA01 Alprostadil C01BD01 Amiodaron C01BD07 Dronedaron C01DX16 Nicorandil C01BC03 Propafenon C01BC04 Flecainid C01CA04 Dopamin C01CA07 Dobutamin C01CA24 Adrenalin C01EB10 Adenosin C01EB15 Trimetazidin C01EB16 Ibuoprofen C01EB17 Ivabradin C01EB19 Icatibant
13 Bilag B 29. juni 2011 Oversigt over lægemidler i ATC-gruppe C01, Hjerteterapi Læsevejledning til skemaer nedenfor : Det eller de lægemidler, med indhold af indholdsstoffet eller indholdsstofferne, der er omfattet af denne revurdering af tilskudsstatus for lægemidler i ATC-gruppe C01, hjerteterapi Revurderingen omfatter alle styrker og pakningsstørrelser af det enkelte lægemiddel, som er eller har været markedsført per den 16. maj : En sammenskrivning af den eller de angivne indikationer for lægemidler med indhold af det pågældende lægemiddelstof og lægemiddelform/administrationsvej, jf. de gældende produktresumeer for de enkelte lægemidler 1. : Beskrivelse af betydningen af de forskellige udleveringsgrupper A, B etc. fremgår af 64 i bekendtgørelse om recepter nr. 155 af den 20. februar : Lægemidlets gældende tilskudsstatus. Behandlingspris per døgn: De angivne behandlingspriser per døgn er baseret på de gennemsnitligt laveste enhedspriser (for tilskudsberettigede lægemidler: tilskudspriser) og beregnet i overensstemmelse med Lægemiddelstyrelsens retningslinjer af 4. juli 2006 for vurdering og sammenligning af lægemidler ved revurdering af lægemidlers tilskudsstatus 3. Den anvendte periode er de 6 prisperioder med første periodestart den 24. januar 2011 og sidste periodestart den 4. april Enkelte lægemidler i gruppen har udleveringsstatus HF og er derfor ikke begrænset til salg fra apotek. Priserne fastsættes lokalt af salgsstedet, og virksomhederne har ikke pligt til at indberette en pris for disse lægemidler til Lægemiddelstyrelsen. De behandlingspriser, som nedenfor er indsat for lægemidler med udleveringsstatus HF, er beregnet på baggrund af de priser, som apotekerne har indberettet til Lægemiddelstyrelsens Lægemiddelstatistikregister for perioden den 8. november 2010 til den 30. januar 2011 for den del, der er solgt på recept. Lidocain udgik af handlen den 24. marts 2008 og glycerylnitrat, depotresoribletter udgik af handlen i efteråret 2005 og der er derfor ikke angivet behandlingspriser for disse lægemidler. * angiver, at behandlingsprisen er per dosis og ikke per døgn. Disse lægemidler anvendes efter behov eller i individuel dosering. Forbrug: Antallet af personer i behandling er fra Lægemiddelstyrelsens Lægemiddelstatistikregister, jf. og omfatter primærsektoren. ** angiver, at tallet omfatter alle lægemiddelformer og administrationsveje for det pågældende stof. Enkelttilskud: Oplysninger om antallet af ansøgninger om enkelttilskud og bevillingsprocent for lægemidler uden generelt tilskud. Antallet er kun anført for ivabradin (C01EB17) og dronedaron (C01BD07), da der ikke har været ansøgninger om enkelttilskud for nogle af de øvrige lægemidler. 1 Lægemiddelstyrelsen. Produktresuméer for de enkelte lægemidler full&q=recepter&activesolution=http%3a%2f%2fdatabases.tarius.com 3 1
14 Bilag B 29. juni 2011 C01A, Hjerteglykosider C01AA05 Digoxin Digoxin DAK tabletter Hjerteinsufficiens. Atrieflimren og atrieflagren med hurtig ventrikelaktion samt andre supraventrikulære takykardier. B Generelt tilskud 0,82 kr./0,25 mg Behandlingspris per døgn* Forbrug personer i behandling i personer i behandling i personer i behandling i 2010 C01B, Anti-arytmika, klasse I og III C01BB01 Lidokain Lidokain SAD infusionsvæske, opløsning (udgået 24. marts 2008) Forebyggelse og behandling af ventrikulære takyarytmier. Ventrikulære ekstrasystoler og ventrikulær takykardi understøttende ved ventrikelflimren med øget pacemakeraktivitet. B Ikke tilskud Behandlingspris per døgn Ikke markedsført siden Forbrug Ikke markedsført siden Intet salg til enkeltpersoner. C01BC03 Propafenon Rytmonorm filmovertrukne tabletter Forebyggelse og behandling af supraventrikulære og ventrikulære arytmier. B Generelt tilskud Behandlingspris per døgn 3,10-4,96 kr. Forbrug personer i behandling i personer i behandling i personer i behandling i 2010 C01BC04 Flecainid (peroral) Flecainid Actavis tabletter Flecainid Stada tabletter Tambocor tabletter Symptomgivende supraventrikulære arytmier, hvor anden behandling har været ineffektiv. Livstruende ventrikulære arytmier. 2
15 Bilag B 29. juni 2011 Eller: Behandling af A-V nodal takykardi og arytmier i forbindelse med Wolff-Parkinson-White s syndrom samt lignende tilstande i de accessoriske ledningsveje, når anden behandling har været utilstrækkelig. Behandling af svær symptomatisk og livstruende paroksystisk ventrikulær arytmi, hvor anden behandling er ineffektiv eller ikke tolereres. Behandling af paroksystiske arytmier i atriet (atrieflimren, atrieflagren og atrietakykardi) hos patienter med invaliderende symptomer efter konvertering, forudsat at der er et udtalt behov for behandling udfra de kliniske symptomers sværhedsgrad og anden behandling har været ineffektiv. Sygdom, der skyldes hjertets fysiske tilstand og/eller nedsat funktion af venstre ventrikel bør udelukkes på grund af øget risiko for proarytmisk effekt. B Generelt tilskud Behandlingspris per døgn 5,66 kr. Forbrug** personer i behandling i personer i behandling i personer i behandling i 2010 C01BC04 Flecainid (til injektion) Tambocor injektionsvæske Symptomgivende supraventrikulære arytmier, hvor anden behandling har været ineffektiv. Livstruende ventrikulære arytmier. B Ikke tilskud 5,48 kr./ml Behandlingspris per døgn* Forbrug** personer i behandling i personer i behandling i personer i behandling i 2010 C01BD01 Amiodaron (peroral) Cordan tabletter Cordarone tabletter Forebyggelse og behandling af supraventrikulære og ventrikulære takyarytmier, hvor andre antiarytmika har utilstrækkelig effekt. NBS (kardiologi) Generelt tilskud Behandlingspris per døgn 1,91-3,82 kr. Forbrug** personer i behandling i personer i behandling i personer i behandling i
16 Bilag B 29. juni 2011 C01BD01 Amiodaron (til injektion) Cordarone injektionsvæske, opløsning Amiodaron Stragen koncentrat til injektions- og infusionsvæske, opløsning Angoron injektionsvæske, opløsning Forebyggelse og behandling af supraventrikulære og ventrikulære takyarytmier, hvor andre antiarytmika har utilstrækkelig effekt. A Ikke tilskud Behandlingspris per døgn* 13,35 kr./ml Forbrug** personer i behandling i personer i behandling i personer i behandling i 2010 C01BD07 Dronedaron Multaq filmovertrukne tabletter Voksne, klinisk stabile patienter med nuværende eller tidligere ikkepermanent atrieflimren (AF) for at forebygge tilbagefald af AF eller at nedsætte ventrikelaktionen. B Ikke tilskud Behandlingspris per døgn 26,68 kr. Forbrug 810 personer i behandling i Markedsført i starten af Ansøgninger om 766 (77 pct.) i 2010 enkelttilskud (andel bevilget) C01C, Hjertestimulerende midler ekskl. hjerteglykosider C01CA04 Behandlingspris per døgn* Forbrug Dopamin Dopmin koncentrat til infusionsvæske, opløsning Kardiogent shock. A Ikke tilskud 6,07 kr./ml Intet salg til enkeltpersoner C01CA07 Dobutamin Dobutrex koncentrat til infusionsvæske opløsning Hjertepumpesvigt. Akut ophævelse eller mindskning af betablokkeres effekt. B Ikke tilskud 4
17 Bilag B 29. juni 2011 Behandlingspris per døgn* Forbrug 3,91 kr./ml Intet slag til enkeltpersoner C01CA24 Adrenalin (ampuller) Adrenalin DAK injektionsvæske, opløsning Asthma bronchiale og anden bronkospasme. Anafylaktisk shock. Hjertestimulering. B Generelt tilskud 17,82 kr./ml Behandlingspris per døgn* Forbrug 384 personer i behandling i personer i behandling i 2010 C01CA24 Adrenalin (til autoinjektion) Epipen injektionsvæske, opløsning Epipen Jr. injektionsvæske, opløsning. Autoinjektorerne er indiceret til akut behandling af alvorligt anafylaktisk shock eller allergisk reaktion overfor allergener f. eks insektstik eller -bid, fødevarer eller lægemidler. B Generelt tilskud Behandlingspris per døgn* 442,98 kr. Forbrug personer i behandling i personer i behandling i 2010 C01D, Vasodilatorer anvendt ved hjertesygdomme C01DA02 Behandlingspris per døgn* Forbrug (Antal personer i receptordineret behandling) Glycerylnitrat (hurtigtvirkende) Glytrin sublingualspray Nitroglycerin DAK resoribletter, sublinguale Nitrolingual sublingualspray Behandling af akut angina pectoris. Forebyggelse af inducérbar angina (f.eks. fysisk anstrengelse, følelsesmæssig stress, udsættelse for kulde). HF Generelt klausuleret tilskud Klausuleret til pensionister og personer med angina pectoris. Sublingualspray: 0,51 kr. Resoribletter: 0,84 kr personer i behandling i personer i behandling i
18 Bilag B 29. juni 2011 C01DA02 Glycerylnitrat (depotpræparater) Suscard depotresoribletter Discotrine depotplastre Depotresoribletter: Forebyggelse af angina pectoris. Hjerteinsufficiens, der ikke kan behandles med anden terapi. Depotplaster 5 mg/24 timer: Forebyggelse af angina pectoris. Forebyggelse af flebit og ekstravasal infusion ved i.v. infusion. Behandlingspris per døgn Forbrug (Antal personer i receptordineret behandling) Depotplaster 10 mg/24 timer og 15 mg/24 timer: Forebyggelse af angina pectoris. HA Generelt klausuleret tilskud Klausuleret til pensionister og personer med angina pectoris. Depotplastre: 5,72-8,18 kr. Depotresoribletter har ikke været markedsført siden personer i behandling i personer i behandling i 2010 Depotresoribletter har ikke været markedsført siden 2005 C01DA08 Behandlingspris per døgn Forbrug (Antal personer i receptordineret behandling) Isosorbiddinitrat Cardopax tabletter Cardopax Retard depottabletter. Tabletter: Forebyggelse af angina pectoris. Hjerteinsufficiens, hvor digoxin og diuretika ikke har tilstrækkelig effekt. Depottabletter: Forebyggelse af angina pectoris. HA Generelt klausuleret tilskud Klausuleret til pensionister og personer med angina pectoris. Tabletter: 4,16-8,32 kr. Depottabletter: 3,30-6,60 kr. Tabletter: personer i behandling i personer i behandling i 2010 Depottabletter: personer i behandling i personer i behandling i 2010 C01DA14 Isosorbidmononitrat 6
19 Bilag B 29. juni 2011 Behandlingspris per døgn Forbrug (Antal personer i receptordineret behandling) Fem-Mono Retard depottabletter Imdur depottabletter Isodur depottabletter Isodur depotkapsler, hårde Isosorbidmononitrat Alternova depottabletter Forebyggelse af angina pectoris. HA Generelt klausuleret tilskud Klausuleret til pensionister og personer med angina pectoris. Depottabletter: 1,18-2,36 kr. Depotkapsler: 3,00-6,00 kr personer i behandling i personer i behandling i 2010 C01DX16 Nicorandil Angicor tabletter Dancor tabletter Ikorel tabletter Forebyggelse af angina pectoris. B Generelt tilskud Behandlingspris per døgn 4,90-10,52 kr. Forbrug personer i behandling i personer i behandling i 2010 C01E, Andre midler til hjerteterapi C01EB10 Adenosin Adenocor injektionsvæske, opløsning Adenosin Life Medical injektions-/infusionsvæske. Injektions-/infusionsvæske.: Afbrydelse af paroksystisk supraventrikulær takykardi, der involverer atri ventrikulærknuden (AV-knuden). Induktion af kortvarigt AV-blok til påvisning og lokalisering af accessoriske ledningsbanermed præexcitation. Behandlingspris per døgn* Forbrug Farmakologisk provokation af iskæmi i hjertet i forbindelse med myokardiescintigrafi (thallium eller Technetium) eller med ekkokardiografi, hvor andre stoffer til farmakologisk belastning ikke kan anvendes. B Ikke tilskud 14,55-34,26 kr./ml Intet salg til enkeltpersoner 7
20 Bilag B 29. juni 2011 C01EB17 Ivabradin Lægemiddelformer Procoralan filmovertrukne tabletter Symptomatisk behandling af kronisk stabil angina pectoris hos voksne med koronararteriesygdom og normal sinusrytme. Ivabradin er indiceret: - til voksne, som ikke tåler betablokkere eller for hvem betablokkere er kontraindiceret - i kombination med betablokkere til patienter, som ikke opnår tilstrækkelig kontrol med optimal dosering af en betablokker, og hvis hjertefrekvens er > 60 slag i minuttet. B Ikke tilskud 22,16 kr. Behandlingspris per døgn Forbrug 211 personer i behandling i personer i behandling i personer i behandling i 2010 Ansøgninger om enkelttilskud (andel bevilget) 2008: 139 (97 pct.) 2009: 109 (99 pct.) 2010: 186 (84 pct.) 8
MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE 1 2300 KØBENHAVN S Tlf. 44 88 95 95
 MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE 1 2300 KØBENHAVN S Tlf. 44 88 95 95 Til Medicintilskudsnævnets medlemmer. Den 7. september 2006 Hermed indkaldes til møde i Medicintilskudsnævnet om
MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE 1 2300 KØBENHAVN S Tlf. 44 88 95 95 Til Medicintilskudsnævnets medlemmer. Den 7. september 2006 Hermed indkaldes til møde i Medicintilskudsnævnet om
C08 Calciumantagonister
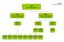 C08 Calciumantagonister Bilag A4 C08C Selektive calciumantagonister m. overv. vaskulær effekt C08D Selektive calciumantagonister m. direkte cardiel effekt C08CA Dihydropyridinderivater C08DA Phenylalkylaminderivater
C08 Calciumantagonister Bilag A4 C08C Selektive calciumantagonister m. overv. vaskulær effekt C08D Selektive calciumantagonister m. direkte cardiel effekt C08CA Dihydropyridinderivater C08DA Phenylalkylaminderivater
Revurdering af tilskudsstatus for lægemidler mod demens
 Den 4. november 2015 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at revurdere tilskudsstatus for lægemidler
Den 4. november 2015 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at revurdere tilskudsstatus for lægemidler
Revurdering af tilskudsstatus for lægemidler mod demens
 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 14. april 2016 Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at
Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 14. april 2016 Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at
Medicintilskudsnævnet
 30. maj 2012 Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Sundhedsstyrelsen har
30. maj 2012 Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Sundhedsstyrelsen har
C02 Antihypertensiva
 C02 Antihypertensiva Bilag A1 C02A Antiadrenerge midler, centralt virkende C02C Antiadrenerge midler, perifert virkende C02K Andre antihypertensiva C02AB C02AC Imidazolin-receptor Agonister C02CA Alfa-adrenoceptor
C02 Antihypertensiva Bilag A1 C02A Antiadrenerge midler, centralt virkende C02C Antiadrenerge midler, perifert virkende C02K Andre antihypertensiva C02AB C02AC Imidazolin-receptor Agonister C02CA Alfa-adrenoceptor
Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA
 Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A04 og A03FA
Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A04 og A03FA
C07. Beta-blokerende midler, Beta-blokerende midler, C07CB Beta-blokkere, selektive, og andre diuretica. C07BB Beta-blokkere, selektive, og thiazider
 C07 Beta-blokerende midler Bilag A3 C07A Beta-blokerende midler, usammensatte C07B Beta-blokerende midler og thiazider C07C Beta-blokkere og andre diuretica C07F Beta-blokkere og andre antihypertensiva
C07 Beta-blokerende midler Bilag A3 C07A Beta-blokerende midler, usammensatte C07B Beta-blokerende midler og thiazider C07C Beta-blokkere og andre diuretica C07F Beta-blokkere og andre antihypertensiva
Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud
 22. marts 2019 Sagsnr. : 2019032928 T +45 44889386 E mss@dkma.dk Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud Vi har vurderet tilskudsstatus for kapsler og depotplastre med indhold
22. marts 2019 Sagsnr. : 2019032928 T +45 44889386 E mss@dkma.dk Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud Vi har vurderet tilskudsstatus for kapsler og depotplastre med indhold
MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE KØBENHAVN S Tlf
 MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE 1 2300 KØBENHAVN S Tlf. 44 88 95 95 Til Medicintilskudsnævnets medlemmer. Den 26. oktober 2006 Hermed indkaldes til møde i Medicintilskudsnævnet om
MEDICINTILSKUDSNÆVNET SEKRETARIATET AXEL HEIDES GADE 1 2300 KØBENHAVN S Tlf. 44 88 95 95 Til Medicintilskudsnævnets medlemmer. Den 26. oktober 2006 Hermed indkaldes til møde i Medicintilskudsnævnet om
Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
 Medicintilskudsnævnet Den 4. november 205 Sagsnr: 20505674 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed Baggrund Sundhedsstyrelsen
Medicintilskudsnævnet Den 4. november 205 Sagsnr: 20505674 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed Baggrund Sundhedsstyrelsen
Medicintilskudsnævnet
 Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen i ATC-gruppe A01 og A07AA02 Baggrund
Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen i ATC-gruppe A01 og A07AA02 Baggrund
Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A08, midler mod fedme, ekskl. diætmidler
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 14. april 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 14. april 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
Medicintilskudsnævnet
 Medicintilskudsnævnet Sagsnr: 2013111155 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A03, midler mod funktionelle gastrointestinale forstyrrelser Baggrund og indhold
Medicintilskudsnævnet Sagsnr: 2013111155 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A03, midler mod funktionelle gastrointestinale forstyrrelser Baggrund og indhold
Generelt tilskud til tabletter med indhold af rosuvastatin
 Til virksomheden 0. september 018 Sagsnr. 0180894 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af rosuvastatin Vi har revurderet tilskudsstatus for tabletter med indhold af rosuvastatin,
Til virksomheden 0. september 018 Sagsnr. 0180894 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af rosuvastatin Vi har revurderet tilskudsstatus for tabletter med indhold af rosuvastatin,
Generelt tilskud til flere lægemidler med indhold af angiotensin-ii antagonister
 Til virksomheder, der per 18. juni 2018 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe C09CA07, C09DA04 og C09DA07. 28. juni 2018 Sagsnr. 2018063702 T +45 4488
Til virksomheder, der per 18. juni 2018 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe C09CA07, C09DA04 og C09DA07. 28. juni 2018 Sagsnr. 2018063702 T +45 4488
Generelt tilskud til tabletter med indhold af ezetimib
 Til virksomheden 0. september 018 Sagsnr. 018089 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af ezetimib Vi har revurderet tilskudsstatus for tabletter med indhold af ezetimib,
Til virksomheden 0. september 018 Sagsnr. 018089 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af ezetimib Vi har revurderet tilskudsstatus for tabletter med indhold af ezetimib,
Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus
 Dato 9. november 2017 Sagsnr. 2017103730 PFR Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus Indledning Formålet med denne vejledning er at orientere om proceduren for den periodiske
Dato 9. november 2017 Sagsnr. 2017103730 PFR Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus Indledning Formålet med denne vejledning er at orientere om proceduren for den periodiske
ikke kan tolereres eller i helt særlige tilfælde efter lægens samlede kliniske vurdering af patientens tilstand ikke er hensigtsmæssig.
 Virksomhed Partshøring - Revurdering af tilskudsstatus for dihydropyridincalciumantagonister - ATC-gruppe C08CA Lægemiddelstyrelsen har foretaget vurdering af spørgsmålet om fremtidig tilskudsstatus for
Virksomhed Partshøring - Revurdering af tilskudsstatus for dihydropyridincalciumantagonister - ATC-gruppe C08CA Lægemiddelstyrelsen har foretaget vurdering af spørgsmålet om fremtidig tilskudsstatus for
Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus og er startet med at se på hypertensionsmidlerne.
 Dansk Hypertensionsselskab Fællessekretariatet Esplanaden 8C, 3. 1263 København K. Hypertensionsbehandling i Danmark 6. marts 2006 Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus
Dansk Hypertensionsselskab Fællessekretariatet Esplanaden 8C, 3. 1263 København K. Hypertensionsbehandling i Danmark 6. marts 2006 Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus
Vejledning til ansøgning om generelt tilskud. Lovgrundlag
 Vejledning til ansøgning om generelt tilskud Lovgrundlag Lægemiddelstyrelsen træffer i henhold til sundhedslovens 144, stk. 1-3, samt sundhedslovens 152, stk. 2 og 4, afgørelse om, hvorvidt Regionsrådet
Vejledning til ansøgning om generelt tilskud Lovgrundlag Lægemiddelstyrelsen træffer i henhold til sundhedslovens 144, stk. 1-3, samt sundhedslovens 152, stk. 2 og 4, afgørelse om, hvorvidt Regionsrådet
Medicintilskudsnævnet
 23. december 2011 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Baggrund og indhold
23. december 2011 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Baggrund og indhold
Patienter, hvor behandling med antipsykotisk lægemiddel med generelt tilskud
 Til virksomheder, der per 31. marts 2016 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe N05AX12 med indhold af aripiprazol som smeltetabletter 31. marts 2016 Sagsnr.
Til virksomheder, der per 31. marts 2016 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe N05AX12 med indhold af aripiprazol som smeltetabletter 31. marts 2016 Sagsnr.
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 357, tirsdag den 23. august 2011. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 23. august 2011. I mødet
Referat af Medicintilskudsnævnets møde nr. 357, tirsdag den 23. august 2011. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 23. august 2011. I mødet
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 15. juni 2009. Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 15. juni 2009. Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 7. september 2006 Axel Heides Gade 1 2300 København S Indstilling til tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 7. september 2006 Axel Heides Gade 1 2300 København S Indstilling til tilskudsstatus for
C09 Midler med virkning på renin-angiotensin systemet
 C09 Midler med virkning på renin-angiotensin systemet ilag A C09C Angiotensin-II antagonister C09D Angiotensin-II antagonister, kombinationer C09X Andre midler med virkning på renin-angiotensinsyst. C09CA
C09 Midler med virkning på renin-angiotensin systemet ilag A C09C Angiotensin-II antagonister C09D Angiotensin-II antagonister, kombinationer C09X Andre midler med virkning på renin-angiotensinsyst. C09CA
Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter
 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 20. december 2016 Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Baggrund Lægemiddelstyrelsen har anmodet om at revurdere
Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 20. december 2016 Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Baggrund Lægemiddelstyrelsen har anmodet om at revurdere
N02 Analgetika. N02A Opioider. N02AB Phenylpiperidinderivater. N02AF Morfinanderivater. N02AG Opioider i komb. med antispasmodika
 N02 Analgetika Bilag A N02A Opioider N02AA Naturlige opiumalkaloider N02AB Phenylpiperidinderivater N02AE Oripavinederivater N02AF Morfinanderivater N02AG Opioider i komb. med antispasmodika N02AX Andre
N02 Analgetika Bilag A N02A Opioider N02AA Naturlige opiumalkaloider N02AB Phenylpiperidinderivater N02AE Oripavinederivater N02AF Morfinanderivater N02AG Opioider i komb. med antispasmodika N02AX Andre
Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens
 Til virksomheden 15. juni 2018 Sagsnr. 2018051042 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens Vi har revurderet tilskudsstatus for
Til virksomheden 15. juni 2018 Sagsnr. 2018051042 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens Vi har revurderet tilskudsstatus for
Til virksomheden 21. juni 2016 Sagsnr Reference usk T E
 Til virksomheden 21. juni 2016 Sagsnr. 20160228 Reference usk T +4 4488930 E usk@dkma.dk Ændring af tilskudsklausul for duloxetin 30 og 60 mg Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Til virksomheden 21. juni 2016 Sagsnr. 20160228 Reference usk T +4 4488930 E usk@dkma.dk Ændring af tilskudsklausul for duloxetin 30 og 60 mg Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Sagsfremstilling Medicintilskudsnævnet har afgivet indstilling om lægemidlernes fremtidige tilskudsstatus den 26. januar 2015.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for NSAID er og lægemidler mod svage smerter i ATC-gruppe M01A (ekskl. glucosamin), M02A, N02BA, N02BB og N02BE Vi afslutter
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for NSAID er og lægemidler mod svage smerter i ATC-gruppe M01A (ekskl. glucosamin), M02A, N02BA, N02BB og N02BE Vi afslutter
Til virksomheden 1. november 2017 Sagsnr Reference usk T E
 Til virksomheden 1. november 2017 Sagsnr. 2017011413 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod migræne Vi har revurderet tilskudsstatus for lægemidler
Til virksomheden 1. november 2017 Sagsnr. 2017011413 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod migræne Vi har revurderet tilskudsstatus for lægemidler
Antallet af ansøgninger om generelt tilskud, som nævnet behandlede på de månedlige møder, fremgår af figur 1.
 Årsrapport fra Medicintilskudsnævnet 2010 Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Årsrapport fra Medicintilskudsnævnet 2010 Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske
 Til virksomheden 7. december 2018 Sagsnr. 2018092970 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Vi har revurderet tilskudsstatus
Til virksomheden 7. december 2018 Sagsnr. 2018092970 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Vi har revurderet tilskudsstatus
Til virksomheden 16. januar 2017 Sagsnr Reference usk T E
 Til virksomheden 16. januar 2017 Sagsnr. 2015122548 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Vi har revurderet tilskudsstatus for
Til virksomheden 16. januar 2017 Sagsnr. 2015122548 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Vi har revurderet tilskudsstatus for
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 378, tirsdag den 21. august 2012. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 21.august 2012. I mødet
Referat af Medicintilskudsnævnets møde nr. 378, tirsdag den 21. august 2012. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 21.august 2012. I mødet
Intern prøve farmakologi den 6. juni 2008 kl til Hold S07V
 den 6. juni 2008 kl. 9.00 til 11.00 Side 1 af 6 Case: En 58-årig kvinde indlægges på mistanke om akut blindtarmsbetændelse. Hun opereres samme aften og ordineres tablet morfin 10 mg p.n. mod postoperative
den 6. juni 2008 kl. 9.00 til 11.00 Side 1 af 6 Case: En 58-årig kvinde indlægges på mistanke om akut blindtarmsbetændelse. Hun opereres samme aften og ordineres tablet morfin 10 mg p.n. mod postoperative
Medicintilskudsnævnet
 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Den 0. september 208 Sagsnr.: 208080020 Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Baggrund Lægemiddelstyrelsen
Lægemiddelstyrelsen Axel Heides Gade 2300 København S Den 0. september 208 Sagsnr.: 208080020 Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Baggrund Lægemiddelstyrelsen
Til Medicintilskudsnævnets medlemmer Den 16. august Revurdering af lægemidlers tilskudsstatus
 Til Medicintilskudsnævnets medlemmer Den 16. august 2011 Hermed indkaldes til møde i Medicintilskudsnævnet om Revurdering af lægemidlers tilskudsstatus Mødet er nr. 358 og finder sted tirsdag den 23. august
Til Medicintilskudsnævnets medlemmer Den 16. august 2011 Hermed indkaldes til møde i Medicintilskudsnævnet om Revurdering af lægemidlers tilskudsstatus Mødet er nr. 358 og finder sted tirsdag den 23. august
Til virksomheden 5. oktober 2018 Sagsnr T E
 Til virksomheden 5. oktober 2018 Sagsnr. 2018080284 T +45 93518614 E dila@dkma.dk Afgørelse om fremtidig tilskudsstatus for lægemidler til behandling af symptomer ved overgangsalder Vi afslutter med denne
Til virksomheden 5. oktober 2018 Sagsnr. 2018080284 T +45 93518614 E dila@dkma.dk Afgørelse om fremtidig tilskudsstatus for lægemidler til behandling af symptomer ved overgangsalder Vi afslutter med denne
Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"7."Lægemiddelstyrelsens"afgørelse"april"2010" " " " Bilag"8."IRF" "skift"fra"a2a"til"ace" " " " "
 Sundheds- og Forebyggelsesudvalget 2013-14 SUU Alm.del Bilag 436 Offentligt Oversigt-over-bilag- " Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"2."Medicintilskudsnævnets"indstilling"januar"2008"
Sundheds- og Forebyggelsesudvalget 2013-14 SUU Alm.del Bilag 436 Offentligt Oversigt-over-bilag- " Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"2."Medicintilskudsnævnets"indstilling"januar"2008"
Medicintilskudsnævnet
 Referat af s møde nr. 480 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 27. februar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Palle Mark
Referat af s møde nr. 480 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 27. februar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Palle Mark
Revurdering af tilskudsstatus for lægemidler mod migræne
 Medicintilskudsnævnet Den 12. oktober 2016 2. forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet om at revurdere
Medicintilskudsnævnet Den 12. oktober 2016 2. forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet om at revurdere
Medicintilskudsnævnet
 Referat af s møde nr. 479 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 23. januar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Nina Bjarnason
Referat af s møde nr. 479 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 23. januar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Nina Bjarnason
Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG
 Til virksomheden 4. juli 2017 Sagsnr. 2015122546 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG Vi har revurderet tilskudsstatus
Til virksomheden 4. juli 2017 Sagsnr. 2015122546 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG Vi har revurderet tilskudsstatus
Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler
 Dato 9. november 2017 Sagsnr. 2017103730 UDKAST Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler Indledning Denne vejledning uddyber reglerne i sundhedslovens
Dato 9. november 2017 Sagsnr. 2017103730 UDKAST Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler Indledning Denne vejledning uddyber reglerne i sundhedslovens
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 1. september 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 1. september 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe
 Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe C10 16. marts 2007 Indledning Folketinget besluttede ved udgangen af 2004 1, at afgørelser om generelt tilskud til lægemidler skal
Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe C10 16. marts 2007 Indledning Folketinget besluttede ved udgangen af 2004 1, at afgørelser om generelt tilskud til lægemidler skal
Medicintilskud I MEDICINTILSKUDSSYSTEMET. Lægemiddelstyrelsen. Generelt om medicintilskud
 MEDICINTILSKUDSSYSTEMET 169 Medicintilskud I Lægemiddelstyrelsen Det danske medicintilskudssystem er bygget op af en række elementer, som tilsammen skal sørge for, at ingen patienter af økonomiske grunde
MEDICINTILSKUDSSYSTEMET 169 Medicintilskud I Lægemiddelstyrelsen Det danske medicintilskudssystem er bygget op af en række elementer, som tilsammen skal sørge for, at ingen patienter af økonomiske grunde
Medicintilskudsnævnet
 Referat af s møde nr. 481 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 20. marts 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Referat af s møde nr. 481 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 20. marts 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Nedenfor følger sagsfremstilling, lovgrundlag, afgørelse, begrundelse, klagevejledning samt information om ændringerne.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Her er oversigt over de af jeres virksomheds lægemidler, der er omfattet af afgørelsen. Afgørelsen følger på de næste sider.
 1. november 2017 Sagsnr. 2015030614 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod Parkinsons sygdom Vi har revurderet tilskudsstatus for lægemidler mod Parkinsons
1. november 2017 Sagsnr. 2015030614 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod Parkinsons sygdom Vi har revurderet tilskudsstatus for lægemidler mod Parkinsons
Medicintilskudsnævnet
 Referat af s møde nr. 482 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 24. april 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Referat af s møde nr. 482 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 24. april 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Medicintilskudsnævnet
 Medicintilskudsnævnet Den. juni 205 Sagsnr: 20505674 Sundhedsstyrelsen Axel Heides Gade 2300 København S Forslag til indstilling Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
Medicintilskudsnævnet Den. juni 205 Sagsnr: 20505674 Sundhedsstyrelsen Axel Heides Gade 2300 København S Forslag til indstilling Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
Medicintilskudsnævnet
 Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 29. januar 2008 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 29. januar 2008 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
Til Virksomheden. Revurdering af tilskudsstatus for lægemidler mod diabetes
 Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod diabetes Sundhedsstyrelsen har revurderet tilskudsstatus for lægemidler i ATCgruppe A10, der per 3. juni 2013 er godkendt til markedsføring
Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod diabetes Sundhedsstyrelsen har revurderet tilskudsstatus for lægemidler i ATCgruppe A10, der per 3. juni 2013 er godkendt til markedsføring
Medicintilskudsnævnet
 Den 22. februar 2019 Sagsnr: 2018113377 Partshøring over forslag om indstilling til Lægemiddelstyrelsen Revurdering af tilskudsstatus for lægemidler til behandling af urinsyregigt Vi er i gang med at revurdere
Den 22. februar 2019 Sagsnr: 2018113377 Partshøring over forslag om indstilling til Lægemiddelstyrelsen Revurdering af tilskudsstatus for lægemidler til behandling af urinsyregigt Vi er i gang med at revurdere
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml. glyceryltrinitrat
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
escitalopram, fluvoxamin Tricykliske antidepressiva: imipramin Fra den 5. marts 2012 kan patienten kun få tilskud til disse lægemidler,
 Til lægen Ændring af medicintilskud til glucosamin og visse lægemidler mod depression og angst Glucosamin Den 28. november 2011 bortfalder tilskuddet til glucosamin. Lægemidler mod depression og angst
Til lægen Ændring af medicintilskud til glucosamin og visse lægemidler mod depression og angst Glucosamin Den 28. november 2011 bortfalder tilskuddet til glucosamin. Lægemidler mod depression og angst
Medicintilskudsnævnet
 29. oktober 2013 Sagsnr: 2013034167 Forslag til indstilling Revurdering af tilskudsstatus for antipsykotiske lægemidler i ATC-gruppe N05A, N03AG01 og N03AX09 Baggrund og indhold Vi har revurderet tilskudsstatus
29. oktober 2013 Sagsnr: 2013034167 Forslag til indstilling Revurdering af tilskudsstatus for antipsykotiske lægemidler i ATC-gruppe N05A, N03AG01 og N03AX09 Baggrund og indhold Vi har revurderet tilskudsstatus
Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB
 Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB Vi har revurderet tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB, der per
Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB Vi har revurderet tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB, der per
Adrenalin, antihistamin, sprøjter, nåle og oversigt med doser til anafylaksi er på sygeplejekontoret hvor SCIT gives.
 SCIT instruks Udarbejdet April 2018 Revideres næste gang April 2021 Ansvarlig KNS/JHH Formål Behandle høfeber, pollen og insektallergi ved langsomt at øge immunsystemets tolerance overfor pollen, støv
SCIT instruks Udarbejdet April 2018 Revideres næste gang April 2021 Ansvarlig KNS/JHH Formål Behandle høfeber, pollen og insektallergi ved langsomt at øge immunsystemets tolerance overfor pollen, støv
Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler
 Sundheds- og Ældreministeriet Enhed: MEDINT Sagsbeh.: DEPRHH Koordineret med: Sagsnr.: 1807871 Dok. nr.: 716616 Dato: 22-10-2018 Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud
Sundheds- og Ældreministeriet Enhed: MEDINT Sagsbeh.: DEPRHH Koordineret med: Sagsnr.: 1807871 Dok. nr.: 716616 Dato: 22-10-2018 Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud
Dansk Cardiologisk Selskab
 Dansk Cardiologisk Selskab www.cardio.dk Kontrolniveau ved behandling med flecainid et holdningspapir fra Dansk Cardiologisk Selskab DCS holdningspapir 2015. Nr. 3 Kardiogent shock 1 DCS holdningspapir,
Dansk Cardiologisk Selskab www.cardio.dk Kontrolniveau ved behandling med flecainid et holdningspapir fra Dansk Cardiologisk Selskab DCS holdningspapir 2015. Nr. 3 Kardiogent shock 1 DCS holdningspapir,
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 442, tirsdag den 19. januar 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. januar 2016. I mødet
Referat af Medicintilskudsnævnets møde nr. 442, tirsdag den 19. januar 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. januar 2016. I mødet
Revurdering af tilskudsstatus for lægemidler mod migræne
 Medicintilskudsnævnet Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 10. januar 2017 Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet
Medicintilskudsnævnet Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 10. januar 2017 Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet
Bilag III. Ændringer til relevante afsnit i produktresuméet og indlægssedlen
 Bilag III Ændringer til relevante afsnit i produktresuméet og indlægssedlen Bemærk: Disse ændringer til relevante afsnit i produktresuméet og indlægssedlen er resultatet af referralproceduren. Præparatoplysningerne
Bilag III Ændringer til relevante afsnit i produktresuméet og indlægssedlen Bemærk: Disse ændringer til relevante afsnit i produktresuméet og indlægssedlen er resultatet af referralproceduren. Præparatoplysningerne
Intern prøve farmakologi den 27. januar 2009 kl. 9.00 til 11.00. Hold S07S
 den 27. januar 2009 kl. 9.00 til 11.00 Side 1 af 6 Case: En 58-årig mand henvender sig til egen læge på grund af anstrengelsesudløste smerter i brystet samt åndenød. Lægen ordinerer, på mistanke om angina
den 27. januar 2009 kl. 9.00 til 11.00 Side 1 af 6 Case: En 58-årig mand henvender sig til egen læge på grund af anstrengelsesudløste smerter i brystet samt åndenød. Lægen ordinerer, på mistanke om angina
Bekendtgørelse om behandlerfarmaceuters virksomhedsområde
 Styrelsen for Patientsikkerhed Bekendtgørelse om behandlerfarmaceuters virksomhedsområde I medfør af 70 e, stk. 8 og 9, i lov om autorisation af sundhedspersoner og om sundhedsfaglig virksomhed, jf. lovbekendtgørelse
Styrelsen for Patientsikkerhed Bekendtgørelse om behandlerfarmaceuters virksomhedsområde I medfør af 70 e, stk. 8 og 9, i lov om autorisation af sundhedspersoner og om sundhedsfaglig virksomhed, jf. lovbekendtgørelse
Til Virksomheden. Revurdering af tilskudsstatus for lægemidler med indhold af glucosamin
 Til Virksomheden Revurdering af tilskudsstatus for lægemidler med indhold af glucosamin Lægemiddelstyrelsen har revurderet tilskudsstatus for aktuelt godkendte lægemidler med indhold af glucosamin, der
Til Virksomheden Revurdering af tilskudsstatus for lægemidler med indhold af glucosamin Lægemiddelstyrelsen har revurderet tilskudsstatus for aktuelt godkendte lægemidler med indhold af glucosamin, der
Medicintilskudsnævnet
 Referat af s møde nr. 485 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 21. august 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John
Referat af s møde nr. 485 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 21. august 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John
Opgave 4: En patient skal have tablet Digoxin 0,250 mg dagligt: Tablet Digoxin findes i styrken 62,5 µg. Hvor mange tabletter skal patienten have?
 Opgave 1: a. 0,05 g = 0,05 g x 1000 mg/g = 50 mg b. 12 mg = 12 mg : 1000 mg/g = 0,012 g c. 75 µg = 75 µg : 1000 µg/mg = 0,075 mg d. 250 mg = 250 mg : 1000 mg/g = 0,25 g e. 8 % = 8% x 10 mg/ml/% = 80 mg/ml
Opgave 1: a. 0,05 g = 0,05 g x 1000 mg/g = 50 mg b. 12 mg = 12 mg : 1000 mg/g = 0,012 g c. 75 µg = 75 µg : 1000 µg/mg = 0,075 mg d. 250 mg = 250 mg : 1000 mg/g = 0,25 g e. 8 % = 8% x 10 mg/ml/% = 80 mg/ml
Medicintilskudsnævnet
 Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi har revurderet tilskudsstatus
Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi har revurderet tilskudsstatus
Medicintilskudsnævnet
 Den 21. august 2019 Sagsnr: 2019033133 FORSLAG Revurdering af tilskudsstatus for centralt virkende muskelrelaksantia (ATC-gruppe M03) Baggrund Lægemiddelstyrelsen har anmodet om at revurdere tilskudsstatus
Den 21. august 2019 Sagsnr: 2019033133 FORSLAG Revurdering af tilskudsstatus for centralt virkende muskelrelaksantia (ATC-gruppe M03) Baggrund Lægemiddelstyrelsen har anmodet om at revurdere tilskudsstatus
Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens
 Medicintilskudsnævnet Den 25. oktober 207 Sagsnr: 20700643 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens aggrund Lægemiddelstyrelsen har
Medicintilskudsnævnet Den 25. oktober 207 Sagsnr: 20700643 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens aggrund Lægemiddelstyrelsen har
Notat om midler mod Alzheimers sygdom i Danmark
 Notat om midler mod Alzheimers sygdom i Danmark En kortlægning af forbruget af demensmidler i perioden 1997-2003 9. oktober, 2003 Indhold Resumé Baggrund Datamateriale og metode Resultater Omsætning og
Notat om midler mod Alzheimers sygdom i Danmark En kortlægning af forbruget af demensmidler i perioden 1997-2003 9. oktober, 2003 Indhold Resumé Baggrund Datamateriale og metode Resultater Omsætning og
ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 MEDLEMMER UDPEGET AF MINISTEREN FOR SUNDHED OG FOREBYGGELSE 20 MØDER I 2014
 ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 Medicintilskudsnævnet rådgiver Sundhedsstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 Medicintilskudsnævnet rådgiver Sundhedsstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 354, tirsdag den 24. maj 2011. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 24. maj 2011. I mødet deltog:
Referat af Medicintilskudsnævnets møde nr. 354, tirsdag den 24. maj 2011. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 24. maj 2011. I mødet deltog:
Nedenfor følger sagsfremstilling, lovgrundlag, afgørelse, begrundelse, klagevejledning samt information om ændringerne.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A09- digestiva, inkl. enzymer, A11-vitaminer, A12- mineralpræparater og A16 - andre midler
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A09- digestiva, inkl. enzymer, A11-vitaminer, A12- mineralpræparater og A16 - andre midler
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 434, tirsdag den 29. september 2015. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 29. september 2015.
Referat af Medicintilskudsnævnets møde nr. 434, tirsdag den 29. september 2015. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 29. september 2015.
Bilag III. Ændringer til relevante afsnit i produktresuméer og indlægssedler
 Bilag III Ændringer til relevante afsnit i produktresuméer og indlægssedler Note: De pågældende punkter i produktresuméet og indlægssedlen er resultatet af referral proceduren. Produktinformationen kan
Bilag III Ændringer til relevante afsnit i produktresuméer og indlægssedler Note: De pågældende punkter i produktresuméet og indlægssedlen er resultatet af referral proceduren. Produktinformationen kan
Medicintilskudsnævnet
 Medicintilskudsnævnet Sagsnr: 2013033446 2. forslag Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
Medicintilskudsnævnet Sagsnr: 2013033446 2. forslag Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Zofran 4 mg og 8 mg frysetørrede tabletter ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Zofran 4 mg og 8 mg frysetørrede tabletter ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Medicintilskudsnævnet
 Sundheds- og Forebyggelsesudvalget 2011-12 SUU alm. del, supplerende svar på spørgsmål 799 Offentligt Medicintilskudsnævnet Den 28. september 2012 Revurdering af lægemidlers tilskudsstatus Referat af Medicintilskudsnævnets
Sundheds- og Forebyggelsesudvalget 2011-12 SUU alm. del, supplerende svar på spørgsmål 799 Offentligt Medicintilskudsnævnet Den 28. september 2012 Revurdering af lægemidlers tilskudsstatus Referat af Medicintilskudsnævnets
Medicintilskudsnævnet
 Referat af s møde nr. 453, tirsdag den 23. august 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 23. august 2016. I mødet deltog: Nævnsmedlemmer: Ellen-Christine Beiter Nina Bjarnason
Referat af s møde nr. 453, tirsdag den 23. august 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 23. august 2016. I mødet deltog: Nævnsmedlemmer: Ellen-Christine Beiter Nina Bjarnason
27-04-2011. Disposition. Markedsfordelingen, AIP 16.000. - Fratagelse af tilskud økonomi på bekostning af kvalitet?
 - Fratagelse af tilskud økonomi på bekostning af kvalitet? Disposition Lidt om pengene Sektor overgange Prioritering eller optimering? Steffen Thirstrup Institutchef, PhD IRF Revurdering af tilskud Sektor
- Fratagelse af tilskud økonomi på bekostning af kvalitet? Disposition Lidt om pengene Sektor overgange Prioritering eller optimering? Steffen Thirstrup Institutchef, PhD IRF Revurdering af tilskud Sektor
Til virksomheden 21. juni 2016 Sagsnr Reference usk T E
 Til virksomheden 21. juni 2016 Sagsnr. 20160221 Reference usk T +4 4488930 E usk@dkma.dk Generelt tilskud til nogle pregabalin kapsler Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Til virksomheden 21. juni 2016 Sagsnr. 20160221 Reference usk T +4 4488930 E usk@dkma.dk Generelt tilskud til nogle pregabalin kapsler Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Angiotensin II antagonister: ordineres lægemidlerne til de rigtige patienter?
 Angiotensin II antagonister: ordineres lægemidlerne til de rigtige patienter? RESUMÉ Højt blodtryk, hjerteinsufficiens og kroniske nyresygdomme kan blandt andet behandles ved påvirkning af renin-angiotensin-systemet
Angiotensin II antagonister: ordineres lægemidlerne til de rigtige patienter? RESUMÉ Højt blodtryk, hjerteinsufficiens og kroniske nyresygdomme kan blandt andet behandles ved påvirkning af renin-angiotensin-systemet
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 415, tirsdag den 19. august 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. august 2014. I mødet
Referat af Medicintilskudsnævnets møde nr. 415, tirsdag den 19. august 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. august 2014. I mødet
Pantoloc pulver til injektionsvæske, opløsning 40 mg
 Pantoloc pulver til injektionsvæske, opløsning 40 mg Læs denne indlægsseddel grundigt inden du begynder at tage medicinen Gem indlægssedlen. Du kan få brug for at læse den igen. Spørg lægen eller på apoteket
Pantoloc pulver til injektionsvæske, opløsning 40 mg Læs denne indlægsseddel grundigt inden du begynder at tage medicinen Gem indlægssedlen. Du kan få brug for at læse den igen. Spørg lægen eller på apoteket
Intern prøve farmakologi den 8. juni 2007 kl til Hold S06V
 Intern prøve farmakologi den 8. juni 2007 kl. 9.00 til 11.00 Hold S06V Side 1 af 5 Case: 62-årig kvinde med kendt hypertension, der igennem mange år har været velbehandlet med thiazid og ACE-hæmmer, henvender
Intern prøve farmakologi den 8. juni 2007 kl. 9.00 til 11.00 Hold S06V Side 1 af 5 Case: 62-årig kvinde med kendt hypertension, der igennem mange år har været velbehandlet med thiazid og ACE-hæmmer, henvender
Visse ACE-hæmmere mister det generelle tilskud Angiotensin-II antagonister og visse dihydropyridincalciumantagonister
 Til lægen Ændring af tilskud til visse typer hjerte-kar lægemidler Lægemiddelstyrelsen ændrer per 13. juli 2009 tilskuddene til en række hjerte-kar lægemidler (blodtrykssænkende lægemidler). De fleste
Til lægen Ændring af tilskud til visse typer hjerte-kar lægemidler Lægemiddelstyrelsen ændrer per 13. juli 2009 tilskuddene til en række hjerte-kar lægemidler (blodtrykssænkende lægemidler). De fleste
Medicintilskudsnævnet
 9. november 2010 Referat af medicintilskudsnævnets møde nr. 343, tirsdag den 26. oktober 2010. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 26.
9. november 2010 Referat af medicintilskudsnævnets møde nr. 343, tirsdag den 26. oktober 2010. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 26.
Behandlingsvejledning for pakkeforløb omfattende følgende sygdomsforløb: hjertesvigt, klapsygdomme, arytmi og angina pectoris.
 Behandlingsvejledning for pakkeforløb omfattende følgende sygdomsforløb: hjertesvigt, klapsygdomme, arytmi og angina pectoris. Ved alle forløb anvendes registreringsskema for patienter i pakkeforløb Hjertesvigt
Behandlingsvejledning for pakkeforløb omfattende følgende sygdomsforløb: hjertesvigt, klapsygdomme, arytmi og angina pectoris. Ved alle forløb anvendes registreringsskema for patienter i pakkeforløb Hjertesvigt
Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Antiarytmika -kliniske aspekter
 Antiarytmika -kliniske aspekter Farmakologi 7. semester Christian Gerdes Hjertemedicinsk afdeling B Århus Universitetshospital Skejby Mål for antiarytmisk behandling At afbryde en akut arytmi At moderere
Antiarytmika -kliniske aspekter Farmakologi 7. semester Christian Gerdes Hjertemedicinsk afdeling B Århus Universitetshospital Skejby Mål for antiarytmisk behandling At afbryde en akut arytmi At moderere
Uddannelsesmateriale. Atomoxetin Teva
 Uddannelsesmateriale Atomoxetin Teva 2019-05 VIGTIG SIKKERHEDSINFORMATION VEDRØRENDE ATOMOXETIN TEVA(ATOMOXETIN) OG RISIKO FOR ØGET BLODTRYK OG PULS Kære sundhedspersonale I overensstemmelse med Lægemiddelstyrelsen,
Uddannelsesmateriale Atomoxetin Teva 2019-05 VIGTIG SIKKERHEDSINFORMATION VEDRØRENDE ATOMOXETIN TEVA(ATOMOXETIN) OG RISIKO FOR ØGET BLODTRYK OG PULS Kære sundhedspersonale I overensstemmelse med Lægemiddelstyrelsen,
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Nitroglycerin DAK 0,25 mg og 0,5 mg sublinguale resoribletter Glyceryltrinitrat
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Nitroglycerin DAK 0,25 mg og 0,5 mg sublinguale resoribletter Glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Nitroglycerin DAK 0,25 mg og 0,5 mg sublinguale resoribletter Glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da
