Anvendelse af antistofpool til differentiering af adenocarcinom og planocellulært carcinom ved sparsomt materiale ved lungecancer
|
|
|
- Rikke Schmidt
- 8 år siden
- Visninger:
Transkript
1 Anvendelse af antistofpool til differentiering af adeno og plano ved sparsomt materiale ved lungecancer The utility of an antibody pool for differentiation of adenoa and squamous cell a for use by small samples of lung cancer. Projekttype: Professionsbachelorprojekt, Modul 14 Studerende: Kristina Jensen, Studienr.: Klinisk vejleder: Kirsten Hartmann. Afdeling for Klinisk Patolog Odense Universitetshospital. Teoretisk vejleder: Tone Elisabeth Bernchou. University College Lillebælt Antal anslag: 94,395 Resume: 246 ord Billede: Illustrer lungernes udseende, samt placering i brystkassen.
2 Resumé Lungecancer inddeles i små-cellede-lunge-er og ikke-små-cellede-lunge-er (NSCLC), hvor NSCLC underinddeles i adeno (AC) og plano (PC). Ved lungecancerudredning anvendes nålebiopsier, som prøvemateriale. Dette er et sparsomt materiale, hvor der evt. ikke kan skæres de ønskede snit, til de klassificerende immunhistokemiske markører, som farves hver for sig. Dette kan medføre, at patologen ikke kan stille en diagnose. Det er formålet at undersøge, fordele og ulemper ved anvendelsen af en antistofpool, der indeholder anti-thyroid-transcripstion-faktor-1 (TTF-1), anti-p63, anti-cytokeratin 5, anti-cytokeratin 14 og anti-napsin-a, til subklassifikation af NSCLC. Der indgik 36 patientprøver, fordelt på 17 AC og 19 PC med forskellig differentieringsgrad. Der er udført immunhistokemi, med den sammensatte antistofpool, som primært antistof. Detektionssystemet; Multivision, skulle resulterede i 2 farvemønstre; Rød kerne/blåt cytoplasma (AC) og blå kerne/ rødt cytoplasma (PC). Til vurdering af vævets morfologi, blev en hæmatoxilin-eosin farvning udført. 15 patientprøver ud af 17 AC blev klassificeret korrekt, hvilket giver en sensitivitet på 88,24 %. 19 patientprøver ud af 19 PC blev klassificeret korrekt, hvilket giver en sensitivitet på 100 %. Anvendelse af antistofpoolen giver mulighed for, at vurdere flere antigener på samme snit. Dette betyder en reducering i antal nødvendige snit, hvilket giver mulighed for yderligere undersøgelser, på det resterende prøvemateriale. Anvendelsen af anti-napsin-a bør revurderes, da AC hovedsageligt blev klassificeret på baggrund af anti-ttf-1. Anvendelsen af anti-ttf-1 og anti-p63 gav en tydelig og brugbar differentiering af NSCLC, men kan ifølge andre studier fremstå positiv ved andre cancertyper, hvilket er en ulempe, der bør tages højde for. 2
3 Forord Forsøget er udført af bioanalytiker studerende Elin Holmarsdottir, Kristina Hansen og Kristina Lis Jensen, som deres afsluttende professionsbachelor projekt. Den følgende rapport er udarbejdet af Kristina Lis Jensen. Forsøget er udført på Afdeling for Klinisk Patologi (AKP) ved Odense Universitets Hospital (OUH) og henvender sig til afdelingen personale, medstuderende, samt alle interesserede. Tak til AKP for lokale, utensilier og udstyr til udførsel af forsøg, reagenser, samt antistoffer. Tak til klinisk vejleder Kirsten Hartmann, AKP/OUH, for hjælp og vejledning under den praktiske udførsel. Tak til Overlæge Karen Ege Olsen, AKP/OUH, for fremskaffelse af prøvemateriale, markering til udstansninger, samt hjælp og vejledning under praktisk udførsel. Tak til bioanalytiker Kirsten Schnor, AKP/OUH, for undervisning i fremstilling af en multiblok. Tak til personalet i laboratoriet for, skæring af den fremstillede multiblok, udførsel af HE-farvning, samt udførsel af de 3 immunhistokemiske farvninger. 3
4 Indholdsfortegnelse Introduktion Problemformulering... 8 Teori... 8 Plano... 8 Adeno... 9 Stor-cellede Nekrose HE-Farvning Immunhistokemi Antigen P Cytokeratin TTF Napsin A Antistof Analyseprincippet Afparaffinering og hydrering Blokering af endogen aktivitet Epitop demaskering Blokering af uspecifik binding Primært antistof Sekundært antistof Substratopløsning Metodiske overvejelser Udvælgelse af prøvemateriale Test af immunhistokemisk metode Subklassifikation af NSCLC Multiblokken Mikrotomi
5 Fremgangsmetoden Antistofpoolen Vurdering Graduering Materiale Prøvemateriale Antistofpool Epitop demaskering Detektionssystem Reagenser HE-farvning Anti-p63, Anti-TTF-1, Anti-napsin-A Fremstilling af multiblok Antistofpoolen Immunhistokemisk metode Mikroskopi Databehandling Metode Test af antistofpool Kontrol materiale Adenoer Adenoer, der er svære at identificere Planocellulære er Planocellulære er, der er svære at identificere Afvigende diagnoser Samlede vurderinger Sensitivitet og specificitet Farvereaktioner Koncentration i antistofpool Nekrotisk væv
6 Reproducerbarhed Diskussion Test af antistofpool Kontrol materiale Adenoer Sensitivitet og specificitet Farvereaktioner Plano Sensitivitet og specificitet Farvereaktioner Afvigende diagnoser Epitop demaskering Antistofpoolen Koncentrationsforholdet i antistofpool Fejldiagnoser Carcinomer, der er svære at identificere Reproducerbarhed Implementering Konklusion Perspektivering Litteraturliste Bilagfortenelse
7 Introduktion Afdeling for Klinisk Patologi (AKP) på Odense Universitets Hospital (OUH) udførte, i samarbejde med Lungemedicinsk Afdeling, 393 lungecancerudredninger i 2012 (1). Der findes forskellige former for lungecancer (LC). Overordnet inddeles LC i små-cellede lunge er (SCLC) og ikke-små-cellede lunge er (NSCLC) (2,3). Før i tiden var det tilstrækkeligt at konstatere at patienter havde NSCLC (3), men i dag, hvor der er udviklet specialiserede behandlingsformer, er det nødvendigt for klinikken, at der differentieres mellem undertyperne af NSCLC, for at kunne give patienterne, den korrekte behandling(3). I forbindelse med lungecancerudredning anvendes nålebiopsier som prøvemateriale. En biopsi er en betegnelse, for en lille vævsprøve, der er udtaget fra et levende individ (4). På AKP arbejdes der udelukkende med biopsier fra mennesker. En biopsi betragtes som den mest betydningsfulde undersøgelsesmetode, når der er tale om tumordiagnostik (4). Pleurahulen, som er omkredset af den lukkede pleurahinde, indeholder en væske, som medfører at ventilationen i lungerne kan foregå uden friktion (5). Når der udtages en nålebiopsi, stikkes en nål, der måler 1,2 mm i diameter (6), igennem pleura og ind i lungen og hvis der i den forbindelse dannes en luftansamling i pleurahulen kan lungerne klappe sammen (5). For at undgå denne sammenklapning, udtages der ikke større biopsier fra lungerne (6). Dette betyder at prøvematerialet, er et meget lille og sparsomt materiale. Til differentiering af NSCLC udføres oversigtsfarvningen Hæmatoxilin-Eosin (HE), samt de klassificerende immunhistokemiske farvninger (IHC) (6). Udfordringen ved at arbejde med lungebiopsier, kan for bioanalytikeren være, at materialet er så sparsomt, at der ikke kan skæres de ønskede snit, der skal anvendes til de klassificerende immunhistokemiske farvninger. Dette kan medføre at patologen ikke får de tilstrækkelige oplysninger, til at fastslå en korrekt diagnose. Mange studier har forsket i anvendelsen af kombinations farvninger, hvor flere immunhistokemiske markører opløses i en pool og anvendes på en gang (3,6-8). Brugbarheden af en lang række markører og kombinationsmuligheder er undersøgt, og flere studier har opnået gode resultater ved anvendelse af Thyroid Transcripstion Faktor-1 (TTF-1), Napsin-A, p63, Cytokeratin 5 (CK5) og cytokeratin 14 (CK14) til differentiering af NSCLC. 7
8 Problemformulering Hvilke fordele og ulemper kan anvendelsen af en antistofpool indeholdende antistoffer rettet mod TTF-1, p63, CK5, CK14 og Napsin-A give i forbindelse med subklassifikation af NSCLC ved sparsomt vævsmateriale? Teori Lungecancer (LC) anses som værende den hyppigste form for cancer verden over (3). I Danmark opstår ca nye tilfælde årligt, og tidlig diagnose har afgørende betydning for chancen for helbredelse (9). Rygning betragtes som værende årsag til 90 % af alle LC tilfælde i Danmark (9), og rygere samt tidligere rygere, med en alder på over 40 år, udgør den største risikogruppe for at udvikle LC (9). På baggrund af patologidata var der i 2012, patienter i Danmark med LC, hvor cancertypen NSCLC udgjorde 82,7 % og cancertypen SCLC udgjorde 12,9 % af det totale antal (1). De resterende 4,5 %, svarende til 192 patienter har en cancer, der er svær at identificere, og er derfor ikke inddelt i en gruppe med en bestemt cancertype (1). NSCLC inddeles i undertyperne plano, adeno og stor-cellede (2). Plano Et plano (PC) udgår fra flerlaget pladeepitel (5), hvilket normalt ikke forekommer i lungerne. Som resultat af fx rygning, kan der opstå metaplasi, som er en betegnelse for omdannelse af væv (5). I lungerne omdannes cylinder epitel til flerlaget pladeepitel (4). Figur 1: Illustrerer metaplasi, hvor cylinder epitel gradvist udskiftes af pladeepitel (4). Metaplasi er en reversibel tilstand, men fortsætter den skadelige påvirkning, som har medført de metaplastiske forandringer, kan der udvikles dysplasi (4), som er de præmaligne tilstande der kan resultere i PC (5). PC lokaliseres oftest centralt i lungen (2), og denne cancertype vil alt efter differentieringsgraden (omtales senere), danne struktur som flerlaget pladeepitel. På figur 2 nedenfor ses PC, farvet med Hæmatoxilin-Eosin (HE) farvning (omtales senere). Der kan observeres store lyse celler (rød pil), som lejres i øer (N), og kan fremstå med struktur som en 8
9 hvirvel omkring centrum af øen (sort cirkel) (2). Derudover kan der observeres dannelse af keratin, som karakteriserer en højt differentieret cancer (2). Keratin kan forekomme i enkelte celler (D) eller i større formationer, kaldet keratin perler (KP) (2). Figur 2: Viser et højt differentieret plano, farvet med Hæmatoxilin-Eosin. Rød pil anviser store lyse celler. N anviser områder, hvor cellerne lejres i øer. Den sorte cirkel anviser et område, der har struktur, som en hvirvel, hvor cellerne lejres omkring centrum af området. D anviser en celler, der indeholder keratin og KP en lejring af celler, der indeholder keratin og kaldes en keratin perle (2). Adeno Et adeno (AC) udgår fra kirtelceller (5) som er en del af det normale lungevæv. Der kan observeres kirtelceller i form af type 2 pneumocytter. Disse celler udskiller surfaktant, som danner en hinde på alveoleoverfladen (10). Derudover findes kirtelceller, i form af bægerceller, som producerer og udskiller mucin til slimhinden i hovedbronkierne, samt bronkierne (10). I bronkiolerne findes Clare-celler, som producerer og udskiller et surfaktant-lignende sekret til bronkiolerne (10). AC lokaliseres oftest perifert i lungerne (2), og denne cancertype vil alt efter differentieringsgraden (omtales senere), danne kirtellignende strukturer (5). På figur 3 nedenfor ses AC, farvet med HE-farvning. Cellerne fremstår med lilla cellekerner (sort pil) og lyst rødt cytoplasma (rød pil). Der kan observeres kirtelstruktur (G) (2), hvor der kan observeres runde kirtelformationer (sort cirkel) og forgrenede kirtelformationer (rød cirkel). Nogle kirtelformationer kan indeholde mucin (blå pil) (2). 9
10 Figur 3: Viser et adeno, farvet med Hæmatoxilin-Eosin. Cellerne fremstår med lilla kerne (sort pil) og rødt cytoplasma (rød pil). G anviser områder, hvor der dannes kirtelstruktur. Den sorte cirkel omkranser en rund kirtelformation, og den røde cirkel omkranser en forgrenet kirtelformation. Den blå pil anviser mucin (2). Stor-cellede Cancerceller kendetegnes bl.a. ved nedsat differentieringsevne, hvilket betyder at cellerne ikke udvikles i samme grad, som de normale celler (4). De stadier af cancer der ligner mest det væv canceren udgår fra, kaldes højt differentieret. Omvendt benævnes de stadier der kun har få ligheder med det væv canceren udgår fra, lav differentieret (4,5). Lavt differentierede cancertyper, kan især være svære at klassificere, da de helt kan mangle de morfologiske karakteristika der kan anvendes til identifikation (11). Hvis en cancer er så lavt differentieret at den ikke ligner det væv canceren udgår fra, klassificeres den som et stor-cellet (2). På figur 4 nedenfor ses et uidentificeret stor-cellede fra lungen farvet med HE-farvning. Cellerne fremstår med store lilla kerner (sort pil) og rødt cytoplasma (rød pil). Strukturen fremstår rodet og udtrykker ikke karakteristika for hverken PC eller AC (2). 10
11 Figur 4: Viser et uidentificeret stor-cellet, farvet med Hæmatoxilin-Eosin. Strukturen fremstår rodet. Den røde pil anviser rødt cytoplasma og den sorte pil anviser lilla cellekerner (2). Adenosquamøst Adenosquamøst er en betegnelse for den LC type, hvor canceren består af både adeno og plano (2). Nekrose Når en cancer udvikles kan blodforsyningen blive den begrænsende faktor, hvorved der opstår nekrose af tumorcellerne (4). Nekrose betegnes, som de morfologiske forandringer der ses ved celledød (4). Mikroskopisk fremstår en nekostisk celle med gradvist opsvulmet og lyst cytoplasma og i cellekernen ses gradvist nedbrydning (4). Det menes at 97 % af alle tumorceller undergår nekrose og det estimeres, at det derfor tager et mikroskopisk lunge omkring 10 år at vokse en cm (4). HE-Farvning HE-farvningen er på AKP automatiseret og anvendes som en oversigtsfarvning der opdeles i 2 metoder; en kernefarvning og en kontrastfarvning (12). Carazzi hæmatoxylin anvendes til kernefarvningen, da det er et metalfarvekompleks, der binder sig til fosfat grupperne i DNA og RNA og farver dem røde. Da DNA og RNA primært findes i cellekernerne, vil farven koncentreres her. Ved efterfølgende at skylde snittene NH 3, sker der pga. ph ændringen et farveskift. Den røde farve skifter til blå. Derfor kaldes dette trin blåning (12). Eosin Y anvendes til kontrast farvningen, da det er et anionfarvestof der binder sig til proteiner og farver dem røde. Da der findes proteiner i bl.a. cytoplasma og bindevæv, vil denne røde farve fremkomme mange steder i vævs snittet. Eosin 11
12 Y vil også farve histonerne, som DNA snor sig omkring. Selvom carazzi hæmatoxylin og eosin Y ikke farver samme komponent af cellekernen, vil der opstå en blandingsfarve, som vil fremstå blåviolet (12). En HE-farvning gør det muligt, at vurderer vævets morfologi, cellernes lejring, differentieringsgraden, og om der evt. er opstået morfologiske forandringer, såsom nekrose (12). Men især i forbindelse med tumordiagnostik, anvendes immunhistokemi, til at fastlægge den korrekte tumorklassifikation (4). Immunhistokemi Immunhistokemi er en teknik, der bygger på antigen-antistof reaktioner (12). Immunhistokemi anvendes til påvisning af makromolekyler i væv kaldet antigener (5). Ved at behandle vævet med specifikt fremstillede antistoffer, der er rette mod bestemte antigener, kan disse påvises, hvis de er til stede i det undersøgte væv.(5) Antigen Ordet antigen stammer fra ordet antistofgenerator, hvilket betyder at et molekyle er i stand til at provokere til antistofdannelse (5). Et antigen indeholder små områder, som kaldes epitoper. Det er epitoperne, der stimulerer til dannelsen af antistof (13). P63 P63 er et kerneprotein, som fungerer som transskriptions faktor og et stamcelleregulerende protein, som i fosterstadiet har afgørende betydning for udvikling af bestemte epiteltyper (13). I normalt lungevæv findes p63 i basalcellerne (13), og i forbindelse med LC kan p63 påvises ved PC (13). Cytokeratin Cytokeratiner (CK) er en bestemt type intermediære filamenter, som findes i alle epitelceller (13). Intermediære filamenter er en del af cellernes cytoskelet, som giver cellerne struktur og styrke (4). I normalt lungevæv udtrykkes CK5 og CK14 i basalceller, og ved LC kan begge CK typer påvises ved PC (13). Derudover kan både CK5 og CK14 være positive i % af cellerne i et AC (13). TTF-1 Thyroid Transcripstion Faktor-1 (TTF-1) er et kerneprotein, der fungerer som transskriptionsfaktor. I normalt væv findes TTF-1 bl.a. i respiratorisk epitel, hvor den transkriberer generne for surfanktant og clara cellernes sekrotoriske protein (7,13). I forbindelse med LC kan TTF-1 påvises 12
13 ved forskellige cancertyper. TTF-1 er bl.a. positiv i 70 % af AC, men udtrykkes også i 90 % af SCLC og 50 % af storcellede neuroendokrine er (13). Napsin A Napsin-A er en protease, der står for modningen af surfaktant protein B (11). I normalt lungevæv findes Napsin-A i cytoplasmaet ved type 2 pneumocytter, alveole makrofager (11). I forbindelse med LC kan Napsin-A påvises i op mod 80 % af alle AC (7). Antistof Et antistof er et stof, der produceres af organismen, som reaktion på stimulans af et antigen. Antistoffer kaldes også immunglobuliner (Ig) og inddeles i 5 klasser; IgA, IgD, IgE, IgG og IgM (4,13). Et antistof er opbygget af en konstant del og en variabel del (V) (4) V-delen er den del af antistoffet, der specifik passer til det antigen, der stimulerede til antistoffets produktion (4). Analyseprincippet Figur 5 nedenfor illustrerer, den immunhistokemiske metode, som udføres i 8 trin: Afparaffinering 1 Hydrering 2 Blokering af endogen aktivitit 3 Epitop demaskering 4 Blokering af uspecifik binding 5 Primært antistof 6 Enzymkonjugeret sekundært antistof 7 Substratopløsning 8 Figur 5: Viser flowskema over den anvendte immunhistokemiske metode 13
14 Afparaffinering og hydrering Ved mikroskopi anvendes meget tynde vævssnit, og for at gøre det muligt at skære disse, støbes vævet i paraffin. Paraffin er et upolært materiale, som stabiliserer vævet, når det størkner. Men før antistofferne, som er polære, kan binde sig til vævet, skal paraffinet fjernes (13). Dette gøres med et upolært opløsningsmiddel. Når vævet er paraffin frit, skal vævet gøres polært, så det kan reagere med antistofferne. Dette gøres med ethanol (13), som er svagt polært, hvilket medfører at det er blandbart, med både det upolære opløsningsmiddel og med vand. Under hydreringen gøres vævet polært. Blokering af endogen aktivitet I humant væv findes forskellige naturlige endogene enzymer, som kan reagere med forskellige detektionssystemer (13). Peroxidase (HRP) og alkalisk phoshatase (AP) findes bl.a. i granolocytter, monocytter, makrofager og erytrocytter (13). Da detektionssystemet anvender HRP og AP (omtales senere), må denne endogene aktivitet blokeres. Epitop demaskering Inden vævet støbes i paraffin, bliver vævet fikseret. Fiksering immobiliserer og stabiliserer vævets bestanddele, ved at danne bindinger mellem antigenerne i vævets proteiner. Dette medfører bevarelse af vævets struktur, hvilket er vigtigt ved diagnosticering, men denne fiksering medfører samtidig at antigenernes epitoper maskeres (13). Denne maskering betyder at epitoperne ofte ikke kan indgå i immunkompleksdannelsen. Epitop demaskering skal altid udføres efter blokering af endogen aktivitet, da epitoperne er følsomme overfor de opløsninger, der anvendes til blokeringen (13). Blokering af uspecifik binding De anvendte antistoffer kan binde sig til vævets proteiner med svage kemiske bindinger. Hvis dette sker, ses en generel farvning af hele vævet, som kaldes baggrundsfarvning, og denne farvning kan gøre det vanskeligt at vurdere vævssnittet (13). Til blokering af uspecifik binding anvendes en protein opløsning, som blokerer vævets proteinerne, således antistofferne ikke kan binde sig til dem (13). Primært antistof Her anvendes det primære antistof, som ved dette forsøg er en antistofpool, som indeholder anti-p63 (14), anti-ck5 (15), anti-ck14 (16), anti-ttf-1 (17) og anti-napsin A (18). Anti-napsin-A og anti- 14
15 p63 er mus-anti-human antistoffer (6,14,18) og anti-ck5, anti-ck14 og anti-ttf-1 er kanin-antihuman antistoffer (6,15-17). Sekundært antistof Det sekundære antistof indeholder 2 antistoffer der henholdsvis binder til mus eller kanin. Det ene antistof er et ged-anti-mus antistof, som har tilkoblet en polymer der indeholder AP (6). Det andet antistof er et ged-anti-kanin, som har tilkoblet en polymer, der indeholder HRP (6). Enzymkonjugeret polymer Sekundært antistof Primært antistof Vævets antigener Figur 6: Illustrere hvorledes det primære antistof binder til vævet, og hvorledes det sekundære antistof binder til det primære antistof. Det sekundære antistof har tilkoblet en enzymkonjugeret polymer. Substratopløsning Til detektion med Multivison, fungerer AP og HRP som enzymer (6). Når substraterne LVBlue og LVRed tilsættes, vil der ske en farvereaktion, i de områder hvor henholdsvis AP og HRP er bundet. AP reagerer med LVBlue og HRP reagerer med LVRed (6). Metodiske overvejelser Udvælgelse af prøvemateriale For at undgå, at antistofpoolen bliver vurderet ikke-brugbar til differentiering af NSCLC, fordi prøvematerialet ikke indeholder det korrekte væv, er alt anvendt prøvemateriale udvalgt af Overlæge Karen Ege Olsen (KEO) fra AKP. Dette er besluttet fordi KEO har erfaring med LC, stort kendskab til afdelingens arkiv, samt patientprøvernes brugbarhed. De anvendte patientprøver blev udvalgt på baggrund af den kendte diagnose; AC eller PC, samt differentieringsgraden. 15
16 Test af immunhistokemisk metode En test af den immunhistokemiske metode, kan påvise om den planlagte opsætning fungerede eller om eventuelle justeringer skal foretages inden BA forsøgets start. Der anvendes 3 vævstyper; normalt væv, væv med AC og væv med PC. Normalt væv er medtaget for at påvise, hvorvidt antistofpoolen (ASP) giver samme resultater, som teori foreskriver. AC og PC er medtaget for at vurdere ASP. Hvis der observeres de foreskrevne farvereaktioner, kan det konkluderes at antistofferne binder specifikt til de ønskede vævskomponenter, fx at anti-ttf-1 binder til TTF-1 i vævet og at dette findes i kernerne. Derudover ønskes det fastlagt, om ASP har den korrekte koncentration, hvilket kontrolleres ved observation af farveintensitet. Hvis ASP ikke har den optimale koncentration, vil det opleves at en eller flere farvereaktioner fremstår svag eller farveløse. Ydermere ønskes en negativ kontrol undersøgt. Dette vil påvise, hvorvidt det sekundære antistof kan binde uspecifikt til vævet, hvilket vil være et mål for validiteten af resultaterne. Subklassifikation af NSCLC Til subklaasifikation af NSCLC indgår 36 patientprøver fordelt på 13 AC, 13 PC og 10 er, der er svære at identificere. Cancer opstår altid på DNA-niveau og udvikles på baggrund af en række genetiske ændringer (4) i det enkelte individ. Dette betyder at der findes mange variationer indenfor samme cancertype. Ved at inddrage 36 patientprøver, kan vi få et indblik i hvilket farvemønster, der knyttes til den pågældende cancertype og kendskab til nogle af de variations muligheder der kan observeres. Ved minimum at anvende 13 AC og 13 PC, kan der vurderes, hvorvidt de observerede farvereaktioner skyldes cancerens biologi eller en tilfældelighed. Derudover skal det undersøges, hvilken betydningen differentieringsgraden har. Dette kan fastslå om farvemetoden kan anvendes til lavt differentieret cancer, såvel som højt differentieret cancer. Multiblokken Det anvendte prøvemateriale er udtaget af en vævsblok, hvilket betyder at forsøget kunne været udført på snit af hele vævsblokken, men for at mindske variationen mellem de undersøgte patientprøver, samles prøverne i 2 multiblokke. På den måde sikres den mest ensartede behandling af alle vævsprøverne, hvilket sikre at de observerede farveforskelle skyldes cancerens biologi og ikke de metodiske variationer. De 36 patientprøver, samt 4 fikspunkter deles op i 2 multiblokke med 20 vævsprøver i hver. Fordelingen er valgt da det ikke er teknisk muligt, at anbringe 40 16
17 vævsprøver i en blok. For at mindske antal af multiblokke, samt reducere den eventuelle variation, der kan opstå mellem blokkene, er 20 vævsprøver pr. multiblok fastlagt. Mikrotomi En analyse er aldrig bedre end det prøvemateriale analysen er udført på. For at udelukke at variationer i farvereaktionerne, ikke skyldes dårligt skåret prøvemateriale, udføres mikrotomi af en erfaren bioanlytiker fra AKP. Fremgangsmetoden Anvendelsen af antistofferne TTF-1, Napsin-A, p63, CK5 og CK14 til differentiering af NSCLC er allerede anvendt, som fast rutine på Patologisk Institut ved Regionshospitalet Holstebro (PIRH) (6). Deres opsætning opnår gode resultater, derfor er fremgangmetoden som de anvender, valgt som udgangspunkt til dette forsøg. Fremgangsmetoden er designet af producenten; Thermo Scientific og kaldes MultiVision Polymer Detection System (19). Fremgangsmetoden er så vidt muligt tilpasset AKP, ved at anvende de opløsninger der er til rådighed på AKP. På den måde gøres forsøget realistisk, hvormed afdelingen efterfølgende, i større grad kan vurdere brugbarheden. I 1. trin under afparaffinering erstattes xylen med HistoClear Histological Clearing Agent, da det er dette medie, der er til rådighed på AKP (Bilag 1). I trin 2, 6, 10, 12 og 18 skal der vaskes med TBST buffer, hvilket er en sammensætning af Tris Buffered Saline og 0,1 % Tween20. Denne vaskebuffer erstattes med den lignende vaskebuffer TNT (Tris-NaCl-Tween), da det er denne vaskebuffer, der er til rådighed på AKP (Bilag 1). Derudover vælges TNT, da indholdet af tween sikre at vævet ikke tørrer ud undervejs i metoden. En ændring i rækkefølgen foretages således at trin 5+6 udføres før trin 3+4 (Bilag 1). Denne ændring foretages, da den læste teori foreskriver at der ikke må udføres blokeringen af endogen aktivitet lige efter epitop demaskering, da epitoperne er følsomme, overfor de opløsninger, der anvendes til blokeringen (13). I trin 3 skal der foretages epitop demaskering, men producenten oplyser ikke hvilken buffer dette skal udføres med (19). Lauridsen,J.L. et al. (6) beskriver anvendelsen, opsætningen og resultater fra PIRH. Her oplyses det, at de anvender apparaturet PT-Link fra Dako (20), som anvender en 3 i 1 buffer, der udfører afparaffinering og epitop demaskering i samme trin (6). Denne buffer indkøbes ikke til forsøget. Yanagita, E. et al. (8) har anvendt 4 af de antistoffer der findes i vores ASP og har opnået gode resultater ved differentiering af NSCLC. Dette studie har anvendt EDTA-buffer ph 8,0 til epitop demaskering. På 17
18 baggrund af denne artikel anvendes EDTA buffer til forsøgets epitop demaskeirng, da denne buffer er til rådighed på AKP. Udførslen i trin 3 erstattes af fremgangsmetoden; Antigendemaskering i mikrobølgeovn (Bilag 2) som anvendes på AKP. Antistofpoolen Som nævnt ovenfor anvender PIRH samme antistofpool som anvendes ved dette forsøg, og der opnås gode resultater herved. Derfor anvendes samme koncentrationsforhold som er oplyst af PIHR: 12 ml diluent, 60µl anti-napsin-a, 60µl anti-ttf-1, 60µl anti-ck14, 120µl anti-ck5, 120 µl anti-p63. Vurdering Diagnosticeringen af de 36 patientprøver vil foregå på baggrund af de farvemønstre, den anvendte teori foreskriver; AC vil fremstå med røde kerner (TTF-1) og blåt cytoplasma (Napsin A) (6) og PC vil fremstå med blå kerner (p63) og rødt cytoplasma (CK 5 og CK 14) (6) Figur 7: Viser en skitse over farveraktionerne ved henholdsvis adeno (rød kerne, blåt cytoplasma) og plano (Blå kerne, rødt cytoplasma) (6). Graduering Patientprøverne vurderes udelukkende med diagnose. Baggrunden for dette valg, er at flere af patientprøverne indeholder forskellige farveintensiteter, da dele af vævet er meget kraftigt farvet, og andre dele af vævet er meget svagt farvet. Det gør det vanskelig at fastlægge en generel graduering af vævets farveintensitet, som kan anvendes til sammenligning af alle vævsprøverne. 18
19 Materiale Prøvemateriale Pilotforsøget udføres på 3 patientprøver der stammer fra 2 patienter. Der er udvalgt normalt væv, væv med adeno og væv med plano. BA forsøget udføres på 36 patientprøver. Som udgangspunkt skal de 36 patientprøver fordeles på 13 adenoer, 13 planocellulære er og 10 er der er svære at identificere. Antistofpool Den anvendte antistofpool, er en sammensætning af antistoffer rettet mod; Napsin-A, TTF-1, CK14, CK5 og p63. Disse antistoffer opløses i diluent med det korrekte koncentrationsforhold. Antistof Klon Producent Batch nr. /Lot nr. Antibody Diluent Dako REAl Napsin A NCL-L-Napsin A Novocastra TTF-1 EP1584Y Abcam YIo72212DS2 CK14 SP53 Cell Marque C CK5 EPY1601Y Cell Marque C P63 4A4 Zeta Corporation L1112 Figur 8: Viser sammensætningen af antistofpoolen, hvilken klon og mængde der anvendes, samt hvilke producenter og batch- eller lot. numre, der er anvendt til denne BA opsætning. Epitop demaskering Til epitop demaskering er der anvendt EDTA-Dinatrium 1mmol/L ph 8,0 fra producenten; Ampliqon. Bacth nr AN10. 19
20 Detektionssystem Det anvendte detektionssystem; MultiViosn Polymer Detection System (19), er produceret af Thermo Scientific, og indeholder nedenstående. Reagens Batch nr. / Lot nr. MultiVision Polymer Detection System MARH MultiVison cocktail MAM Ultra V block AUB Hydrogen Peroxidase Block AHP LVBlue AP Buffer TMM LVBlue Chromogen Vial 1 AB LVBlue Chromogen Vial 2 AB LVBlue Chromogen Vial 3 AB LVRed Chromogen Vial 1 HR LVRed Chromogen Vial 2 HR LVRed Chromogen Vial 3 HR LVRed Chromogen Vial 4 HR Mounting Media AUA Figur 9: Viser indholdet i kittet MultiVision Polymer Detection System, samt hvilke batch- eller lot numre, der er anvendt til denne BA opsætning. 20
21 Reagenser Udover antistofpoolen og detektionssystemet er der anvendt, Histo-Clear Histological Clearing Agent, til afparaffinering. Der er anvendt Ethanol med henholdsvis 99 %, 96 % og 77 % til hydreringen, samt TNT buffer ph 7,53 til vaske procedurerne. HE-farvning HE-farvningen blev udført af personalet i laboratoriet på apparaturet SAKURA Tissue-Tek Prisma. Her anvendes Histo-Clear Histological Clearing Agent til afparaffinering, samt 96 % og 99 % ethanol til hydrering. Derudover anvendes reagenserne Carazzi hæmatoxylin og Eosin Y til farvning, samt NH 3 til blåning. 96 % og 99 % ethanol anvendes til dehydrering. Anti-p63, Anti-TTF-1, Anti-napsin-A De immunhistokemiske farvninger af anti-p63, anti-napsin-a og anti-ttf-1 blev udført af personalet i laboratoriet, på apparaturet Ventana BenchMark ULTRA. Her anvendes reagenset EZ Prep til afparaffinering, Cell Conditioning 1 (CC1) til epitop demaskering, OptiView DAB IHC Detection Kit anvendes som detektionssystem, men indeholder samtidig en peroxidase hæmmer til blokering af endogen aktivitet. 21
22 Metode Fremstilling af multiblok Til fremstilling af en multiblokkene anvendes indstøbningsmaskinen SAKURA Tissue-Tek TEC. Indledningsvis hældes lidt varm paraffin i en metalform, således at der er noget at placere vævsprøverne i. For at sikre det korrekte prøvemateriale har KEO markeret den del af vævsblokken der indeholder cancerceller. Markeringen er anvist på et objektglas, hvor der tidligere er udført en HE-farvning. Objektglasset sammenholdes med den tilhørende blok, således udstansningen, sker det anviste sted i blokken (Bilag 3, Billede 1). Udstanseren presses ned i vævsblokken og drejes let, således vævsprøven slipper blokken. Herefter skubbes vævsprøven ud af udstanseren med en træpind og placeres med snitfladen nedad i metalformen. Vævsprøverne placeres i metalformen, ud fra en forudbestemt skitse over multiblokken (Bilag 4). For at kontrollere at udstansningerne er udført de anviste steder, sammenholdes den brugte vævsblok med objektglasset (Bilag 3, billede 2). Når vævsprøverne placeres i metalformen, presses de let mod bunden, hvorefter metalformen føres over på kuldepladen, så vævet kan fæstne sig i paraffin bunden. Når alle vævsprøver er placeret i metalformen, sættes en kapsel på og der fyldes op med paraffin. Når metal formen og kapslen er fyldt med paraffin skal multiblokken størkne på en kuldeplade. Når multiblokken er kold, kan blokken løsnes fra metalformen og den er nu klar til vurdering. Antistofpoolen Test af antistofpoolen Til pilotforsøget skal der fremstilles en antistofpool med en mængde der kan anvendes på 3 glas. Total volumen skal derfor minimum være på (3 300 µl) 900 µl, da der anvendes ca. 300 µl pr. glas. Der tages udgangspunkt i at fremstille en antistofpool med et slutvolumen på ca µl. Alle antistofferne opløses i 12 ml diluent, hvilket svarer til µl. Da µl divideret med 12 giver µl, som var den ønskede slut volumen, divideres alle koncentrationer med 12, således at det oprindelige koncentrationsforhold bibeholdes. Følgende beregninger er udført: 12 ml diluent: ( µl / 12 ) = µl 22
23 60 µl Napsin A: ( 60 µl / 12 ) = 5 µl 60 µl TTF-1: ( 60 µl / 12 ) = 5µl 60 µl CK 14: ( 60 µl / 12 ) = 5µl 120 µl CK 5: ( 120 µl / 12 ) = 10 µl 120 µl p63: ( 120 µl / 12 ) = 10 µl Antistofpoolen blev fremstillet dagen før pilotforsøget blev udført. Antistofpoolen blev efter fremstilling opbevaret i køleskab ved en temperatur på 5. Subklassifikation af NSCLC Til forsøget skal der fremstilles en antistofpool med en mængde der kan anvendes på 8 glas. Total volumen skal derfor minimum være på (8 300 µl) µl. Der tages udgangspunkt i at fremstille en antistofpool med et slutvolumen på ca µl. Alle antistofferne skal opløses i 12 ml diluent, hvilket svarer til µl. Da µl divideret med 4 giver µl, som var den ønskede slut volumen, dividere alle koncentrationer med 4, således at det oprindelige koncentrationsforhold bibeholdes. Følgende beregninger er udført: 12 ml diluent: ( µl / 4 ) = µl 60 µl Napsin A: ( 60 µl / 4 ) = 15 µl 60 µl TTF-1: ( 60 µl / 4 ) = 15 µl 60 µl CK 14: ( 60 µl / 4 ) = 15 µl 120 µl CK 5: ( 120 µl / 4 ) = 30 µl 120 µl p63: ( 120 µl / 4 ) = 30 µl Antistofpoolen blev fremstillet samme dag, som forsøget blev udført. Antistofpoolen blev efter fremstilling opbevaret i køleskab ved en temperatur på 5. 23
24 Immunhistokemisk metode Alle objektglas placeres i en Tissue-Tek slideholder (vugge) og gennemgår en fælles afparaffinering og hydrering (Bilag 5). Til afparaffinering anvendes 2 kar med ca. 200 ml Histo- Clear i hver. Vuggen anbringes i 1. kar i 5 min, hvorefter den flyttes til 2. kar i endnu 5 min. Efter afparaffinering skal der udføres en hydrering, hvor vuggen anbringes i ethanol med forskellig koncentration; 2 kar med ca. 250 ml 99 %, 2 kar med ca. 250 ml 96 % og 1 kar med ca. 250 ml 77 %. Vuggen anbringes 2 min i hvert kar. For at afslutte hydreringen anbringes vuggen i rindende vand i 5 min. Når objektglassene i de efterfølgende trin behandles hvert for sig, følges den samme rækkefølge med samme tidsinterval, således at alle objektglas får samme behandling. Vævssnittene skyldes med TNT buffer, hvorefter hvert objekt glas tørres på bagsiden, samt tørres så tæt på vævsstykket som muligt, uden at ramme vævet. Øverst på objektglasset lavet en væskeafvisende barriere, med en DAKO Pen (21). Herefter dryppes reagenset; Hydrogen Peroxidase Block, over vævssnittet, således at alt væv er dækket. Vævssnittene skal inkubere 10 min i fugtkammer ved stuetemperatur. Efter de 10 min skylles hvert objektglas med TNT buffer, hvorefter de placeres i en vugge. Vuggen fyldes op med objektglas og placeres i en Tissue-Tek farveskål med præcis 250 ml EDTA buffer. 2 andre vugger fyldes med objektglas og placeres i tilsvarende farveskåle der indeholder præcis 250 ml destilleret vand. De 3 farveskåle placeres i en mikroovn, som anvist på bilag 2. Først udføres en opvarmning, hvor mikroovnen indstilles til max effekt i 9min. Herefter skal der udføres en kogning, hvor mikroovnen indstilles til 440 W i 15 min. Efter kogning tages beholderne ud af mikroovnen og efterlades til afkøling i minimum 15 min. Efter afkøling anbringes vuggen med vævssnittene i rindende vand i 2 min (Bilag 2). Efter de 2 min. tørres hvert objekt glas på for- og bagside, som tidligere beskrevet. Herefter dryppes reagenset; Ultra V Block, over vævssnittet, således at alt væv er dækket. Vævssnittene skal inkubere 10 min i fugtkammer ved stuetemperatur. Vævssnittet må herefter ikke skylles, så reagenset fjernes, ved at tippe væsken af. Den fremstillede antistofpool dryppes over de vævssnit, der skal behandles med primært antistof, hvorimod der dryppes TNT buffer over de negative kontroller. Vævssnittene skal inkubere 30 min i fugtkammer ved stuetemperatur. Efter de 30 min skylles hvert objektglas med TNT buffer og tørres som tidligere omtalt. Nu dryppes reagenset; MultiVision Polymer Cocktail: anti-rabbit/hrp + anti-mouse/ap, over alle vævssnittene, således at alt væv er dækket. Vævsnittene skal inkubere i 30 min i fugtkammer ved stuetemperatur. Efter min fremstilles 24
25 LVBlue ved at blande 2,5 ml AP-buffer med 1 dråbe af hver LVBlue vial 1, 2 og 3. Denne blanding skal anvendes inden 15 min efter fremstilling, da sensitiviteten herefter falder (19). Når vævsnittene har inkuberet med MultiVision i 30 min skylles objektglassene med TNT buffer, inden der dryppes LVBlue over, som vævssnittene skal inkubere med i 10 min i fugtkammer ved stuetemperatur. Efter 5 min fremstilles LVRed ved at blande 5 ml demineraliseret vand med 3 dråber af LVRed vial 1 og 2 dråber af hver LVRed 2, 3 og 4. Denne blanding skal anvendes inden 15 min efter fremstilling, da sensitiviteten herefter falder (19). Når vævsnittene har inkuberet med LVBlue i 10 min skylles objektglassene med TNT buffer inden der dryppes LVRed over vævssnittene. Vævsnittene skal inkubere i 10 min i fugtkammer ved stuetemperatur. Efter 10 min kan hvert objektglas skylles med demineraliseret vand, hvorefter der tørres på bagsiden af glasset. Forsiden af objektglasset tørres, ved let at trykke filter papir mod vævssnittet uden at ødelægge vævet. Alle objektglas skal herefter tørre natten over, da vævets skal være helt tørt inden dækglasset monteres. Dagen efter monteres dækglas med monteringsmediet Mounting. Her placeres en dråbe over vævs snittene og en dråbe over kontrolsnittet, hvorefter dæk glasset placeres ovenpå. Hvis Mounting mediet ikke flyder helt ud, presses let mod dækglasset med en pincet. Hvis der kan observeres bobler under dækglasset, forsøges disse fjernes ved let at presse en pincet mod dækglasset og føre boblen ud. Efter montering skal Mounting mediet tørre i ca. 1 time ved stuetemperatur. Mikroskopi Til orientering ved mikroskopi anvendes skitsen, anvist på bilag 7. Her er vævsprøvernes placering spejlvendt, i forhold til den placeringen man anvendte ved fremstilling af multiblokken. Dette skyldes at paraffin blokken vendes, når den skal skæres, som anvist i figur 10 nedenfor Figur 10: Viser hvorfor man ved mikroskopi skal forholde sig spejlvendt til den fremstillede multiblok. Billede A viser vævsprøvernes placering når man ser ned i metalformen. Billede B viser hvordan kapslen lægges ovenpå metalformen inden den fyldes med paraffin. Billede C viser at kapslen vendes 180º når den sættes op til mikrotomi. Billede D viser vævsprøvernes placering som blokken skæres. Billede E viser vævsprøvernes placering efter montering på kontrol glas. 25
26 Databehandling Samlede vurderinger Der er udført en optælling af de foretaget vurderinger, hvor de oprindelige diagnoser er opgjort til 17 adenoer (AC) og 19 planocellulære er (PC). Derudover er der opgjort, hvilke diagnoser de 3 studerende, individuelt er kommet frem til og overskueliggjort i resultatafsnittet. Farvereaktioner Der er udført en optælling af hvilke farvereaktioner, der er observeret i BA forsøget. Vævsprøverne er kronologisk gennemgået og farvereaktionerne er noteret og anvist i resultatafsnit. De valgte kategorier, er fastlagt på baggrund af de mange farvereaktioner, der er noteret ved AC. Ved PC er 2 vævsprøver ud af de 19 prøver, observeret med meget svag kernefarve. De 2 prøver er ved denne opgørelse noteret som farveløs og placeres i kategorien kun rødt cytoplasma. Sensitivitet og specificitet For at kunne vurdere metodens brugbarhed, er der beregnet en sensitivitet og en specificitet. Sensitiviteten er beregnet på baggrund af Sandt positive tilfælde, divideret med de sandt positive tilfælde og de falsk negative tilfælde (22). Dette tal er ganget med 100, for at opnå et procenttal. Specificiteten er beregnet på baggrund af sandt negative tilfælde, divideret med sandt negative og falsk positive tilfælde (22). Dette tal er ligeledes ganget med 100, for at opnå et procenttal. Patientprøve 24, som er vurderet til at indeholde celler fra både AC og PC, er i forbindelse med disse beregninger fastslået, som PC, da det er denne celletype der dominere cellebilledet. 26
27 Resultater Test af antistofpool Tabel 1 viser de opnåede resultater ved den udførte test af antistofpoolen (ASP). Når normalt lungevæv farves med ASP, kan der observeres kraftigt farvede røde kerner (rød pil), og kraftigt farvet blåt cytoplasma (blå pil). Der udover ses makrofager, som fremstår med blåt cytoplasma og farveløse kerner (blå cirkel) Når AC farves med ASP, kan der observeres røde kerner (rød pil) og blåt cytoplasma (blå pil). Derudover kan der observeres områder med røde kerner og ingen cytoplasma farvning (sort cirkel). Når PC farves med ASP, kan der observeres blå kerner (blå pil) og rødt cytoplasma (rød pil). Alle 3 udførte negativ kontroller, fremstår med lyse vævsstrukturer. Vævstype Antistofpool Negativ kontrol Normalt Lungevæv AC Fortsættes.. 27
28 PC Tabel 1: Viser resultaterne fra den udførte test af antistofpoolen. Alle vævsprøver er afbilledet ved forstørrelse 20x. Testen er udført på normalt væv, adeno (AC) og plano (PC). De blå pile anviser blå farvereaktion, som lokaliseret i kernerne ved PC og i cytoplasma, ved normalt væv og AC. De røde pile anviser rød farvereaktion, som lokaliseres i cytoplasma ved PC og i kernerne ved normalt væv og AC. Den sorte cirkel omkranser et område, hvor kernerne er røde og der ikke kan observeres en cytoplasma farvning. Den blå cirkel omkranser makrofager, som farves blå i cytoplasma med farveløs kerne. Kontrol materiale K2 kontrollerne Farveintensitet Vævstype MB Farvereaktion Svag Middel Kraftig Colon 1 Rød farvereaktion i bunden af slimhindens krypter. 2 Rød farvereaktion i bunden af slimhindens krypter. Lever 1 Ingen farvereaktion 2 Ingen farvereaktion Nyre 1 Blåt cytoplasma i de tubulære celler 2 Blåt cytoplasma i de tubulære celler Tonsil 1 Rødt cytoplasma og blå kerner. 2 Rødt cytoplasma og blå kerner. Fortsættes.. 28
29 Hud 1 Rødt cytoplasma og blå kerner i epidermis. Blå farvereaktion i dermis. 2 Rødt cytoplasma og blå kerner i epidermis. Blå farvereaktion i dermis Cerebellum 1 Ingen farvereaktion 2 Ingen farvereaktion. Malignt Melanom 1 Rød farvereaktion. 2 Rød farvereaktion. Prostata 1 Basalceller: blå kerner og rødt cytoplasma. 2 Basalceller: blå kerner og rødt cytoplasma. Tabel 2: Viser de resultaterne af K2 kontrollerne (Bilag 8), efter farvningen med antistofpoolen. Der indgår 2 kontroller, som er monteret sammen med henholdsvis MB1 og MB2. Alle vævsprøver har parvis opnået samme farvereaktion og samme farveintensitet. Adenoer Tabel 3 nedenfor viser 3 eksempler ud af de 17 AC, der indgik i forsøget (Bilag 9). Når de 17 vævsprøver farves med ASP, kan der observeres røde kerner og cytoplasma med vekslende farve. Som eksempel på en kraftig farveintensitet, er vævsprøve 17 udvalgt. Her ses kraftigt farvet blåt cytoplasma (blå pil) og kraftigt farvede røde cellekerner (rød pil). Som eksempel på en svag farveintensitet, er vævsprøve 1 udvalgt. Der kan observeres røde kerner, som stedvist fremstår med middel farveintensitet (rød pil) og stedvist med svag farveintensitet (sort pil). Derudover kan der stedvist observeres, en meget svag blå cytoplasmafarvning (blå pil). Som eksempel på 2 farvemønstre, der kan observeres ved mange af de 17 AC, er vævsprøve 5 udvalgt. Stedvist kan der observeres røde kerner med rødt cytoplasma (rød cirkel) og stedvist kan der observeres røde kerner, med farveløst cytoplasma (sort cirkel). Derudover præsenterer denne vævsprøve cytoplasma, med en middel farveintensitet (blå pil) 29
30 Vævsprøve Adeno Tabel 3: Viser 3 AC ud af de 17 adenoer, der indgik i forsøget. Alle vævsprøver er afbilledet ved forstørrelse 20x. Røde kerner er anvist med rød pil, blåt cytoplasma er anvist med blå pil. Den sorte pil viser cellekerner, med meget svag farveintensitet. Den sorte cirkel omkranser et område, hvor cytoplasma fremstår farveløse og den røde cirkel omkranser et område med røde kerner og rødt cytoplasma. 30
31 Adenoer, der er svære at identificere Tabel 4 nedenfor viser 2 AC ud af 4 AC, der oprindeligt var svære at identificere (Bilag 9). 1 vævsprøve ud af de 4, fremstår med det farvemønster der knytter sig til PC (omtales senere). 3 vævsprøver ud af de 4 fremstår med det farvemønstre, der knytter sig til AC. Vævsprøve 11 og 26 er udvalgt, da de fremviser 2 forskellige farveresultater. Vævsprøve 11 fremstår med en kraftig farveintensitet, hvorimod vævsprøve 26 fremstår med en svag farveintensitet. Begge vævsprøver fremstår med røde cellekerner (rød pil) og blåt cytoplasma (blå pil). Vævsprøve Antistofpool Tabel 4: Viser 2 vævsprøver, ud af de 4 adenoer, der oprindeligt var svære at identificere. Alle vævsprøver er afbilledet ved forstørrelse 20x Vævsprøve 11 har en kraftig farveintensitet, hvorimod vævsprøve 26 har en svag farveintensitet. Begge vævsprøver fremstår med blåt cytoplasma, anvist af blå pile og røde kerner, anvist med røde pile. 31
32 Planocellulære er Tabel 5 nedenfor viser 3 eksempler ud af de 19 PC, der indgik i forsøget (Bilag 10). Når de 19 patientprøver farves med ASP, kan der observeres blå kerner og rødt cytoplasma. Begge farvereaktioner veksler i farveintensitet. Ved vævsprøve 4 ses kraftigt farvet rødt cytoplasma (rød pil) og blåt farvede kerner. Generelt fremstår kerner, med en middel farveintensitet (sort pil). Enkelte steder fremstår kernerne, med kraftig farveintensitet (blå pil). Som eksempel på et farvemønster, der er observeret i 2 vævsprøver, er vævsprøve 6 udvalgt. Her ses en rød cytoplasmafarvning med middel farveintensitet (rød pil) og en kernefarvning, der udtrykkes, så svagt, at kernerne fremstår farveløse (blå pil). Som eksempel på en vævsprøve med vekslende farveintensitet, er vævsprøve 33 udvalgt. Her ses områder med middel farveintensitet (sort cirkel) og områder med svag farveintensitet (rød cirkel). Vævsprøve Plano 4 6 Fortsættes.. 32
33 33 Tabel 5: Viser 3 PC ud af de 19 planocellulære er, der indgik i forsøget. Alle vævsprøver er afbilledet ved forstørrelse 20x. Blå kerner med vekslende farveintensitet, er anvist med blå pil, rødt cytoplasma med vekslende farveintensitet, er anvist med rød pil. Den sorte pil viser cellekerner, med middel farveintensitet. Den sorte cirkel anviser et område med middel farveintensitet og den røde cirkel anviser et område, med svag farveintensitet. Planocellulære er, der er svære at identificere Tabel 6 nedenfor viser 2 vævsprøver ud af 5 PC, der oprindeligt var svære at identificere (Bilag 10). Alle 5 vævsprøver fremstår med det farvemønster der knytter sig til PC. Vævsprøve 18 og 22 er udvalgt, da de fremviser 2 forskellige farveresultater. Vævsprøve 18 fremstår med kraftigt farvede blå kerner (blå pil) og rødt cytoplasma med veksler farveintensitet. Generelt observeres en middel farveintensitet (rød pil), men stedvist observeres kraftigt farvet cytoplasma (sort pil). Vævsprøve 22 fremstår med blå kerner, der veksler i farveintensitet, fra en middel (blå pil) til svag (Brun pil). Derudover observeres et område, hvor kernerne fremstår farveløse (sort cirkel). Vævsprøven fremstår med svagt rødt cytoplasma (rød pil). Vævsprøve Antistofpool 18 Fortsættes.. 33
34 22 Tabel 6: Viser 2 vævsprøver ud af 5 planocellulære er, der oprindeligt var svære at identificere. Alle vævsprøver er afbilledet ved forstørrelse 20x. De blå pile anviser blå kerner. De røde pile anviser rødt cytoplasma. Den brune pil anviser svagt farvede blå kerner og den sorte pil anviser kraftig farvet cytoplasma. Derudover omkranser den sorte cirkel, et område med farveløse kerner. Afvigende diagnoser Tabel 7 nedenfor viser de 3 patientprøver, hvor de vurderede diagnoser ikke stemmer overens med de oprindelige diagnoser. Vævsprøve 15 er AC, som fremstår med svage røde kerner (rød pil) og middel farvet rødt cytoplasma (blå pil). Vævsprøve 24 er PC, som fremstår med 2 forskellige farvemønstre. Generelt fremstår vævet med blå kerner og rødt cytoplasma (sort pil), men et enkelt sted fremstår vævet med røde kerner og blåt cytoplasma (brun pil). Vævsprøve 27 er AC, som fremstår med blå kerner (blå pil) og rødt cytoplasma (rød pil), som er det farvemønster, der knytter sig til PC. Vævsprøve Antistofpool 15 Fortsættes.. 34
35 24 27 Tabel 7: Viser 3 vævsprøver, hvor diagnosen stillet ud fra antistofpollen, ikke stemmer overens med den oprindelige diagnose. Alle vævsprøver er afbilledet ved forstørrelse 20x. De røde pile anviser rød farvereaktion, som ved adeno (AC) lokaliseres i kernerne og i cytoplasma ved plano (PC). De blå pile anviser blå farvereaktion, som lokaliseres i cytoplasma ved AC og i kernerne ved PC. I 2-delt væv anviser den sorte pil område med blå kerner og rødt cytoplasma og den brune pil anviser område med røde kerner og blåt cytoplasma. Samlede vurderinger Tabel 8 nedenfor viser en oversigt over hvilke diagnoser, der er anvendt og hvor hyppigt. De oprindelige diagnoser opdeles med 17 AC og 19 PC. Alle 3 studerende har vurderet at 15 vævsprøver var AC, 20 vævsprøver var PC og 1 var både AC+PC. 35
36 Vævstype Oprindelig diagnose Studerende 1 Studerende 2 Studerende 3 AC PC AC+PC Tabel 8: Viser hvilke diagnoser, der er anvendt i forsøgt og hvor hyppigt. Oprindeligt er der 17 adenoer (AC) og 19 planocellulære er (PC). De 3 studerende har diagnosticeret 15 AC, 20 PC og 1 AC+PC. Sensitivitet og specificitet I tabel 9 nedenfor, ses hvilke tal der anvendes til beregningen af sensitiviteten og specificiteten til AC. Ud af de oprindelige 17 AC, diagnosticerede de studerende 15 AC, som indgår i beregningerne, som sandt positive. De resterende 2 AC indgår, som falsk negative. Ud af de 19 PC, diagnosticerede de studerende 19 PC, som indgår i beregningerne, som sandt negative for AC. Som kontrol, der er udført en summering af det antal prøver, der indgår i beregningerne. Her opnås et total på 36 prøver. AC Ikke AC Total Positiv 15 (Sandt positiv) 0 (Falsk positive) 15 Negativ 2 (Falsk negative) 19 (Sandt negative) 21 Total Tabel 9: Viser fordelingen af de vurderinger, der er udført af de studerende. Sandt positiv:15 patientprøver. Falsk negativ: 2 patientprøver. Sandt negativ: 19 patientprøver. Beregningerne er udført på et totalt antal af 36 patientprøver. 36
37 I tabel 10 nedenfor ses hvilke tal der danner grundlag for beregningerne af sensitiviteten og specificiteten til PC. Ud af de oprindelige 19 PC, diagnosticerede de studerende 19 PC, som indgår i beregningerne, som sandt positive. Ud af de 17 AC, diagnosticerede de studerende 15 AC, som indgår i beregningerne, som sandt negative for PC. Ud af de 17 AC, blev 2 prøver diagnosticeret som PC, og indgår som falsk positive. Som kontrol, der er udført en summering af det antal prøver, der indgår i beregningerne. Her opnås et total på 36 prøver. PC Ikke PC Total Positiv 19 (Sandt positiv) 2 (Falsk positive) 21 Negativ 0 (Falsk negative) 15 (Sandt negative) 15 Total Tabel 10: Viser fordelingen af de vurderinger, der er udført af de studerende. Sandt positive: 19 patientprøver. Falsk positive: 2 patientprøver. Sandt negative: 15 patientprøver. Beregningerne er udført på et totalt antal af 36 patientprøver. Tabel 11 nedenfor viser den beregnede sensitivitet og specificitet, som blev gennemgået i metode afsnittet. Diagnosticering af AC har en sensitivitet på 88,24 % og en specificitet på 100 %. Diagnosticering af PC har en sensitivitet på 100 % og en specificitet på 88,24 %. Vævstype Sensitivitet Specificitet AC 88,24 % 100 % PC 100 % 88,24 % Tabel 11: Viser sensitivitet og specificitet for henholdsvis adeno (AC) og plano (PC). 37
38 Farvereaktioner Tabel 12 nedenfor viser hvilke farvemønstre der er observeret ved de 36 patientprøver. Ud af de 17 AC, der indgik i forsøget er 9 prøver observeret med dobbeltfarvningen; røde kerner og blåt cytoplasma. 2 prøver er observeret med dobbeltfarvningen; røde kerner og rødt cytoplasma. 2 prøver er observeret med røde kerner og stedvist rødt cytoplasma og stedvist blåt cytoplasma. Ved 3 prøver ud af 17 AC observeres kun røde kerner og 1 prøve fremstår med blå kerne og rødt cytoplasma. Ud af de 19 PC, der indgik i forsøget er 17 prøver, observeret med dobbeltfarvningen; blå kerner og rødt cytoplasma. Ved 2 patientsprøver registres kun rødt cytoplasma. Røde kerner og blåt cytoplasma Røde kerner og rødt cytoplasma Røde kerner og rødt + blåt cytoplasma Kun røde kerner Kun blåt cytoplasma Blå kerner og rødt cytoplasma Kun blå kerne Kun rødt cytoplasma 17 AC (52,9 %) (11,8 %) (11,8 %) (17,6 %) (5,9 %) 19 PC (89,5 %) 0 2 (10,5 %) Tabel 12: Viser opgørelse over hvilke farvereaktioner, der er observeret i forsøget. De 17 adenoer (AC), der indgik i forsøget, blev fordelt på 5 forskellige farvemønstre. De 19 planocellulære er (PC), der indgik i forsøget, blev fordelt på 2 farvemønstre. Koncentration i antistofpool Tabel 13 nedenfor viser sammenligning mellem ASP og 3 af de anvendte immunhistokemiske markører. De individuelle farvninger er udført på AKPs immunhistokemiske system; Ventana Benchmark ULTRA (Ventana ). Som eksempel på anti-p63 er vævsprøve 16 udvalgt. Anti-p63 er en kernefarvning, som med ASP fremstår med vekslende farveintensitet. Den blå pil anviser kraftigt farvede kerner. Når anti-p63 farves individuelt ses en brun kerne farvning med vekslende farveintensitet. De kerner med kraftigst farveintensitet er anvist med en blå pil. Som eksempel på anti-ttf-1 er vævsprøve 4 udvalgt. Anti-TTF-1 er en kernefarvning, som med ASP fremstår med middel til kraftigt farvede røde kerner (rød pil), Når anti-ttf-1 farves individuelt ses en kraftig brun kernefarvning (rød pil). Som eksempel på anti-napsin-a er vævsprøve 28 udvalgt. Antinapsin-A er en cytoplasma farvning, som med ASP fremstår blå, med middelfarveintensitet (blå 38
39 pil). Når anti-napsin-a farves individuelt ses brun cytoplasma farvning (sort pil) og en kobber farve, der dækker store dele af vævet (sort cirkel). Antistofpool Individuel markør Anti-p63 (Kerne) Anti-TTF-1 (Kerne) Anti- Napsin-A (Cytoplasma) Tabel 13: Viser sammenligningen mellem farvningen med antistofpoolen (ASP) og 3 markører farvet på afdelingens apparatur; Ventana. Alle vævsprøver er afbilledet ved forstørrelse 20x. De blå pile anviser positivt p63, som farves blåt med ASP og brunt ved Ventana. De røde pile anviser positivt TTF-1, som farves rødt med ASP og brunt ved Ventana. De sorte pile anviser positivt Napsin-A, som farves blåt med ASP og brunt ved Ventana. Den sorte cirkel anviser et område, med kubber farve. 39
40 Nekrotisk væv Tabel 14 nedenfor viser 5 farvemetoder, udført på vævsprøve 15. De individuelle markører er udført på Ventana. Ved ASP observeres rødlige kerner (rød pil) og rødt cytoplasma (brun pil). Ved HEfarvening observeres lilla kerner (lilla pil) og røde vævstrukture (pink pil). Når anti-ttf-1 farves individuelt observeres enkelte brune kerner med kraftig farveintensitet (rød pil). Når anti-napsin-a farves individuelt observeres stedvist brunt cytoplasma, med kraftig farveintensitet (orange pil). Når anti-p63 farves individuelt observeres enkelte brune kerner, med middel farveintensitet. Antistofpool HE-farvning TTF-1 Napsin-A P63 Tabel 14: Viser 5 farvemetoder, udført på vævsprøve 15. Alle vævsprøver er afbilledet ved forstørrelse 20x Rød pil anviser røde kerner. Brun pil anviser rødt cytoplasma. Lille pil anviser lilla kerner. Pink pil anviser røde vævsstrukturer. De blå pile anviser brune kerner. Orange pil anviser brunt cytoplasma. Reproducerbarhed Tabel 15 nedenfor viser 3 af de 36 vævsprøver, der indgik i forsøget. Der er udført 2 adskilte farvninger, hvor alle 36 vævsprøver er farvet med den sammensatte ASP. Når de 36 vævsprøver gennemgås for de 2 farvninger, ses samme reaktionsmønster. Vævsprøve 5 er et AC, med røde kerner (rød pil) og blåt cytoplasma (blå pil). Derudover kan der observeres et område (sort cirkel), 40
41 der er bedre repræsenteret ved 1. farvning i forhold til 2. farvning. Vævsprøve 4 er et PC, med rødt cytoplasma (rød pil) og blå kerner (blå pil). Der kan observeres et område af vævsprøven, som ved 1. farvning er godt repræsenteret og ved 2. farvning, er mindre godt repræsenteret (sort cirkel). Vævsprøve 13 er et AC, med røde kerner (rød pil) og ingen cytoplasma farvning. Der kan observeres normalt væv (sort pil). Vævsprøve 1. farvning 2. farvning Tabel 15: Viser 3 ud af de 36 vævsprøver der indgik i forsøget. Alle vævsprøver er afbilledet ved forstørrelse 20x. Vævsprøve 5 og 13 er AC og vævsprøve 4 er et PC De røde pile anviser rød farvereaktion, som lokaliseret i kerne ved AC og i cytoplasma ved PC. De blå pile anviser, som lokaliseres i cytoplasma ved AC og i kernerne ved PC. De sorte cirkler anviser et område, hvor mængden af farvede celler ikke stemmer over ens. Den sorte pil anviser normalt væv. 41
42 Diskussion I det følgende diskussions afsnit anvendes forkortelsen; BA, for det udførte forsøg, med antistofpoolen (ASP). Denne forkortelse anvendes ved sammenligning med resultater fra andre studier. Test af antistofpool Tabel 1 viser resultaterne fra den udførte test af antistofpoolen (ASP). Når ASP anvendes på normalt lungevæv, kan der observeres de farvereaktioner teorien beskrev. Cellekernerne er farvet kraftigt røde og er tydeligt afgrænsede. Da kernerne er farvet røde, stemmer resultatet godt overens med teorien om at TTF-1 farves rødt og er lokaliseret i kernerne. Cytoplasma er farvet svagt blåt, hvilket ikke var helt forventet. Flere studier (6,8) har fremvist illustrationer, samt billeder hvor cytoplasmafarvningen fremstår kraftigt og heldækkende, hvorimod det opnåede resultat fremviser en stedvist granulær farvning. Den blå cytoplasmafarvning, stemmer overens med teorien om at napsin-a farves blåt og er lokaliseret i cytoplasma. Den blå cirkel omkranser en celletype, der har kunnet observeres i alle 3 vævstyper der indgik i testen. Ifølge teorien vil makrofager fremstå Napsin-A positive (11), hvilket stemmer godt overens med, at farvereaktionen er blå og at den er lokaliseret i cytoplasma, og da celletypen kunne observeres ved alle 3 vævstyper, taler det for at det er makrofager. Når et adeno (AC), farves med ASP, kan der observeres røde cellekerner, som tydeligt adskilles fra det omkringliggende blå cytoplasma. Denne farvereaktion stemmer godt overens med teorien om TTF-1 og napsin-a, som beskrevet ovenfor. De celletyper der fremstår med rødt cytoplasma, stemmer ligeledes overens med det forventede, da både CK5 og CK14 kan være positive i % af cellerne i AC. Dog er farvereaktionen så svag, at det må forventes at det kun er en af de 2 markører, der er positiv i dette tilfælde. Kombinationen af røde kerner og blåt cytoplasma giver en god genkendelse og kan nemt differentieres til AC, hvorimod kombinationen af røde kerner og rødt cytoplasma giver en mindre sikker genkendelse, da cellekerne og cytoplasma kan fremstå som en helhed og ikke adskilte strukturer. Når et plano (PC), farves med ASP, observeres et kraftigt farvet rødt cytoplasma. Når farvereaktionen er rød og er lokaliseret i cytoplasma henvises til CK5 og CK14, hvilket kan bekræfte teorien. Når kerner observeres, ses en meget svag farvning, som ikke tydeligt adskiller 42
43 kernerne fra det omkringliggende cytoplasma. Denne farvereaktion kan skyldes at p63 svækkes i ASP, men kan også være et resultat af fejl ved afpipettering, hvor der enten er udtaget et for lille volumen af anti-p63 eller et for stor volumen af CK5 og CK14. Begge afpipetteringsfejl vil kunne medfører overskud af CK5 og CK14, hvorved p63 domineres. Ved de negative kontroller, kan der ikke observeres uspecifikke bindinger. Vævet fremstår med lyse vævsstrukturer, hvilket opstår ved lyset i mikroskopet og ikke på baggrund af en farvereaktion. På baggrund af de gennemgåede resultater, kan der sættes tvivl om, hvorvidt koncentrationsforholdet mellem de 5 antistoffer er korrekt. Dog kan det svage udtryk af p63, skyldes en afpipetteringsfejl, hvilket må revurderes, når ASP anvendes på multiblokkene. Resultaterne bekræfter teorien om de farvereaktioner, der knyttes til de forskellige vævstyper og da der ikke er observeret uspecifikke bindinger, må det kunne konkluderes, at hvis farvereaktioner i de 36 patientprøver varierer, kan det ikke skyldes ASP, men derimod biologien i de individuelle cancere. Kontrol materiale Tabel 2 fremviser de farvereaktioner, der blev observeret ved K2 kontrollerne. Alle 8 vævsprøver fra de 2 kontroller, fremstod parvis med samme farvereaktion, hvor farverne lokaliseres til samme vævskomponenter. Derudover observeres samme farveintensitet i alle parvise reaktioner (Bilag 8). Da kontrolsnittene er monteret sammen med henholdsvis MB1 og MB2 må det, kunne udledes at de 2 multiblokke, har gennemgået samme behandling, og at de små variationer, der evt. har været, ikke har haft betydning for det endelige resultat. Dermed må det kunne konkluderes, hvis farvereaktioner varierer, mellem patientprøverne i de 2 multiblokke, kan variationen ikke skyldes forskellig behandling, men derimod biologien i de individuelle cancere. Adenoer Tabel 3 præsentere 3 udvalgte patientprøver med AC, som repræsenterer de forskellige farvereaktioner, der kunne observeres ved de 17 AC der indgik i BA (Bilag 9). Når et AC fremstår med en middel til kraftig farveintensitet, som vævsprøve 17, er der tydelige fordele ved anvendelse af en ASP. Både cellekerner og cytoplasma kan hurtigt lokaliseres, ved hjælp af farveforskellen. Når cytoplasmafarvningen fremstår svag eller farveløs, såsom vævsprøve 1, giver anvendelsen af en ASP, ikke samme tydelige differentiering af AC. Ved vævsprøve 5 anviser den røde cirkel, celler med rød farvereaktion, og her kan der tvivles på, hvorvidt det er en kernefarvning af anti-ttf-1, 43
44 eller en cytoplasma farvning af anti-ck5 og/eller anti-ck14, der kan observeres. Dette ville ikke være et problem, hvis antistofferne var farvet hver for sig, da en positiv reaktion, kun vil kunne knyttes til det antistof, der er farvet med. Ved vævsprøve 5 omkranser den sorte cirkel, celler der har røde kerner og ingen cytoplasmafarvning. I sådanne tilfælde giver anvendelsen af en ASP hverken en fordel eller en ulempe, da det er samme resultat, som hvis anti-ttf-1 var farvet for sig selv. Adenoer, der er svære at identificere Ud af de 17 AC, der indgik i BA, var 4 udvalgt på baggrund af, at de oprindeligt var svære at identificere (Bilag 9). De 2 vævsprøver i tabel 4, er udvalgt fordi de repræsentere 2 forskellige farveresultater. Ved vævsprøve 11 kan der observeres middel til kraftig farveintensitet ved begge farvereaktioner. Farvningen skelner tydeligt mellem kerner og cytoplasma. Vævsstrukturen er velbevaret, da det tydeligt kan ses, at canceren danner forgrenede strukturer, som kendetegner en kirtel. Denne vævsprøve betragtes ikke som svært at identificere, hvormed det må udledes, at ASP har bidraget med brugbart til differentieringen. Ved vævsprøve 26, kan der kun observeres enkelte farvede celler, med svag farveintensitet. På trods af, at der kun kan observeres enkelte farvede celler, skelner farvningen tilstrækkeligt mellem kerner og cytoplasma. Det kan diskuteres, hvorvidt disse celler kan kaldes et godt grundlag for diagnosticering, men en biopsi, som normalvis anvendes til udredning af LC, kan risikere ikke at indeholde flere celler, eller bedre farvede celler, end hvad der ses ved vævsprøve 26. Og da cellerne fremstår med tilstrækkelig farvereaktion, må det udledes at ASP med har bidraget til differentieringen. Selvom visse farvereaktioner kan fremstå tvivlsomme ved AC, er det en fordel ved ASP, at kunne bedømme flere antistoffer på samme snit, da dette generelt giver en god adskillelse af cellekerne og cytoplasma ved AC. Sensitivitet og specificitet Tabel 8 viser en opsummering af de vurderinger, der er foretaget på de 36 patientprøver (Bilag 9 og 10). Når de opnået resultater sammenlignes med de oprindelige diagnoser, ses en god overensstemmelse. Der er 17 patientprøver, der oprindeligt er vurderet til AC, og ud af de 17, er der fundet 15 patientprøver. På baggrund af de viste tal i tabel 9, er sensitiviteten og specificiteten udregnet. Som anvist i tabel 11 fremkommer en sensitivitet på 88,24 % og en specificitet på 100 %. Metoden har en rigtig god specificitet, hvilket betyder at den er god til at diagnosticere dem, der 44
45 ikke har AC. Metoden er derimod ikke så god til at diagnosticere dem der har AC, da (100 % - 88,24 %) 11,76 % af patientprøverne blev fejldiagnosticeret. I vores forsøg omhandler det 2 patientprøver, men hvis sensitiviteten er repræsentativ, vil det svare til, at der for hver 1000 patienter med AC, fejldiagnosticeres ( ,76 / 100) 117 patienter. Dette er en stor del af det samlede antal. Dog kan der stilles spørgsmålstegn ved de vurderede diagnoser, som danner grundlag for den udregnede sensitivitet. I vores forsøg er patientprøve 15 og 27 fejldiagnosticeret. Vævsprøve 27 fremstår med blå kerner og rødt cytoplasma og kan efter den læste litteratur kun vurderes som PC (omtales senere). Men vurderingsresultatet ved patientprøve 15 kan diskuteres, da cellerne fremstår med røde kerner og/eller rødt cytoplasma (omtales senere). Hvis den vurderede diagnose for vævsprøve 15 ændres, vil dette medføre en langt bedre sensitivitet på (16 / ) = 94,12 %. Med denne sensitivitet vil der for hver 1000 patienter med AC, fejldiagnosticeres (1000 5,88 / 100) 59 patienter. Yanagita,E. et al. (8) har undersøgt 39 AC og har opnået en sensitivitet på 97,4 % og en specificitet på 100 %, hvilket er sammenlignelig med sensitiviteten og specificiteten fra BA. Hermed må det kunne udledes, at de anvendte patientprøver repræsenterer variationerne indenfor AC, hvilket sandsynliggør korrektheden af resultaterne fra BA til subklassifikation af AC. Farvereaktioner Som det fremgår af tabel 12 er der opnåede lidt forskellige farvereaktioner, når de 17 AC behandles med den sammensatte ASP. 52,9 % svarende til 9 prøver, fremstår med det forventede farvemønster der knytter sig til AC. Derudover ses 7 prøver, der har opnået den forventede røde kernefarvning, hvoraf 2 prøver fremstod med rødt cytoplasma, 2 vævsprøver med dobbelt cytoplasma farvning, og 3 prøver uden cytoplasma farvning. Der blev observeret 1 prøve med farvemønsteret der knytter sig til PC. Yanagita,E. et al. (8) har ligeledes, registret opnåede farvereaktioner ved AC. Studiet har observeret 33 vævsprøver, svarende til 84,6 %, med det fuldstændige farvemønster der knytter sig til AC. Derudover er der registreret 4 prøver der kun er positive for kernefarvningen, samt 1 prøve hvor cytoplasma farvningen er eneste farvereaktion. Dette reaktionsmønster har ikke kunnet genfindes i resultaterne ved BA. I studiet har de opnået et blandings resultat som de kalder ikke informativt. I BA blev der observeret flere blandings resultater, som fremstod med røde kerner og rødt cytoplasma. 45
46 Når resultaterne fra Yanagita,E. et al. (8) sammenholdes med resultaterne fra BA, kan det tyde på, at der findes mange varierende farvemønstre for AC, hvilket gør det svært at fastslå et enkelt farvemønster, der er konkret for denne cancertype. Plano Tabel 5 præsentere 3 udvalgte patientprøver med PC, som repræsenterer de forskellige farvereaktioner der kunne observeres ved de 19 PC, der indgik i BA (Bilag 10). Selvom der kan observeres forskel i farveintensiteten i de forskellige vævsprøver, giver anvendelsen af ASP en stor fordel ved differentiering af PC. Ved vævsprøve 4 og 6, kan der tydeligt skelnes mellem cellekerner og cytoplasma, hvilket giver et valid grundlag for differentiering af PC. Ved vævsprøve 33 anviser den røde cirkel et område hvor farveintensitet er meget svag. Dette område kan være vanskeligt at vurdere, da farvereaktionerne kun tilstrækkeligt kan adskilles, hvilket nævnes som en ulempe. Planocellulære er, der er svære at identificere Ud af de 19 PC, der indgik i BA, var 5 udvalgt på baggrund af, at de oprindeligt var svære at identificere (Bilag 10). De 2 vævsprøver i tabel 6, er udvalgt fordi de repræsenterer 2 forskellige farveresultater. Ved vævsprøve 18 kan der observeres middel til kraftig farveintensitet ved begge farvereaktioner. Farvningen skelner tydeligt mellem kerner og cytoplasma, samt præsentere vævsstrukturen overskueligt. Ved vævsprøve 22 omkranser den sorte cirkel et område med farveløse kerner, her foregår differentiering udelukkende på cytoplasmafarvningen. I det resterende væv kan der observeres farvereaktioner, der tilstrækkeligt skelner mellem cellekerner og cytoplasma. Disse 2 vævsprøver betragtes ikke, som svære at identificere efter farvning med ASP, hvormed det må udledes at ASP har bidraget med brugbar differentiering af PC. Selvom visse dele af vævsprøverne kan fremstå med tvivlsomme farvereaktioner, er det ligesom ved vurdering af AC, en fordel ved ASP, at kunne bedømme flere antistoffer på samme snit, da dette giver en god adskillelse af cellekerne og cytoplasma ved PC. Sensitivitet og specificitet Tabel 8 viser en opsummering af de vurderinger der er foretaget på de 36 patientprøver (Bilag 9 og 10). Når de opnåede resultater sammenlignes, med de oprindelige diagnoser, ses en rigtig god overensstemmelse. Der er 19 patientprøver der oprindeligt er vurderet til PC, og alle disse er 46
47 diagnosticeret i BA. På baggrund af de viste tal i tabel 10 er sensitiviteten og specificiteten beregnet. Som anvist i tabel 11 fremkommer en sensitivitet på 100 %, en specificitet på 88,24 %. Metoden har en rigtig god sensitivitet, hvilket betyder at den er god til at diagnosticere dem der har PC. Metoden er derimod ikke så god til at diagnosticere dem der ikke har PC. Dette stemmer også godt overens med de opnåede resultater for AC, da de patientprøver, der indgår i beregningerne, som 'ikke PC' er dem der har AC. Yanagita,E. et al. (8) har undersøgt 25 PC og har opnået den samme sensitivitet på 100 % og har opnået en specificitet på 100 %. Da resultaterne fra BA og Yanagita,E. et al. (8) stemmer godt overens, sandsynliggøres korrektheden af de opnåede resultater fra BA til subklassifikation af PC. Farvereaktioner Som det fremgår af tabel 12, er der opnåede enkelte variationer i farvereaktioner, når de 19 PC behandles med den sammensatte ASP. 89,5 % svarende til 17 prøver, fremstår med det forventede farvemønster, der knytter sig til PC. Derudover ses 2 patientprøver, der kun har opnået den forventede røde cytoplasma farvning. Ved forsøget er der ikke i forbindelse med PC, registret nogle blandings farvereaktioner eller farvereaktioner der knytter sig til AC. Yanagita,E. et al. (8) har ligeledes, registret opnåede farvereaktioner ved PC. I studiets tabel 3 er der opstået en tastefejl under kolonnen +/+. Der er observeret 22 vævsprøver (ikke 25), svarende til 88 %, med det fuldstændige farvemønster, der knytter sig til PC. Studiet har registreret 1 vævsprøve, der kun er positiv for cytoplasmafarvningen, samt 2 prøver, hvor kernefarvningen er den eneste farvereaktion. Dette reaktionsmønster har ikke kunnet genfindes i resultaterne ved BA. Når resultaterne fra Yanagita,E. et al. (8), sammenholdes med resultaterne fra BA, kan det tyde på, at der findes få varierende farvemønstre for PC, hvilket gør det nemt at fastslå et enkelt farvemønster, der er korrekt for denne cancertype. Afvigende diagnoser Tabel 7 viser de 3 vævsprøver, hvor de vurderede diagnoser, ikke stemmer overens med de oprindelige diagnoser. Vævsprøve 15 oplyses som et AC, men alle 3 studerende har vurderet at prøven var et PC (Bilag 9). Vævsprøven fremstår kun med rød farvereaktion. Når de enkelte celler iagttages, er det svært at vurdere hvorvidt farvereaktionen er lokaliseret i kernerne eller om der er 47
48 tale om en cytoplasmafarvning. Alle 3 studerende har vurderet at farvereaktionen var lokaliseret i cytoplasma, svarende til et PC. Ved denne vævsprøve, har anvendelsen af ASP ikke vævet en fordel, da det er svært at skelne mellem kerne og cytoplasma. Havde de anvendte markører været farvet hver for sig, ville der ikke være tvivl om, hvilken markør der var farvet positivt på det pågældende snit. Ud fra farvningen med ASP, vil man kun kunne konkludere at det er et stor-cellet og at der er brug for yderligere undersøgelser for at kunne differentiere patientprøven. Vævsprøve 24 oplyses som et PC, men alle 3 studerende har vurderet at prøven indeholdte både AC og PC. Vævsprøven dominerede af den farvereaktion (rødt cytoplasma/blå kerner), som knytter sig til PC. Det anviste område, hvor cellerne fremstår med røde kerner og blåt cytoplasma (blå pil), kan diskuteres hvorvidt dette er normalt væv. Området ser meget velafgrænset ud og kunne evt. være en bronkie. Vævsprøve 24 indeholder mange makrofager, som fremstår med blåt cytoplasma og farveløse kerner. Disse celler har evt. påvirket diagnosticeringen, hvor de er vurderet som AC celler; positive for napsin-a og negative for TTF-1. Efter nærmere undersøgelse kan diagnosen AC ikke fastholdes og vurderingen er her fejlagtig. Fejldiagnosen skyldes ikke ASP, men må tillægges manglende erfaring hos de 3 studerende. Vævsprøve 27 oplyses som et AC, men fremstår med blå kerner og rødt cytoplasma, hvilket er det farvemønster der knyttes til PC. Efter revurdering, dobbelttjek af den anvendt vævsblok, samt tjek af udstansning, må diagnosen AC fastholdes og fejlen kan ikke identificeres. Denne cancer fremstår ikke som forventet, da den har opnået modsat farvereaktion, end hvad der ellers kan observeres ved AC og denne reaktion kan ikke forklares. Det må nævnes at de anvendte udstansninger, kun er et lille uddrag af en stor tumor. Og i dette tilfælde er udstansningen, ikke repræsentativ for tumorens helhed. Det kan heraf udledes, at ingen immunhistokemisk markører er 100 % valide, men et positivt eller et negativt resultat, taler for en bestemt diagnose, og resultatet skal indgår, som en del af et større beslutningsgrundlag. Epitop demaskering Lauridsen,J.L. et al. (6) anvender en ASP, der indeholder de samme 5 antistoffer, som ASP ved BA. Lauridsen,J.L. et al. (6) fremviser i figur 3 et farveresultat for et AC, og i figur 2 fremvises et farveresultat for et PC. Det må antages at de udvalgte billeder repræsenterer de farveresultater, der opnås ved Patologisk Institut ved Regionshospitalet Holstebro (PIRH). Resultatet fra figur 3 (6), stemmer godt overens med de farveintensiteter, der blev observeret ved AC i BA, dvs. kraftigt røde 48
49 kerner og diffust blåt cytoplasma. Resultatet fra figur 2 (6) stemmer ikke overens med de opnåede resultater ved PC i BA, da der ved BA er opnået et modsat resultat, i forhold til farveintensiteten. Anti-p63 observeres meget kraftig i figur 2 (6), hvorimod anti-p63 er observeres med vekslende farveintensitet ved BA. Derimod kan der observeres en langt kraftigere og mere udbredt cytoplasma farvning ved PC i BA, end der er opnået ved PIRH, hvor der kan observeres en diffus og stedvist farvning. Denne tydelige forskel, kan skyldes forskellig epitop demaskering. Epitop demaskering er et vigtigt trin i det immunhistokemiske analyseprincip. Hvis dette trin ikke udføres korrekt, vil epitoperne være maskerede, hvormed antigenerne evt. ikke vil kunne indgå i en antigen-antistof reaktion. Til BA er der anvendt EDTA buffer med en ph på 8,0 til epitop demaskering. Lauridsen,J.L. et al. (6) beskriver at de anvender apparaturet PT-Link fra Dako (20), som anvender en 3 i 1 buffer; Target Retrieval Solution ph 9 (23), som er en Tris/EDTA buffer, der udfører afparaffinering og epitop demaskering i samme trin (6,23). Selvom det ikke er helt den samme epitop demaskering, anvendes EDTA i begge opsætninger, dog med forskellig ph, hvilket evt. kan medfører forskel i resultaterne. Producenterne af antistofferne; anti-ttf-1, anti-p63, anti-ck5 og anti-ck14, oplyser ikke, hvilket epitop demaskering de anbefaler (14-17). Hermed vides det ikke, hvorvidt de observerede farveforskelle mellem PIRHs PC (figur 2 (6)) og resultaterne fra PC ved BA, skyldes forskellig demaskering. Anti-napsin-A er produceret af Novocastra og ifølge det medfølgende data sheet, oplyser producenten (på side 3), at de anbefaler anvendelse af en buffer med en ph på 6 (18). Dette kan forklare de svage farveresultater, der er opnået med anti-napsin-a ved AC, ved både BA og PIRH (figur 3 (6)), da de anvendte bufferers ph på henholdsvis 8,0 og 9,0 (23), hvilket kan have været for højt til anti-napsin-a. AKP anvender anti-ttf-1, anti-p63 og anti-napsin-a i rutinen, hvilket gør det muligt, at sammenholde resultaterne fra ASP med resultater, fra de 3 immunhistokemiske markører, når de farves hver for sig. Ventana anvender reagenset Cell Conditioning 1 (CC1) (24), til epitop demaskering. Ventana oplyser ikke indholdsstofferne i CC1, hvormed det ikke vides hvilken buffer, der er anvendt til epitop demaskering. Dog oplyses det på side 5, i det tilhørende data sheet, at CC1 har en ph på 8,5 (24). Da Ventana anvender ph 8,5 og PIRH anvender ph 9, må det kunne udledes, at det ikke var fejlagtigt, at anvende en buffer med ph 8,0, men det bør undersøges, om der kan opnås bedre resultater, ved anvendelse af anden epitop demaskerings buffer. 49
50 Antistofpoolen Andre studier anvender anti-ck5/6 og opnår gode resultater ved differentiering af NSCLC (25,26). I BA anvendes anti-ck5, klon EP1601Y fra producenten; Cell Marque, som oplyser at CK5 er positiv i næsten alle PC, hvilket gør CK5 til en meget sensitiv markør for PC (15). En anden antistofproducent; Biocare MEDICAL, oplyser at CK5 er en mere sensitiv og specifik markør for PC end CK5/6 (27), da CK5 har en sensitivitet på 84 % og en specificitet på 100 %, hvorimod CK5/6 har en sensitivitet på 80 % og en specificitet på 97 %. Hvorvidt CK5 er mere sensitiv markør for PC end CK5/6, kan dette forsøg ikke afklare, men kombinationen af CK5 og CK14 kan noteres, som farvereaktion ved samtlige 19 PC der indgik i BA, hvormed der opstår en sensitivitet på 100 %. I BA anvendes anti-ck14, klon SP53, fra samme producent; Cell Marque. Producenten oplyser at anti-ck14 er meget brugbar til identifikation af PC og især ved lavt differentierede tumorer (16). Dette vil evt. kunne forklare at visse vævsprøver med PC, fremstår med svag farvereaktion og andre med kraftig farvereaktion, som præsenteret i tabel 5. Hvis de PC, der er svagt farvet, er så lavt differentieret, at de kun udtrykkes CK14 i cytoplasma, må farven blive mindre intens, end ved et højt differentieret PC, hvor både CK5 og CK14 udtrykkes. CK5/CK14 farveintensitet Yanagita,E. et al. (8) har, som tidligere nævnt, undersøgt 4 af de antistoffer, som der er medtaget i den sammensatte ASP. Yanagita,E. et al. (8) præsentere i figur 4 en farvereaktion for et PC og man må forvente at dette udvalgte billede repræsentere de opnåede resultater. Sammenlignes dette billede med de farvereaktioner, der blev observeret ved PC i BA (Tabel 5 og 6), ses en tydelig forskel. Yanagita,E. et al. (8) opnår en kraftig blå kernefarvning med anti-p63, hvorimod kernefarvning i BA generelt fremstår med svag farveintensitet. Omvendt kan det siges resultaterne fra BA fremstår med en kraftigere og mere udbredt cytoplasma farvning, end hvad der kan observeres i Yanagita,E. et al. figur 4 (8), hvor der ses en diffus cytoplasmafarvning. Denne sammenligning kan tyde på at brugen af både anti-ck5 og anti-ck14, resultere i en kraftig cytoplasmafarvning, hvilket bekræfter teorien, om at de danner en dimer og farver cytoplasmaet sammen. Men sammenligningerne tyder også på, at den kraftige cytoplasmafarvning fremstår, på bekostning af kernefarvning. Anti-p63 opnår ikke samme farveintensitet i den sammensatte ASP, som resultaterne fra Yanagita,E. et al. (8) fremviser. Denne observering giver anledning til nærmere undersøgelse af koncentrationsforholdet i den sammensatte antistofpool. 50
51 Koncentrationsforholdet i antistofpool Tabel 11 viser hvordan de 3 immunhistokemiske markører; anti-p63, anti-ttf-1 og anti-napsin-a fremstår i ASP og ved adskilt farvning. På trods af farveforskellen (brun og blå) ved anti-p63 og anti-napsin-a kan farveintensiteten alligevel vurderes. Anti-p63 er en kernefarvning, der i ASP er blevet observeret med meget vekslende farveintensitet. Til sammenligningen er vævsprøve 16 udvalgt, fordi denne vævsprøve repræsenterer en kraftig anti-p63 farvning. Som nævnt ovenfor fremstår anti-p63 ikke med samme intensitet i BA, i sammenligning med andre studier. Vurderes anti-p63 alene på vævsprøve 16 kan der observeres samme intensitetsmønster, hvor der stedvist ses en meget svag farvning og stedvist ses en meget kraftigt farvning. Denne variation må knyttes til cancerens biologi. Ved sammenligningen kan der yderligere observeres en tydelig forskel, i den maksimalt opnåede farveintensiteten. Anti-p63 fremstår meget kraftigere ved enkelt farvning end i ASP. Dette tyder på at anti-p63 svækkes i ASP, hvilket er en ulempe. Dog må det nævnes at anti-p63 ikke blev svækkes så markant, at den ikke kunne anvendes til differentiering ved BA. 17 ud af 19 PC fremstod med tydelig blå farvereaktion i kernerne, farvet af anti-p63. Anti-TTF-1 er en kernefarvning, der i BA har farvet 16 vævsprøver ud af i alt 17 anvendte prøver. Til sammenligningen er vævsprøve 4 udvalgt, fordi denne vævsprøve repræsenterer en farveintensitet fra middel til kraftig anti-ttf-1 farvning. Ved sammenligningen kan der observeres en tydelig forskel i intensiteten, hvor anti-ttf-1 fremstår meget kraftigere som enkelt farvning end som en del af ASP. Dette tyder på at anti-ttf-1 svækkes, ligesom anti-p63, når den anvendes i ASP. Dette er en ulempe man skal være opmærksom på, når man anvender ASP til differentiering af NSCLC. Dog må det nævnes at dette ikke var et markant problem i BA. 16 AC ud af de 17 AC der indgik i forsøget, fremstod med tydelige røde kerner, farvet af anti-ttf-1. Anti-napsin-A er en cytoplasmafarvning, der i BA har farvet 11 AC ud af de 17 AC, der indgik i forsøget. De fleste patientprøver fremstår med svag farvning af anti-napsin-a, hvilket tyder på en markant svækkelse af dette antistof når det anvendes ASP. Til sammenligningen er vævsprøve 28 udvalgt, fordi denne vævsprøve repræsenterer en svag anti.napsin-a farvning. Vurderes anti-napsin- A alene på vævsprøve 28, kan der observeres en kraftig og mere udbredt farvning af vævet. Denne markante forskel tyder på, at Ventana har en fordel, frem for den sammensatte ASP. 51
52 Når farvemetoden fra Ventana undersøges, kan det udledes at den markante forskel, skyldes deres detektionssystem; OptiView (28), hvilket indebærer en forstærkningsreaktion. Positive reaktioner fremkaldes med farven brun, hvortil der kobles en kobber forstærkning (28). Dette kan forklare de intensitetsforskelle, der blev observeret ved både anti-p63, anti-ttf-1 og anti-napsin-a. Det må konkluderes at farvemetoden fra Ventana har en fordel, frem for den manuelle farvning, ved at kunne forstærke sine positive reaktioner. Denne forstrækning vil ikke være nødvendig ved alle vævsprøver, men ved enkelte tilfælde, såsom vævsprøve 26 (tabel 4), kunne en kraftigere farvereaktion, have bidraget til differentieringen. Fejldiagnoser I BA blev 3 patientprøver fejldiagnosticeret. 3 studier har undersøgt hvorvidt udvalgte immunhistokemiske markører for LC, reagere med andre cancertyper og metastaser. Stoll, M.L. et al (11) har undersøgt anti-napsin-a og anti-ttf-1 på 75 vævsprøver med AC (omtales senere), samt 95 vævsprøver, fordelt på 16 SCLC og 79 forskellige metastaser. Resultaterne viser at anti-napsin-a var negativ i alle SCLC, men farvede positivt ved 4 vævsprøver; 1 clear cell og 3 papillære er. Anti-TTF-1 farvede 13 vævsprøver ud af de 16 SCLC, der indgik i forsøget, samt 2 lavt differentierede PC og 2 metastaser fra stor-cellede neuroendokrine er. Metastaser fra bl.a. bryst var negativ for begge markører. Masai, K. et al. (25) har undersøgt en række markører for NSCLC på 227 vævsprøver, der var fordelt på 52 carcinoide tumorer (CT), 106 stor-cellede neuroendokrine er (NEC) og 69 SCLC. Studiet har bl.a. inddraget anti-p63, 2 kloner af anti-ttf-1 og anti-napsin-a. Anti-p63 observeres positiv ved 3 CT, 14 NEC og 15 SCLC. Anti-napsin-A blev ikke observeret positiv ved nogen af de inddragede vævsprøver. Anti-TTF-1, klon 8G7G3/1 blev observeret positiv ved 2 CT, 24 NEC og 46 SCLC. Hvorimod klon SPT24 blev observeret positiv ved 12 CT, 50 NEC og 59 SCLC. Bishop, J.A. et al. (29) har undersøgt anti-p63 i forhold til anti-p40. Der er inddraget 81 PC og 237 AC, som er undersøgt for p63 og 205 AC undersøgt for p40. De 81 PC var alle positive for både p63 og p40. Derudover var 74 AC ud af de 237 AC, der indgik i forsøget, positive for p63, hvilket inkluderede 11 højt-, 40 moderat- og 23 lavt differentierede AC. Ud af 205 prøver (som inkluderede de 74 p63 positive prøver), var p40 positivt i 7 prøver. 52
53 Resultaterne fra Stoll, M.L. et al. (11), Masai, K. et al (25) og Bishop, J.A. et al. (29) tyder på at anti-napsin-a med fordel kan anvendes til differentiering af NSCLC, da denne markør ikke reagere med mange andre cancertyper. Ud fra resultaterne må der sættes tvivl ved brugbarheden af anti- TTF-1 og anti-p63, da disse markører farver flere forskellige cancertyper, hvilket kan danne grundlag for fejldiagnoser. Stoll, M.L. et al. (11) oplyser ikke hvilke antistof kloner der er anvendt ved forsøget og Masai, K. et al. (25) anvender ikke samme kloner af anti-napsin-a og anti-ttf-1, som blev anvendt ved BA. Dermed vides det ikke, hvorvidt deres resultater kan kobles til de antistoffer der indgik i ASP. Men både Masai, K. et al (25) og Bishop, J.A. et al. (29), anvender anti-p63, klon A4A, som indgår i BA, hvormed deres resultater kan kobles til antistoffet i ASP. Carcinomer, der er svære at identificere Ifølge årsrapportens opgørelse, kan der observeres et faldende antal patienter, i gruppen med ingen data (1). Dette betyder at cancertyperne i stigende grad kan differentieres. I 2012 var der 192 patienter med en cancertype, der var svære at identificere, hvilket svare til 4,5 % af det samlede antal (1). Årsagerne til den manglende differentiering kendes ikke, men når en cancer er svær at identificere, kan det bl.a. skyldes fejl ved biopsi udtagning, lav differentierings grad (11) og/eller nekrose. Nålebiopsier I forbindelse med udredning af LC, anvender AKP nålebiopsier, som prøvemateriale. Dette betyder at prøvematerialet er meget sparsomt og kan kun indeholde et lille udsnit af den pågældende cancer. I værste tilfælde, indeholder biopsien kun enkelte cancerceller, hvilket stiller store krav til analyse metoden. Sker der fejl ved biopsi udtagningen eller hvis biopsien ikke indeholder celler der kan vurderes, kan dette skabe problemer. Hsiao, S.H. et al. (26), har undersøgt brugbarheden af nålebiopsier til differentiering af NSCLC. Studiet undersøgte 352 nålebiopsier med antistofferne anti-ck5/6, anti-p63 og anti-ttf-1. Prøver uden vævsspecifikke karakteristika og prøver der negative for de 3 anvendte markører, blev identificeret som NSCLC - ikke yderligere specificeret (not otherwise specified = NSCLC-NOS). Ud af de 352 biopsier blev 209 biopsier klassificeret som NSCLC. 197 biopsier, svarende til 94,3 %, blev yderligere opdelt i undertyperne AC, PC, adenosquamøs og stor cellede. 12 biopsier, svarende til 5,7 %, blev klassificeret som NSCLC-NOS, hvilket vurderes 53
54 som et relativt lavt antal (26). Disse resultater stemmer godt overens med de procentvise fordelinger der observeres i Danmark (1). Studiet opnår en sensitivitet på 92,2 % og en specificitet på 100 % og konkluderer afslutningsvis at biopsier er velegnet som prøvemateriale, til klassifikation af NSCLC. Selvom brugbarheden af biopsier kan diskuteres, må det nævnes at biopsiernes størrelse er begrænset af lungernes anatomi. Lungerne risikerer at klappe sammen, hvis der anvendes større nåle, og hertil kan det nævnes, at biopsierne er den bedste løsning, da der ikke findes et tilsvarende alternativ som kan erstatte biopsierne i forbindelse med udredning af LC. Differentieringsgraden Når en cancer er svært at identificere, kan det skyldes en lav differentieringsgrad, da canceren evt. slet ikke udtrykker specifikke karakteristika, såsom morfologi og antigener (11). Stoll, M.L et al. (11), har undersøgt hvorvidt differentieringsgraden påvirker udtrykket af Napsin-A og TTF-1. Studiet har undersøgt 75 prøver, hvor 56 prøver havde fået diagnosen; lavt differentieret med kirtel struktur eller lavt differentieret lignende AC. 19 prøver havde fået diagnosen NSCLC-NOS. Resultaterne viste en fordeling på 28 AC og 47 metastaser. Ud af de 28 AC der indgik, blev 16 prøver positive for både anti-napsin-a og anti-ttf-1, 4 prøver var kun positive for anti-ttf-1 og 8 prøver var negative for begge markører. Resultater fra Stoll, M.L. et al. (11) stemmer godt overens med de resultater, der blev observeret i BA (tabel 10). Studiet opnåede 57 % (16 ud af 28) (11) og BA opnåede 52,9 % (9 ud af 17), der var positive for begge markører. Anti-TTF-1 var fraværende i 29 % af studiets prøver, hvorimod antinapsin-a var fraværende i 12 prøver ud af 28. Dette svare til (( 12 / 28 ) 100) 43 %. I BA var anti-ttf-1 fraværende i (( 1 / 17) 100 ) 6 %, hvorimod anti-napsin-a var fraværende i (( 6 / 17 ) 100) 35 % af prøverne (Se tabel 10). Resultaterne fra både Stoll, M.L. et al. (11) og BA tyder på at både TTF-1 og Napsin-A påvirkes af differentieringsgraden. Derudover kan det tyde på at napsin-a påvirkes mere end TTF-1. Dog kan de oplyste procenttal fra Stoll, M.L et al. og BA, ikke direkte sammenlignes, da det Stoll, M.L et al. kun har undersøgt lavt differentierede AC, hvor BA har undersøgt prøver med varierede differentieringsgrad. Der kan dog stadig observeres en tendens. BA har ydermere resultater fra PC, hvor anti-ck5, anti-ck14 og anti-p63 er positive i 89, 5 % af prøverne, og i de resterende 10,5 %, svarende til 2 prøver observeres anti-p63 så svag, at denne 54
55 markør vurderes negativ (Tabel 10). Vores resultater typer på at CK5, CK14 og p63 påvirkes i lille grad af differentieringsgraden. Nekrose Teorien foreskriver, at omkring 97 % af alle tumorceller, i løbet af cancerens udvikling, undergår nekrose (4). Med denne viden må der være stor sandsynlighed for at en biopsi indeholder nekrotiske celler. I BA observeres bl.a. vævsprøve 15, hvor der kun var farvereaktion ved meget få celler i den udstansede vævsprøve. Ud fra resultatet ville en korrekt diagnose, være svær at stille. Tabel 12 viser resultaterne af vævsprøve 15, når den farves med en HE-farvning, ASP og anti-ttf-1, anti-p63 og anti-napsin-a. Når vævsprøven betragtes ved HE-farvning, bærer vævet tydelige præg af nekrose. Cellerne er opsvulmet med vakuoliseret cytoplasma. Cellekernerne fremstår vesikulære, med opdelt kromatin og stedvist helt opløste kerner. Når anti-ttf-1 vurderes kan der observeres enkelte kraftigt farve cellekerner. Når anti-napsin-a vurderes kan der ligeledes observeres enkelte positive celler, hvor cytoplasma er kraftigt farvet. Ydermere kan der observeres få p63-positive celler i den pågældende vævsprøve. ASP gav ikke brugbare resultater når den anvendes på vævsprøve 15. Dog gav ASP ikke færre informationer end anti-ttf-1, anti-p63 og anti-napsin-a, når de anvendes hver for sig. Det må derfor konkluderes at immunhistokemi generelt ikke er brugbart, hvis prøvematerialet er nekrotisk. Reproducerbarhed Tabel 13 viser udvalgte resultater fra 2 farvninger med ASP. De 2 farvninger er udført med samme ASP og kan derfor danne grundlag for vurdering af reproducerbarheden. Vævsprøve 5 og 13 er AC og begge vævsprøver fremstår tydeligere ved 1. farvning, frem for 2. farvning. Ved vævsprøve 4 ses et PC, som farvemæssigt har en god overensstemmelse mellem de 2 udførte farvninger, da vævet ved de anviste pile fremstår med samme farveintensitet. Derudover anviser den sorte cirkel ved vævsprøve 4 og 5 et område, der ved 1. farvning fremviser tydelige celler. Det tilsvarende område ved 2. farvning, er meget dårligt repræsenteret, hvilket kan tyde på at de 2 farvningerne er udført forskelligt. Dog skal prøvematerialet tages med i betragtning. Der er skåret 15 snit i samme niveau på hver multiblok, hvor 1. farvning er udført på snit nr. 1 og 2. farvning er udført på snit nr. 5. Dette kan evt. have medført en ændring i cellebilledet, da cellerne ikke ligger i samme niveau igennem hele vævet. 55
56 Ud fra resultaterne kan det udledes at farvningerne ikke er udført ens, hvilket har haft betydning for det endelige resultat. Men da begge farvninger fremstår med brugbare resultater, må forskellen knyttes til manglende erfaring hos de 3 studerende. Det er et håndværk at udfører manuelle farvninger, hvilket kræver oplæring og erfaring, men det bør undersøges, hvorvidt en erfaren bioanalytiker, kan opnå ensartede resultater, hver gang farvningen udføres. Da farveforskellen mellem 1. og 2. farvning vurderes til at være et resultat af de studerendes manglende erfaring, må det konkluderes at metoden er reproducerbar. Implementering Lauridsen,J.L. et al. (6) beskriver de fordele der er observeret ved PIRH, ved implementering af ASP. Ved at vurdere alle markører på samme snit, har de ved PIRH kunne spare på prøvematerialet, da de ikke skal skære så mange snit, hvilket har åbnet for nye diagnostiske muligheder, såsom gentest. Lauridsen,J.L. et al. (6) oplyser ydermere, når de anvendte ressourcer opgøres, har implementeringen medført tidsbesparelser ved mikroskopi og besparelser på reagenser og antistoffer. Det oplyses at tidsbesparelserne ved mikroskopi er på mellem % og besparelserne på reagenser og antistoffer angives til omkring 36 %. I en travl hverdag med stramme budgetter, må de nævnte besparelser anses som værende en stor fordel, ved anvendelse af ASP. Om de omtalte besparelser vil kunne opnås på AKP, vides ikke. AKP anvender apparaturet Ventana til immunhistokemiske analyser. Ventana kan ikke anvende samme fremgangsmetode, som blev anvendt ved BA, da vævssnittene behandles i sekvenser. Dette betyder at hver antigen-antistof reaktion og hver detektion skal udføres hver for sig. Derudover anvender Ventana detektionsfarverne rød og rødbrun, hvilket kan vanskeliggøre den efterfølgende diagnosticering, hvis farverne ikke kan adskilles. Hvis farvningen skal udføres manuelt, må det overvejes, hvor ofte farvningen kan udføres. Detektionssystemet; MultiVision Polymer Detection System anvender LVRed / LVBlue og hver af disse opløsninger må højest fremstilles 15 min før brug (19), hvilket er en ulempe, da dette kan gøre det vanskeligt at udføre farvningen kontinuerligt. En løsning på dette problem, kan dog være at farvningen udføres 1 gang dagligt. 56
57 Konklusion Ud fra resultaterne fra subklasifikationen af plano er (PC) kan det konkluderes at kombinationen af anti-p63, anti-cytokeratin 5 (CK5) og anti-cytokeratin 14 (CK14) medfører tydelig og brugbar klassifikation ved alle differentieringsgrader. 19 PC ud af de 19 PC, der indgik i forsøget, blev diagnosticeret korrekt, hvilket giver en sensitivitet på 100 %. Ud fra resultaterne fra subklasifikationen af adenoer (AC) opnåede kombinationen af antinapsin-a og anti-thyroid transcripstion faktor-1 (TTF-1) en sensitivitet på 88,24 %, hvormed der må stilles tvivl ved kombinationens brugbarhed. Napsin-A kunne påvises ved 11 AC ud af de 17 AC, der indgik i forsøget. Tilstedeværelsen af napsin-a i vævet, påvirkes af differentieringsgraden og nekrose, hvilket er en ulempe ved differentiering. TTF-1 blev påvist ved 16 AC ud af de 17 AC, hvormed det kan konkluderes at anti-ttf-1 giver en god og brugbar klassifikation af AC, ved alle differentieringsgrader. Dog må det nævnes at både anti-ttf-1 og anti-p63, ifølge andre studier, kan fremstå positive ved forskellige metastaserede cancertyper, hvilket er en ulempe der bør tages højde for, hvis markørerne skal anvendes på sparsomt materiale. Selvom antistofpoolen generelt gav tydeligt adskillelse af cellekerner og cytoplasma, kunne muligheden for at forstærke positive reaktioner være brugbart ved meget svage farveintensiteter. MultiVision Polymer Detection System, anvender LVRed og LVBlue til detektion af antigenantistof reaktioner. Disse opløsninger skal fremstilles 15 min før brug, hvilket gør det vanskeligt at udfører farvningen kontinuerligt, dog kan en løsning være, at udføre farvningen 1 gang dagligt. Anvendelse af en antistofpool indeholdende anti-ttf-1, anti-napsin-a, anti-p63, anti-ck5 og anti- CK14, giver god mulighed for at identificere flere antigener på samme vævssnit. Dette er en fordel, da der kan spares på det antal snit, der skal anvendes til immunhistokemi, hvilket giver mulighed for, at udfører yderligere undersøgelser på det resterende prøvemateriale. 57
58 Perspektivering Resultaterne fra det udførte forsøg tyder på, at visse antistoffer har en svaghed ved subklaasifikationen af NSCLC. I den forbindelse bør det undersøges, hvorvidt andre antistoffer kan anvendes. Det bør undersøges hvorvidt fx anti-p63 kan erstattes med anti-p40, og hvorvidt antinapsin-a, kan erstattes med CK7. Det bør yderligere undersøges, om der kan findes et alternativ til anti-ttf-1. For at kunne erstatte et antistof, skal en række praktiske ting undersøges. Det antigen, man ønsker at detektere, skal være lokaliseret i samme cellekomponent som det antigenet man ønsker at erstatte. Eksempelvis findes p63 i cellekernen, hvormed p40 også skal findes i cellekernen, ellers fremkommer der ikke de samme farvekombinationer, hvor cellekernen og cytoplasma adskilles. Samtidig skal antistoffet være af samme dyreart, som det antistof man ønsker at erstatte. Eksempelvis er anti-p63 et mus-antistof, hvilket betyder at anti-p40 også skal være et mus-antistof, ellers kan antistoffet ikke danne binding med det sekundære antistof, hvorved det ikke vil kunne detekteres. Derudover skal koncentrationsforholdet bestemmes, da det ikke kan forventes, at det nye antistof kan anvendes med samme koncentration, som det antistof der bliver erstattet. 58
59 Litteraturliste (1) Dansk Lunge Cancer Gruppe og Dansk Lunge Cancer Register. Årsrapport : Anvendt: Tabel 29 s. 53, Tabel s. 56 (2) Young B, Stewart W, O'Dowd G, Wheater PR. Wheater's Basic pathology: a text, atlas and review of histopathology. 5. ed. ed. Edinburgh: Churchill Livingstone; Anvendt: s. 72, Figur 7.6 s. 72, , Figur s. 136, Figur s (3) Kim MJ, Shin HC, Shin KC, Ro JY. Best immunohistochemical panel in distinguishing adenoa from squamous cell a of lung: tissue microarray assay in resected lung cancer specimens. Ann Diagn Pathol 2013 Feb;17(1): (4) Vyberg M. Patologi & farmakologi. 2. udgave. ed. Kbh.: Munksgaard Danmark; Anvendt: 30-31, 34, 48, 54, 57, 61, (5) Nørgaard JOR. Medicinske fagudtryk: en klinisk ordbog med kommentarer. 2001:861 sider. Anvendt: 18, 54, 58, , 131,184, 234, 362, 489, , (6) Lauridsen JL. Pentalung-farvning med Multivision. 2013((09/13)): (7) Fatima N, Cohen C, Lawson D, Siddiqui MT. TTF-1 and Napsin A double stain: a useful marker for diagnosing lung adenoa on fine-needle aspiration cell blocks. Cancer Cytopathol 2011 Apr 25;119(2): (8) Yanagita E, Imagawa N, Ohbayashi C, Itoh T. Rapid multiplex immunohistochemistry using the 4-antibody cocktail YANA-4 in differentiating primary adenoa from squamous cell a of the lung. Appl Immunohistochem Mol Morphol 2011 Dec;19(6): (9) Sundhedsstyrelsen. Pakkeforløb for Lungekræft. Version ; Anvendt: Afsnit 3.1 s. 21, afsnit 4.1 s. 24. (10) Geneser F. Histologi - på molekylærbiologisk grundlag. Kbh.: Munksgaard; Anvendt: Kap. 19 s (11) Stoll LM, Johnson MW, Gabrielson E, Askin F, Clark DP, Li QK. The utility of napsin-a in the identification of primary and metastatic lung adenoa among cytologically poorly differentiated as. Cancer Cytopathol 2010 Dec 25;118(6):
60 (12) Hallager K, Jelsbak V, Meyer T editors. Farvning af celler og væv. 3. udgave. Kap 4. s ed.: VIA University College Bioanalytikeruddannelsen; Anvendt: Kap. 3 (s ). (13) Vyberg M. Anvendt immunhistokemi. 6. udgave, 2. oplag ed.: Bioanalytikeruddannelsen København; Anvendt: 11-15, 18-23, 27-28, Figur 2.14 s. 37, , , 173. (14) Ventana. Anti-p63 (4A4) (15) Cell Marque. Cytokeratin 5 (EPY1601Y). 5-EP1601Y.asp (16) Cell Marque. Cytokeratin 14 (SP53). SP53.asp (17) Abcam. Anti-TTF-1 (EP1584Y) (18) Novostatra. Napsin-A (NCL-L). s/napsina-l-ce.pdf (19) Thermo Scientific. MultiVision Polymer Detection System: MultiVision anti-rabbit/hrp + anti-mouse/ap polymers. Instructions for use. Oktober, (20) DAKO. PT Link, Pre-treatment Module for Tissue Specimens (21) DAKO. Dako Pen. Oktober, (22) Bendsen T. Noter i statistik. VIA University College Bioanalytikeruddannelsen ; (23) DAKO. Target Retrieval Solution ph (24) Ventana. Cell Conditioning 1 (CC1) (25) Masai K, Tsuta K, Kawago M, Tatsumori T, Kinno T, Taniyama T, et al. Expression of squamous cell a markers and adenoa markers in primary pulmonary neuroendocrine as. Appl Immunohistochem Mol Morphol 2013 Jul;21(4):
61 (26) Hsiao SH, Chung CL, Lee CM, Chen WY, Chou YT, Wu ZH, et al. Suitability of Computed Tomography-Guided Biopsy Specimens for Subtyping and Genotyping of Non-Small-Cell Lung Cancer. Clin Lung Cancer 2013 Jul 24. (27) Biocare Medical. Cytokeratin 5 (CK5) (28) Ventana. OptiView Detection Chemistry (29) Bishop JA, Teruya-Feldstein J, Westra WH, Pelosi G, Travis WD, Rekhtman N. p40 (DeltaNp63) is superior to p63 for the diagnosis of pulmonary squamous cell a. Mod Pathol 2012 Mar;25(3):
62 Bilags fortegnelse 1. Immunhistokemiske metode Epitop demaskering Udstansninger Multiblok skitser Afparaffinering og hydrering Mikroskopi skitse K2 kontrol skitse K2 kontrollerne (Rådata) Adenoer (Rådata) Planocellulære er (Rådata) Fikspunkter (Rådata) Tro og love erklæring 81 62
63 Bilag 1 Immunhistokemiske metode TNT Buffer Trin 1 udføres jf. forskrift: Afparaffinering med Histo- Clear (Bilag 5) Trin 5+6 udføres før trin 3+4 TNT Buffer Trin udføres jf. forskrift: Antigendemaskering i mikrobølgeovn (Bilag 2) med EDTA Buffer TNT Buffer TNT Buffer TNT Buffer Lad vævssnit tørre natten over i stinkskab 63
64 Bilag 2 Epitop demaskering Svarende til indstillingen: MAX 9 min. 440W 64
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Kode K8010 5. udgave Sættet indeholder reagenser til 400 600 analyser. Til Dako Autostainer/Autostainer Plus. Valgfri reagenser: Kode Produktnavn
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Kode K8010 5. udgave Sættet indeholder reagenser til 400 600 analyser. Til Dako Autostainer/Autostainer Plus. Valgfri reagenser: Kode Produktnavn
Herlev og Gentofte Hospital. The influence of different fixatives and preparation methods on morphology, immunohistochemistry and molecular analyses
 Herlev og Gentofte Hospital The influence of different fixatives and preparation methods on morphology, immunohistochemistry and molecular analyses Problem Rutinemæssigt bruges 10% neutralbuffet formalin
Herlev og Gentofte Hospital The influence of different fixatives and preparation methods on morphology, immunohistochemistry and molecular analyses Problem Rutinemæssigt bruges 10% neutralbuffet formalin
PROFESSIONSBACHELORPROJEKT Bioanalytikeruddannelsen UCL i Odense. Maria Erlinda Haugaard Gozun Studienummer: 32110505 Hold: SB 510 11-12-2013
 PROFESSIONSBACHELORPROJEKT Bioanalytikeruddannelsen UCL i Odense Optimering af FNA-materiale til forbedret subklassificering af lungecancer Optimization of FNA material for improvement of subclassification
PROFESSIONSBACHELORPROJEKT Bioanalytikeruddannelsen UCL i Odense Optimering af FNA-materiale til forbedret subklassificering af lungecancer Optimization of FNA material for improvement of subclassification
Dako REAL EnVision Detection System, Peroxidase/DAB+, Rabbit/Mouse
 Dako REAL EnVision Detection System, Peroxidase/DAB+, Rabbit/Mouse Kode K5007 3. udgave Til brug sammen med automatiske Dako instrumenter til immunfarvning. Sættet indeholder reagenser til 500 analyser.
Dako REAL EnVision Detection System, Peroxidase/DAB+, Rabbit/Mouse Kode K5007 3. udgave Til brug sammen med automatiske Dako instrumenter til immunfarvning. Sættet indeholder reagenser til 500 analyser.
2UJDQLVNHýVWRIJUXSSHUýLýSODQWHIU
 3ODQWHI\VLRORJL,QWURGXNWLRQ 2UJDQLVNHýVWRIJUXSSHUýLýSODQWHIU I et plantefrø findes bl.a. anlægget til en ny plante i form af det såkaldte kimanlæg. Dette anlæg skal kunne udvikle sig til en ny plante under
3ODQWHI\VLRORJL,QWURGXNWLRQ 2UJDQLVNHýVWRIJUXSSHUýLýSODQWHIU I et plantefrø findes bl.a. anlægget til en ny plante i form af det såkaldte kimanlæg. Dette anlæg skal kunne udvikle sig til en ny plante under
EnVision G/2 dobbeltfarvning med antistofferne CD31 og DBA44.
 EnVision G/2 dobbeltfarvning med antistofferne CD31 og DBA44. Bachelorprojekt Projektperiode: November 2008 januar 2009 Forfatter: Winni Pedersen CPR nr. 230362 Bivejleder: Lone Bojesen, Herlev patologi
EnVision G/2 dobbeltfarvning med antistofferne CD31 og DBA44. Bachelorprojekt Projektperiode: November 2008 januar 2009 Forfatter: Winni Pedersen CPR nr. 230362 Bivejleder: Lone Bojesen, Herlev patologi
Evaluering af antistofferne p63 og p40
 VIA UNIVERSITY COLLEGE BIOANALYTIKERUDDANNELSEN Evaluering af antistofferne p63 og p4 Kernemarkører til at differentiere mellem adenokarcinom og planocellulært karcinom 18-12-213 Antal tegn inkl. mellemrum:
VIA UNIVERSITY COLLEGE BIOANALYTIKERUDDANNELSEN Evaluering af antistofferne p63 og p4 Kernemarkører til at differentiere mellem adenokarcinom og planocellulært karcinom 18-12-213 Antal tegn inkl. mellemrum:
Optimering af detektionen til diagnosticering. ved anvendelse af antistofferne HMB45 og Melan A
 20-12-2016 Optimering af detektionen til diagnosticering af maligne melanomer ved anvendelse af antistofferne HMB45 og Melan A Optimization of the detection to the diagnosis of malignant melanoma by use
20-12-2016 Optimering af detektionen til diagnosticering af maligne melanomer ved anvendelse af antistofferne HMB45 og Melan A Optimization of the detection to the diagnosis of malignant melanoma by use
Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse
 Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse Kode K5001 6. udgave Til brug sammen med automatiske Dako instrumenter til immunfarvning. Sættet indeholder reagenser til 500 analyser. (129655-001)
Dako REAL Detection System, Peroxidase/DAB+, Rabbit/Mouse Kode K5001 6. udgave Til brug sammen med automatiske Dako instrumenter til immunfarvning. Sættet indeholder reagenser til 500 analyser. (129655-001)
Proteiner: en introduktion. Modul 1; F13 Rolf Andersen, 18/2-2013
 Proteiner: en introduktion Modul 1; F13 Rolf Andersen, 18/2-2013 4 facts om proteiner Proteiner udgør én af de vigtigste stofgrupper i vores organisme; de varetager en lang række forskellige funktioner.
Proteiner: en introduktion Modul 1; F13 Rolf Andersen, 18/2-2013 4 facts om proteiner Proteiner udgør én af de vigtigste stofgrupper i vores organisme; de varetager en lang række forskellige funktioner.
Immunfarvning med ny antistofcocktail som led i cancerdiagnostik af pleuravæskekoagler
 Immunfarvning med ny antistofcocktail som led i cancerdiagnostik af pleuravæskekoagler Professionsbachelorprojekt 18-03-2013 29-05-2013 Bioanalytikeruddannelsen VIA UC, Campus Aarhus Nord Udarbejdet af:
Immunfarvning med ny antistofcocktail som led i cancerdiagnostik af pleuravæskekoagler Professionsbachelorprojekt 18-03-2013 29-05-2013 Bioanalytikeruddannelsen VIA UC, Campus Aarhus Nord Udarbejdet af:
EnVision FLEX+, Mouse, High ph, (Link)
 EnVision FLEX+, Mouse, High ph, (Link) Kode K8002 5. udgave Sættet indeholder reagenser til 400 600 analyser. Til Autostainer Link-instrumenter. Valgfri reagenser Kode Produktnavn Analyser K8004 EnVision
EnVision FLEX+, Mouse, High ph, (Link) Kode K8002 5. udgave Sættet indeholder reagenser til 400 600 analyser. Til Autostainer Link-instrumenter. Valgfri reagenser Kode Produktnavn Analyser K8004 EnVision
En sammenligning af farvekvalitet og økonomi
 Evaluering af monoklonale murine og kaninantistofkloner til Desmin, TTF-1 og CD1a En sammenligning af farvekvalitet og økonomi Udarbejdet af bioanalytikerstuderende fra VIA University College, December
Evaluering af monoklonale murine og kaninantistofkloner til Desmin, TTF-1 og CD1a En sammenligning af farvekvalitet og økonomi Udarbejdet af bioanalytikerstuderende fra VIA University College, December
IHC påvisning af CD3 og F4/80 antigen i CIA musepotevæv
 IHC påvisning af CD3 og F4/80 antigen i CIA musepotevæv Bachelorprojekt af Mikkel Malik Høegh Nygaard Nielsen Kilde Billede fra laboratoriet på Novo Nordisk Bioanalytikeruddannelsen CVU Øresund Nordisk
IHC påvisning af CD3 og F4/80 antigen i CIA musepotevæv Bachelorprojekt af Mikkel Malik Høegh Nygaard Nielsen Kilde Billede fra laboratoriet på Novo Nordisk Bioanalytikeruddannelsen CVU Øresund Nordisk
Opgavens omfang: anslag. Klinisk Diagnostisk Afdeling, Patologi, Finsensgade 35, 6700 Esbjerg. Vejledere: Liselotte Olesen og Inge Marie Bayer
 Optimering af immunhistokemisk metode til diagnosticering af maligne melanomer ved brug af antistofferne Mel A og HMB45. Optimization of immunohistochemical method for the diagnosis of malignant melanoma
Optimering af immunhistokemisk metode til diagnosticering af maligne melanomer ved brug af antistofferne Mel A og HMB45. Optimization of immunohistochemical method for the diagnosis of malignant melanoma
Analyse af proteiner Øvelsesvejledning
 Center for Undervisningsmidler, afdeling København Analyse af proteiner Øvelsesvejledning Formål At separere og analysere proteiner i almindelige fødevarer ved brug af gelelektroforese. Teori Alle dele
Center for Undervisningsmidler, afdeling København Analyse af proteiner Øvelsesvejledning Formål At separere og analysere proteiner i almindelige fødevarer ved brug af gelelektroforese. Teori Alle dele
Test'af'EML4.ALK'fusion'i'lungeadenokarcinom.
 Test'af'EML4.ALK'fusion'i'lungeadenokarcinom. Anbefalingerne udarbejdede af: Overlæge,Dr.Med.BirgitGuldhammerSkov.BispebjergHospital,PatologiskAfdeling. Professor,overlægeMogensVyberg.AalborgUniversitetshospital,PatologiskInstitut.
Test'af'EML4.ALK'fusion'i'lungeadenokarcinom. Anbefalingerne udarbejdede af: Overlæge,Dr.Med.BirgitGuldhammerSkov.BispebjergHospital,PatologiskAfdeling. Professor,overlægeMogensVyberg.AalborgUniversitetshospital,PatologiskInstitut.
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Kode K8012 6. udgave Sættet indeholder reagenser til 400 600 analyser. Til Dako Autostainer/Autostainer Plus. Valgfri reagenser: Kode
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Kode K8012 6. udgave Sættet indeholder reagenser til 400 600 analyser. Til Dako Autostainer/Autostainer Plus. Valgfri reagenser: Kode
Spørgsmål Svar # 2. af d vedrørende. Offentligt udbud vedr. sag nr. MT2008/1042
 Udbud af automatiseret til håndtering af immunhisto- og cytokemiske analyser på 1 Spørgsmål Svar # 2 af d. 03.03.2009 vedrørende Offentligt udbud vedr. sag nr. MT2008/1042 Udbud af automatiseret til håndtering
Udbud af automatiseret til håndtering af immunhisto- og cytokemiske analyser på 1 Spørgsmål Svar # 2 af d. 03.03.2009 vedrørende Offentligt udbud vedr. sag nr. MT2008/1042 Udbud af automatiseret til håndtering
Tissue micro array en udfordring. Molekylærenheden Patologiafdelingen Herlev Hospital Danmark
 Tissue micro array en udfordring Molekylærenheden Patologiafdelingen Herlev Hospital Danmark Kræft og kræftrelateret behandling UDFORDRING: Flere tilbud til medicinsk behandling Individuel behandling Antallet
Tissue micro array en udfordring Molekylærenheden Patologiafdelingen Herlev Hospital Danmark Kræft og kræftrelateret behandling UDFORDRING: Flere tilbud til medicinsk behandling Individuel behandling Antallet
Regnskovens hemmeligheder
 Center for Undervisningsmidler, afdeling København Regnskovens hemmeligheder Øvelsesvejledning Formål Et gen for et kræfthelbredende protein er blevet fundet i nogle mystiske blade i regnskoven. Forskere
Center for Undervisningsmidler, afdeling København Regnskovens hemmeligheder Øvelsesvejledning Formål Et gen for et kræfthelbredende protein er blevet fundet i nogle mystiske blade i regnskoven. Forskere
Påvisning af collagen colitis ved lymfocytær colitis diagnosticeret væv
 Påvisning af collagen colitis ved lymfocytær colitis diagnosticeret væv - udført med masson trichrom, picrosiriusrød og optimering af anti-tenascin Detection of collagenous colitis in lymphocytic colitis
Påvisning af collagen colitis ved lymfocytær colitis diagnosticeret væv - udført med masson trichrom, picrosiriusrød og optimering af anti-tenascin Detection of collagenous colitis in lymphocytic colitis
ELISA Immuno Explorer TM Kit
 - 1 - ELISA Immuno Explorer TM Kit Katalog nummer 166-2400EDU Til læreren Dette kit er lavet for at lette og illustrere immunologiundervisningen og kan give en øget forståelse af antigen-antistof interaktionen,
- 1 - ELISA Immuno Explorer TM Kit Katalog nummer 166-2400EDU Til læreren Dette kit er lavet for at lette og illustrere immunologiundervisningen og kan give en øget forståelse af antigen-antistof interaktionen,
Isolering af DNA fra løg
 Isolering af DNA fra løg Formål: At afprøve en metode til isolering af DNA fra et levende væv. At anvende enzymer.. Indledning: Isolering af DNA fra celler er første trin i mange molekylærbiologiske undersøgelser.
Isolering af DNA fra løg Formål: At afprøve en metode til isolering af DNA fra et levende væv. At anvende enzymer.. Indledning: Isolering af DNA fra celler er første trin i mange molekylærbiologiske undersøgelser.
Optimering af specialfarvningen Masson Trichrom
 Optimering af specialfarvningen Masson Trichrom Lonnie Frederiksen, 110632@via.dk VIA University College, Campus Aarhus N, Bioanalytikeruddannelsen I-vejleder: Inge Rasmussen, Lektor v Bioanalytikerunderviser
Optimering af specialfarvningen Masson Trichrom Lonnie Frederiksen, 110632@via.dk VIA University College, Campus Aarhus N, Bioanalytikeruddannelsen I-vejleder: Inge Rasmussen, Lektor v Bioanalytikerunderviser
Øvelse med tarmkræftceller i kultur.
 Øvelse med tarmkræftceller i kultur. Baggrund Hver 3. dansker bliver ramt af kræft, inden de er blevet 75 år. Tyktarmskræft er den 3. hyppigste kræftform hos både mænd og kvinder, hvor henholdsvis 7.3
Øvelse med tarmkræftceller i kultur. Baggrund Hver 3. dansker bliver ramt af kræft, inden de er blevet 75 år. Tyktarmskræft er den 3. hyppigste kræftform hos både mænd og kvinder, hvor henholdsvis 7.3
EnVision FLEX, High ph (Dako Omnis)
 EnVision FLEX, High ph (Dako Omnis) Code GV800 2. udgave Sættet indeholder reagenser til 600 analyser. Til Dako Omnis-instrumenter. Valgfri reagenser: Kode Produktnavn Analyser GV804 GV805 EnVision FLEX
EnVision FLEX, High ph (Dako Omnis) Code GV800 2. udgave Sættet indeholder reagenser til 600 analyser. Til Dako Omnis-instrumenter. Valgfri reagenser: Kode Produktnavn Analyser GV804 GV805 EnVision FLEX
Fikseringstidens indvirkning på vævsmorfologi, antigenisitet og DNA-bevarelse i væv
 Fikseringstidens indvirkning på vævsmorfologi, antigenisitet og DNA-bevarelse i væv Navn: Charlotte Fischer Rasmussen Studienummer: 99946 I-vejleder: Lektor, Cand. Scient. Birte Bunch Larsen K-vejleder:
Fikseringstidens indvirkning på vævsmorfologi, antigenisitet og DNA-bevarelse i væv Navn: Charlotte Fischer Rasmussen Studienummer: 99946 I-vejleder: Lektor, Cand. Scient. Birte Bunch Larsen K-vejleder:
Dobbeltfarvning med p16/ki-67 (CINtec PLUS) på cervixcytologiske prøver med low grade of intraepithelial lesion (LSIL)
 Dobbeltfarvning med p16/ki-67 (CINtec PLUS) på cervixcytologiske prøver med low grade of intraepithelial lesion (LSIL) Cytologisk årsmøde 2-3 marts 2012, Odense Marianne Waldstrøm Specialechef, ledende
Dobbeltfarvning med p16/ki-67 (CINtec PLUS) på cervixcytologiske prøver med low grade of intraepithelial lesion (LSIL) Cytologisk årsmøde 2-3 marts 2012, Odense Marianne Waldstrøm Specialechef, ledende
Banan DNA 1/6. Formål: Formålet med øvelsen er at give eleverne mulighed for at se DNA strenge med det blotte øje.
 Banan DNA Formål: Formålet med øvelsen er at give eleverne mulighed for at se DNA strenge med det blotte øje. Baggrundsviden: Om vi er mennesker, dyr eller planter, så har alle organismer DNA i deres celler.
Banan DNA Formål: Formålet med øvelsen er at give eleverne mulighed for at se DNA strenge med det blotte øje. Baggrundsviden: Om vi er mennesker, dyr eller planter, så har alle organismer DNA i deres celler.
Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting
 Center for Undervisningsmidler, afdeling København Western blotting Øvelsesvejledning Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting Teori Proteomik er studiet af celleproteiners
Center for Undervisningsmidler, afdeling København Western blotting Øvelsesvejledning Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting Teori Proteomik er studiet af celleproteiners
Immunhistokemi kombineret med special farvninger
 BACHELOR 2015 Immunhistokemi kombineret med special farvninger - Udført med CD3, Alcian Blue, PAS og DPAS med henblik på diagnosticering af MB Sjögrens Syndrom Maria Villadsen Studienummer 60080725 Vejleder
BACHELOR 2015 Immunhistokemi kombineret med special farvninger - Udført med CD3, Alcian Blue, PAS og DPAS med henblik på diagnosticering af MB Sjögrens Syndrom Maria Villadsen Studienummer 60080725 Vejleder
Sommereksamen 2012 Med korte, vejledende svar
 1 Sommereksamen 2012 Med korte, vejledende svar Titel på kursus: Uddannelse: Semester: ksamensdato: Tid: Bedømmelsesform Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin
1 Sommereksamen 2012 Med korte, vejledende svar Titel på kursus: Uddannelse: Semester: ksamensdato: Tid: Bedømmelsesform Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin
Selvsamlende enkeltlag elevvejledning
 Nano ScienceCenter,KøbenhavnsUniversitet Selvsamlende enkeltlag elevvejledning Fremstilling af enkeltlag på sølv Formål I dette forsøg skal du undersøge, hvordan vand hæfter til en overflade af henholdsvis
Nano ScienceCenter,KøbenhavnsUniversitet Selvsamlende enkeltlag elevvejledning Fremstilling af enkeltlag på sølv Formål I dette forsøg skal du undersøge, hvordan vand hæfter til en overflade af henholdsvis
Biotechnology Explorer ELISA Immuno Explorer Kit. Instruktionsmanual
 Biotechnology Explorer ELISA Immuno Explorer Kit Instruktionsmanual Katalognummer 166-2400EDU explorer.bio-rad.com Delene i dette kit er sendt i separate æsker. Opbevar posen med reagenser i køleskab indefor
Biotechnology Explorer ELISA Immuno Explorer Kit Instruktionsmanual Katalognummer 166-2400EDU explorer.bio-rad.com Delene i dette kit er sendt i separate æsker. Opbevar posen med reagenser i køleskab indefor
EnVision DuoFLEX Doublestain System, (Link)
 EnVision DuoFLEX Doublestain System, (Link) Kode SK110 Udgave 06/15 Dette sæt indeholder reagenser til 100-150 analyser. Til Autostainer Link instrumenter. (127841-001) P04070DK_01/SK110/2015.06 s. 1/11
EnVision DuoFLEX Doublestain System, (Link) Kode SK110 Udgave 06/15 Dette sæt indeholder reagenser til 100-150 analyser. Til Autostainer Link instrumenter. (127841-001) P04070DK_01/SK110/2015.06 s. 1/11
Creation of a tissue microarray(tma)-block intended for implementation of antibodies for diagnostication of endometrialcancer
 Bachelorprojekt: Fremstilling af tissue microarray(tma)-blok til implementering af antistoffer til diagnosticering af endometriecancer Creation of a tissue microarray(tma)-block intended for implementation
Bachelorprojekt: Fremstilling af tissue microarray(tma)-blok til implementering af antistoffer til diagnosticering af endometriecancer Creation of a tissue microarray(tma)-block intended for implementation
Tissue micro array til klinisk rutine analyse. Molekylærenheden Patologiafdelingen Herlev Hospital Danmark
 Tissue micro array til klinisk rutine analyse Molekylærenheden Patologiafdelingen Herlev Hospital Danmark Brug af TMA i forskning TMA er hovedsageligt brugt indenfor forskning, typisk til analyse af større
Tissue micro array til klinisk rutine analyse Molekylærenheden Patologiafdelingen Herlev Hospital Danmark Brug af TMA i forskning TMA er hovedsageligt brugt indenfor forskning, typisk til analyse af større
Påvisning af p16 på celleblokke fra cervixcytologisk materiale
 Påvisning af p16 på celleblokke fra cervixcytologisk materiale Immunfarvning med p16(jc8) fra ASC-H 8(2) forstørrelse x40 Forsøg udført af: Anne Obling Madsen og Marie Kjøller-Hansen Professionsbachelorrapport
Påvisning af p16 på celleblokke fra cervixcytologisk materiale Immunfarvning med p16(jc8) fra ASC-H 8(2) forstørrelse x40 Forsøg udført af: Anne Obling Madsen og Marie Kjøller-Hansen Professionsbachelorrapport
Elevguide Forsøg I: Tjekliste Materialer pr. gruppe.
 Elevguide Forsøg I: Opsporing af sygdomsudbrud en sygdoms smitteveje. I dette forsøg skal I prøve at kortlægge smittevejene for koppe-virus. For at stoppe sygdommens fremmarch mest muligt, ønsker man at
Elevguide Forsøg I: Opsporing af sygdomsudbrud en sygdoms smitteveje. I dette forsøg skal I prøve at kortlægge smittevejene for koppe-virus. For at stoppe sygdommens fremmarch mest muligt, ønsker man at
focus PATOLOGI Immunhistokemi Tissue Micro Array Biobank Molekylærbiologi Cytologi
 focus PATOLOGI AH diagnostics har Nordens bredeste udvalg af primære antistoffer og markedets nyeste generation af højsensitive detektionssystemer til immunhistokemi. AH diagnostics tilbyder desuden moderne,
focus PATOLOGI AH diagnostics har Nordens bredeste udvalg af primære antistoffer og markedets nyeste generation af højsensitive detektionssystemer til immunhistokemi. AH diagnostics tilbyder desuden moderne,
Studieplan Bioanalyse Semester 1
 OMRÅDET FOR SUNDHEDSUDDANNELSER Studieplan Bioanalyse Semester 1 Bioanalytikeruddannelsen i Odense Efterår 2017 Semester 1 Indhold 1. Fagets fokus og emner... 3 2. Lektionsplan... 4 3. Litteraturliste:...
OMRÅDET FOR SUNDHEDSUDDANNELSER Studieplan Bioanalyse Semester 1 Bioanalytikeruddannelsen i Odense Efterår 2017 Semester 1 Indhold 1. Fagets fokus og emner... 3 2. Lektionsplan... 4 3. Litteraturliste:...
Vestsjællands Amtssygehus Klinisk Biokemisk Afdeling Centralsygehuset i Slagelse
 Bilag D Vestsjællands Amtssygehus Klinisk Biokemisk Afdeling Centralsygehuset i Slagelse INTERN RAPPORT Afprøvning af Immunofixation af M-komponenter (Bestemmelse af immunoglobulin-klasse og -type) på
Bilag D Vestsjællands Amtssygehus Klinisk Biokemisk Afdeling Centralsygehuset i Slagelse INTERN RAPPORT Afprøvning af Immunofixation af M-komponenter (Bestemmelse af immunoglobulin-klasse og -type) på
Biotechnology Explorer. Protein Fingerprinting
 Biotechnology Explorer Protein Fingerprinting Instruktionsmanual Katalognummer 166-0100EDU explorer.bio-rad.com Delene i dette kit er sendt i seperate æsker. Opbevar proteinstandarderne i fryseren, ved
Biotechnology Explorer Protein Fingerprinting Instruktionsmanual Katalognummer 166-0100EDU explorer.bio-rad.com Delene i dette kit er sendt i seperate æsker. Opbevar proteinstandarderne i fryseren, ved
Appendix 1: Udregning af mængde cellesuspention til udsåning. Faktor mellem total antal celler og antal celler der ønskes udsås:
 Appendix Appendix 1: Udregning af mængde cellesuspention til udsåning Fortyndingsfaktor: Efter trypsinering og centrifugering af celler fra cellestokken, opblandes cellerne i 1 ml medie. For at lave en
Appendix Appendix 1: Udregning af mængde cellesuspention til udsåning Fortyndingsfaktor: Efter trypsinering og centrifugering af celler fra cellestokken, opblandes cellerne i 1 ml medie. For at lave en
Validering af gramfarvning af bakterier
 Valideringsrapport Gramfarvning af bakterier Formålet med valideringen At dokumentere at KMA, OUHs kan anvende gramfarvning til at identificere grampositive og negative bakterier, samt karakterisere morfologi/lejring.
Valideringsrapport Gramfarvning af bakterier Formålet med valideringen At dokumentere at KMA, OUHs kan anvende gramfarvning til at identificere grampositive og negative bakterier, samt karakterisere morfologi/lejring.
Billedet viser udseendet af livmodermunden ved en klinisk undersøgelse.
 Tekst til billede 1 Billedet viser udseendet af livmodermunden ved en klinisk undersøgelse. Skeden er udvidet med et såkaldt speculum. Lige under instrumentets øverste gren ses en blomkålslignende svulst,
Tekst til billede 1 Billedet viser udseendet af livmodermunden ved en klinisk undersøgelse. Skeden er udvidet med et såkaldt speculum. Lige under instrumentets øverste gren ses en blomkålslignende svulst,
Kemiøvelse 2 C2.1. Buffere. Øvelsens pædagogiske rammer
 Kemiøvelse 2 C2.1 Buffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 2 C2.1 Buffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
INDIVIDUALISERET BEHANDLING ETABLERING OG KARAKTERISERING AF PRIMÆRE LUNGECANCER CELLELINJER
 Protokolresume - LUCELLI INDIVIDUALISERET BEHANDLING ETABLERING OG KARAKTERISERING AF PRIMÆRE LUNGECANCER CELLELINJER 6. oktober 2014 Version 1 Forfattere og afdelinger: Birgitte Brinkmann Olsen, Nuklearmedicinsk
Protokolresume - LUCELLI INDIVIDUALISERET BEHANDLING ETABLERING OG KARAKTERISERING AF PRIMÆRE LUNGECANCER CELLELINJER 6. oktober 2014 Version 1 Forfattere og afdelinger: Birgitte Brinkmann Olsen, Nuklearmedicinsk
Metodesammenligning af serøse væsker præpararet med udstrygningsteknik og væskebaseret teknik, samt Cellient celleblokke og plasma-thrombin koagler
 Metodesammenligning af serøse væsker præpararet med udstrygningsteknik og væskebaseret teknik, samt Cellient celleblokke og plasma-thrombin koagler Bachelorprojekt: 10 oktober 2011 10 november 2011. Bioanalytikeruddannelsen
Metodesammenligning af serøse væsker præpararet med udstrygningsteknik og væskebaseret teknik, samt Cellient celleblokke og plasma-thrombin koagler Bachelorprojekt: 10 oktober 2011 10 november 2011. Bioanalytikeruddannelsen
Jernindhold i fødevarer bestemt ved spektrofotometri
 Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Atomic force mikroskopi på blodceller
 1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
Puffere. Øvelsens pædagogiske rammer. Sammenhæng. Formål. Arbejdsform: Evaluering
 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
Mælkesyrebakterier og holdbarhed
 Mælkesyrebakterier og holdbarhed Formål Formålet med denne øvelse er at undersøge mælkesyrebakteriers og probiotikas evne til at øge holdbarheden af kød ved at: 1. Undersøge forskellen på bakterieantal
Mælkesyrebakterier og holdbarhed Formål Formålet med denne øvelse er at undersøge mælkesyrebakteriers og probiotikas evne til at øge holdbarheden af kød ved at: 1. Undersøge forskellen på bakterieantal
Proteiner. Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde
 Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
Biotechnology Explorer
 Biotechnology Explorer Oprensning af genomisk DNA fra plantemateriale Manual Katalog nr. 166-5005EDU explorer.bio-rad.com Oversat og bearbejdet af Birgit Sandermann Justesen, Nærum Gymnasium, februar 2009
Biotechnology Explorer Oprensning af genomisk DNA fra plantemateriale Manual Katalog nr. 166-5005EDU explorer.bio-rad.com Oversat og bearbejdet af Birgit Sandermann Justesen, Nærum Gymnasium, februar 2009
Som substrat i forsøgene anvender vi para nitrophenylfosfat, der vha. enzymet omdannes til paranitrofenol
 Enzymkinetik Introduktion I disse forsøg skal I arbejde med enzymet alkalisk fosfatase. Fosfataser er meget almindelige i levende organismer og er enzymer med relativt bred substrat specificitet. De katalyserer
Enzymkinetik Introduktion I disse forsøg skal I arbejde med enzymet alkalisk fosfatase. Fosfataser er meget almindelige i levende organismer og er enzymer med relativt bred substrat specificitet. De katalyserer
MODULPLAN Bioanalytikeruddannelsen
 Obligatorisk Modulbeskrivelse præsenterer de studerende til bioanalytikerprofessionen og har fokus på basale laboratoriefærdigheder herunder den til grundlæggende naturvidenskabelige teori. Undervisningen
Obligatorisk Modulbeskrivelse præsenterer de studerende til bioanalytikerprofessionen og har fokus på basale laboratoriefærdigheder herunder den til grundlæggende naturvidenskabelige teori. Undervisningen
lys har potentiale til diagnose af sygdom i nethinden og synsnerven
 Nyt fra forskningsfronten Måling af pupilreaktionen for farvet lys har potentiale til diagnose af sygdom i nethinden og synsnerven Kristina Herbst Læge, ph.d.-studerende Øjenafdelingen, Glostrup Universitetshospital
Nyt fra forskningsfronten Måling af pupilreaktionen for farvet lys har potentiale til diagnose af sygdom i nethinden og synsnerven Kristina Herbst Læge, ph.d.-studerende Øjenafdelingen, Glostrup Universitetshospital
Skriftlig tværfaglig mappe-eksamen. onsdag den 25. aug. 2010 kl. 10.00 torsdag den 26. aug. kl. 10.00
 Skriftlig tværfaglig mappe-eksamen S5 onsdag den 25. aug. 2010 kl. 10.00 torsdag den 26. aug. kl. 10.00 Væsentligste hjælpemidler: Mappen, Dansk Laboratoriemedicin, Databog i fysik og kemi og lommeregner.
Skriftlig tværfaglig mappe-eksamen S5 onsdag den 25. aug. 2010 kl. 10.00 torsdag den 26. aug. kl. 10.00 Væsentligste hjælpemidler: Mappen, Dansk Laboratoriemedicin, Databog i fysik og kemi og lommeregner.
E 10: Fremstilling af PEC-solceller
 E 10: Fremstilling af PEC-solceller Formål Formålet med forsøget er at fremstille PEC (Photo Electro Chemical) solceller ud fra vinduesruder, plantesaft, hvid maling og grafit fra en blyant. Apparatur
E 10: Fremstilling af PEC-solceller Formål Formålet med forsøget er at fremstille PEC (Photo Electro Chemical) solceller ud fra vinduesruder, plantesaft, hvid maling og grafit fra en blyant. Apparatur
Colostrum FAQ. Hyppig stillede spørgsmål vedr. Colostrum
 Colostrum FAQ Hyppig stillede spørgsmål vedr. Colostrum 1 Indhold 1. Hvad er Colostrum?... 3 2. Fra hvilket dyr udvindes Colostrum?... 3 3. Hvad sker der med kalvene?... 3 4. Hvorfor er Colostrum fra køer
Colostrum FAQ Hyppig stillede spørgsmål vedr. Colostrum 1 Indhold 1. Hvad er Colostrum?... 3 2. Fra hvilket dyr udvindes Colostrum?... 3 3. Hvad sker der med kalvene?... 3 4. Hvorfor er Colostrum fra køer
Fra Bekendtgørelse om prøver og eksamen i erhvervsrettede uddannelser
 Sammenligning af FISH og Duo-CISH Fluorescerende og chromogen in situ hybridisering til detektion af translokationer i lymfomer ved brug af en break-apart probe Bachelorprojekt efterår 2009 Professionshøjskolen
Sammenligning af FISH og Duo-CISH Fluorescerende og chromogen in situ hybridisering til detektion af translokationer i lymfomer ved brug af en break-apart probe Bachelorprojekt efterår 2009 Professionshøjskolen
PCR (Polymerase Chain Reaction): Opkopiering af DNA
 PCR (Polymerase Chain Reaction): Opkopiering af DNA PCR til at opkopiere bestemte DNA-sekvenser i en prøve er nu en af genteknologiens absolut vigtigste værktøjer. Peter Rugbjerg, Biotech Academy PCR (Polymerase
PCR (Polymerase Chain Reaction): Opkopiering af DNA PCR til at opkopiere bestemte DNA-sekvenser i en prøve er nu en af genteknologiens absolut vigtigste værktøjer. Peter Rugbjerg, Biotech Academy PCR (Polymerase
Sammenligning af kort og lang vævspræpareringsmetode
 Bachelorprojekt Patologiafdelingen Rigshospitalet Sammenligning af kort og lang vævspræpareringsmetode Udarbejdet af: Mette Bang Nyholm (14.12.1974) I perioden: 3. november 28 24. marts 29 Vejledere: Merete
Bachelorprojekt Patologiafdelingen Rigshospitalet Sammenligning af kort og lang vævspræpareringsmetode Udarbejdet af: Mette Bang Nyholm (14.12.1974) I perioden: 3. november 28 24. marts 29 Vejledere: Merete
ELISA Kvantitativ bestemmelse af human IgA i brystmælk Elevvejledning.
 ELISA Kvantitativ bestemmelse af human IgA i brystmælk Elevvejledning. Professionshøjskolen University College Nordjyland Laborantafdelingen 2012 Side 1 Indledning En kvinde føder og bliver mor til sit
ELISA Kvantitativ bestemmelse af human IgA i brystmælk Elevvejledning. Professionshøjskolen University College Nordjyland Laborantafdelingen 2012 Side 1 Indledning En kvinde føder og bliver mor til sit
Kemiøvelse 2 1. Puffere
 Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
IDÉ-KATALOG BACHELORPROJEKTER
 IDÉ-KATALOG BACHELORPROJEKTER Bioanalytikeruddannelsen, UCL Forår 2013 Indhold Vigtig læsning!... 3 Klinisk Biokemisk Afdeling, Svendborg (KBAsv)... 4 Afdeling for Klinisk Biokemi og Farmakologi (KBF)...
IDÉ-KATALOG BACHELORPROJEKTER Bioanalytikeruddannelsen, UCL Forår 2013 Indhold Vigtig læsning!... 3 Klinisk Biokemisk Afdeling, Svendborg (KBAsv)... 4 Afdeling for Klinisk Biokemi og Farmakologi (KBF)...
DNA-smykke Simpel ekstraktion af DNA fra kindceller fra mennesket, som er velegnet til at bruge i et halssmykke
 145678 John Schollar and Dean Madden National Centre for Biotechnology Education, University of Reading Science and Technology Centre, Earley Gate, Reading RG6 6BZ UK E: J.W.Schollar@reading.ac.uk Simpel
145678 John Schollar and Dean Madden National Centre for Biotechnology Education, University of Reading Science and Technology Centre, Earley Gate, Reading RG6 6BZ UK E: J.W.Schollar@reading.ac.uk Simpel
Algedråber og fotosyntese
 Algedråber og fotosyntese Fotosyntesen er en utrolig kompleks proces, som kan være svær at forstå. Heldigvis kan fotosyntesen illustreres på en måde, så alle kan forstå, hvad der helt præcist foregår i
Algedråber og fotosyntese Fotosyntesen er en utrolig kompleks proces, som kan være svær at forstå. Heldigvis kan fotosyntesen illustreres på en måde, så alle kan forstå, hvad der helt præcist foregår i
Fælles svartider. Dansk Patologiselskab Revideret 2013
 Fælles svartider Dansk Patologiselskab Revideret 2013 Biopsimateriale som indgår i planlagte patientforløb 3 hele arbejdsdage DAG 0 Modtages Inden kl. 13.30 Fikseres (mindst 12 timer) Anbringes i kapsel
Fælles svartider Dansk Patologiselskab Revideret 2013 Biopsimateriale som indgår i planlagte patientforløb 3 hele arbejdsdage DAG 0 Modtages Inden kl. 13.30 Fikseres (mindst 12 timer) Anbringes i kapsel
Studieplan Bioanalyse Semester 2
 OMRÅDET FOR SUNDHEDSUDDANNELSER Studieplan Bioanalyse Semester 2 Bioanalytikeruddannelsen i Odense Forår 2017 Semester 2 Indhold 1. Fagets fokus og emner... 3 2. Lektionsplan... 4 3. Litteraturliste...
OMRÅDET FOR SUNDHEDSUDDANNELSER Studieplan Bioanalyse Semester 2 Bioanalytikeruddannelsen i Odense Forår 2017 Semester 2 Indhold 1. Fagets fokus og emner... 3 2. Lektionsplan... 4 3. Litteraturliste...
ScanGel Monoclonal ABO/RH1/K 86495 48 kort 86485 288 kort
 ScanGel Monoclonal ABO/RH1/K 86495 48 kort 86485 288 kort GELER INDEHOLDENDE MONOKLONALE REAGENSER AF MURIN ELLER HUMAN OPRINDELSE ABO1, ABO2, RH1, KEL1 Ag BESTEMMELSE IVD Alle de af Bio-Rad producerede
ScanGel Monoclonal ABO/RH1/K 86495 48 kort 86485 288 kort GELER INDEHOLDENDE MONOKLONALE REAGENSER AF MURIN ELLER HUMAN OPRINDELSE ABO1, ABO2, RH1, KEL1 Ag BESTEMMELSE IVD Alle de af Bio-Rad producerede
PNA ISH Detection Kit Kodenr. K5201
 PNA ISH Detection Kit Kodenr. K5201 9. udgave Til in situ hybridisering ved brug af fluoresceinkonjugerede PNA-prober. Sættet indeholder reagenser til mindst 40 tests*. * Antallet af tests er baseret på
PNA ISH Detection Kit Kodenr. K5201 9. udgave Til in situ hybridisering ved brug af fluoresceinkonjugerede PNA-prober. Sættet indeholder reagenser til mindst 40 tests*. * Antallet af tests er baseret på
Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010
 MedIS, AAU. Det hæmatologiske system og immunforsvaret, 7. Juni 2010 1 Navn: Studienummer: Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010 Dette eksamenssæt
MedIS, AAU. Det hæmatologiske system og immunforsvaret, 7. Juni 2010 1 Navn: Studienummer: Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010 Dette eksamenssæt
Fremstilling af ferrofluids
 Fremstilling af ferrofluids Eksperiment 1: Fremstilling af ferrofluids - Elevvejledning Formål I dette eksperiment skal du fremstille nanopartikler af magnetit og bruge dem til at lave en magnetisk væske,
Fremstilling af ferrofluids Eksperiment 1: Fremstilling af ferrofluids - Elevvejledning Formål I dette eksperiment skal du fremstille nanopartikler af magnetit og bruge dem til at lave en magnetisk væske,
Citat Det synes altid umuligt, indtil det er gjort. Professionsbachelorprojekt
 1 Citat Det synes altid umuligt, indtil det er gjort. NELSON MANDELA Professionsbachelorprojekt Titel : Gordon and Sweets overfor CD271 ved farvning af retikulære fibre Engelsk : Staining for reticular
1 Citat Det synes altid umuligt, indtil det er gjort. NELSON MANDELA Professionsbachelorprojekt Titel : Gordon and Sweets overfor CD271 ved farvning af retikulære fibre Engelsk : Staining for reticular
[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]
![[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU] [BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]](/thumbs/39/19540330.jpg) Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
Thermo. Shandon RAPID-CHROME Iron Stain and RAPID-CHROME Nuclear Fast Red Counterstain ELECTRON CORPORATION. Rev. 5, 09/03 P/N 238997
 Shandon RAPID-CHROME Iron Stain and RAPID-CHROME Nuclear Fast Red Counterstain Thermo ELECTRON CORPORATION Anatomical Pathology USA Clinical Diagnostics 171 Industry Drive Pittsburgh, PA 15275, USA Tel:
Shandon RAPID-CHROME Iron Stain and RAPID-CHROME Nuclear Fast Red Counterstain Thermo ELECTRON CORPORATION Anatomical Pathology USA Clinical Diagnostics 171 Industry Drive Pittsburgh, PA 15275, USA Tel:
AXLAB A/S PRÆSENTERER AS-410 AUTOMATISK SKÆRING AF PARAFFINBLOKKE
 AXLAB A/S PRÆSENTERER AS-410 AUTOMATISK SKÆRING AF PARAFFINBLOKKE VI ARBEJDER FOR LØSNINGER, DER SIKRER KUNDERNE EFFEKTIVITET LANGT IND I FREMTIDEN. I DEN FORBINDELSE RÅDER VI IKKE BARE OVER DET MEST AVANCEREDE
AXLAB A/S PRÆSENTERER AS-410 AUTOMATISK SKÆRING AF PARAFFINBLOKKE VI ARBEJDER FOR LØSNINGER, DER SIKRER KUNDERNE EFFEKTIVITET LANGT IND I FREMTIDEN. I DEN FORBINDELSE RÅDER VI IKKE BARE OVER DET MEST AVANCEREDE
HTERT ANTISTOF TIL ICC PÅ URINCYTOLOGISKE PRÆPARATER
 HTERT ANTISTOF TIL ICC PÅ URINCYTOLOGISKE PRÆPARATER Cytologisk Årsmøde 1. marts 2019 Uddannelsesansvarlig bioanalytikerunderviser Marianne Schou Martiny Patologi, Aarhus Universitetshospital URINVEJSCYTOLOGI
HTERT ANTISTOF TIL ICC PÅ URINCYTOLOGISKE PRÆPARATER Cytologisk Årsmøde 1. marts 2019 Uddannelsesansvarlig bioanalytikerunderviser Marianne Schou Martiny Patologi, Aarhus Universitetshospital URINVEJSCYTOLOGI
Kemi Kulhydrater og protein
 Kemi Kulhydrater og protein Formål: Formålet med forsøget er at vise hvordan man kan påvise protein, fedtstof, simple sukkerarter eller stivelse i forskellige fødevarer. Samtidig kan man få en fornemmelse
Kemi Kulhydrater og protein Formål: Formålet med forsøget er at vise hvordan man kan påvise protein, fedtstof, simple sukkerarter eller stivelse i forskellige fødevarer. Samtidig kan man få en fornemmelse
Forårseksamen Titel på kursus: Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin med industriel specialisering
 Studienummer: 1/10 Forårseksamen 2014 Titel på kursus: Det hæmatologiske system og immunsystemet Uddannelse: Bacheloruddannelsen i Medicin/Medicin med industriel specialisering Semester: 2. semester Eksamensdato:
Studienummer: 1/10 Forårseksamen 2014 Titel på kursus: Det hæmatologiske system og immunsystemet Uddannelse: Bacheloruddannelsen i Medicin/Medicin med industriel specialisering Semester: 2. semester Eksamensdato:
CEREBROSPINALVÆSKER: KLINIK OG MORFOLOGI
 Årsmøde Dansk Cytologiforening 2015 CEREBROSPINALVÆSKER: KLINIK OG MORFOLOGI Ved Helle Broholm Overlæge Patologiafd. Rigshospitalet CSV -CSF cerebro spinal væske (rygmarvsvæske) Hvad er cerebrospinalvæske?
Årsmøde Dansk Cytologiforening 2015 CEREBROSPINALVÆSKER: KLINIK OG MORFOLOGI Ved Helle Broholm Overlæge Patologiafd. Rigshospitalet CSV -CSF cerebro spinal væske (rygmarvsvæske) Hvad er cerebrospinalvæske?
Kemiøvelse 3 C3.1. Na-ISE. Øvelsens pædagogiske rammer
 Kemiøvelse 3 C3.1 Na-ISE Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 7 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 3 C3.1 Na-ISE Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 7 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
FYSISKE MÅLINGER PÅ MÆLK
 FYSISKE MÅLINGER PÅ MÆLK Fysiske målinger på mælk - Hvordan måler man, om koen er syg? 1 Introduktion til forsøget Yverbetændelse, også kaldet mastitis, er en ofte forekommende produktionssygdom hos malkekøer
FYSISKE MÅLINGER PÅ MÆLK Fysiske målinger på mælk - Hvordan måler man, om koen er syg? 1 Introduktion til forsøget Yverbetændelse, også kaldet mastitis, er en ofte forekommende produktionssygdom hos malkekøer
PATOLOGI. Materiale... 1. Cytologi:... 1. Exfoliativ:... 1. Nåleaspiration:... 1. Svartiden... 3. Histologi:... 2
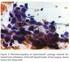 PATOLOGI Materiale... 1 Cytologi:... 1 Exfoliativ:... 1 Nåleaspiration:... 1 Svartiden... 1 Histologi:... 2 Materiale ved operativ behandling af lungetumor... 2 Svartiden... 2 Diagnostik... 2 Metoderne...
PATOLOGI Materiale... 1 Cytologi:... 1 Exfoliativ:... 1 Nåleaspiration:... 1 Svartiden... 1 Histologi:... 2 Materiale ved operativ behandling af lungetumor... 2 Svartiden... 2 Diagnostik... 2 Metoderne...
Kemiøvelse 2 C2.1. Puffere. Øvelsens pædagogiske rammer
 Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Det lyder enkelt, men for at forstå hvilket ærinde forskerne er ude i, er det nødvendigt med et indblik i, hvordan celler udvikles og specialiseres.
 Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr
 Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr Besøget retter sig primært til elever med biologi på B eller A niveau Program for besøget Hvis besøget foretages af en hel klasse,
Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr Besøget retter sig primært til elever med biologi på B eller A niveau Program for besøget Hvis besøget foretages af en hel klasse,
Mikroskopering af fotosyntesens maskineri
 Øvelsesvejledning og journal for Mikroskopering af fotosyntesens maskineri Navn: Klasse: Dato: Baggrund Plan Find følgende organeller og cellebestanddele i figur 34 i Vækstlys og forklar hvilken funktion
Øvelsesvejledning og journal for Mikroskopering af fotosyntesens maskineri Navn: Klasse: Dato: Baggrund Plan Find følgende organeller og cellebestanddele i figur 34 i Vækstlys og forklar hvilken funktion
non-hodgkin lymfom Børnecancerfonden informerer
 non-hodgkin lymfom i non-hodgkin lymfom 3 Årsagen til, at NHL hos børn opstår, kendes endnu ikke. I mange tilfælde af NHL kan der i kræftcellernes arvemateriale påvises forandringer, der forklarer, hvorfor
non-hodgkin lymfom i non-hodgkin lymfom 3 Årsagen til, at NHL hos børn opstår, kendes endnu ikke. I mange tilfælde af NHL kan der i kræftcellernes arvemateriale påvises forandringer, der forklarer, hvorfor
CYTOLOGISK TEKNIK. Sebastian Frische, Anatomisk Institut
 CYTOLOGISK TEKNIK Sebastian Frische, Anatomisk Institut VÆV BESTÅR AF: Vand Proteiner (i cytoplasma, i organeller, i membraner) Lipider (lipiddråber, membraner) Kulhydrater (glykogengranula, glykosyleringer)
CYTOLOGISK TEKNIK Sebastian Frische, Anatomisk Institut VÆV BESTÅR AF: Vand Proteiner (i cytoplasma, i organeller, i membraner) Lipider (lipiddråber, membraner) Kulhydrater (glykogengranula, glykosyleringer)
Vi går derfor ud fra, at I ved, at DNA molekyler er meget lange molekyler
 DNA-profil analyse Indledning DNA-profil analyser eller i daglig tale DNA-fingeraftryk er en metode, der bruges, når man skal finde ud af, hvem der er far et barn, hvis der altså er flere muligheder. Det
DNA-profil analyse Indledning DNA-profil analyser eller i daglig tale DNA-fingeraftryk er en metode, der bruges, når man skal finde ud af, hvem der er far et barn, hvis der altså er flere muligheder. Det
Forstå dine laboratorieundersøgelser. myelomatose
 Forstå dine laboratorieundersøgelser ved myelomatose Denne vejledning giver indblik i de målinger og undersøgelser, der udføres hos patienter med myelomatose. Resultaterne af disse målinger og undersøgelser
Forstå dine laboratorieundersøgelser ved myelomatose Denne vejledning giver indblik i de målinger og undersøgelser, der udføres hos patienter med myelomatose. Resultaterne af disse målinger og undersøgelser
Undersøgelse af forskellige probiotiske stammer
 Undersøgelse af forskellige probiotiske stammer Formål Formålet med denne øvelse er: 1. At undersøge om varer med probiotika indeholder et tilstrækkeligt antal probiotiske bakterier, dvs. om antallet svarer
Undersøgelse af forskellige probiotiske stammer Formål Formålet med denne øvelse er: 1. At undersøge om varer med probiotika indeholder et tilstrækkeligt antal probiotiske bakterier, dvs. om antallet svarer
DIAGNOSTIK AF INDSENDTE GRISE HOS LABORATORIUM FOR SVINESGYDOMME
 DIAGNOSTIK AF INDSENDTE GRISE HOS LABORATORIUM FOR SVINESGYDOMME ERFARING NR. 1717 Ledbetændelse, mavesår, PCV2, Helicobacter og PRRS blev i højere grad observeret hos slagtesvin end hos smågrise ved obduktion
DIAGNOSTIK AF INDSENDTE GRISE HOS LABORATORIUM FOR SVINESGYDOMME ERFARING NR. 1717 Ledbetændelse, mavesår, PCV2, Helicobacter og PRRS blev i højere grad observeret hos slagtesvin end hos smågrise ved obduktion
Diagnostik af pneumonier - og hvad med den kolde
 Diagnostik af pneumonier og hvad med den kolde Klinisk Mikrobiologisk Afdeling Odense Universitetshospital Pneumoni Diagnosen: HOSPITAL: Stilles på klinik og bekræftes af røntgenundersøgelse af thorax
Diagnostik af pneumonier og hvad med den kolde Klinisk Mikrobiologisk Afdeling Odense Universitetshospital Pneumoni Diagnosen: HOSPITAL: Stilles på klinik og bekræftes af røntgenundersøgelse af thorax
HVAD GØR RØGEN VED KROPPEN?
 42 www.op-i-røg.dk GÅ OP I RØG Kræftens Bekæmpelse KAPITEL 5: HVAD GØR RØGEN VED KROPPEN? www.op-i-røg.dk 43 Kapitel 5: Indhold Dette kapitel tager udgangspunkt i, hvad der sker med røgen i kroppen på
42 www.op-i-røg.dk GÅ OP I RØG Kræftens Bekæmpelse KAPITEL 5: HVAD GØR RØGEN VED KROPPEN? www.op-i-røg.dk 43 Kapitel 5: Indhold Dette kapitel tager udgangspunkt i, hvad der sker med røgen i kroppen på
