VUC Århus Laboratoriekursus for selvstuderende i kemi højniveau
|
|
|
- Philippa Jespersen
- 7 år siden
- Visninger:
Transkript
1 Øvelse 1: Bestemmelse af reaktionshastighed Apparatur: 100 ml bægerglas, pipetter 10 ml og 20 ml, sugebold, reagensglas, spatel, stopur. Kemikalier: M Na 2 S 2 O 8 ; M Na 2 S 2 O 8 (opløsningen er også M m.h.t. Na 2 SO 4 ) ; M Na 2 S 2 O 3 (opl. indeholder også stivelse) ; M KI ; M NaCl Øvelsen består af 2 dele. I første del (A) bestemmes hvordan reaktionshastigheden for den undersøgte reaktion afhænger af koncentrationen af reaktanterne. I anden del (B) bestemmes hvordan reaktionshastigheden afhænger af temperaturen. Teori: Den reaktion der skal undersøges er reaktionen mellem persulfationer (S 2 O 2-8 ) og iodidioner (I- ) : S 2 O I - 2 SO I 2 (1) Reaktionshastigheden (egentlig middelhastigheden) for denne reaktion kan udtrykkes som formindskelsen i persulfatkoncentrationen pr. tidsenhed : - [S 2 O8 2- ] v = t Vi antager desuden, at reaktionshastigheden kan udtrykkes v = k [S 2 O 2-8 ] m [I - ] n ( hvor m og n er små, hele tal ) Ved alle forsøgene (i både A og B) måles den tid det tager for koncentrationen af persulfat at formindskes med M. Altså er [S 2 O8 2- ] = M i alle forsøg. Ved starten af hvert forsøg blandes opløsninger der indeholder S 2 O 2-8 og I - samt en lille mængde thiosulfationer (S 2 O 2-3 ) og stivelse. Stivelse kan bruges til at påvise diiodmolekyler, idet opløsninger der indeholder stivelse og diiodmolekyler vil være karakteristisk mørk- eller blåfarvede. Ved reaktion (1) dannes diiodmolekyler, men disse reagerer straks med thiosulfationerne ved denne reaktion: 2 S 2 O I 2 S 4 O I - (2) Så længe opløsningen indeholder thiosulfationer, vil der derfor ikke dannes frie diiodmolekyler selv om reaktion (1) forløber - og man vil derfor heller ikke se nogen farvereaktion med stivelse. Så snart thiosulfationerne slipper op, vil de dannede diiodmolekyler forblive i opløsningen, og denne vil straks blive farvet. Ved hvert forsøg benyttes samme startkoncentration af thiosulfationer: [S 2 O 2-3 ] start = M. Når disse er brugt op ved reaktion med diiod, er [S 2 O 2-8 ] formindsket med M. (Forklar dette i rapporten). Side 1 af 1
2 Forsøgene foregår alle ved at man blander reaktanterne i et bægerglas. Samtidigt startes et stopur. Uret stoppes netop når der viser sig en mørk farve i opløsningen. Det har betydning for reaktionshastighederne at den samlede ionkoncentration i reaktionsblandingerne holdes konstant. Derfor tilsættes NaCl til opløsningen når koncentrationen af KI sænkes, på samme måde erstattes Na 2 S 2 O 8 med Na 2 SO 4. A. Reaktionshastighedens afhængighed af reaktanternes koncentration. Før hvert forsøg skylles glasapparaturet grundigt med demineraliseret vand, hvorefter vandet så vidt muligt rystes af. Man overfører med pipette 20.0 ml Na 2 S 2 O 8 - opløsning til bægerglasset. Derefter tilsættes (også med pipette) 10.0 ml af den M Na 2 S 2 O 3 opløsning der også indeholder stivelse. De angivne volumener M KI og M NaCl, (se tabellen herunder) tappes fra buretter ned i et reagensglas. Indholdet fra reagensglasset hældes ned i bægerglasset samtidigt med at stopuret startes. Sørg for at opløsningerne blandes grundigt. Stands stopuret netop når den først farvning af opløsningen viser sig. Der udføres 2 måleserier: Serie 1 forsøg nr. Volumen M Na 2 S 2 O 8 Volumen M KI Volumen M NaCl 1 20,0 ml 20.0 ml 0 ml ml 15.0 ml 5.0 ml ml 10.0 ml 10.0 ml ml 5.0 ml 15.0 ml Serie 2 Volumen Volumen Volumen forsøg nr M Na 2 S 2 O M KI M NaCl 5 20,0 ml 20.0 ml 0 ml ml 15.0 ml 5.0 ml ml 10.0 ml 10.0 ml ml 5.0 ml 15.0 ml Reaktionstid t Reaktionstid t 1. Anfør resultaterne i en tabel med kolonner for [S 2 O 2-8 ], [I - v ], v og [S 2 O 2-8 ] m [I - ] n 2. Lav en grafisk afbildning for hver måleserie af v som funktion af [I - ]. Kommenter graferne. Hvilken værdi har n? 3. Sammenlign de to måleserier. Hvilken værdi har m? v 4. Beregn [S 2 O 2-8 ]m [I - n for hvert forsøg og anfør resultatet i tabellen. Anfør en værdi for ] hastighedskonstanten. Opskriv hastighedsudtrykket for reaktionen. Side 2 af 2
3 5. Er [S 2 O 2-8 ] og [I- ] begge konstante under målingerne? Hvis ikke hvor mange % ændres de så i løbet af forsøget? Har ændringen nogen væsentlig betydning for forsøgets resultat? B. Reaktionshastighedens afhængighed af temperaturen. Formålet med denne del af øvelsen er, at bestemme reaktionstiden ved forskellige temperaturer, samt at bestemme aktiveringsenergien for reaktionen. Hastighedskonstantens afhængighed af temperaturen kan beskrives ved hjælp af Arrheniusligningen: k = k o exp - E A R T Denne ligning kan omformes ln k = - E A R 1 T + ln k o Ifølge dette udtryk får man en ret linie hvis man afbilder den naturlige logaritme til hastighedskonstanten (ln k) som en funktion af den reciprokke værdi af kelvintemperaturen 1 T. Udfra grafen kan aktiveringsenergien (E A ) og k o bestemmes. Der skal foretages målinger ved 4 temperaturer i intervallet 0-30 C. Der fremstilles derfor vandbade (store bægerglas el. lign) med temperaturer spredt så vidt muligt i intervallet. Til hvert forsøg benyttes 3 reagensglas med henholdsvis 10.0 ml M Na 2 S 2 O 8, 10.0 ml M KI og 5.0 ml M Na 2 S 2 O 3 (med stivelse). De tre glas der hører til et forsøg stilles i vandbadet i mindst et kvarter før de anvendes. Indholdet fra glassene hældes samtidigt ned i et bægerglas idet stopuret startes. Når reaktionsblandingen bliver farvet stoppes uret og temperaturen i blandingen måles så nøjagtigt som muligt (1/10 grads nøjagtighed). Anfør resultaterne fra de 4 forsøg i en tabel som nedenstående: t Temp. ( C) v k ln k T 1/T 1. Beregn reaktionshastigheden og hastighedskonstanten for hvert forsøg. (Brug startkoncentrationer for S 2 O 2-8 og I - ). 2. Beregn værdierne i de resterende kolonner i skemaet. 3. Afbild ln k som funktion af 1/T. Kommentér grafen. Find E A og k o. 4. Find udfra grafen hastighedskonstanten ved en temperatur udenfor måleområdet. Side 3 af 3
4 Øvelse 2: Bestemmelse af styrkekonstanten for ethansyre Apparatur: Kemikalier: Ledningsevnemåler med dyppecelle, 50 ml bægerglas, 50 ml pipette med sugebold, 2 stk 250 ml målekolber. 1, M HCl, 1, M CH 3 COONa, 1, M NaCl, M CH 3 COOH. Formålet med øvelsen er at bestemme styrkeskonstanten K s for ethansyre (CH 3 COOH) ved måling af ledningsevnen på en række opløsninger af ethansyre med forskellig koncentration. Da ethansyre er en svag syre, er den kun delvist protolyseret i vandig opløsning. CH 3 COOH + H 2 O CH 3 COO - + H 3 O + Protolysegraden α afhænger af den formelle koncentration c s. Protolysegraden er defineret ved α = [H 3O + ] c s Ifølge Ostwalds fortyndingslov kan syrens styrkekonstant K s udtrykkes ved: α 2 K s = c s 1 - α hvor c s er ethansyrens formelle koncentration. Ved øvelsen bestemmes α ved forskellige koncentrationer c s af ethansyre. Herudfra beregnes K s ved hjælp af ovenstående formel. Protolysegraden α bestemmes ved først at måle opløsningernes konduktivitet, κ. Ved hjælp af disse værdier kan ethansyrens molare konduktivitet λ beregnes, når den formelle koncentration c s af ethansyre er kendt. λ = κ c s Herefter beregnes protolysegraden ved hjælp af formlen: α = λ λ ο λ o som indgår i brøkens nævner, er den molare konduktivitet ved uendelig fortynding. Denne kan kun bestemmes ved direkte måling for stærke elektrolytter. Da ethansyre er en svag elektroly må værdien bestemmes indirekte ved først at måle λ o for nogle passende stærke elektrolytter og derpå beregne λ o for ethansyre ved hjælp af Kohlrauchs lov: λ o (CH 3 COOH) = λ o (H 3 O + ) + λ o (CH 3 COO - ) De to værdier på højre side (og dermed λ o (CH 3 COOH)) findes ved at måle på tre opløsninger af henholdsvis HCl, NaCl og CH 3 COONa. Målingerne foretages på 1, molære opløsninger af disse stærke elektrolytter, og man kan ved denne koncentration tilnærmelsesvis regne med, at man måler λ o. Der gælder λ o (HCl) = λ o (H 3 O + ) + λ o (Cl - ) λ o (CH 3 COONa) = λ o (CH 3 COO - ) + λ o (Na + ) λ o (NaCl) = λ o ((Na + ) + λ o (Cl - ) Side 4 af 4
5 Ved hjælp af de målte værdier kan λ o (CH 3 COOH) bestemmes: λ o (CH 3 COOH) = λ o (HCl) + λ o (CH 3 COONa) - λ o (NaCl) (Gør rede for dette i rapporten) Før målingerne justeres konduktivitetsmåleren med opløsning med kendt konduktivitet. Herefter måles konduktiviteten κ for de 1, molære opløsninger af HCl, NaCl og CH 3 COONa. Målingerne udføres i et 50 ml bægerglas. Målecellen skylles med demineraliseret vand før hver måling. Derefter skylles bægerglas og målecelle med den opløsning der skal måles på. Den mængde opløsning, som er brugt til skylningen, hældes ud. Der fyldes en ny portion opløsning i bægerglasset og målingen foretages. Værdierne opstilles i en tabel som denne: Opløsning κ λ 1, M HCl 1, M NaCl 1, M CH 3 COONa På tilsvarende måde måles på opløsningerne af ethansyre. Der startes med den udleverede molære opløsning. De følgende opløsninger fremstilles ved at fortynding ved hjælp af en 50 ml pipette og 250 ml målekolbe. Resultaterne indføres i en tabel som denne: c s κ λ α 5, M 1, M 2, M 4, M 8, M c s α2 1 - α 1. Beregn λº for de tre stærke elektrolytter ved hjælp af ligningen λº = κ c. Indsæt koncentrationen i mol/ cm 3. λº angives i S cm 2 /mol. 2. Beregn λ o for ethansyre udfra de fundne værdier for λ for de tre stærke elektrolytter. 3. Beregn størrelserne κ, λ, α, c s α2 1 - α som er angivet i tabellen herover. 4. Angiv en værdi for ethansyres styrkekonstant K s. Sammenlign med en tabelværdi. 5. Sammenlign de målte molare konduktiviteter for HCl, NaCl, CH 3 COONa og CH 3 COOH med tabelværdier. Side 5 af 5
6 Øvelse 3: Bestemmelse af G o, H o og S o for en ligevægtsreaktion Apparatur: 4 stk. 250 ml koniske kolber ; 3 magnetomrørere ; 2 vandbade ; termometer (1/10 grads inddeling) ; tragt ; filtrerpapir ; 100 ml konisk kolbe ; 25 ml pipette ; sugebold. Kemikalier: M AgNO 3 ; M KI ; PbSO 4 (findelt) Teori: Formålet med øvelsen er, at undersøge temperaturens indflydelse på ligevægtskonstanten for ligevægten PbSO 4 (s) + 2 I - (aq) PbI 2 (s) + SO -2 4 (aq) Forsøget startes med at tilsætte PbSO 4 (s) til en M opløsning af KI. Både PbSO 4 og KI er tungtopløselige i vand og ovenstående ligevægt indstiller sig. Når ligevægten har indstillet sig filtreres en del af opløsningen fra, så bundfaldet fjernes. En kendt mængde af den filtrerede opløsning titreres med M AgNO 3 for at bestemme koncentrationen af I - i ligevægtsblandingen. Ved titreringen sker følgende reaktion: Ag + (aq) + I - (aq) AgI (s) Da begyndelseskoncentrationen af I - også er kendt, kan [SO -2 4 ] i ligevægtsblandingen beregnes, og dermed ligevægtskonstanten for ligevægten: K = [SO-2 4 ] [I - ] 2 Ved at titrere ligevægtsopløsninger for forskellige temperaturer, kan ligevægtskonstanten ved disse forskellige temperaturer findes. Udfra de beregnede værdier for K, kan G o, H o og S o for reaktionen findes. G o kan findes ved de forskellige temperaturer udfra ligevægtskonstanten K ved at benytte sammenhængen G o = - R T ln K Målingerne foretages indenfor temperaturintervallet 10 C - 30 C. Indefor et så lille temperaturinterval kan man regne H o og S o for konstante. Afbilder man G o som funktion af temperaturen (absolut temperatur), kan H o og S o bestemmes grafisk, idet G ο afhænger lineært af T: G o = H o - T S o H o og - S o findes som henholdsvis liniens skæring med y-aksen og dens hældning. Side 6 af 6
7 Fremstil 2 vandbade med temperaturer på ca. 10 C og 30 C. De 3 ligevægtsopløsninger fremstilles ved at blande 2 g fast PbSO 4 med ca. 100 ml M KI i tre 250 ml koniske kolber. Anbring en røremagnet i hver af kolberne. Placer de to af kolberne i hver sit vandbad, på en magnetomrører. Kontrollér vandbadets temperatur med jævne mellemrum. Kolberne i vandbadene bør stå en times tid inden der udtages prøver til titrering. Imens laves forsøget med den tredje kolbe, som har stuetemperatur. Når denne kolbe har stået et kvarters tid med omrøring måles temperaturen i blandingen (med 1/10 grads nøjagtighed) og der filtreres ca. 60 ml af kolbens indhold over i en 100 ml konisk kolbe ml af filtratet overføres med en pipette til en 250 ml konisk kolbe. Denne opløsning titreres under magnetomrøring med M AgNO 3. I starten af titreringen vil opløsningen se mælket hvid ud p.g.a. dannelsen af et fint bundfald af AgI. Ækvivalenspunktet er nået når en dråbe AgNO 3 pludselig får krystallerne til at klumpe sig sammen. Afpipettér yderligere ml af opløsningen og gentag titreringen. De to tempererede ligevægtsblandinger behandles på samme måde. Mål temperaturen i ligevægtsblandingerne lige inden de filtreres (husk 1/10 grads nøjagtighed). Filtrer derefter hurtigt 60 ml af opløsningen fra. Udtag ml af filtratet med pipette og titrer med M AgNO 3. Vær meget omhyggelig med alle titreringerne. Foretag 2 titreringer ved hver temperatur. Måleresultaterne og beregnede værdier kan f.eks. samles i en tabel som dette: t ( C) T (K) V(AgNO 3 ) [I - ] (M) [SO -2 4] (M) K G ο 1. Hvordan kan man se, at der sker en reaktion når den faste PbSO 4 sættes til KI opløsningen? 2. Hvilken betydning har det, at bundfaldet filtreres fra inden opløsningen titreres? 3. Beregn koncentrationen af I - i ligevægtsblandingerne udfra resultaterne fra titreringerne. 4. Beregn koncentrationen af SO -2 4 i ligevægtsblandingerne. 5. Beregn K og G o for hvert forsøg. 6. Afbild G o grafisk som funktion af T (Kelvin). Tegn bedste rette linie og benyt denne til at finde H o og S o. 7. Find udfra grafen G o ved 298 K. 8. Sammenlign de fundne værdier for H o og S o og G o ved 298 K med tabelværdier. Side 7 af 7
8 Øvelse 4: Frysepunktssænkning Apparatur: Kemikalier: 1 stk. 250 ml bægerglas ; reagensglas ; termometer (1/10 grads inddeling). cyclohexan ; naphthalen ; propansyre. Øvelsen består af 2 næsten ens halvdele. Den eneste forskel er, at man i første del benytter naftalen som opløst stof, mens man i anden del benytter propansyre. I øvelsen skal den molare masse af henholdsvis naftalen og propansyre bestemmes ved at måle frysepunktssænkningen af en opløsning af stofferne i cyclohexan. Frysepunktssænkningen er en kolligativ egenskab. Det vil sige den afhænger kun af antallet af partikler, men ikke af hvilke partikler det drejer sig om. Frysepunktssænkningen for en opløsning kan beskrives ved udtrykket: T f = K f c molal Hvor T f er frysepunktssænkningen, K f er den molale frysepunktskonstant (en konstant der er karakteristisk for opløsningsmidlet) og c molal er den samlede molale koncentration af partikler i opløsningen.. Den molale koncentration c molal er stofmængden af opløst stof pr. kg n opløst stof opløsningsmiddel: c molal = m opløsningsmiddel Cyclohexan er specielt velegnet til denne øvelse, da dette stof har en relativt stor molal frysepunktskonstant: K f = 20,4 K kg mol -1 (cyclohexan) Lav et kuldebad ved at fylde et 250 ml bægerglas 2/3 op med knust is, hvorefter der tilsættes koldt vand, så glasset er fyldt næsten til randen. Det er vigtigt at have et effektivt kuldebad under hele forsøget. Med pipette (og sugebold) overføres 10.0 ml cyclohexan til et rent, tørt reagensglas. Derefter anbringes et termometer (digitalt, indstillet til visning af 1/10 grader) i reagensglasset. Reagensglasset placeres i isbadet, så man kan se væsken i glasset udefra. Rør grundigt (men forsigtigt) rundt i reagensglasset med termometeret. Iagttag reagensglassets indhold under fortsat omrøring. Aflæs termometret, når væsken begynder at krystallisere. Det kan være svært at se krystallerne, men man kan se på termometeret, når man når frysepunktet. Så holder temperaturen sig konstant i længere tid. Reagensglasset skal blive stående i isbadet, mens termometret aflæses. Når frysepunktet er aflæst, tages reagensglasset op. Kontrollér, at der er sket en krystallisation. Lad derpå stoffet smelte helt og gentag forsøget, indtil målingen af frysepunktet er helt sikker. Side 8 af 8
9 Tag derefter reagensglasset op. Afvej nøjagtigt mellem 0.20 og 0.22 g naphthalen (0.001 grams nøjagtighed). Overfør stoffet til reagensglasset og opløs det fuldstændigt i cyclohexan ved omrøring med termometret. Mål opløsningens frysepunkt på samme måde som før. Denne gang kan man bedre se krystallerne. De dannes som små fnug, der svæver rundt i væsken. Frysepunktet skal aflæses, når krystallisationen begynder, dvs. så snart man kan se tydelig krystallisation. Husk, at reagensglasset skal blive stående i isbadet, mens temperaturen aflæses. Tag reagensglasset op, så krystallerne får lov at smelte og gentag derpå målingen indtil frysepunktet er bestemt med sikkerhed Måleresultaterne kan i rapporten f.eks. samles i en tabel som denne: Frysepunkt for ren cyclohexan Masse af naphthalen Frysepunkt for cyclohexan med naphthalen 1. Beregn naphthalens molare masse udfra resultaterne. 2. Beregn den procentiske afvigelse mellem den fundne værdi og tabelværdien. Herefter udføres et helt tilsvarende forsøg med propansyre i stedet for naphthalen. Frysepunkt for ren cyclohexan Masse af propansyre Frysepunkt for cyclohexan med propansyre 1. Beregn propansyres molare masse udfra resultaterne. 2. Beregn den procentiske afvigelse mellem den fundne værdi og tabelværdien. 3. Hvad kan forklaringen / forklaringerne være til eventuelle afvigelser mellem tabelværdien og det eksperimentelle resultat? Nævn eksempler på andre kolligative egenskaber. Side 9 af 9
10 Øvelse 5: Nernsts ligning Apparatur: 2 stk 50 ml bægerglas ; 10 ml pipette ; 20 ml pipette ; filtrerpapir i strimler ; sandpapir ; voltmeter ; 2 ledninger med krokodillenæb Kemikalier: Kobbertråd ; sølvtråd ; 1.00 M CuSO 4 ; M AgNO 3 ; 10% NH 4 NO 3 opløsning Formålet med øvelsen er at bekræfte Nernsts lov ved en række målinger på en elektrokemisk celle. Denne celle kan beskrives ved cellediagrammet: med den strømgivende reaktion Cu(s) Cu 2+ (aq) Ag + (aq) Ag(s) Cu(s) + 2 Ag + (aq) Cu 2+ (aq) + 2 Ag(s) I øvelsen måles U 0 for forskellige værdier af [Ag + ]. [Cu 2+ ] holdes derimod konstant lig 1.00 M i alle målinger. Nernsts lov kan da udtrykkes: U 0 = U -o 0-59 mv 2 log [Cu2+ ] [Ag + ] 2 = U-o 0-59 mv 2 log 1 [Ag + ] 2 U 0 = U -o mv log [Ag + ] Når målingerne foretages ved forskellige koncentrationer af Ag +, får man ifølge Nernsts lov en ret linie med hældningen 59 mv ϒ hvis man afbilder U 0 som funktion af log [Ag + ]. De to halvceller fremstilles i hver sit rene (!) 50 ml bægerglas. Glassene fyldes halvt op med henholdsvis M AgNO 3 og 1.00 M CuSO 4. De placeres ved siden af hinanden og forbindes med en saltbro bestående af en 1-2 cm bred strimmel af filtrerpapir, der er gennemvædet med 10% NH 4 NO 3. Kobber- og sølvtråden renses omhyggeligt med sandpapir og skylles med demineraliseret vand før de placeres i deres opløsninger. Metaltrådene må hverken røre siderne af glasset eller saltbroen under målingen. ϒ De 59 mv som indgår i Nernsts ligning er i virkeligheden størrelsen R T F Som det ses er denne størrelse temperaturafhængig. Værdien 59 mv gælder ved 25 C. Hvis målingerne foretages ved en anden temperatur, skal konstanten korrigeres. Side 10 af 10
11 Metaltrådene forbindes til voltmeteret ved hjælp af to ledninger med isolerede krokodillenæb. Vælg det måleområde, som giver den mest nøjagtige måling og aflæs U 0 når apparatets visning har stabiliseret sig. De øvrige målinger udføres på samme måde, hver gang med en 3 gange lavere værdi af [Ag + ]. Fortyndingen foretages ved at udtage 10.0 ml af sølvnitratopløsningen i sølvhalvcellen med en pipette. Disse 10.0 ml hældes ud. Derefter udtages yderligere 10.0 ml med den samme pipette og det resterende indhold i sølhalvcellen hældes ud. Bægerglasset skylles med demineraliseret vand og så meget som muligt af vandet rystes af. Derpå hældes de 10.0 ml AgNO 3 - opløsning tilbage i glasset. Med en anden pipette tilsættes 20.0 ml demineraliseret vand. [Ag + ] i glasset er nu 1/3 af koncentrationen i det forrige forsøg. Foretag målinger med de Ag + koncentrationer, der er angivet i tabellen herunder: Forsøg nr. [Ag + ] U 0 log[ag + ] M M M M M M M 1. Afbild U 0 på et stykke millimeterpapir som funktion af log [Ag + ] 2. Tegn "bedste rette linie" på grundlag af målepunkterne og find hældningskoefficienten. 3. Kommenter grafen. Er Nernsts lov blevet bekræftet? 4. Find U -o 0 udfra den grafiske afbildning og sammenlign med en tabelværdi. Side 11 af 11
12 Øvelse 6: Opløselighedsprodukt Apparatur: 2 stk 50 ml bægerglas ; 25 ml pipette ; burette; stativ ; filtrerpapir i strimler ; sandpapir ; voltmeter ; 2 ledninger med krokodillenæb Kemikalier: 2 stk. sølvtråd ; M AgNO 3 ; M KCl ; 10% NH 4 NO 3 opløsning Formålet med øvelsen er, at finde opløselighedsproduktet K o for sølvchlorid, og vise, at ionproduktet for ligevægten er konstant. Hvis dette er tilfældet, er ligevægtsloven AgCl (s) Ag + (aq) + Cl - (aq) (I) eftervist. [Ag + ] [Cl - ] = K o Der foretages en række målinger på en elektrokemisk celle, hvis ene halvcelle indeholder M AgNO 3. I den anden halvcelle findes ligevægtssystemet beskrevet ved reaktion (I). Sammensætningen af opløsningen med ligevægtsreaktionen varieres i løbet af øvelsen. [Ag + ] bestemmes ved elektrokemiske målinger. [Cl - ] beregnes udfra kendskab til de benyttede opløsninger. Når de to koncentrationer er bestemt for et givet forsøg, kan ionproduktet [Ag + ] [Cl - ] og dermed K o beregnes. De to halvceller fremstilles i hver sit rene (!) 50 ml bægerglas. Det ene glas fyldes halvt op med M AgNO 3. I det andet afpipetteres 25.0 ml KCl. De placeres ved siden af hinanden og forbindes med en saltbro bestående af en 1-2 cm bred strimmel af filtrerpapir, der er gennemvædet med 10% NH 4 NO 3. Der fyldes M AgNO 3 i en burette, som nulstilles. Tilsæt fra buretten 5.0 ml AgNO 3 -opløsning til bægerglasset med KCl. Rør grundigt rundt, så ligevægten indstiller sig. Sølvtrådene renses omhyggeligt med sandpapir og skylles med demineraliseret vand før de placeres i opløsningerne. Metaltrådene må hverken røre siderne af glasset eller saltbroen under målingen. Aflæs U o (husk fortegn) når apparatets visning er blevet konstant. Tilsæt yderligere 5.0 ml AgNO 3 opløsning fra buretten, rør grundigt om og mål U o igen. Fortsæt på sammen måde til der er lavet 5 målinger med de volumener, som er angivet i tabellen på næste side. Side 12 af 12
13 Volumen M AgNO 3 U o [Ag + ] [Cl - ] [Ag + ] [Cl - ] 5.0 ml 10.0 ml 15.0 ml 20.0 ml 23.0 ml (bemærk, at der kun er tilsat i alt 23.0 ml AgNO 3 i sidste forsøg) 1. Vis, at log [Ag + ] kan beregnes ved log [Ag + ] = U o mv 59 mv for hvert forsøg og beregn [Ag + ] 2. Beregn [Cl - ] for hvert forsøg. Gå i denne beregning ud fra, at al tilsat Ag + fældes som AgCl. Husk at opløsningens volumen ændres for hvert forsøg. 3. Beregn ionproduktet for hvert forsøg. Kommenter resultaterne. Er ionproduktet konstant? 4. Angiv - udfra dine resultater - en værdi for sølvchlorids opløselighedsprodukt. Sammenlign med en tabelværdi. 5. Hvilken indflydelse vil det have for det beregnede opløselighedsprodukt, hvis ikke al sølvchlorid i opløsningerne er fældet ud (dvs. hvis målingerne er foretaget på overmættede opløsninger). 6. I punkt 2 antages at al tilsat Ag + udfældes som AgCl. I punkt 1 er den reelle [Ag + ] bestemt. Beregn for ét af forsøgene hvor stor en brøkdel af de tilsatte Ag + ioner der faktisk findes som Ag + (aq) i opløsningen. Kommenter herefter den tilnærmelse der blev gjort i pkt. 2. Side 13 af 13
Noter til kemi A-niveau
 Noter til kemi A-niveau Grundlæggende kemi til opgaveregning 2.0 Af Martin Sparre INDHOLD 2 Indhold 1 Kemiske ligevægte 3 1.1 En simpel kemisk ligevægt.................... 3 1.2 Forskydning af ligevægte.....................
Noter til kemi A-niveau Grundlæggende kemi til opgaveregning 2.0 Af Martin Sparre INDHOLD 2 Indhold 1 Kemiske ligevægte 3 1.1 En simpel kemisk ligevægt.................... 3 1.2 Forskydning af ligevægte.....................
Kemiøvelse 2 1. Puffere
 Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT. Litteratur: Klasse: Dato: Ark 1 af. Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV
 Fag: KEMI Journal nr. Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT Navn: Litteratur: Klasse: Dato: Ark 1 af Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV Formålet er at bestemme opløseligheden
Fag: KEMI Journal nr. Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT Navn: Litteratur: Klasse: Dato: Ark 1 af Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV Formålet er at bestemme opløseligheden
Øvelse 4.2 1/5 KemiForlaget
 KST G ERNÆRING Benthe Schou ØVELSE 4. Øvelse: Iodtal for fedtstoffer Indledning Et fedtstofs ernæringsmæssige sundhed bestemmes af hvilke fedtsyrer, der indgår i fedtstoffet. Fedtstoffets sundhed er stærkt
KST G ERNÆRING Benthe Schou ØVELSE 4. Øvelse: Iodtal for fedtstoffer Indledning Et fedtstofs ernæringsmæssige sundhed bestemmes af hvilke fedtsyrer, der indgår i fedtstoffet. Fedtstoffets sundhed er stærkt
Kemiøvelse 2 C2.1. Puffere. Øvelsens pædagogiske rammer
 Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Et fedtstofs iodtal. Problemstilling. Kapitel 2: Uorganisk kemi (iodometri) R 1 CH 2 O C R 2 O R 3. H + Br Br C C Br Br
 Et fedtstofs iodtal Kapitel 2: Uorganisk kemi (iodometri) Problemstilling Additionsreaktionen til dobbeltbindinger mellem -atomer, 8?7, kan vises ved addition af dibrom til et fedtstof. Reaktionen benyttes
Et fedtstofs iodtal Kapitel 2: Uorganisk kemi (iodometri) Problemstilling Additionsreaktionen til dobbeltbindinger mellem -atomer, 8?7, kan vises ved addition af dibrom til et fedtstof. Reaktionen benyttes
Øvelse: Ligevægt. Aflever de udfyldte journalark på Fronter individuelt
 KEMI kl.2.1 Øvelse Oprettet 2007-05-20 hjsn@rts.dk videreforarbejdet af 2008-09 bos@rts.dk Øvelse: Ligevægt Læremål at kunne anvende Le Chateliers princip til bestemmelse af forskydningen af en ligevægt
KEMI kl.2.1 Øvelse Oprettet 2007-05-20 hjsn@rts.dk videreforarbejdet af 2008-09 bos@rts.dk Øvelse: Ligevægt Læremål at kunne anvende Le Chateliers princip til bestemmelse af forskydningen af en ligevægt
Kemiøvelser (til eleverne)
 Fra ressourceforbandelse til grøn omstilling Kemiøvelser (til eleverne) Udviklet af Kjeld Lundgaard, kemilærer på Ingrid Jespersens Gymasieskole 1. Eksperiment: Opløselighed af lithiumchlorid Formål: Bestemme
Fra ressourceforbandelse til grøn omstilling Kemiøvelser (til eleverne) Udviklet af Kjeld Lundgaard, kemilærer på Ingrid Jespersens Gymasieskole 1. Eksperiment: Opløselighed af lithiumchlorid Formål: Bestemme
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Puffere. Øvelsens pædagogiske rammer. Sammenhæng. Formål. Arbejdsform: Evaluering
 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
Forsæbning af kakaosmør
 Side: 1/10 Forsæbning af kakaosmør Forfattere: Lone Berg Redaktør: Thomas Brahe Faglige temaer: Kompetenceområder: Introduktion: Formålet med denne øvelse er at bestemme kakaosmørs gennemsnitlige molare
Side: 1/10 Forsæbning af kakaosmør Forfattere: Lone Berg Redaktør: Thomas Brahe Faglige temaer: Kompetenceområder: Introduktion: Formålet med denne øvelse er at bestemme kakaosmørs gennemsnitlige molare
Teori Hvis en aminosyre bringes til at reagere med natriumhydroxid, dannes et natriumsalt: NH 2
 Øvelser om aminosyrer og peptider Øvelse 2 Identifikation af et aminosyrehydrochlorid Formål Forsøgets formål er at undersøge et af tre forskellige aminosyrehydrochlorider, som udleveres til klassen. Identifikationen
Øvelser om aminosyrer og peptider Øvelse 2 Identifikation af et aminosyrehydrochlorid Formål Forsøgets formål er at undersøge et af tre forskellige aminosyrehydrochlorider, som udleveres til klassen. Identifikationen
Kemiøvelse 2 C2.1. Puffere. Øvelsens pædagogiske rammer
 Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 2 C2.1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Jernindhold i fødevarer bestemt ved spektrofotometri
 Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Bioteknologi 4, Tema 8 Forsøg www.nucleus.dk Linkadresserne fungerer pr. 1.7.2011. Forlaget tager forbehold for evt. ændringer i adresserne. Jernindhold i fødevarer bestemt ved spektrofotometri Formål
Måling af ph i syrer og baser
 Kemiøvelse 1 1.1 Måling af ph i syrer og baser Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 1 ved bioanalytikeruddannelsen. Øvelsen skal betragtes som en
Kemiøvelse 1 1.1 Måling af ph i syrer og baser Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 1 ved bioanalytikeruddannelsen. Øvelsen skal betragtes som en
Øvelsesvejledninger til laboratoriekursus i Kemi A. VUC Aarhus, GSK-afdelingen
 Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, GSK-afdelingen 2014 Indholdsfortegnelse Velkommen til laboratoriekursus i Kemi A på VUC Aarhus 2014.... 3 Laboratoriearbejdet.... 3 Sikkerheden
Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, GSK-afdelingen 2014 Indholdsfortegnelse Velkommen til laboratoriekursus i Kemi A på VUC Aarhus 2014.... 3 Laboratoriearbejdet.... 3 Sikkerheden
Højere Teknisk Eksamen maj Kemi A. - løse opgaverne korrekt. - tegne og aflæse grafer. Ved bedømmelsen vægtes alle opgaver ens.
 054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
KOSMOS. 7.1 Spaltning af sukker. Materialer MADENS KEMI KEMISKE STOFFER I MADEN DISACCHARIDER
 KEMISKE STOFFER I MADEN DISACCHARIDER 7.1 Spaltning af sukker I skal undersøge, hvordan sukker spaltes ved kontakt med en syre. Almindelig hvidt sukker er et disaccharid. Det kan spaltes i to monosaccharider:
KEMISKE STOFFER I MADEN DISACCHARIDER 7.1 Spaltning af sukker I skal undersøge, hvordan sukker spaltes ved kontakt med en syre. Almindelig hvidt sukker er et disaccharid. Det kan spaltes i to monosaccharider:
Syre-base titreringer
 Syre-base titreringer Titrering: Er en analytisk metode til bestemmelse af mængden af et stof (A) i et kendt volumen af en opløsning. Metode: Et kendt volumen af opløsningen der indeholder A udtages. En
Syre-base titreringer Titrering: Er en analytisk metode til bestemmelse af mængden af et stof (A) i et kendt volumen af en opløsning. Metode: Et kendt volumen af opløsningen der indeholder A udtages. En
UNDERSØGELSE AF JORDRESPIRATION
 UNDERSØGELSE AF JORDRESPIRATION Formål 1. At bestemme omsætningen af organisk stof i jordbunden ved at måle respirationen med en kvantitative metode. 2. At undersøge respirationsstørrelsen på forskellige
UNDERSØGELSE AF JORDRESPIRATION Formål 1. At bestemme omsætningen af organisk stof i jordbunden ved at måle respirationen med en kvantitative metode. 2. At undersøge respirationsstørrelsen på forskellige
[H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2
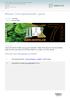
![[H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2 [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b. m ph + poh = 14 [H 3 O + ][OH ] = m 2 pk s + pk b = 14 K s K b = m 2](/thumbs/48/24964855.jpg) ph = -log [H 3 O + ] poh = -log [OH ] pk s = -log K s pk b = -log K b [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b m ph + poh = 1 [H 3 O + ][OH ] = 10 1 m 2 pk s + pk b = 1 K s K
ph = -log [H 3 O + ] poh = -log [OH ] pk s = -log K s pk b = -log K b [H 3 O + ] = 10 ph m [OH ] = 10 poh m K s = 10 pks m K b = 10 pk b m ph + poh = 1 [H 3 O + ][OH ] = 10 1 m 2 pk s + pk b = 1 K s K
Exoterme og endoterme reaktioner (termometri)
 AKTIVITET 10 (FAG: KEMI) NB! Det er i denne øvelse ikke nødvendigt at udføre alle forsøgene. Vælg selv hvilke du/i vil udføre er du i tvivl så spørg. Hvis du er interesseret i at måle varmen i et af de
AKTIVITET 10 (FAG: KEMI) NB! Det er i denne øvelse ikke nødvendigt at udføre alle forsøgene. Vælg selv hvilke du/i vil udføre er du i tvivl så spørg. Hvis du er interesseret i at måle varmen i et af de
Dialyse og carbamidanalyse
 C.12.1 Dialyse og carbamidanalyse Formål: Ved dialyse af en vandig opløsning af proteinet albumin og det lavmolekylære stof carbamid trænes forskellige laboratorieprocedurer (afpipettering, tidtagning,
C.12.1 Dialyse og carbamidanalyse Formål: Ved dialyse af en vandig opløsning af proteinet albumin og det lavmolekylære stof carbamid trænes forskellige laboratorieprocedurer (afpipettering, tidtagning,
Opgaver til: 6. Syrer og baser
 Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Skriftlig eksamen i Kemi F2 (Fysisk kemi)
 Skriftlig eksamen i Kemi F2 (Fysisk kemi) Onsdag 16 April 2008 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 8 sider
Skriftlig eksamen i Kemi F2 (Fysisk kemi) Onsdag 16 April 2008 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 8 sider
E 10: Fremstilling af PEC-solceller
 E 10: Fremstilling af PEC-solceller Formål Formålet med forsøget er at fremstille PEC (Photo Electro Chemical) solceller ud fra vinduesruder, plantesaft, hvid maling og grafit fra en blyant. Apparatur
E 10: Fremstilling af PEC-solceller Formål Formålet med forsøget er at fremstille PEC (Photo Electro Chemical) solceller ud fra vinduesruder, plantesaft, hvid maling og grafit fra en blyant. Apparatur
1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA
 1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA Formålet med denne øvelse er at bestemme indholdet af krystalvand i krystalsoda, som har den kemiske formel Na 2 CO 3 xh 2 O. Teori: En del ionforbindelser (salte)
1. BESTEMMELSE AF KRYSTALVAND I KRYSTALSODA Formålet med denne øvelse er at bestemme indholdet af krystalvand i krystalsoda, som har den kemiske formel Na 2 CO 3 xh 2 O. Teori: En del ionforbindelser (salte)
Bilag til Kvantitativ bestemmelse af glucose
 Bilag til Kvantitativ bestemmelse af glucose Det synlige formål med øvelsen er at lære, hvorledes man helt præcist kan bestemme små mængder af glucose i en vandig opløsning ved hjælp af målepipetter, spektrofotometer
Bilag til Kvantitativ bestemmelse af glucose Det synlige formål med øvelsen er at lære, hvorledes man helt præcist kan bestemme små mængder af glucose i en vandig opløsning ved hjælp af målepipetter, spektrofotometer
Kvantitativ bestemmelse af reducerende sukker (glukose)
 Kvantitativ bestemmelse af reducerende sukker (glukose) Baggrund: Det viser sig at en del af de sukkerarter vi indtager med vores mad er hvad man i fagsproget kalder reducerende sukkerarter. Disse vil
Kvantitativ bestemmelse af reducerende sukker (glukose) Baggrund: Det viser sig at en del af de sukkerarter vi indtager med vores mad er hvad man i fagsproget kalder reducerende sukkerarter. Disse vil
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT
 1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
Projekt Vandløb 1p uge 43 og 44, 2012. Projekt Vandløb
 Projekt Vandløb Denne projektopgave markerer afslutningen på det fællesfaglige emne Vand. I skal enten individuelt eller i mindre grupper (max fire personer pr gruppe) skrive en rapport, som sammenfatter
Projekt Vandløb Denne projektopgave markerer afslutningen på det fællesfaglige emne Vand. I skal enten individuelt eller i mindre grupper (max fire personer pr gruppe) skrive en rapport, som sammenfatter
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Øvelse: Chlorofylindholdet i spinat
 Forløb: Smagen af frugt og grønt: Kemimateriale modul 2-8 Aktivitet: Øvelse: Chlorofylindholdet i spinat Fag: Kemi Klassetrin: 1. g, 2. g, 3. g Side: 1/6 Øvelse: Chlorofylindholdet i spinat Forfattere:
Forløb: Smagen af frugt og grønt: Kemimateriale modul 2-8 Aktivitet: Øvelse: Chlorofylindholdet i spinat Fag: Kemi Klassetrin: 1. g, 2. g, 3. g Side: 1/6 Øvelse: Chlorofylindholdet i spinat Forfattere:
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Det store energikørekort
 Blik- og Rørarbejderforbundet - i forbund med fremtiden El- og Vvs-branchens Uddannelsessekretariat - Højnæsvej 71-2610 Rødovre - tlf.: 36 72 64 00 www.vvs-uddannelse.dk/folkeskole - E-mail: folkeskole@vvsu.dk
Blik- og Rørarbejderforbundet - i forbund med fremtiden El- og Vvs-branchens Uddannelsessekretariat - Højnæsvej 71-2610 Rødovre - tlf.: 36 72 64 00 www.vvs-uddannelse.dk/folkeskole - E-mail: folkeskole@vvsu.dk
Matematiske modeller Forsøg 1
 Matematiske modeller Forsøg 1 At måle absorbansen af forskellige koncentrationer af brilliant blue og derefter lave en standardkurve. 2 ml pipette 50 og 100 ml målekolber Kuvetter Engangspipetter Stamopløsning
Matematiske modeller Forsøg 1 At måle absorbansen af forskellige koncentrationer af brilliant blue og derefter lave en standardkurve. 2 ml pipette 50 og 100 ml målekolber Kuvetter Engangspipetter Stamopløsning
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Øvelser 10. KlasseCenter Vesthimmerland Kaj Mikkelsen
 Indholdsfortegnelse Indholdsfortegnelse... 1 Bygning af et glucosemolekyle... 2 Bygning af et poly- sakkarid.... 3 Påvisning af glukose (1)... 4 Påvisning af glucose (2)... 5 Påvisning af disakkarider....
Indholdsfortegnelse Indholdsfortegnelse... 1 Bygning af et glucosemolekyle... 2 Bygning af et poly- sakkarid.... 3 Påvisning af glukose (1)... 4 Påvisning af glucose (2)... 5 Påvisning af disakkarider....
TI-B 9 (85) Prøvningsmetode Hærdnet betons chloridindhold
 Hærdnet betons chloridindhold Teknologisk Institut, Byggeri Hærdnet betons chloridindhold Deskriptorer: - Udgave: 1 Dato: 1985-05-7 Sideantal: / Bilag: 1 Udarbejdet af: BF/JKU Hærdnet betons chloridindhold
Hærdnet betons chloridindhold Teknologisk Institut, Byggeri Hærdnet betons chloridindhold Deskriptorer: - Udgave: 1 Dato: 1985-05-7 Sideantal: / Bilag: 1 Udarbejdet af: BF/JKU Hærdnet betons chloridindhold
Øvelsesvejledninger til laboratoriekursus i Kemi A. VUC Aarhus, HF-afdelingen
 Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, HF-afdelingen 2013 Indholdsfortegnelse: side Indholdsfortegnelse 2 Velkommen til laboratoriekursus i kemi A på VUC Aarhus 3 Laboratoriearbejdet
Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, HF-afdelingen 2013 Indholdsfortegnelse: side Indholdsfortegnelse 2 Velkommen til laboratoriekursus i kemi A på VUC Aarhus 3 Laboratoriearbejdet
Task 1. Gær til hverdag og fest. DM i Science for 1.g Finale 2015 Onsdag 25.februar 2015 kl. 14-17.
 Task 1 Gær til hverdag og fest DM i Science for 1.g Finale 2015 Onsdag 25.februar 2015 kl. 14-17. Opgave 1: Opgave 2: Opgave 3: Opgave 4: 25 point 29 point 31 point 29 point Gær kan bruges til lidt af
Task 1 Gær til hverdag og fest DM i Science for 1.g Finale 2015 Onsdag 25.februar 2015 kl. 14-17. Opgave 1: Opgave 2: Opgave 3: Opgave 4: 25 point 29 point 31 point 29 point Gær kan bruges til lidt af
Test din viden B-forløb
 Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2012 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2012 Københavns
Øvelsesvejledninger til laboratoriekursus i Kemi A. VUC Aarhus, GSK-afdelingen
 Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, GSK-afdelingen 2015 Indholdsfortegnelse Velkommen til laboratoriekursus i Kemi A på VUC Aarhus 2015.... 3 Laboratoriearbejdet.... 3 Sikkerheden
Øvelsesvejledninger til laboratoriekursus i Kemi A VUC Aarhus, GSK-afdelingen 2015 Indholdsfortegnelse Velkommen til laboratoriekursus i Kemi A på VUC Aarhus 2015.... 3 Laboratoriearbejdet.... 3 Sikkerheden
ph-beregning September 2003 Revideret november 2010 Niels Frederiksen November 2010, Niels Frederiksen
 ph-beregning September 2003 Revideret november 2010 Niels Frederiksen ph-beregning side 1 af 6 I lærebogen er der angivet formler til beregning af ph i opløsninger af en stærk syre, en middelstærk syre
ph-beregning September 2003 Revideret november 2010 Niels Frederiksen ph-beregning side 1 af 6 I lærebogen er der angivet formler til beregning af ph i opløsninger af en stærk syre, en middelstærk syre
Biologisk rensning Fjern opløst organisk stof fra vand
 Spildevandscenter Avedøre Biologisk rensning Fjern opløst organisk stof fra vand Øvelse I Formål: På renseanlægget renses et mekanisk, biologisk og kemisk. I den biologiske rensning på renseanlægget benyttes
Spildevandscenter Avedøre Biologisk rensning Fjern opløst organisk stof fra vand Øvelse I Formål: På renseanlægget renses et mekanisk, biologisk og kemisk. I den biologiske rensning på renseanlægget benyttes
Syrer, baser og salte
 Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Der tilsættes 50,0 ml 1,00 M saltsyre. Hvor stor en masse af jern opløses, hvis reaktionen forløber fuldstændigt, og der er overskud af Fe(s)?
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
Isolering af DNA fra løg
 Isolering af DNA fra løg Formål: At afprøve en metode til isolering af DNA fra et levende væv. At anvende enzymer.. Indledning: Isolering af DNA fra celler er første trin i mange molekylærbiologiske undersøgelser.
Isolering af DNA fra løg Formål: At afprøve en metode til isolering af DNA fra et levende væv. At anvende enzymer.. Indledning: Isolering af DNA fra celler er første trin i mange molekylærbiologiske undersøgelser.
Na + -selektiv elektrode
 C.11.1 Na + -selektiv elektrode Formål: Øvelsens formål er at kalibrere en Na + -ISE (ionselektiv elektrode) finde elektrodens linearitetsområde anvende elektroden til koncentrationsbestemmelse belyse
C.11.1 Na + -selektiv elektrode Formål: Øvelsens formål er at kalibrere en Na + -ISE (ionselektiv elektrode) finde elektrodens linearitetsområde anvende elektroden til koncentrationsbestemmelse belyse
UNDERVISNINGS MINISTERIET KVALITETS- OG TILSYNSSTYRELSEN. KeiTii A. Studenterel<saTilen. Onsdag den 3.juni 2015 kl. 9.00-14.00
 - UNDERVISNINGS MINISTERIET KVALITETS- OG TILSYNSSTYRELSEN KeiTii A Studenterel
- UNDERVISNINGS MINISTERIET KVALITETS- OG TILSYNSSTYRELSEN KeiTii A Studenterel
Intro5uktion: I'" Acetylsalicylsyre. Salicylsyre
 Intro5uktion: H'11t frem til omkring 1850 var alle tilgængelige smertestillende midler "naturstoffer", dvs oftest ekstrakter fra planter eller dyr. Det første syntetisk fremstillede smertestillende stof
Intro5uktion: H'11t frem til omkring 1850 var alle tilgængelige smertestillende midler "naturstoffer", dvs oftest ekstrakter fra planter eller dyr. Det første syntetisk fremstillede smertestillende stof
Vejledning. Prøven Opgavesættet består af 4 opgaver med i alt 16 delopgaver. Alle hjælpemidler er tilladt.
 Vejledning Prøven Opgavesættet består af 4 opgaver med i alt 16 delopgaver. Alle hjælpemidler er tilladt. Opgavebesvarelsen Din opgavebesvarelse skal afleveres i et samlet dokument. Kildehenvisning Du
Vejledning Prøven Opgavesættet består af 4 opgaver med i alt 16 delopgaver. Alle hjælpemidler er tilladt. Opgavebesvarelsen Din opgavebesvarelse skal afleveres i et samlet dokument. Kildehenvisning Du
Øvelser 10. KlasseCenter Vesthimmerland
 Indholdsfortegnelse Sådan kan du påvise ilt (O 2 )... 2 Sådan kan du påvise CO 2... 3 Sådan kan du påvise SO 2... 4 Sådan kan røg renses for SO 2... 5 Sammenligning af indåndings- og udåndingsluft....
Indholdsfortegnelse Sådan kan du påvise ilt (O 2 )... 2 Sådan kan du påvise CO 2... 3 Sådan kan du påvise SO 2... 4 Sådan kan røg renses for SO 2... 5 Sammenligning af indåndings- og udåndingsluft....
Eksamensspørgsmål 2c ke, juni Fag: Kemi C-niveau. Censor: Andreas Andersen, Skanderborg Gymnasium
 Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2013 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2013 Københavns
Kemiaflevering uge 37
 Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Kemiøvelse 2 C2.1. Buffere. Øvelsens pædagogiske rammer
 Kemiøvelse 2 C2.1 Buffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemiøvelse 2 C2.1 Buffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt
Kemi A. Højere teknisk eksamen
 Kemi A Højere teknisk eksamen htx111-kem/a-2-19052011 Torsdag den 19. maj 2011 kl. 9.40-14.40 Side 1 af 6 sider Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt
Kemi A Højere teknisk eksamen htx111-kem/a-2-19052011 Torsdag den 19. maj 2011 kl. 9.40-14.40 Side 1 af 6 sider Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt
Daniells element Louise Regitze Skotte Andersen
 Louise Regitze Skotte Andersen Fysikrapport. Morten Stoklund Larsen - Lærer K l a s s e 1. 4 G r u p p e m e d l e m m e r : N i k i F r i b e r t A n d r e a s D a h l 2 2-0 5-2 0 0 8 2 Indhold Indledning...
Louise Regitze Skotte Andersen Fysikrapport. Morten Stoklund Larsen - Lærer K l a s s e 1. 4 G r u p p e m e d l e m m e r : N i k i F r i b e r t A n d r e a s D a h l 2 2-0 5-2 0 0 8 2 Indhold Indledning...
Skriftlig eksamen i Kemi F2 (Fysisk kemi)
 Skriftlig eksamen i Kemi F2 (Fysisk kemi) Tirsdag d. 7 April 2009 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 9
Skriftlig eksamen i Kemi F2 (Fysisk kemi) Tirsdag d. 7 April 2009 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 9
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest.
 Jordbundsanalyse ph Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest 31 21 - Vejledning til Rapitest Læs vejledningen fra Rapitesten: Nu er det let at forbedre sin have med den nye Rapitest
Jordbundsanalyse ph Bestem en jordprøves surhedsgrad, ph-værdien, med en Rapitest 31 21 - Vejledning til Rapitest Læs vejledningen fra Rapitesten: Nu er det let at forbedre sin have med den nye Rapitest
Olfaktometrisk titrering
 Side: 1/8 Olfaktometrisk titrering Forfattere: Henrik Parbo Redaktør: Morten Christensen, Thomas Brahe Faglige temaer: Olfaktometri, ph, Titrering, Thioler Kompetenceområder: Introduktion: Titrering med
Side: 1/8 Olfaktometrisk titrering Forfattere: Henrik Parbo Redaktør: Morten Christensen, Thomas Brahe Faglige temaer: Olfaktometri, ph, Titrering, Thioler Kompetenceområder: Introduktion: Titrering med
Hæld 25 ml NaOH(aq) op i et bægerglas. Observer væsken. Er den gennemsigtig? Hvilke ioner er der i ionsuppen?
 Fældningsreaktion (som erstatning for titrering af saltvand) Opløs 5 g CuSO 4 i 50 ml vand Opløses saltet? Følger det teorien? Hvilke ioner er der i ionsuppen? Hæld 25 ml NaOH(aq) op i et bægerglas. Observer
Fældningsreaktion (som erstatning for titrering af saltvand) Opløs 5 g CuSO 4 i 50 ml vand Opløses saltet? Følger det teorien? Hvilke ioner er der i ionsuppen? Hæld 25 ml NaOH(aq) op i et bægerglas. Observer
Aminosyrer. Ionstyrke. Bufferkapacitet.
 Aminosyrer. onstyrke. Bufferkapacitet. Biologisk vigtige aminosyrer er af formen H 2 N CH(R) COOH, hvor sidekæden R f. eks. kan indeholde alifatiske grupper som methyl eller ethyl, eller den kan indeholde
Aminosyrer. onstyrke. Bufferkapacitet. Biologisk vigtige aminosyrer er af formen H 2 N CH(R) COOH, hvor sidekæden R f. eks. kan indeholde alifatiske grupper som methyl eller ethyl, eller den kan indeholde
3. april 2014 Task B. Alt om salt. - Svarark - Country and Team No. Denmark Team:
 3. april 2014 Task B Alt om salt - Svarark - Country and Team No. Denmark Team: Name Name Name Signature Signature Signature 1 Opgave B1 Opgave B.1.1 Målinger af den Optiske Densitet (OD 750 ) 7 Marks
3. april 2014 Task B Alt om salt - Svarark - Country and Team No. Denmark Team: Name Name Name Signature Signature Signature 1 Opgave B1 Opgave B.1.1 Målinger af den Optiske Densitet (OD 750 ) 7 Marks
Roskilde Tekniske Gymnasium Klasse 2,5 Kemi Jonas Kalmark, Daniel Blankenstejner & Ticho Nielsen. Organisk kemi for dummies
 Organisk kemi for dummies 1 Indholdsfortegnelse Projektets formål:... 2 Målgruppe:... 4 Resume af interviewet:... 5 Teori:... 6 forsøg:... 6 Indledning:... 6 Materialer... 7 kalier:... 8 Fremgangs måde:...
Organisk kemi for dummies 1 Indholdsfortegnelse Projektets formål:... 2 Målgruppe:... 4 Resume af interviewet:... 5 Teori:... 6 forsøg:... 6 Indledning:... 6 Materialer... 7 kalier:... 8 Fremgangs måde:...
Nye metoder til bestemmelse af KCl i halm
 RESUME for Eltra PSO-F&U projekt nr. 3136 Juli 2002 Nye metoder til bestemmelse af KCl i halm Indhold af vandopløselige salte som kaliumchlorid (KCl) i halm kan give anledning til en række forskellige
RESUME for Eltra PSO-F&U projekt nr. 3136 Juli 2002 Nye metoder til bestemmelse af KCl i halm Indhold af vandopløselige salte som kaliumchlorid (KCl) i halm kan give anledning til en række forskellige
Øvelsesvejledninger til laboratoriekursus i Kemi B. VUC Aarhus, HF-afdelingen
 Øvelsesvejledninger til laboratoriekursus i Kemi B VUC Aarhus, F-afdelingen 2015 Indholdsfortegnelse: side Indholdsfortegnelse 2 Velkommen til laboratoriekursus i kemi B på VUC Aarhus 3 Laboratoriearbejdet
Øvelsesvejledninger til laboratoriekursus i Kemi B VUC Aarhus, F-afdelingen 2015 Indholdsfortegnelse: side Indholdsfortegnelse 2 Velkommen til laboratoriekursus i kemi B på VUC Aarhus 3 Laboratoriearbejdet
Fra spild til penge brug enzymer
 Fra spild til penge brug enzymer Køreplan 01005 Matematik 1 - FORÅR 2010 Denne projektplan er udarbejdet af Per Karlsson og Kim Knudsen, DTU Matematik, i samarbejde med Jørgen Risum, DTU Food. 1 Introduktion
Fra spild til penge brug enzymer Køreplan 01005 Matematik 1 - FORÅR 2010 Denne projektplan er udarbejdet af Per Karlsson og Kim Knudsen, DTU Matematik, i samarbejde med Jørgen Risum, DTU Food. 1 Introduktion
Skriftlig eksamen i Kemi F2 (Fysisk kemi)
 Skriftlig eksamen i Kemi F2 (Fysisk kemi) Fredag d 29 januar 2010 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 6
Skriftlig eksamen i Kemi F2 (Fysisk kemi) Fredag d 29 januar 2010 Læs først denne vejledning! Du får udleveret to eksemplarer af dette opgavesæt. Kontroller først, at begge hæfter virkelig indeholder 6
1st April 2014 Task A. Alt om olivenolie. - Svarark -
 1st April 2014 Task A Alt om olivenolie - Svarark - Country and Team No. Denmark Team: Name Signature Name Signature Name Signature OPGAVE A1: Undersøgelse af fordampning Biologi - Svarark (TOTAL MARKS
1st April 2014 Task A Alt om olivenolie - Svarark - Country and Team No. Denmark Team: Name Signature Name Signature Name Signature OPGAVE A1: Undersøgelse af fordampning Biologi - Svarark (TOTAL MARKS
C2014 alle øvelsesvejledninger
 C2014 alle øvelsesvejledninger Øvelsesvejledning Lys, varme & energi Forsøg iltbobler og vandpest (biologi) 1 liter bægerglas med vand Frisk afklippet vandpeststilk. Det er vigtigt at finde en god stilk,
C2014 alle øvelsesvejledninger Øvelsesvejledning Lys, varme & energi Forsøg iltbobler og vandpest (biologi) 1 liter bægerglas med vand Frisk afklippet vandpeststilk. Det er vigtigt at finde en god stilk,
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Københavns
Kvantitativ bestemmelse af glukose
 Kvantitativ bestemmelse af glukose Baggrund: Det viser sig at en del af de sukkerarter, vi indtager med vores mad, er, hvad man i fagsproget kalder reducerende sukkerarter. Disse vil i en stærk basisk
Kvantitativ bestemmelse af glukose Baggrund: Det viser sig at en del af de sukkerarter, vi indtager med vores mad, er, hvad man i fagsproget kalder reducerende sukkerarter. Disse vil i en stærk basisk
Analyse af proteiner Øvelsesvejledning
 Center for Undervisningsmidler, afdeling København Analyse af proteiner Øvelsesvejledning Formål At separere og analysere proteiner i almindelige fødevarer ved brug af gelelektroforese. Teori Alle dele
Center for Undervisningsmidler, afdeling København Analyse af proteiner Øvelsesvejledning Formål At separere og analysere proteiner i almindelige fødevarer ved brug af gelelektroforese. Teori Alle dele
Mundtlige eksamensopgaver
 Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Bestemmelse af koffein i cola
 Bestemmelse af koffein i cola 1,3,7-trimethylxanthine Koffein i læskedrikke Læs følgende links, hvor der blandt andet står nogle informationer om koffein og regler for hvor meget koffein, der må være i
Bestemmelse af koffein i cola 1,3,7-trimethylxanthine Koffein i læskedrikke Læs følgende links, hvor der blandt andet står nogle informationer om koffein og regler for hvor meget koffein, der må være i
STUDENTEREKSAMEN MAJ 2007 Vejledende opgavesæt nr. 1 KEMI A-NIVEAU. Xxxxdag den xx. måned åååå. Kl STX071-KEA V
 STUDENTEREKSAMEN MAJ 2007 Vejledende opgavesæt nr. 1 KEMI A-NIVEAU Xxxxdag den xx. måned åååå Kl. 09.00 14.00 STX071-KEA V pgavesættet består af 4 opgaver med i alt 16 spørgsmål samt 2 bilag i 2 eksemplarer.
STUDENTEREKSAMEN MAJ 2007 Vejledende opgavesæt nr. 1 KEMI A-NIVEAU Xxxxdag den xx. måned åååå Kl. 09.00 14.00 STX071-KEA V pgavesættet består af 4 opgaver med i alt 16 spørgsmål samt 2 bilag i 2 eksemplarer.
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Regnskovens hemmeligheder
 Center for Undervisningsmidler, afdeling København Regnskovens hemmeligheder Øvelsesvejledning Formål Et gen for et kræfthelbredende protein er blevet fundet i nogle mystiske blade i regnskoven. Forskere
Center for Undervisningsmidler, afdeling København Regnskovens hemmeligheder Øvelsesvejledning Formål Et gen for et kræfthelbredende protein er blevet fundet i nogle mystiske blade i regnskoven. Forskere
Identifikation af aminosyre
 Identifikation af aminosyre Kapitel 8: Bioteknologi proteiner, DNA og bioethanol Problemstilling Aminosyrer er opløselige i vand og har syre-baseegenskaber. Et 2-aminosyremolekyle indeholder mindst én
Identifikation af aminosyre Kapitel 8: Bioteknologi proteiner, DNA og bioethanol Problemstilling Aminosyrer er opløselige i vand og har syre-baseegenskaber. Et 2-aminosyremolekyle indeholder mindst én
%2fAfleveringsportal%2fopgaveaflevering.aspx%3felementId%3d461315
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
Øvelsesvejledninger. til kemi C. Københavns VUC
 Øvelsesvejledninger til kemi C Københavns VUC Efterår 2015 Kemi C laboratoriekursus efterår 2015 Københavns VUC Vognmagergade 8, 1120 København K Indholdsfortegnelse Side 2 Side 3 Side 4 Sikkerhed i laboratoriet
Øvelsesvejledninger til kemi C Københavns VUC Efterår 2015 Kemi C laboratoriekursus efterår 2015 Københavns VUC Vognmagergade 8, 1120 København K Indholdsfortegnelse Side 2 Side 3 Side 4 Sikkerhed i laboratoriet
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Skriftlig eksamen i Almen Kemi I
 Skriftlig eksamen i Almen Kemi I Molekylær Biomedicin November 2005 Hjælpemidler tilladt: Lærebøger, undervisningsmateriale, opgavebesvarelser, noter, molekylbyggesæt, lommeregner og sædvanlige skrive-
Skriftlig eksamen i Almen Kemi I Molekylær Biomedicin November 2005 Hjælpemidler tilladt: Lærebøger, undervisningsmateriale, opgavebesvarelser, noter, molekylbyggesæt, lommeregner og sædvanlige skrive-
Kemi A. Højere teknisk eksamen
 Kemi A Højere teknisk eksamen htx101-kem/a-31052010 Mandag den 31. maj 2010 kl. 9.40-14.40 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt begrunde løsningerne
Kemi A Højere teknisk eksamen htx101-kem/a-31052010 Mandag den 31. maj 2010 kl. 9.40-14.40 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt begrunde løsningerne
Gæringsprocessen ved fremstillingen af alkohol tager udgangspunkt i glukose molekylet (C
 Molekyler af alkohol Byg molekylerne af forskellige alkoholer, og tegn deres stregformler Byg alkoholmolekyler med 1, 2 og 3 C atomer og 1 OH gruppe. Tegn deres stregformler her og skriv navnet ved. Byg
Molekyler af alkohol Byg molekylerne af forskellige alkoholer, og tegn deres stregformler Byg alkoholmolekyler med 1, 2 og 3 C atomer og 1 OH gruppe. Tegn deres stregformler her og skriv navnet ved. Byg
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Øvelse: Analyse af betanin i rødbede
 Forløb: Smagen af frugt og grønt: Kemimateriale modul 2-8 Aktivitet: Øvelse: Analyse af betanin i rødbede Fag: Kemi Klassetrin: 1. g, 2. g, 3. g Side: 1/14 Øvelse: Analyse af betanin i rødbede Forfattere:
Forløb: Smagen af frugt og grønt: Kemimateriale modul 2-8 Aktivitet: Øvelse: Analyse af betanin i rødbede Fag: Kemi Klassetrin: 1. g, 2. g, 3. g Side: 1/14 Øvelse: Analyse af betanin i rødbede Forfattere:
Fremstilling af ferrofluids
 Fremstilling af ferrofluids Eksperiment 1: Fremstilling af ferrofluids - Elevvejledning Formål I dette eksperiment skal du fremstille nanopartikler af magnetit og bruge dem til at lave en magnetisk væske,
Fremstilling af ferrofluids Eksperiment 1: Fremstilling af ferrofluids - Elevvejledning Formål I dette eksperiment skal du fremstille nanopartikler af magnetit og bruge dem til at lave en magnetisk væske,
Mælkesyrebakterier og holdbarhed
 Mælkesyrebakterier og holdbarhed Formål Formålet med denne øvelse er at undersøge mælkesyrebakteriers og probiotikas evne til at øge holdbarheden af kød ved at: 1. Undersøge forskellen på bakterieantal
Mælkesyrebakterier og holdbarhed Formål Formålet med denne øvelse er at undersøge mælkesyrebakteriers og probiotikas evne til at øge holdbarheden af kød ved at: 1. Undersøge forskellen på bakterieantal
Reaktionshastighed og ligevægt
 Reaktionshastighed og ligevægt Reaktionshastighed Kemiske reaktioners hastigheder er meget forskellige - nogle er så hurtige, at de næsten er umulige at måle, mens andre helt åbenlyst tager tid. Blander
Reaktionshastighed og ligevægt Reaktionshastighed Kemiske reaktioners hastigheder er meget forskellige - nogle er så hurtige, at de næsten er umulige at måle, mens andre helt åbenlyst tager tid. Blander
Er dit reaktionsskema afstemt? Dvs. undersøg for hvert grundstof, om der er lige mange atomer af grundstoffet før reaktionen som efter reaktionen.
 7.12 Bagning med hjortetaksalt I skal undersøge, hvilke egenskaber bagepulveret hjortetaksalt har. Hjortetaksalt bruges i bagværk som kiks, klejner, brunkager m.m. Saltet giver en sprødhed i bagværket.
7.12 Bagning med hjortetaksalt I skal undersøge, hvilke egenskaber bagepulveret hjortetaksalt har. Hjortetaksalt bruges i bagværk som kiks, klejner, brunkager m.m. Saltet giver en sprødhed i bagværket.
Dokumentation til Kemi for dummies Mike, Mark, Ida, Daniel og Max
 Dokumentation til Kemi for dummies Mike, Mark, Ida, Daniel og Max 1 Indskanning af vores krav til posterne, skrevet på papir: Første udkast til et design af vores poster: Det første udkast er en hurtig
Dokumentation til Kemi for dummies Mike, Mark, Ida, Daniel og Max 1 Indskanning af vores krav til posterne, skrevet på papir: Første udkast til et design af vores poster: Det første udkast er en hurtig
