BILAG BETINGELSER ELLER BEGRÆNSNINGER SOM SKAL IMPLEMENTERES AF MEDLEMSSTATERNE MED HENSYN TIL SIKKER OG EFFEKTIV BRUG AF LÆGEMIDLET.
|
|
|
- Katrine Jensen
- 8 år siden
- Visninger:
Transkript
1 BILAG BETINGELSER ELLER BEGRÆNSNINGER SOM SKAL IMPLEMENTERES AF MEDLEMSSTATERNE MED HENSYN TIL SIKKER OG EFFEKTIV BRUG AF LÆGEMIDLET. 1
2 Medlemsstaterne skal sikre, at alle betingelser eller begrænsninger med hensyn til sikker og effektiv anvendelse af det nedenfor nævnte lægemiddel implementeres: 1. Medlemsstaterne skal være enige om detaljerne vedrørende et kontrolleret distributionssystem med indehaveren af markedsføringstilladelsen i overensstemmelse med de nationale bestemmelser og sundhedssystemer og skal implementere et sådant program nationalt for at sikre, at: o Alle læger og farmaceuter, som har til hensigt at ordinere eller udlevere Thalidomide Pharmion, inden lancering modtager et Kære sundhedspersonale-brev som beskrevet nedenfor. o Alt sundhedspersonale, som har til hensigt at ordinere (og i overensstemmelse med den nationale, kompetente myndighed udlevere) Thalidomide Pharmion, inden ordinationen foretages modtager undervisningsmateriale, der indeholder følgende: Brochure til sundhedspersonale Patientbrochurer Patientkort Produktresumé, indlægsseddel og etikettering 2. Medlemsstaterne skal etablere forholdsregler for at sikre, at: o Den maksimale behandlingsvarighed af en ordination må være 4 uger for kvinder i den fertile alder 12 uger for mænd og kvinder, som ikke er i den fertile alder o Lægemidlet kan kun udleveres inden for 7 dage efter receptens dato 3. Medlemsstaterne skal sikre, at indehaveren af markedsføringstilladelsen implementerer et svangerskabsforebyggelsesprogram inden for deres område. Detaljer vedrørende måden, hvorpå svangerskabsforebyggelsesprogrammet vil blive implementeret skal aftales med indehaveren af markedsføringstilladelsen og etableres inden produktet markedsføres. 4. Medlemsstaterne skal blive enige om den lokale implementering af patientkortsystemet. 5. Medlemsstaterne skal sikre, at indehaveren af markedsføringstilladelsen udleverer oplysningsmaterialerne til de nationale patientorganisationer til gennemsyn eller, hvis en sådan organisation ikke findes eller ikke kan være involveret, til en relevant patientgruppe. Involverede patienter bør helst være ubekendte med thalidomids historie. Resultaterne af brugerafprøvningen skal udleveres til den nationale, kompetente myndighed og det endelige materiale godkendes på nationalt niveau. 6. Medlemsstaterne skal blive enige med indehaveren af markedsføringstilladelsen inden lancering af produktet om: o De mest hensigtmæssige strategier til monitorering af off-labelanvendelse inden for nationale grænser o Indsamling af detaljerede data, der som minimum omfatter patientdemografi og indikation for nøje at monitorere off-label anvendelse på nationalt område o Opstilling af nationale forholdsregler med henblik på at vurdere effektivitet og overholdelse af svangerskabsforebyggelsesprogrammet. 7. Medlemsstaterne skal indberette følgende information til EMEA med 6 månedlige intervaller efter kommissionsbeslutningen: o Status for implementeringen af svangerskabsforebyggelsesprogrammet 2
3 i det respektive land o Vurdering af brug i det respektive land 8. Medlemsstaterne skal sikre, at følgende nøgleelementer er indeholdt i det relevante materiale: Kære Sundhedspersonale-brev Kære Sundhedspersonale-brevet vil bestå af to dele: En kernetekst som skal godkendes af CHMP Specifikke, nationale krav som skal godkendes af de kompetente, nationale instanser med hensyn til: o Produktdistribution o Procedurer til at sikre at alle relevante forholdsregler er blevet taget, inden thalidomid ordineres Undervisningsmateriale til sundhedspersonale Undervisningsmaterialet til sundhedspersonalet skal indeholde følgende elementer: Brochure til sundhedspersonale o Thalidomids historie, baggrundsoplysninger om Thalidomide Pharmion og den godkendte indikation o Dosering o Maksimal varighed af ordinering 4 uger for kvinder i den fertile alder 12 uger for mænd og kvinder, som ikke er i den fertile alder o Teratogenicitet og nødvendigheden af at undgå føtal eksponering o Sundhedspersonalets pligter ved ordinering og salg af Thalidomide Pharmion, herunder Nødvendigheden af at yde omfattende vejledning og rådgivning til patienterne At patienterne skal være i stand til at efterkomme krav i forbindelse med sikker anvendelse af thalidomid Nødvendigheden af at udlevere relevant patientoplysningsmateriale Indberetning om graviditet, neuropati eller andre utilsigtede hændelser til Pharmion og den lokale sundhedsmyndighed ved brug af formularerne i "Undervisningsmateriale til sundhedspersonale" (hvis relevant i en medlemsstat) o Sikkerhedsrådgivning, der er relevant for alle patienter Beskrivelse og håndtering af tromboemboliske og kardiovaskulære hændelser og perifer neuropati Bortskaffelse af uønsket medicin Ikke at donere blod under behandlingen og i en uge efter behandlingsophør o Algoritme til implementering af planen for svangerskabsforebyggelse Dette skal hjælpe med kategorisering af patienter og bestemmelse af de fornødne forholdsregler vedrørende svangerskabsforebyggelse og graviditetstests. o Oplysninger om svangerskabsforebyggelsesprogrammet Definition af kvinder i den fertile alder (women of childbearing potential (WCBP)) samt hvorledes den ordinerende læge skal handle, hvis der er uklarhed om graviditetsstatus Oplysninger om hvad effektiv svangerskabsforebyggelse er 3
4 Sikkerhedsråd til WCBP Krav til svangerskabsforebyggelse, definition og nødvendighed af hensigtsmæssige svangerskabsforebyggende metoder At hun, hvis hun har brug for at ændre eller stoppe sin svangerskabsforebyggende metode, skal informere - den læge, der ordinerer det svangerskabsforebyggende middel, om at hun er i behandling med thalidomid - den læge, der ordinerer thalidomid, om at hun har stoppet eller ændret sin svangerskabsforebyggende metode Krav til graviditetstests o Råd om brugbare prøver o Frekvens (før påbegyndelse af, månedligt under og efter behandling) Nødvendigheden af øjeblikkeligt ophør med anvendelsen af Thalidomide Pharmion ved mistanke om graviditet Nødvendigheden af øjeblikkelig orientering af den behandlende læge ved mistanke om graviditet Sikkerhedsråd til mænd At thalidomid udskilles i sæd og nødvendigheden af at anvende kondom, hvis den seksuelle partner er gravid, eller er en kvinde i den fertile alder og ikke bruger en effektiv graviditetsforebyggende metode At han, hvis hans partner bliver gravid, skal underrette sin behandlende læge med det samme og altid bruge kondom under samleje At han ikke må donere sæd under behandlingen og i en uge o Krav vedrørende indberetning af graviditet Øjeblikkeligt ophør med indtagelse af Thalidomide Pharmion ved mistanke om graviditet Henvis patienten til vurdering og rådgivning hos en læge, der er specialiseret i eller har erfaring med teratologi Udfyld formularerne til indberetning af graviditet som udleveret i "Undervisningsmateriale til sundhedspersonale" Lokale kontaktoplysninger for indberetning af mistanke om graviditet Formularer til første indberetning og udfald af graviditet Post-markedsføring og kompliansvurdering (som relevant for den pågældende medlemsstat) Formularer til indberetning af neuropati og bivirkninger Formularer til påbegyndelse af behandling o Der bør være 3 formularer til påbegyndelse af behandling: Kvindelig patient i den fertile alder Kvindelig patient, som ikke er i den fertile alder Mandlig patient o Alle formularer, hvor behandling kan påbegyndes, bør indeholde følgende 4
5 elementer: Advarsel om teratogenicitet Dato for rådgivning Bekræftelse af patientens forståelse mht. risikoen for thalidomid og forholdsreglerne i svangerskabsforebyggelsesprogrammet Patientoplysninger, underskrift og dato Ordinerende læge, dennes underskrift samt dato Hensigten med dette dokument, dvs. som formuleret i svangerskabsforebyggelsesprogrammet: "Hensigten med formularen til påbegyndelse af behandling er at beskytte patienterne og eventuelle fostre ved at sikre, at patienterne er fuldstændigt informeret om og forstår risikoen for teratogenicitet og andre bivirkninger forbundet med brugen af thalidomid. Det er ikke en kontrakt og frikender ikke nogen for deres ansvar mht. sikker anvendelse af produktet og forebyggelse af føtal eksponering." o Formularer til påbegyndelse af behandling for kvindelige patienter i den fertile alder bør også omfatte: Bekræftelse af, at lægen har talt med patienten om: At hun, hvis hun er gravid eller forventer at blive gravid, ikke må tage Thalidomide Pharmion Nødvendigheden af effektiv svangerskabsforebyggelse uden afbrydelse 4 uger før behandlingen påbegyndes, under hele behandlingens varighed og 4 uger efter behandlingens afslutning At hun, hvis hun har brug for at ændre eller stoppe sin præventionsmetode, skal informere - den læge, der ordinerer det svangerskabsforebyggende middel, om at hun er i behandling med thalidomid - den læge, der ordinerer thalidomid, om at hun har stoppet eller ændret sin præventionsmetode Nødvendigheden af graviditetstest dvs. før behandling, hver 4. uge under behandlingen og efter behandling Nødvendigheden af øjeblikkeligt ophør med anvendelse af Thalidomide Pharmion ved mistanke om graviditet Nødvendigheden af øjeblikkelig orientering af den behandlende læge ved mistanke om graviditet At hun ikke må dele behandlingen med nogen anden person At hun ikke må donere blod under behandlingen og i en uge At hun skal levere kapslerne tilbage til apoteket ved behandlingens afslutning o Formularer til påbegyndelse af behandling for kvinder, som ikke er i den fertile alder, bør også indeholde: Bekræftelse af, at lægen har talt med patienten om: At hun ikke må dele behandlingen med nogen anden person At hun ikke må donere blod under behandlingen og i en uge At hun skal levere kapslerne tilbage til apoteket ved behandlingens afslutning 5
6 o Formularer til påbegyndelse af behandling for mandlige patienter bør også indeholde: Bekræftelse af, at lægen har talt med patienten om: At thalidomid kan findes i sæd og nødvendigheden at anvende kondom, hvis seksualpartneren er gravid eller er en kvinde i den fertile alder, som ikke bruger et effektivt præventionsmiddel At han, hvis hans partner bliver gravid, skal underrette den behandlende læge med det samme, og altid anvende kondom At han ikke bør donere blod eller sæd under behandlingen og i en uge At han ikke må dele behandlingen med nogen anden person At han skal levere kapslerne tilbage til apoteket ved behandlingens afslutning Patientkort og/eller tilsvarende værktøjer o bekræftelse af, at relevant rådgivning har fundet sted o dokumentation vedrørende muligheden for at blive gravid o boks (el. lign.) som lægen krydser af for at bekræfte, at patienten anvender effektiv prævention (hvis kvinde i den fertile alder) o bekræftelse af første negativ graviditetstest inden påbegyndelse af behandling (hvis kvinde i den fertile alder) o dato for graviditetstests og resultater heraf Oplysningsbrochurer til patienter o Der kan være 3 typer oplysningsbrochurer til patienterne eller en enkelt patientbrochure, som sammenfatter oplysningerne for hver patientkategori: Brochure for kvindelige patienter i den fertile alder og deres partner Brochure for kvindelige patienter, som ikke er i den fertile alder Brochure for mandlige patienter o Alle patientbrochurer bør indeholde følgende oplysninger: At Thalidomide Pharmion er teratogent At Thalidomide Pharmion kan forårsage thromboemboliske og kardiovaskulære hændelser samt neuropati Beskrivelse af patientkortet og dets anvendelse i den enkelte medlemsstat Nationale og andre relevante forholdsregler for ordination af Thalidomide Pharmion At Thalidomide Pharmion ikke må videregives til andre At patienten ikke børe donere blod under behandlingen og i en uge At patienten skal fortælle lægen om alle utilsigtede hændelser At ikke anvendte kapsler skal leveres tilbage til apoteket ved afslutning af behandling o Følgende oplysninger bør også gives i de relevante brochurer: Kvindelig patient i den fertile alder Nødvendigheden af effektiv prævention At hun, hvis hun har brug for at ændre eller stoppe sin præventionsmetode, skal informere 6
7 - den læge, der ordinerer det svangerskabsforebyggende middel, om at hun er i behandling med thalidomid - den læge, der ordinerer thalidomid, om at hun har stoppet eller ændret sin præventionsmetode Nødvendigheden af graviditetstests, dvs. før behandlingen, hver 4. uge under behandlingen, og efter behandlingen Nødvendigheden af øjeblikkeligt ophør med anvendelse af Thalidomide Pharmion ved mistanke om graviditet Nødvendigheden af øjeblikkelig orientering af den behandlende læge ved mistanke om graviditet Mandlige patienter At thalidomid kan findes i sæd og nødvendigheden at anvende kondom, hvis seksualpartneren er gravid eller er en kvinde i den fertile alder, som ikke bruger et effektivt præventionsmiddel At han, hvis hans partner bliver gravid, skal underrette den behandlende læge med det samme, og altid anvende kondom At han ikke bør donere sæd under behandlingen og i en uge 7
For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1:
 Uddannelsesmateriale For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1: Materiale til læger Tjekliste til læger/bekræftelsesskema til ordinering
Uddannelsesmateriale For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1: Materiale til læger Tjekliste til læger/bekræftelsesskema til ordinering
For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1:
 Uddannelsesmateriale For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1: Materiale til læger Tjekliste til læger/bekræftelsesskema til ordinering
Uddannelsesmateriale For alle orale retinoidprodukter, der indeholder acitretin, alitretinoin og isotretinoin, nævnt i tabel 1: Materiale til læger Tjekliste til læger/bekræftelsesskema til ordinering
Isotretinoin Orion (isotretinoin) Svangerskabsforebyggelsesprogram. Lægens vejledning til ordinering af isotretinoin
 Isotretinoin Orion (isotretinoin) Svangerskabsforebyggelsesprogram Lægens vejledning til ordinering af isotretinoin Introduktion Isotretinoin kapsler indeholder det aktive stof isotretinoin som er stærkt
Isotretinoin Orion (isotretinoin) Svangerskabsforebyggelsesprogram Lægens vejledning til ordinering af isotretinoin Introduktion Isotretinoin kapsler indeholder det aktive stof isotretinoin som er stærkt
Bilag III Ændringer til relevante punkter i produktinformationen
 Bilag III Ændringer til relevante punkter i produktinformationen Bemærk: Disse ændringer til de relevanter punkter i produktinformationen er resultatet af referralproceduren. Produktresuméet kan efterfølgende
Bilag III Ændringer til relevante punkter i produktinformationen Bemærk: Disse ændringer til de relevanter punkter i produktinformationen er resultatet af referralproceduren. Produktresuméet kan efterfølgende
Risikominimeringsprogram Patientbrochurer
 Risikominimeringsprogram Patientbrochurer INDHOLDSFORTEGNELSE Information til alle patienter 4-9 Patientbrochure til kvinder i den fødedygtige alder 10 15 Patientbrochure til kvindelige patienter, som
Risikominimeringsprogram Patientbrochurer INDHOLDSFORTEGNELSE Information til alle patienter 4-9 Patientbrochure til kvinder i den fødedygtige alder 10 15 Patientbrochure til kvindelige patienter, som
Sundhedsudvalget (2. samling) SUU alm. del - Bilag 263 Offentligt. Resumé
 Sundhedsudvalget (2. samling) SUU alm. del - Bilag 263 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser
Sundhedsudvalget (2. samling) SUU alm. del - Bilag 263 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser
Information til sundhedspersonale
 Information til sundhedspersonale Ordination eller udlevering af Thalidomide Celgene Thalidomide Celgene Svangerskabsforebyggelsesprogram Kontaktoplysninger for Celgene: Celgene ApS Kristianiagade 8, 3.
Information til sundhedspersonale Ordination eller udlevering af Thalidomide Celgene Thalidomide Celgene Svangerskabsforebyggelsesprogram Kontaktoplysninger for Celgene: Celgene ApS Kristianiagade 8, 3.
Myfortic (mycophenolsyre): risiko for medfødte misdannelser VEJLEDNING TIL SUNDHEDSPERSONALE
 Myfortic (mycophenolsyre): risiko for medfødte misdannelser VEJLEDNING TIL SUNDHEDSPERSONALE Indledning Denne vejledning er udarbejdet for at understrege de risici for fostre, der er forbundet med eksponering
Myfortic (mycophenolsyre): risiko for medfødte misdannelser VEJLEDNING TIL SUNDHEDSPERSONALE Indledning Denne vejledning er udarbejdet for at understrege de risici for fostre, der er forbundet med eksponering
Bilag III. Ændringer i relevante afsnit af produktinformationen
 Bilag III Ændringer i relevante afsnit af produktinformationen Bemærk: Disse ændringer til de relevante afsnit af produktresuméet og indlægssedlen er resultatet af Referralproceduren. Produktinformationen
Bilag III Ændringer i relevante afsnit af produktinformationen Bemærk: Disse ændringer til de relevante afsnit af produktresuméet og indlægssedlen er resultatet af Referralproceduren. Produktinformationen
Vejledning til læger der ordinerer acitretin
 Vejledning til læger der ordinerer acitretin Acitretin Orifarm (acitretin) 10 mg og 25 mg hårde kapsler Forebyggelse af graviditet og fostereksponering Introduktion Acitretin Orifarm indeholder det aktive
Vejledning til læger der ordinerer acitretin Acitretin Orifarm (acitretin) 10 mg og 25 mg hårde kapsler Forebyggelse af graviditet og fostereksponering Introduktion Acitretin Orifarm indeholder det aktive
9 13 Patientbrochure til fødedygtige kvinder
 Patientbrochure Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får.
Patientbrochure Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får.
Mycophenolat natrium (Myfortic ) VEJLEDNING OM MYCOPHENOLAT TIL SUNDHEDSPERSONALE Risiko for medfødte misdannelser
 Mycophenolat natrium (Myfortic ) VEJLEDNING OM MYCOPHENOLAT TIL SUNDHEDSPERSONALE Risiko for medfødte misdannelser Indledning Denne vejledning er udarbejdet for at understrege de risici, der er forbundet
Mycophenolat natrium (Myfortic ) VEJLEDNING OM MYCOPHENOLAT TIL SUNDHEDSPERSONALE Risiko for medfødte misdannelser Indledning Denne vejledning er udarbejdet for at understrege de risici, der er forbundet
Thalidomide Celgene Svangerskabsforebyggelsesprogram
 Patientbrochure Thalidomide Celgene Svangerskabsforebyggelsesprogram Advarsel: Alvorlige livstruende fødselsdefekter. Hvis Thalidomide Celgene tages under graviditet, kan det forårsage alvorlige fødselsdefekter
Patientbrochure Thalidomide Celgene Svangerskabsforebyggelsesprogram Advarsel: Alvorlige livstruende fødselsdefekter. Hvis Thalidomide Celgene tages under graviditet, kan det forårsage alvorlige fødselsdefekter
BILAG I VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF BETINGELSERNE FOR MARKEDSFØRINGSTILLADELSEN/-TILLADELSERNE
 BILAG I VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF BETINGELSERNE FOR MARKEDSFØRINGSTILLADELSEN/-TILLADELSERNE 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
BILAG I VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF BETINGELSERNE FOR MARKEDSFØRINGSTILLADELSEN/-TILLADELSERNE 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Indlægsseddel: Information til patienten
 Indlægsseddel: Information til patienten Imnovid 1 mg hårde kapsler Imnovid 2 mg hårde kapsler Imnovid 3 mg hårde kapsler Imnovid 4 mg hårde kapsler pomalidomid Dette lægemiddel er underlagt supplerende
Indlægsseddel: Information til patienten Imnovid 1 mg hårde kapsler Imnovid 2 mg hårde kapsler Imnovid 3 mg hårde kapsler Imnovid 4 mg hårde kapsler pomalidomid Dette lægemiddel er underlagt supplerende
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne
 Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Toctino (alitretinoin)
 Præventionsprogram TOC-010-250908-D PATIENTBROCHURE Toctino (alitretinoin) Om denne brochure Denne brochure indeholder vigtig information om din behandling med Toctino og risikoen for fosterskader ved
Præventionsprogram TOC-010-250908-D PATIENTBROCHURE Toctino (alitretinoin) Om denne brochure Denne brochure indeholder vigtig information om din behandling med Toctino og risikoen for fosterskader ved
ISOTRETINOIN TEVA til behandling af svær acne
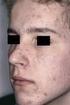 17.07.2015 ISOTRETINOIN TEVA til behandling af svær acne Information til læger Det Europæiske Lægemiddelagenturs (EMAs) komité for lægemidler til mennesker (CHMP) har besluttet, at man skal følge et nøje
17.07.2015 ISOTRETINOIN TEVA til behandling af svær acne Information til læger Det Europæiske Lægemiddelagenturs (EMAs) komité for lægemidler til mennesker (CHMP) har besluttet, at man skal følge et nøje
Europaudvalget EUU alm. del - Bilag 360 Offentligt
 Europaudvalget EUU alm. del - Bilag 360 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse for lægemidlet til sjældne sygdomme
Europaudvalget EUU alm. del - Bilag 360 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse for lægemidlet til sjældne sygdomme
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml. glyceryltrinitrat
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
Lokal instruks for håndtering af medicin:
 Lokal instruks for håndtering af medicin: August 2012. Medicinordination: Ordinationen foretages af en læge. Den kan både være skriftligt, elektronisk og mundligt. Ordination registreres i Bosted i dagbog
Lokal instruks for håndtering af medicin: August 2012. Medicinordination: Ordinationen foretages af en læge. Den kan både være skriftligt, elektronisk og mundligt. Ordination registreres i Bosted i dagbog
Hvis du ønsker praktisk vejledning om anvendelsen af Revlimid, kan du læse indlægssedlen eller kontakte din læge eller dit apotek.
 EMA/113870/2017 EMEA/H/C/000717 EPAR sammendrag for offentligheden lenalidomid Dette er et sammendrag af den europæiske offentlige vurderingsrapport (EPAR) for. Det forklarer, hvordan agenturet vurderede
EMA/113870/2017 EMEA/H/C/000717 EPAR sammendrag for offentligheden lenalidomid Dette er et sammendrag af den europæiske offentlige vurderingsrapport (EPAR) for. Det forklarer, hvordan agenturet vurderede
Indlægsseddel: Information til brugeren. Levodonna 1,5 mg tabletter. levonorgestrel
 Indlægsseddel: Information til brugeren Levodonna 1,5 mg tabletter levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Tag
Indlægsseddel: Information til brugeren Levodonna 1,5 mg tabletter levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Tag
140620_V18.0_Thal_EU_PI_DA
 Indlægsseddel: Information til brugeren Thalidomide Celgene 50 mg hårde kapsler Thalidomid ADVARSEL Thalidomid forårsager fødselsdefekter og fosterdød. Tag ikke thalidomid, hvis du er gravid eller muligvis
Indlægsseddel: Information til brugeren Thalidomide Celgene 50 mg hårde kapsler Thalidomid ADVARSEL Thalidomid forårsager fødselsdefekter og fosterdød. Tag ikke thalidomid, hvis du er gravid eller muligvis
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelserne
 Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelserne Videnskabelige konklusioner Under hensyntagen til PRAC s vurderingsrapport om PSUR en for
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelserne Videnskabelige konklusioner Under hensyntagen til PRAC s vurderingsrapport om PSUR en for
Indlægsseddel: Information til brugeren. Finasterid Orion 5 mg filmovertrukne tabletter. Finasterid
 Indlægsseddel: Information til brugeren Finasterid Orion 5 mg filmovertrukne tabletter Finasterid Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige
Indlægsseddel: Information til brugeren Finasterid Orion 5 mg filmovertrukne tabletter Finasterid Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige
Indlægsseddel: Information til patienten
 GE Healthcare Indlægsseddel: Information til patienten SeHCAT, 370 kbq, kapsel Tauroselkolsyre ( 75 Se) Læs denne indlægsseddel grundigt, inden du får dette lægemiddel, da den indeholder vigtige oplysninger.
GE Healthcare Indlægsseddel: Information til patienten SeHCAT, 370 kbq, kapsel Tauroselkolsyre ( 75 Se) Læs denne indlægsseddel grundigt, inden du får dette lægemiddel, da den indeholder vigtige oplysninger.
Informationsbrochure til patienter
 Jinarc (tolvaptan) Informationsbrochure til patienter Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette
Jinarc (tolvaptan) Informationsbrochure til patienter Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette
Indlægsseddel: Information til brugeren. Arax Junior 250 mg tabletter paracetamol
 INDLÆGSSEDDEL 1 Indlægsseddel: Information til brugeren Arax Junior 250 mg tabletter paracetamol Læs denne indlægsseddel grundigt, inden du begynder at tage dette læge middel, da den indeholder vigtige
INDLÆGSSEDDEL 1 Indlægsseddel: Information til brugeren Arax Junior 250 mg tabletter paracetamol Læs denne indlægsseddel grundigt, inden du begynder at tage dette læge middel, da den indeholder vigtige
Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé. Mifepristone Linepharma 200 mg Tafla
 Bilag I Liste over lægemidlernes navne, lægemiddelformer, styrker, administrationsveje, ansøgere/indehavere af markedsføringstilladelser i medlemsstaterne. 1 Medlemsstat EU/EØS Indehaver af markedsføringstilladelsen
Bilag I Liste over lægemidlernes navne, lægemiddelformer, styrker, administrationsveje, ansøgere/indehavere af markedsføringstilladelser i medlemsstaterne. 1 Medlemsstat EU/EØS Indehaver af markedsføringstilladelsen
Bilag II. Videnskabelige konklusioner
 Bilag II Videnskabelige konklusioner 8 Videnskabelige konklusioner Solu-Medro 40 mg pulver og solvens til injektionsvæske, opløsning, (herefter benævnt "Solu- Medrol") indeholder methylprednisolon og,
Bilag II Videnskabelige konklusioner 8 Videnskabelige konklusioner Solu-Medro 40 mg pulver og solvens til injektionsvæske, opløsning, (herefter benævnt "Solu- Medrol") indeholder methylprednisolon og,
Rettigheder, ansvar og forpligtigelser ved brug af Fælles Medicinkort (FMK) og udfordringer i praksis. Henrik L Hansen
 Rettigheder, ansvar og forpligtigelser ved brug af Fælles Medicinkort (FMK) og udfordringer i praksis Henrik L Hansen Det Fælles Medicinkort Nye muligheder og nye udfordringer FMK består af en central
Rettigheder, ansvar og forpligtigelser ved brug af Fælles Medicinkort (FMK) og udfordringer i praksis Henrik L Hansen Det Fælles Medicinkort Nye muligheder og nye udfordringer FMK består af en central
Indlægsseddel: Information til brugeren. CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol
 Indlægsseddel: Information til brugeren CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Tevas datafortrolighedspolitik for lægemiddelovervågning. Definitioner, der anvendes i denne fortrolighedspolitik
 Tevas datafortrolighedspolitik for lægemiddelovervågning Definitioner, der anvendes i denne fortrolighedspolitik Bivirkning betyder en uønsket, utilsigtet eller skadelig hændelse i forbindelse med brug
Tevas datafortrolighedspolitik for lægemiddelovervågning Definitioner, der anvendes i denne fortrolighedspolitik Bivirkning betyder en uønsket, utilsigtet eller skadelig hændelse i forbindelse med brug
Toctino (alitretinoin)
 PRÆVENTIONSPROGRAM Toctino (alitretinoin) Patientkort Patientnavn TOC 010 250908 C Toctino tilhører en lægemiddelgruppe, som en kendt for at kunne forårsage fosterskader. Hvis Toctino tages under graviditeten,
PRÆVENTIONSPROGRAM Toctino (alitretinoin) Patientkort Patientnavn TOC 010 250908 C Toctino tilhører en lægemiddelgruppe, som en kendt for at kunne forårsage fosterskader. Hvis Toctino tages under graviditeten,
Regler for ansvar for medicinering og forebyggelse af medicineringsfejl. Anne Mette Dons Chef for Tilsyn Sundhedsstyrelsen
 Regler for ansvar for medicinering og forebyggelse af medicineringsfejl Anne Mette Dons Chef for Tilsyn Sundhedsstyrelsen Vejledning om ordination og håndtering af lægemidler Vejl. nr. 9429 af 30/06/2006
Regler for ansvar for medicinering og forebyggelse af medicineringsfejl Anne Mette Dons Chef for Tilsyn Sundhedsstyrelsen Vejledning om ordination og håndtering af lægemidler Vejl. nr. 9429 af 30/06/2006
BILAG III TILLÆG TIL PRODUKTRESUME OG INDLÆGSSEDDEL. Disse ændringer til produktresumé og indlægsseddel er gældende fra Kommissionens beslutning.
 BILAG III TILLÆG TIL PRODUKTRESUME OG INDLÆGSSEDDEL Disse ændringer til produktresumé og indlægsseddel er gældende fra Kommissionens beslutning. Efter Kommissionens beslutning vil myndighederne i de enkelte
BILAG III TILLÆG TIL PRODUKTRESUME OG INDLÆGSSEDDEL Disse ændringer til produktresumé og indlægsseddel er gældende fra Kommissionens beslutning. Efter Kommissionens beslutning vil myndighederne i de enkelte
Indlægsseddel: Information til brugeren. Canesten, vaginalcreme 1 % clotrimazol
 Indlægsseddel: Information til brugeren Canesten, vaginalcreme 1 % clotrimazol Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
Indlægsseddel: Information til brugeren Canesten, vaginalcreme 1 % clotrimazol Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
Diane 35 grundlæggende version af patientkort og tjekliste til den ordinerende læge 2/11/2014
 Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får. Se i indlægssedlen,
Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får. Se i indlægssedlen,
Bilag I. Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne
 Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag III Ændringer til produktresuméet og indlægssedlen
 Bilag III Ændringer til produktresuméet og indlægssedlen Bemærk: Disse ændringer skal indføres i det gældende produktresumé, etikettering og indlægsseddel. Det er de endelige versioner, der blev opnået
Bilag III Ændringer til produktresuméet og indlægssedlen Bemærk: Disse ændringer skal indføres i det gældende produktresumé, etikettering og indlægsseddel. Det er de endelige versioner, der blev opnået
Ministeren for Sundhed og Forebyggelse har i brev af 19. november 2013 bedt Danske Regioner om en redegørelse vedr. håndtering af henvendelser
 N O T A T Ministeriet for Sundhed og Forebyggelse Regionernes svar på ministerens spørgsmål vedr. håndtering af henvendelser fra patienter med alvorlige formodede bivirkninger ved HPV-vaccination. 16-12-2013
N O T A T Ministeriet for Sundhed og Forebyggelse Regionernes svar på ministerens spørgsmål vedr. håndtering af henvendelser fra patienter med alvorlige formodede bivirkninger ved HPV-vaccination. 16-12-2013
Informationsbrochure til patienter
 Jinarc (tolvaptan) Informationsbrochure til patienter Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette
Jinarc (tolvaptan) Informationsbrochure til patienter Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette
Dosisdispensering. Information om dosispakket medicin til den praktiserende læge, hjemmesygeplejen, plejehjemmet m.m.
 Dosisdispensering Information om dosispakket medicin til den praktiserende læge, hjemmesygeplejen, plejehjemmet m.m. Hvad er dosisdispensering? Ved dosisdispensering forstås at et apotek pakker den enkelte
Dosisdispensering Information om dosispakket medicin til den praktiserende læge, hjemmesygeplejen, plejehjemmet m.m. Hvad er dosisdispensering? Ved dosisdispensering forstås at et apotek pakker den enkelte
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Wartec 0,15 % creme Podophyllotoxin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Gem indlægssedlen.
Indlægsseddel: Information til brugeren Wartec 0,15 % creme Podophyllotoxin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Gem indlægssedlen.
Europaudvalget EUU alm. del - Bilag 143 Offentligt. Resumé
 Europaudvalget EUU alm. del - Bilag 143 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for lægemidlet
Europaudvalget EUU alm. del - Bilag 143 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for lægemidlet
- om behandling af kronisk leddegigt med Sandimmun Neoral
 Patientinformation - om behandling af kronisk leddegigt med Sandimmun Neoral - Ciclosporin Velkommen til Vejle Sygehus Medicinsk Afdeling Rev. dec. 2008 Sandimmun Neoral (Ciclosporin) Sandimmun Neoral
Patientinformation - om behandling af kronisk leddegigt med Sandimmun Neoral - Ciclosporin Velkommen til Vejle Sygehus Medicinsk Afdeling Rev. dec. 2008 Sandimmun Neoral (Ciclosporin) Sandimmun Neoral
GENERELLE BRUGERBETINGELSER FOR
 GENERELLE BRUGERBETINGELSER FOR mypku Disse generelle brugerbetingelser ( Betingelser ) fastsætter de betingelser, der gælder mellem dig som bruger ( Brugeren ) og Nutricia A/S, CVR.: 73128110 ( Nutricia
GENERELLE BRUGERBETINGELSER FOR mypku Disse generelle brugerbetingelser ( Betingelser ) fastsætter de betingelser, der gælder mellem dig som bruger ( Brugeren ) og Nutricia A/S, CVR.: 73128110 ( Nutricia
Indlægsseddel: Information til brugeren. CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol
 Indlægsseddel: Information til brugeren CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol Læs denne indlægsseddel grundigt. Den indeholder vigtige informationer. Du kan få Canesten uden recept. For at
Indlægsseddel: Information til brugeren CANESTEN, vaginalcreme 1 % Aktivt stof: Clotrimazol Læs denne indlægsseddel grundigt. Den indeholder vigtige informationer. Du kan få Canesten uden recept. For at
Europaudvalget (2. samling) EUU alm. del - Bilag 207 Offentligt. Resumé
 Europaudvalget (2. samling) EUU alm. del - Bilag 207 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for
Europaudvalget (2. samling) EUU alm. del - Bilag 207 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for
De vigtigste risici du bør være opmærksom på når du udskriver Arava omfatter:
 ARAVA leflunomid Praktisk vejledning til læger specifik sikkerhedsinformation Arava (leflunomid) er et sygdomsmodificerende antirheumatisk middel ( Disease Modifying Antirheumatic Drug, DMARD), der er
ARAVA leflunomid Praktisk vejledning til læger specifik sikkerhedsinformation Arava (leflunomid) er et sygdomsmodificerende antirheumatisk middel ( Disease Modifying Antirheumatic Drug, DMARD), der er
KOMMISSIONENS GENNEMFØRELSESDIREKTIV 2012/25/EU
 10.10.2012 Den Europæiske Unions Tidende L 275/27 DIREKTIVER KOMMISSIONENS GENNEMFØRELSESDIREKTIV 2012/25/EU af 9. oktober 2012 om informationsprocedurer i forbindelse med udveksling af menneskelige organer
10.10.2012 Den Europæiske Unions Tidende L 275/27 DIREKTIVER KOMMISSIONENS GENNEMFØRELSESDIREKTIV 2012/25/EU af 9. oktober 2012 om informationsprocedurer i forbindelse med udveksling af menneskelige organer
Indlægssedler opdateres løbende. Du kan se den nyeste indlægsseddel for Brentan på
 Indlægsseddel: Information til brugeren Brentan 400 mg bløde vaginalkapsler Miconazolnitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Brentan 400 mg bløde vaginalkapsler Miconazolnitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Toctino (alitretinoin)
 Præventionsprogram TOC-010-250908-B VEJLEDNING TIL LÆGER OG APOTEKER Toctino (alitretinoin) Vejledning til læger der ordinerer Toctino Læs venligst denne vejledning grundigt, før De diskuterer muligheden
Præventionsprogram TOC-010-250908-B VEJLEDNING TIL LÆGER OG APOTEKER Toctino (alitretinoin) Vejledning til læger der ordinerer Toctino Læs venligst denne vejledning grundigt, før De diskuterer muligheden
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Lacrofarm Junior, pulver til oral opløsning, enkeltdosisbeholder Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder
Indlægsseddel: Information til brugeren Lacrofarm Junior, pulver til oral opløsning, enkeltdosisbeholder Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder
Zovir 5 % creme Aciclovir
 11. november 2016 Zovir 5 % creme Aciclovir Der findes to pakningsstørrelser af Zovir 5 % creme. Den fås med henholdsvis 10 g og 2 g med hver sin indlægsseddel. Se de følgende sider. Første indlægsseddel
11. november 2016 Zovir 5 % creme Aciclovir Der findes to pakningsstørrelser af Zovir 5 % creme. Den fås med henholdsvis 10 g og 2 g med hver sin indlægsseddel. Se de følgende sider. Første indlægsseddel
Klar besked om P-PILLER / MINIPILLER
 Klar besked om PPILLER / MINIPILLER PPILLER Ppiller er tabletter, der indeholder to hormoner: Østrogen og gestagen. Ppiller forhindrer ægløsning ved at blokere for dannelsen af de overordnede kønshormoner.
Klar besked om PPILLER / MINIPILLER PPILLER Ppiller er tabletter, der indeholder to hormoner: Østrogen og gestagen. Ppiller forhindrer ægløsning ved at blokere for dannelsen af de overordnede kønshormoner.
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Wartec 5 mg/ml kutanopløsning Podophyllotoxin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Wartec 5 mg/ml kutanopløsning Podophyllotoxin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Agomelatin Mylan til behandling af svære depressive episoder hos voksne
 Vigtig information Må ikke smides ud! Agomelatin Mylan til behandling af svære depressive episoder hos voksne Ordinationsvejledning Information til læger og sundhedspersonale Anbefalinger vedrørende: Monitorering
Vigtig information Må ikke smides ud! Agomelatin Mylan til behandling af svære depressive episoder hos voksne Ordinationsvejledning Information til læger og sundhedspersonale Anbefalinger vedrørende: Monitorering
Europaudvalget EUU alm. del - Bilag 146 Offentligt. Resumé
 Europaudvalget EUU alm. del - Bilag 146 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for lægemidlet
Europaudvalget EUU alm. del - Bilag 146 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse med betingelser for lægemidlet
Bilag I. Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne
 Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne 1 Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag III. Ændringer til relevante afsnit af produktinformationen
 Bilag III Ændringer til relevante afsnit af produktinformationen Bemærk: Disse ændringer til de relevante afsnit i produktresuméet og indlægssedlen er resultatet af referral-proceduren. Produktinformationen
Bilag III Ændringer til relevante afsnit af produktinformationen Bemærk: Disse ændringer til de relevante afsnit i produktresuméet og indlægssedlen er resultatet af referral-proceduren. Produktinformationen
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Levodonna 1,5 mg tabletter Levonorgestrel
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Levodonna 1,5 mg tabletter Levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Levodonna 1,5 mg tabletter Levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
VIGTIG INFORMATION OM CYPRETYL OG RISIKOEN FOR BLODPROPPER
 Patientkort: Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får. Se
Patientkort: Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får. Se
Indlægsseddel: Information til brugeren Dulcolax 10 mg, suppositorier Bisacodyl
 Indlægsseddel: Information til brugeren Dulcolax 10 mg, suppositorier Bisacodyl Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
Indlægsseddel: Information til brugeren Dulcolax 10 mg, suppositorier Bisacodyl Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug
BILAG III. Ændringer i relevante afsnit af produktresumeet, etiketteringen og indlægssedlen
 BILAG III Ændringer i relevante afsnit af produktresumeet, etiketteringen og indlægssedlen 19 PRODUKTRESUME Dette lægemiddel er underlagt supplerende overvågning. Dermed kan nye sikkerhedsoplysninger hurtigt
BILAG III Ændringer i relevante afsnit af produktresumeet, etiketteringen og indlægssedlen 19 PRODUKTRESUME Dette lægemiddel er underlagt supplerende overvågning. Dermed kan nye sikkerhedsoplysninger hurtigt
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Cholestagel 625 mg filmovertrukne tabletter Colesevelam hydroklorid
 B. INDLÆGSSEDDEL 21 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Cholestagel 625 mg filmovertrukne tabletter Colesevelam hydroklorid Læs hele denne indlægsseddel grundigt, inden De begynder at tage medicinen.
B. INDLÆGSSEDDEL 21 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Cholestagel 625 mg filmovertrukne tabletter Colesevelam hydroklorid Læs hele denne indlægsseddel grundigt, inden De begynder at tage medicinen.
Nordjysk Praksisdag 12/9-14 AK-behandling - hvordan hjælper vi patienten bedst muligt? Helle Ravnslund Sørensen Sygeplejerske Trombosecenter Aalborg
 Nordjysk Praksisdag 12/9-14 AK-behandling - hvordan hjælper vi patienten bedst muligt? Helle Ravnslund Sørensen Sygeplejerske Trombosecenter Aalborg Trombosecenter Aalborg, Funktioner Rådgivning Placering:
Nordjysk Praksisdag 12/9-14 AK-behandling - hvordan hjælper vi patienten bedst muligt? Helle Ravnslund Sørensen Sygeplejerske Trombosecenter Aalborg Trombosecenter Aalborg, Funktioner Rådgivning Placering:
Kondom er en effektiv præventionsmetode
 Kondom K L A R B E S K E D Kondom Kondom er en nem præventionsmetode, der kan bruges af alle. Kondomet er lavet af meget tyndt naturgummi og formet som et langt hylster, der rulles på mandens rejste penis
Kondom K L A R B E S K E D Kondom Kondom er en nem præventionsmetode, der kan bruges af alle. Kondomet er lavet af meget tyndt naturgummi og formet som et langt hylster, der rulles på mandens rejste penis
Indlægsseddel: Information til brugeren Brentan 20 mg/g creme Miconazolnitrat
 Indlægsseddel: Information til brugeren Brentan 20 mg/g creme Miconazolnitrat Læs denne indlægsseddel grundigt inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid
Indlægsseddel: Information til brugeren Brentan 20 mg/g creme Miconazolnitrat Læs denne indlægsseddel grundigt inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid
Tværsektoriel vejledning om anbefalede arbejdsgange i forbindelse med implementering af Fælles Medicinkort (FMK) på sygehuse og i praksissektoren
 Region Syddanmark Sagsnr. 13/31059 Tværsektoriel vejledning om anbefalede arbejdsgange i forbindelse med implementering af Fælles Medicinkort (FMK) på sygehuse og i praksissektoren Indholdsfortegnelse.....Side
Region Syddanmark Sagsnr. 13/31059 Tværsektoriel vejledning om anbefalede arbejdsgange i forbindelse med implementering af Fælles Medicinkort (FMK) på sygehuse og i praksissektoren Indholdsfortegnelse.....Side
TALEPAPIR. Det talte ord gælder. Samråd BF ( lykkepiller ) Tid og sted: Folketinget, onsdag den 25. maj 2011, kl. 13. Dok nr.
 Sundhedsudvalget 2010-11 SUU alm. del, endeligt svar på spørgsmål 761 Offentligt TALEPAPIR Det talte ord gælder Anledning: Taletid: Samråd BF ( lykkepiller ) (8-9 min.) Tid og sted: Folketinget, onsdag
Sundhedsudvalget 2010-11 SUU alm. del, endeligt svar på spørgsmål 761 Offentligt TALEPAPIR Det talte ord gælder Anledning: Taletid: Samråd BF ( lykkepiller ) (8-9 min.) Tid og sted: Folketinget, onsdag
clotrimazol Information til dig om svamp i underlivet
 clotrimazol Information til dig om svamp i underlivet Indhold Svamp i underlivet hvad er det?...4 Faktorer der kan forårsage svampeinfektion... 6 Hvad er symptomerne?...8 Smitter svamp?... 8 Kan mænd få
clotrimazol Information til dig om svamp i underlivet Indhold Svamp i underlivet hvad er det?...4 Faktorer der kan forårsage svampeinfektion... 6 Hvad er symptomerne?...8 Smitter svamp?... 8 Kan mænd få
At forberede sig på at se en fertilitetsspecialist. Spørgsmål til den kvindelige partner. Tag endnu et skridt fremad
 At forberede sig på at se en fertilitetsspecialist Tag endnu et skridt fremad Det kræver stor dygtighed at identificere kilden til fertilitetsproblemer og anbefale den rette behandling. En fertilitetsklinik
At forberede sig på at se en fertilitetsspecialist Tag endnu et skridt fremad Det kræver stor dygtighed at identificere kilden til fertilitetsproblemer og anbefale den rette behandling. En fertilitetsklinik
Kræftens Bekæmpelse, Scleroseforeningen, Gigtforeningen, Danske Patienter, Epilepsiforeningen og Lægeforeningen
 Notat Jr. /2015-2120 Emne: Til: Fra: En sikker model for forsøgsordning med medicinsk cannabis Folketingets Sundhedsudvalg Kræftens Bekæmpelse, Scleroseforeningen, Gigtforeningen, Danske Patienter, Epilepsiforeningen
Notat Jr. /2015-2120 Emne: Til: Fra: En sikker model for forsøgsordning med medicinsk cannabis Folketingets Sundhedsudvalg Kræftens Bekæmpelse, Scleroseforeningen, Gigtforeningen, Danske Patienter, Epilepsiforeningen
INDLÆGSSEDDEL : INFORMATION TIL BRUGEREN. Redap 1 mg/g gel. Adapalen
 INDLÆGSSEDDEL : INFORMATION TIL BRUGEREN Redap 1 mg/g gel Adapalen Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. - Gem indlægssedlen.
INDLÆGSSEDDEL : INFORMATION TIL BRUGEREN Redap 1 mg/g gel Adapalen Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. - Gem indlægssedlen.
Information om. levonorgestrel. Mirena 1
 Information om levonorgestrel Mirena 1 Hvad er Mirena? Indhold Hvad er Mirena?... 2 Hvordan virker Mirena?... 3 Kan Mirena blive udstødt?... 3 Mirena er et receptpligtigt lægemiddel med høj præventiv sikkerhed
Information om levonorgestrel Mirena 1 Hvad er Mirena? Indhold Hvad er Mirena?... 2 Hvordan virker Mirena?... 3 Kan Mirena blive udstødt?... 3 Mirena er et receptpligtigt lægemiddel med høj præventiv sikkerhed
Behandling af stærke smerter
 PATIENTVEJLEDNING Behandling af stærke smerter MÅ KUN UDLEVERES I FORBINDELSE MED LÆGEORDINERING Janssen-Cilag A/S Kære patient Til behandling af Deres smerter har Deres læge ordineret Jurnista. Jurnista
PATIENTVEJLEDNING Behandling af stærke smerter MÅ KUN UDLEVERES I FORBINDELSE MED LÆGEORDINERING Janssen-Cilag A/S Kære patient Til behandling af Deres smerter har Deres læge ordineret Jurnista. Jurnista
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Mucomyst brusetabletter 200 mg. Acetylcystein
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Mucomyst brusetabletter 200 mg Acetylcystein Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Mucomyst brusetabletter 200 mg Acetylcystein Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Bilag III. Ændringer til relevante afsnit i produktresuméer og indlægssedler
 Bilag III Ændringer til relevante afsnit i produktresuméer og indlægssedler Note: De pågældende punkter i produktresuméet og indlægssedlen er resultatet af referral proceduren. Produktinformationen kan
Bilag III Ændringer til relevante afsnit i produktresuméer og indlægssedler Note: De pågældende punkter i produktresuméet og indlægssedlen er resultatet af referral proceduren. Produktinformationen kan
Tevas fortrolighedserklæring lægemiddelovervågning (pharmacovigilance og kvalitet) Definitioner, der anvendes i denne fortrolighedserklæring
 Tevas fortrolighedserklæring lægemiddelovervågning (pharmacovigilance og kvalitet) Definitioner, der anvendes i denne fortrolighedserklæring Bivirkning betyder en uønsket, utilsigtet eller skadelig hændelse
Tevas fortrolighedserklæring lægemiddelovervågning (pharmacovigilance og kvalitet) Definitioner, der anvendes i denne fortrolighedserklæring Bivirkning betyder en uønsket, utilsigtet eller skadelig hændelse
Jordemoderuddannelsen Aalborg. EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00
 Jordemoderuddannelsen Aalborg EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00 1 DEL I - ingen hjælpemidler tilladt Varighed 2 timer (65 point kan opnås) 1. Beskriv de 3 faser som farmakokinetikken
Jordemoderuddannelsen Aalborg EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00 1 DEL I - ingen hjælpemidler tilladt Varighed 2 timer (65 point kan opnås) 1. Beskriv de 3 faser som farmakokinetikken
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. NorLevo 1,5 mg tablet Levonorgestrel
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN NorLevo 1,5 mg tablet Levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN NorLevo 1,5 mg tablet Levonorgestrel Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid
Bilag 2. Medicininstruks for Elleslettegård
 Bilag 2 Medicininstruks for Elleslettegård Formålet: Formålet med denne medicininstruks er at sikre en sikker medicinhåndtering og dermed at forebygge utilsigtede hændelser. Eleven skal have den rigtige
Bilag 2 Medicininstruks for Elleslettegård Formålet: Formålet med denne medicininstruks er at sikre en sikker medicinhåndtering og dermed at forebygge utilsigtede hændelser. Eleven skal have den rigtige
Bilag I. Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne
 Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Bilag I Videnskabelige konklusioner og begrundelser for ændring af betingelserne for markedsføringstilladelsen/-tilladelserne Videnskabelige konklusioner Under hensyntagen til PRAC's vurderingsrapport
Indlægsseddel: Information til brugeren. Benaliv 0,5 mg/ml øjendråber, suspension. Levocabastin
 Indlægsseddel: Information til brugeren Benaliv 0,5 mg/ml øjendråber, suspension Levocabastin Læs denne indlægsseddel grundigt inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Benaliv 0,5 mg/ml øjendråber, suspension Levocabastin Læs denne indlægsseddel grundigt inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Zovir 5 % creme Aciclovir
 11. januar 2018 Zovir 5 % creme Aciclovir Der findes to pakningsstørrelser af Zovir 5 % creme. Den fås med henholdsvis 10 g og 2 g med hver sin indlægsseddel. Se de følgende sider. Første indlægsseddel
11. januar 2018 Zovir 5 % creme Aciclovir Der findes to pakningsstørrelser af Zovir 5 % creme. Den fås med henholdsvis 10 g og 2 g med hver sin indlægsseddel. Se de følgende sider. Første indlægsseddel
Indlægsseddel: Information til brugeren. ZYTIGA 250 mg tabletter abirateronacetat
 Indlægsseddel: Information til brugeren ZYTIGA 250 mg tabletter abirateronacetat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. - Gem
Indlægsseddel: Information til brugeren ZYTIGA 250 mg tabletter abirateronacetat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. - Gem
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Syntocinon, næsespray, opløsning 6,7 mikrogram/dosis oxytocin
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Syntocinon, næsespray, opløsning 6,7 mikrogram/dosis oxytocin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Syntocinon, næsespray, opløsning 6,7 mikrogram/dosis oxytocin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige
Europaudvalget EUU alm. del - Bilag 421 Offentligt
 Europaudvalget EUU alm. del - Bilag 421 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse for lægemidlet INCRELEX til sjældne
Europaudvalget EUU alm. del - Bilag 421 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsføringstilladelse for lægemidlet INCRELEX til sjældne
(Meddelelser) EUROPA-KOMMISSIONEN
 2.8.2013 Den Europæiske Unions Tidende C 223/1 (Meddelelser) MEDDELELSER FRA DEN EUROPÆISKE UNIONS INSTITUTIONER, ORGANER, KONTORER OG AGENTURER EUROPA-KOMMISSIONEN Retningslinjer for de forskellige kategorier
2.8.2013 Den Europæiske Unions Tidende C 223/1 (Meddelelser) MEDDELELSER FRA DEN EUROPÆISKE UNIONS INSTITUTIONER, ORGANER, KONTORER OG AGENTURER EUROPA-KOMMISSIONEN Retningslinjer for de forskellige kategorier
Indlægsseddel: Information til brugeren Doloproct 1 mg/g + 20 mg/g rektalcreme
 Indlægsseddel: Information til brugeren Doloproct 1 mg/g + 20 mg/g rektalcreme Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger Gem indlægssedlen.
Indlægsseddel: Information til brugeren Doloproct 1 mg/g + 20 mg/g rektalcreme Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger Gem indlægssedlen.
Finasterid Actavis bruges til behandling og sygdomskontrol af godartet (ikke cancer) forstørrelse af blærehalsen.
 Indlægsseddel: Information til brugeren Finasterid Actavis 5 mg filmovertrukne tabletter Finasterid Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige
Indlægsseddel: Information til brugeren Finasterid Actavis 5 mg filmovertrukne tabletter Finasterid Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Heracillin 500 mg, filmovertrukne tabletter Heracillin 1 g, filmovertrukne tabletter. flucloxacillinnatrium
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Heracillin 500 mg, filmovertrukne tabletter Heracillin 1 g, filmovertrukne tabletter flucloxacillinnatrium Læs denne indlægsseddel grundigt, inden du begynder at
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Heracillin 500 mg, filmovertrukne tabletter Heracillin 1 g, filmovertrukne tabletter flucloxacillinnatrium Læs denne indlægsseddel grundigt, inden du begynder at
Indlægsseddel: Information til brugeren. Nix 5 %, creme permethrin
 Indlægsseddel: Information til brugeren Nix 5 %, creme permethrin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug altid Nix nøjagtigt
Indlægsseddel: Information til brugeren Nix 5 %, creme permethrin Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger. Brug altid Nix nøjagtigt
Information for Kodimagnyl Ikke-stoppende DAK filmovertrukne tabletter
 Information for Kodimagnyl Ikke-stoppende DAK filmovertrukne tabletter Denne information findes i 2 udgaver. Hvis du har købt en pakning med op til 20 tabletter, skal du læse den information, der starter
Information for Kodimagnyl Ikke-stoppende DAK filmovertrukne tabletter Denne information findes i 2 udgaver. Hvis du har købt en pakning med op til 20 tabletter, skal du læse den information, der starter
Indlægsseddel: Information til brugeren. Antepsin 1g tabletter Sucralfat. Den senest reviderede indlægsseddel kan findes på
 Indlægsseddel: Information til brugeren Antepsin 1g tabletter Sucralfat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid dette
Indlægsseddel: Information til brugeren Antepsin 1g tabletter Sucralfat Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger. Tag altid dette
