Skriftlig prøve i kursus 26173/F14 Side 1 af 15 UORGANISK KEMI Torsdag den 22. maj 2014
|
|
|
- Sidsel Aagaard
- 7 år siden
- Visninger:
Transkript
1 Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for O 2. 5% b) Angiv bindingsorden for O 2. c) Angiv de magnetiske egenskaber for O 2.
2 Skriftlig prøve i kursus 26173/F14 Side 2 af Hvis O 2 oxideres et trin kan ionen O 2 + dannes. Argumenter ud fra dit diagram i opgave 1.2 om bindingen i denne ion er stærkere eller svagere end i O 2 molekylet. 3% Opgave Navngivning. Navngiv følgende forbindelser: 5% Na 2 O H 2 SO 4 MnO 2 KMnO 4 FeS 2.2 Færdiggør og afstem følgende reaktionsskemaer: 5% Na(s) + H 2 O(l) BaO(s) + H 2 O(l) Sr 2+ (aq) + SO 4 2 (aq) AgNO 3 (aq) + HI(aq) Al(s) + NO 3 (aq) (basisk)
3 Skriftlig prøve i kursus 26173/F14 Side 3 af 15 Opgave 3. Kompleksforbindelser 3.1 Navngiv følgende kompleksforbindelser: [Mn(H 2 O) 6 ]Cl 2, [Fe(H 2 O) 6 ](NO 3 ) 2, [Co(H 2 O) 6 ]SO 4 3% 3.2 Opskriv d-orbital diagrammer for følgende kompleksioner: [Mn(H 2 O) 6 ] 2+, [Fe(H 2 O) 6 ] 2+, [Co(H 2 O) 6 ] 2+ 4%
4 Skriftlig prøve i kursus 26173/F14 Side 4 af Tegn en rumlig struktur af [Mn(H 2 O) 6 ] 2+. 3% Opgave 4. Lewisstrukturer og VSEPR 4.1 Angiv Lewisstrukturer og eventuelle resonansstrukturer (med formelle ladninger) for H 2 O, BeCl 2, BF 4, SO 2, NO 2 : 4% 4.2 Tegn en tydelig tredimensionel struktur og angiv omtrentlige bindingsvinkler for H 2 O, BeCl 2, BF 4, SO 2, NO 2. 4%
5 Skriftlig prøve i kursus 26173/F14 Side 5 af Angiv for hvert af følgende molekyler/ioner, om de har et dipolmoment, der er forskelligt fra 0: H 2 O, BeCl 2, BF 4, SO 2, NO 2. Opgave 5. Reaktioner 5.1 Færdiggør og afstem følgende reaktionsskemaer for følgende stoffers reaktion med rigeligt ilt eller rigeligt vand: 5% Mg(s) + O 2 (g) Cu(s) + O 2 (g) Li(s) + O 2 (g) SO 3 (g) + H 2 O(l) P 4 O 10 (s) + H 2 O(l)
6 Skriftlig prøve i kursus 26173/F14 Side 6 af 15 Jern metal fremstilles ud fra forskellige jernmineraler for eksempel jern(ii)disulfid også kaldet svovlkis eller narreguld. Først omdannes jern(ii)disulfid til jern(iii)oxid ved opvarmning i luft (ristning). Derefter reduceres jern(iii)oxid med fx koks for at fremstille metallet. 5.2 Opskriv en afstemt reaktionsligning for fremstilling af jern(iii)oxid ud fra jern(ii)disulfid. 3% 5.3 Opskriv en afstemt reaktionsligning for fremstilling af jern ud fra jern(iii)oxid.
7 Skriftlig prøve i kursus 26173/F14 Side 7 af 15 Bilag 1. Periodisk system med atommasser og elektronegativiteter 1 1, ,0026 H He 2,1 3 6, , , , , , , ,180 Li Be B C N O F Ne 1,0 1,5 2,0 2,5 3,0 3,5 4, , , , , , , , ,948 Na Mg Al Si P S Cl Ar 0,9 1,2 1,5 1,8 2,1 2,5 3, , , , , , , , , , , , , , , , , , ,80 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 0,8 1,0 1,3 1,5 1,6 1,6 1,5 1,8 1,9 1,9 1,9 1,6 1,6 1,8 2,0 2,4 2, , , , , , ,94 43 (97,907) , , , , , , , , , , ,29 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 0,8 1,0 1,2 1,4 1,6 1,8 1,9 2,2 2,2 2,2 1,9 1,7 1,7 1,8 1,9 2,1 2, , , , , , , , , , , , , , , ,98 84 (209) 85 (210) 86 (222) Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 0,7 0,9 1,0 1,3 1,5 1,7 1,9 2,2 2,2 2,2 2,4 1,9 1,8 1,9 1,9 2,0 2,2 87 (223) 88 (226) 89 (227) 104 (261) 105 (262) 106 (263) 107 (262) 108 (265) 109 (266) Fr Ra Ac Rf Db Sg Bh Hs Mt 0,7 0, , , ,24 61 (144,91) , , , , , , , , , ,97 Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu , , ,03 93 (237,05) 94 (244,06) 95 (243,06) 96 (247) 97 (247,07) 98 (251,08) 99 (252,08) 100 (257,1) 101 (258,1) 102 (259,1) 103 (262,1) Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
8 Skriftlig prøve i kursus 26173/F14 Side 8 af 15 Opgave 6. Hydrogen 6.1 Anvend standardreduktionspotentialer til at forudsige om følgende reaktion er spontan: 2 H + + Cu H 2 + Cu Anvend tabelværdier for bindingsenthalpier til at beregne reaktionsenthalpien for forbrænding af hydrogen: 4% 2 H 2 (g) + O 2 (g) 2 H 2 O(g) 6.3 Anvend standardenthalpier til at beregne reaktionsenthalpien for reaktionen givet i 6.2. Husk at være opmærksom på tilstandsformer. 3% 6.4 Angiv om reaktionen i 6.2 er endotherm eller exotherm. 1%
9 Skriftlig prøve i kursus 26173/F14 Side 9 af 15 Opgave 7. Farver og energier Lys med en bølgelængde på 450 nm er blåt. 7.1 Beregn energien (i enheden kj mol -1 ) af lys med en bølgelængde på 450 nm. 3% 7.2 Energien af bindingen i O 2 er 498 kj mol -1. Kan det blå lys bryde denne binding? 7.3 [VO(H 2 O) 5 ] 2+ er en forbindelse af vanadium(iv) hvor liganderne sidder i et oktaeder omkring centralatomet. Opskriv et d-orbital diagram for denne forbindelse under antagelse af, at den er oktaedrisk. 3% Forbindelsen er blå. 7.4 Foreslå ved brug af farvehjulet en cirka værdi for bølgelængden af det lys som forbindelsen absorberer.
10 Skriftlig prøve i kursus 26173/F14 Side 10 af 15 Opgave 8. Krystalstrukturer ZnS(s), zinksulfid kaldes også zinkblende. Det krystalliserer i en kubisk enhedscelle, se figur. 8.1 Angiv hvor mange Zn 2+ ioner og hvor mange S 2 ioner en enhedscelle indeholder. Densiteten af ZnS er 3,71 g cm Beregn volumen af enhedscellen. 3% 8.3 Beregn sidelængden af enhedscellen. S 2 sidder tetraedrisk omkring Zn 2+ i krystallen, se figuren. 8.4 Beregn den korteste afstand mellem Zn 2+ og S 2 ud fra sidelængden af enhedscellen. (Dette kan for eksempel gøres ved at konstruere retvinklede trekanter og bruge pythagoras sætning, se bilag 2.) 3%
11 Skriftlig prøve i kursus 26173/F14 Side 11 af 15 Opgave 9. Kobber(II)oxid 9.1 Opstil en Born-Haber cyklus for reaktionsskemaet: 4% Cu(s) + ½ O 2 (g) CuO(s) 9.2 Beregn gitterenthalpien, gitter H, for CuO(s) ved beregning ud fra Born-Haber cyklussen ovenfor. 4% 9.3 Opskriv afstemte reaktionsskemaer for, hvorledes CuO(s) kan fremstilles ved at opløse kobber metal i salpetersyre og derefter opvarme opløsningen til høj temperatur.
12 Skriftlig prøve i kursus 26173/F14 Side 12 af 15 Opgave 10. Identifikation af ionisk forbindelse En opløsning af en ren ionisk forbindelse er blevet undersøgt og observationerne er blevet noteret: 1. Indikatorpapir viser, at opløsningen er nogenlunde neutral. 2. Opløsningen er farveløs. 3. Hvis opløsningen først tilsættes lidt HNO 3 (aq) og derefter AgNO 3 (aq) sker der ingen udfældning. 4. Hvis opløsningen først tilsættes lidt HNO 3 (aq) og derefter H 2 SO 4 (aq) sker der ingen udfældning. 5. Hvis opløsningen først tilsættes lidt HNO 3 (aq) og derefter BaCl 2 (aq) fremkommer et hvidt bundfald. 6. Hvis opløsningen først tilsættes lidt HNO 3 (aq) og derefter gradvist NaOH(aq) sker der en udfældning af et hvidt stof, der ikke går i opløsning igen med overskud af NaOH(aq). 7. Hvis opløsningen tilsættes Na 2 S(aq) sker der udfældning af et hvidt stof Foreslå 2 forskellige ioner, der er farvede. (Og derfor kan udelukkes fordi opløsningen ifølge pkt. 2 er farveløs.) 10.2 Hvilke kationer udelukkes ved punkt 4? 10.3 Hvilken anion påvises ved punkt 5? 10.4 Opskriv mindst 2 kationer, der udelukkes ved punkt 6.
13 Skriftlig prøve i kursus 26173/F14 Side 13 af 15 Påvisningen af kationen i den ioniske forbindelse er ikke helt entydig ud fra punkt 1-7 og der er stadig to muligheder for identiteten af saltet. Med den yderligere oplysning at den ioniske forbindelse er letopløselig kan identiteten bestemmes Angiv de to muligheder for den ioniske forbindelse. Angiv den letopløselige af de to eller angiv en anden måde at skelne mellem kationerne.
14 Skriftlig prøve i kursus 26173/F14 Side 14 af 15 Bilag 2. Data til brug i beregninger Fysiske konstanter: Avogadros konstant: L = 6, mol 1 Plancks konstant: h = 6, J s Lysets hastighed: c = 2, m s 1 Standard reduktionspotentialer: E (Cu 2+ (aq)/cu(s)) = 0,34 V E (2H + (aq)/h 2 (g)) = 0 V Alle E er ved 25 C, tryk 1 bar og koncentrationer 1 M. Termodynamiske data: Bindingsenergi for O=O b H(O=O) = 498 kj mol 1 Bindingsenergi for H H b H(H H) = 436 kj mol 1 Bindingsenergi for H O b H(H O) = 464 kj mol 1 Dannelsesenthalpi for H 2 O(l) f H(H 2 O(l)) = 286 kj mol 1 Dannelsesenthalpi for CuO(s) f H(CuO(s)) = 157 kj mol 1 Fordampningsenthalpi for H 2 O(l) evap H(H 2 O(l)) = 44 kj mol 1 Atomiseringsenthalpi for Cu(s) a H(Cu(s)) = 338 kj mol 1 1. ioniseringssenthalpi for Cu(g) ΙΕ1(Cu(g)) = 746 kj mol 1 2. ioniseringssenthalpi for Cu(g) ΙΕ2(Cu(g)) = 1958 kj mol 1 1. elektronaffinitet for O(g) EA1(O(g)) = 141 kj mol 1 2. elektronaffinitet for O(g) EA2(O(g)) = 798 kj mol 1 Pythagoras sætning for sidelængderne (a og b) og hypotenusen (c) i en retvinklet trekant: a 2 + b 2 = c 2 Farvehjulet: Orange Rød Gul Violet Grøn Blå
15 Skriftlig prøve i kursus 26173/F14 Side 15 af 15 Periodisk system med atommasser og elektronegativiteter 1 1, ,0026 H He 2,1 3 6, , , , , , , ,180 Li Be B C N O F Ne 1,0 1,5 2,0 2,5 3,0 3,5 4, , , , , , , , ,948 Na Mg Al Si P S Cl Ar 0,9 1,2 1,5 1,8 2,1 2,5 3, , , , , , , , , , , , , , , , , , ,80 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 0,8 1,0 1,3 1,5 1,6 1,6 1,5 1,8 1,9 1,9 1,9 1,6 1,6 1,8 2,0 2,4 2, , , , , , ,94 43 (97,907) , , , , , , , , , , ,29 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 0,8 1,0 1,2 1,4 1,6 1,8 1,9 2,2 2,2 2,2 1,9 1,7 1,7 1,8 1,9 2,1 2, , , , , , , , , , , , , , , ,98 84 (209) 85 (210) 86 (222) Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 0,7 0,9 1,0 1,3 1,5 1,7 1,9 2,2 2,2 2,2 2,4 1,9 1,8 1,9 1,9 2,0 2,2 87 (223) 88 (226) 89 (227) 104 (261) 105 (262) 106 (263) 107 (262) 108 (265) 109 (266) Fr Ra Ac Rf Db Sg Bh Hs Mt 0,7 0, , , ,24 61 (144,91) , , , , , , , , , ,97 Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu , , ,03 93 (237,05) 94 (244,06) 95 (243,06) 96 (247) 97 (247,07) 98 (251,08) 99 (252,08) 100 (257,1) 101 (258,1) 102 (259,1) 103 (262,1) Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 UORGANISK KEMI Tirsdag den 18. december 2012
 Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E14 Side 1 af 16 UORGANISK KEMI Fredag den 19. december 2014
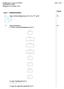 Skriftlig prøve i kursus 26173/E14 Side 1 af 16 pgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for, Al, e 3+ og Br. : [He]2s 2 2p 4 Al: [Ne]3s 2 3p 1 e 3+ : [Ar]3d 5 Br : [Kr] 1.2 Molekylorbitalteori.
Skriftlig prøve i kursus 26173/E14 Side 1 af 16 pgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for, Al, e 3+ og Br. : [He]2s 2 2p 4 Al: [Ne]3s 2 3p 1 e 3+ : [Ar]3d 5 Br : [Kr] 1.2 Molekylorbitalteori.
Skriftlig prøve i kursus 26173/E15 Side 1 af 13 UORGANISK KEMI Fredag den 18. december 2015
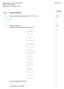 Skriftlig prøve i kursus 26173/E15 Side 1 af 13 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. C: [He]2s 2 2p 2 P: [Ne]3s 2 3p 3 Zn 2+ : [Ar]3d 10 I : [Xe] 1.2 Molekylorbitalteori.
Skriftlig prøve i kursus 26173/E15 Side 1 af 13 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. C: [He]2s 2 2p 2 P: [Ne]3s 2 3p 3 Zn 2+ : [Ar]3d 10 I : [Xe] 1.2 Molekylorbitalteori.
DET PERIODISKE SYSTEM
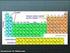 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Danmarks Tekniske Universitet
 Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Danmarks Tekniske Universitet
 Danmarks Tekniske Universitet Side 1 af 18 sider Skriftlig prøve, tirsdag den 18. december 2012 Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer Opgave 1, 2, 3, 4 og 5: Ingen
Danmarks Tekniske Universitet Side 1 af 18 sider Skriftlig prøve, tirsdag den 18. december 2012 Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer Opgave 1, 2, 3, 4 og 5: Ingen
Sporgrundstof definition:
 Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Platin komplekser i kampen mod kræft. Koordinationskemi i aktion. cis-ptcl 2 (NH 3 ) 2. Essentiel, nyttig eller toxisk. Hvad der faktisk skete
 Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold
 Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Test din viden E-forløb
 OPGAVE E8 Test din viden E-forløb Har du styr på E-forløbets kernestof? Nu har du lært en masse om spændingsrækken og redoxreaktioner. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle områder,
OPGAVE E8 Test din viden E-forløb Har du styr på E-forløbets kernestof? Nu har du lært en masse om spændingsrækken og redoxreaktioner. Ved at lave opgaverne nedenfor finder du ud af, om der er nogle områder,
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Økologi kemisk fingerprinting
 Konference om fødevareautencitet: Mg P K B Mn S Cl Cu Zn Fe Ca Mo Ni 0 50 100 150 200 250 Mass (m/z) Økologi kemisk fingerprinting Søren Husted, Institut for Jordbrug og Økologi, IJØ, Det Biovidenskabelige
Konference om fødevareautencitet: Mg P K B Mn S Cl Cu Zn Fe Ca Mo Ni 0 50 100 150 200 250 Mass (m/z) Økologi kemisk fingerprinting Søren Husted, Institut for Jordbrug og Økologi, IJØ, Det Biovidenskabelige
OPGAVER OM DANNELSE AF IONER. OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal.
 OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
Forelæsning 8. Stabile isotoper. Iltisotoper anvendt i paleoklimastudier, magmadannelse, termometri, vand-bjergart reaktion.
 Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Geokemisk differentiation af Jorden oversigt
 Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Mundtlige eksamensopgaver
 Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Dagens program TIL GAVN FOR GARTNERE
 Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Eksamensspørgsmål 2z ke (ikke godkendte) Fag: Kemi C Dato: 7. juni 2013 Lærer: Peter R Nielsen (PN) Censor: Tanja Krüger, VUC Aarhus
 1. Kemisk Binding Gør rede for øvelsen Kovalent- eller Ionbinding? Beskriv ionbinding og kovalent binding og forklar hvordan forskellene på de to typer af kemisk binding udnyttes i for66søget. Stikord
1. Kemisk Binding Gør rede for øvelsen Kovalent- eller Ionbinding? Beskriv ionbinding og kovalent binding og forklar hvordan forskellene på de to typer af kemisk binding udnyttes i for66søget. Stikord
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Eksamensspørgsmål 2c ke, juni Fag: Kemi C-niveau. Censor: Andreas Andersen, Skanderborg Gymnasium
 Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Anvendt kemi 2 - ekstraopgaver
 1 Anvendt kemi - ekstraopgaver Enthalpiberegninger Stoffet ethan (H6) kan afbrændes. a) Opskriv og afstem reaktionsskemaet for forbrændingen. b) Beregn H for reaktionen. Opgave Betragt følgende redoxreaktionsskema:
1 Anvendt kemi - ekstraopgaver Enthalpiberegninger Stoffet ethan (H6) kan afbrændes. a) Opskriv og afstem reaktionsskemaet for forbrændingen. b) Beregn H for reaktionen. Opgave Betragt følgende redoxreaktionsskema:
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017
 EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.
 Indhold 1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.... 2 2. Fældningsreaktioner herunder eksperimentet Saltes opløselighed i vand.... 3 3. Stofmængdekoncentration
Indhold 1. Kovalent binding herunder eksperimentet Undersøgelse af stoffers opløselighed.... 2 2. Fældningsreaktioner herunder eksperimentet Saltes opløselighed i vand.... 3 3. Stofmængdekoncentration
Anvendt kemi 1 ekstraspørgsmål. Koncentration
 Anvendt kemi 1 ekstraspørgsmål Koncentration Til et kemiforsøg skal der fremstilles en række opløsninger af letopløselige salte. Udregn for hver af de følgende opløsninger, hvor mange gram af det aktuelle
Anvendt kemi 1 ekstraspørgsmål Koncentration Til et kemiforsøg skal der fremstilles en række opløsninger af letopløselige salte. Udregn for hver af de følgende opløsninger, hvor mange gram af det aktuelle
Facitliste Anvendt Kemi 1
 Facitliste Anvendt Kemi 1 pgave 1.1 a) NaH 1 stk Na, 1 stk, 1 stk H b) H 2 2 2 stk H 2 stk c) Mg(H) 2 1 stk Mg, 2 stk, 2 stk H d) us 4 1 stk u, 1 stk S 4 stk pgave 1.2 a) M = 9,9969 g/mol b) M = 95,211
Facitliste Anvendt Kemi 1 pgave 1.1 a) NaH 1 stk Na, 1 stk, 1 stk H b) H 2 2 2 stk H 2 stk c) Mg(H) 2 1 stk Mg, 2 stk, 2 stk H d) us 4 1 stk u, 1 stk S 4 stk pgave 1.2 a) M = 9,9969 g/mol b) M = 95,211
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014
 Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Opgaver i atomer. c) Aflæs atommassen for Mg i det periodiske system eller på de udskrevne ark, og skriv det ned.
 Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
Eksamensspørgsmål. Spørgsmål : Atomer og bindinger (Hvilken type stof?) Spørgsmål : Ionforbindelser (Saltes opløselighed i vand
 Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
Eksamensspørgsmål KemiC (17KeC80) Med forbehold for censors godkendelse Oversigt Spørgsmål 1 + 14: Atomer og bindinger (Hvilken type stof?) Spørgsmål 2 + 15: Ionforbindelser (Saltes opløselighed i vand
1 Atomets opbygning. Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom.
 1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
Du skal også komme ind på øvelsen Saltes opløselighed i vand.
 1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
1 Ioner og ionforbindelser
 1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
Eksamensopgaver. NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL
 Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD).
 Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Opgaver til: 9. Radioaktivitet
 Opgaver til: 9. Radioaktivitet 1. Opskriv henfaldskemaet for α-henfaldet af: 229 90 Th 92 U 86 Rn 2. Opskriv henfaldskemaet for β - -henfaldet af: 209 82 Pb 10 4 Be 79 Au 3. Opskriv henfaldskemaet for
Opgaver til: 9. Radioaktivitet 1. Opskriv henfaldskemaet for α-henfaldet af: 229 90 Th 92 U 86 Rn 2. Opskriv henfaldskemaet for β - -henfaldet af: 209 82 Pb 10 4 Be 79 Au 3. Opskriv henfaldskemaet for
Kemirapport 5. Henning hvp@inano.dk 20031325. 13. december 2004
 Kemirapport 5 Henning hvp@inano.dk 20031325 13. december 2004 Vi får fem ukendte stoffer udleveret, og vi skal identificere hvert af dem ved hjælp af metoderne fra øvelserne 1-4. Vi har en liste med mulige
Kemirapport 5 Henning hvp@inano.dk 20031325 13. december 2004 Vi får fem ukendte stoffer udleveret, og vi skal identificere hvert af dem ved hjælp af metoderne fra øvelserne 1-4. Vi har en liste med mulige
Opgaver til: 5. Mængdeberegninger
 Opgaver til: 5. Mængdeberegninger 1. Beregn molarmassen for følgende forbindelser: a) SO 3 b) N 2 O 3 c) Na 2 CO 3 d) Fe 3 (PO 4 ) 2 e) Cl 2 O 7 f) (N 4 ) 2 CO 3 g) C 3 C 2 O 2. Beregn stofmængden, n,
Opgaver til: 5. Mængdeberegninger 1. Beregn molarmassen for følgende forbindelser: a) SO 3 b) N 2 O 3 c) Na 2 CO 3 d) Fe 3 (PO 4 ) 2 e) Cl 2 O 7 f) (N 4 ) 2 CO 3 g) C 3 C 2 O 2. Beregn stofmængden, n,
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
Der tilsættes 50,0 ml 1,00 M saltsyre. Hvor stor en masse af jern opløses, hvis reaktionen forløber fuldstændigt, og der er overskud af Fe(s)?
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E15 / Opgaver Eksamen Almen Kemi 26171, 15. December 2015 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Jern reagerer med saltsyre
Vejbelægningens indflydelse på stærkt trafikerede gadestrækninger i Danmark
 AARHUS UNIVERSITET Vejbelægningens indflydelse på partikelforureningen (PM1) på stærkt trafikerede gadestrækninger i Danmark Thomas Ellermann, Peter Wåhlin, Claus Nordstrøm og Matthias Ketzel Danmarks
AARHUS UNIVERSITET Vejbelægningens indflydelse på partikelforureningen (PM1) på stærkt trafikerede gadestrækninger i Danmark Thomas Ellermann, Peter Wåhlin, Claus Nordstrøm og Matthias Ketzel Danmarks
Eksamensopgaverne offentliggøres selvfølgelig med det forbehold, at censor kan komme med ændringsforslag.
 VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Syrer, baser og salte
 Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Syrer, baser og salte Navn: Indholdsfortegnelse: Ion begrebet... 2 Ætsning af Mg bånd med forskellige opløsninger... 5 Elektrolyse af forskellige opløsninger... 7 Påvisning af ioner i forskellige opløsninger
Bio- Den lille kemitime. - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt
 Bio- Den lille kemitime - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt Søren Husted, Institut for Plante- og Miljøvidenskab, Det Natur- og Biovidenskablige Fakultet, Københavns Universitet
Bio- Den lille kemitime - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt Søren Husted, Institut for Plante- og Miljøvidenskab, Det Natur- og Biovidenskablige Fakultet, Københavns Universitet
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Diana Christensen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Diana Christensen
Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor
 Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Lokalenhed Midtjylland (MJL). Bilagsoversigt.
 Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Storstrøm (STO). Bilagsoversigt.
 Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Fyn (FYN). Bilagsoversigt.
 Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Sjælland (SJL). Bilagsoversigt.
 Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
%2fAfleveringsportal%2fopgaveaflevering.aspx%3felementId%3d461315
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi E14 / Opgaver Eksamen Almen Kemi 26171 Efterår 2014 Side 1 Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Navngiv HBrO 4 hydrogenbromat perbromsyre
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
Spørgsmål 1 Den kemiske reaktion
 Spørgsmål 1 Den kemiske reaktion Du skal gennemgå eksperimentet Fyrfadslys inddrag gerne dine forsøgsresultater og vurder om de understøtter modellen reaktionskemaet. Du skal endvidere give eksempler på
Spørgsmål 1 Den kemiske reaktion Du skal gennemgå eksperimentet Fyrfadslys inddrag gerne dine forsøgsresultater og vurder om de understøtter modellen reaktionskemaet. Du skal endvidere give eksempler på
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Uorganisk kemi. HF HCl HBr HI Hydrogenchlorid 10/27/2009. Halogener. H F Cl Br I. Forekomst.87%.07% 1.4% 2.5ppm.3ppm
 Halogener 15.09.09 3 1 Noter 7 H F Cl Br I Forekomst.87%.07% 1.% 2.5ppm.3ppm Ionisationsenergi 1312 1681 125 113 1009 /kjmol 1 (cf.) 517(Li) 93(Na) 16(K) 01(Rb) 373(Cs) Elektronaffinitet 72 333 39 325
Halogener 15.09.09 3 1 Noter 7 H F Cl Br I Forekomst.87%.07% 1.% 2.5ppm.3ppm Ionisationsenergi 1312 1681 125 113 1009 /kjmol 1 (cf.) 517(Li) 93(Na) 16(K) 01(Rb) 373(Cs) Elektronaffinitet 72 333 39 325
Opgaver til: 6. Syrer og baser
 Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Opgaver til: 6. Syrer og baser 1. Færdiggør følgende syre-basereaktioner: a) HNO 3 + H 2 O b) H 2 SO 4 + H 2 O c) HNO 3 + NH 3 d) SO 2-3 + H 2O e) PO 3-4 + H 2O f) H 3 PO 4 + H 2 O g) O 2- + H 2 O h) CO
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse for: 1kec16v 0816 ke
 Undervisningsbeskrivelse for: 1kec16v 0816 ke Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års efterår Termin: December 2016 Uddannelse: HF-enkeltfag Lærer(e):
Undervisningsbeskrivelse for: 1kec16v 0816 ke Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års efterår Termin: December 2016 Uddannelse: HF-enkeltfag Lærer(e):
Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk
 Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk Billedkunst 47 1g bi Biologi 10 41 2a BI Biologi 45 95 2c
Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk Billedkunst 47 1g bi Biologi 10 41 2a BI Biologi 45 95 2c
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Rapport over Fældningsreaktioner
 Rapport over Fældningsreaktioner Formål: at undersøge, hvilke salte der dannes ud fra forskellige fældningsreaktioner, og efterfølgende at undersøge hvilke af disse salte, der er tungtopløselige og hvilke,
Rapport over Fældningsreaktioner Formål: at undersøge, hvilke salte der dannes ud fra forskellige fældningsreaktioner, og efterfølgende at undersøge hvilke af disse salte, der er tungtopløselige og hvilke,
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 10/11 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Flemming Madsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 10/11 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Flemming Madsen
1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation
 Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Thy-Mors HF & VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi-C Gunnsteinn Agnar
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Thy-Mors HF & VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi-C Gunnsteinn Agnar
Kemi A. Højere teknisk eksamen
 Kemi A Højere teknisk eksamen htx131-kem/a-31052013 Fredag den 31. maj 2013 kl. 9.00-14.40 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt begrunde løsningerne
Kemi A Højere teknisk eksamen htx131-kem/a-31052013 Fredag den 31. maj 2013 kl. 9.00-14.40 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at løse opgaverne korrekt begrunde løsningerne
1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas
 Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
BASISKEMI C. Facit HELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN HAASE & SØNS FORLAG
 BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
1. Jern og redoxreaktioner Øvelse: Rustbeskyttelse (se bilag)
 1. Jern og redoxreaktioner Øvelse: Rustbeskyttelse (se bilag) Fremstilling af jern i højovn ud fra hæmatit Støbejern, stål og smedejern og legeringer. BOS(basisk oxygen stålfremstilling) Opskriv og afstem
1. Jern og redoxreaktioner Øvelse: Rustbeskyttelse (se bilag) Fremstilling af jern i højovn ud fra hæmatit Støbejern, stål og smedejern og legeringer. BOS(basisk oxygen stålfremstilling) Opskriv og afstem
Eksaminationsgrundlag for selvstuderende
 Eksaminationsgrundlag for selvstuderende Skolens eksaminationsgrundlag: Jeg ønsker at gå til eksamen i nedennævnte eksaminationsgrundlag (pensum), som skolen har lavet. Du skal ikke foretage dig yderligere
Eksaminationsgrundlag for selvstuderende Skolens eksaminationsgrundlag: Jeg ønsker at gå til eksamen i nedennævnte eksaminationsgrundlag (pensum), som skolen har lavet. Du skal ikke foretage dig yderligere
Undervisningsbeskrivelse for: 1kec17s 0816 ke
 Undervisningsbeskrivelse for: 1kec17s 0816 ke Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års forår Termin: Juni 2017 Uddannelse: HF-enkeltfag Lærer(e):
Undervisningsbeskrivelse for: 1kec17s 0816 ke Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års forår Termin: Juni 2017 Uddannelse: HF-enkeltfag Lærer(e):
Test din viden B-forløb
 Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Test din viden B-forløb Har du styr på B forløbets kernestof? Nu har du lært en masse om ionforbindelser, molekylforbindelser, fældningsreaktioner, elektronegativitet, polaritet, opløselighed og mængdeberegninger
Kemiaflevering uge 37
 Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Kemiaflevering uge 37 Kenneth Buchwald Johansen, 1laba0807 Opgave 1: Afstem redoxligningen Cl 2 Cl +ClO 3 : 0 1 5 3( 2) Cl 2 Cl + ClO 3 (basisk væske). Vi kan se at Cl 2 både reduceres og oxideres. Det
Fremstilling af enkeltlag på sølv
 Fremstilling af enkeltlag på sølv Formål I dette eksperiment skal du undersøge, hvordan vand hæfter til en overflade af henholdsvis metallisk sølv, et nanometer tykt enkeltlag af hexadekanthiol og et nanometer
Fremstilling af enkeltlag på sølv Formål I dette eksperiment skal du undersøge, hvordan vand hæfter til en overflade af henholdsvis metallisk sølv, et nanometer tykt enkeltlag af hexadekanthiol og et nanometer
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT
 1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
1. OPVARMNING AF NATRIUMHYDROGENCARBONAT At undersøge hvilken kemisk reaktion, der finder sted ved opvarmning af natriumhydrogencarbonat. Natriumhydrogencarbonat (natron) har formlen NaHCO 3 og er et fast
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2018 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2018 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Spørgsmål 1 Carbonhydrider
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
%2fAfleveringsportal%2fopgaveaflevering.aspx%3felementId%3d476671
 In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi F15 / Opgaver Eksamen F15 Side 1 Navngivning Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Vægtning 1 % Opskriv den kemiske formel for kobber(i)oxid
In English Log ud Peter Fristrup CampusNet / 26171 Almen kemi F15 / Opgaver Eksamen F15 Side 1 Navngivning Vis rigtige svar Skjul rigtige svar Spørgsmål 1 Vægtning 1 % Opskriv den kemiske formel for kobber(i)oxid
