Forord 3. Udgave. Januar 2012 Jørgen Christoffersen
|
|
|
- Lone Carlsen
- 10 år siden
- Visninger:
Transkript
1 Forord 3. Udgave Denne udgave er en lettere revidering af 2. udgave. Afsnittet om radioaktivitet er forbedret ved indsættelse af et appendiks. Jeg takker lektor, dr.phil. Niels Grunnet for hjælp til udarbejdelsen af dette afsnit. Det er mit håb, at bogen vil være til nytte ikke blot for læge- og tandlægestuderende, men også for bl.a. gymnasieelever med kemi på højt niveau, studerende på seminarier, og for forskellige bachelorstuderende med fysik/kemi på højt niveau. Mette Kjær Schou takkes varmt for hjælp med udarbejdelse også af denne udgave. På modtager jeg med tak forslag til forbedringer af bogen. Januar 2012 Jørgen Christoffersen
2 Forord 1. Udgave Denne håndbog er udarbejdet til brug ved undervisningen af tandlæge- og lægestuderende i Medicinsk Kemi ved Københavns Universitet. Bogen bygger i høj grad på bogen Kemiske Data 5. udgave af Arne E. Nielsen, redigeret af Jørgen Christoffersen og Margaret R. Christoffersen. Bogens data stammer fra forskellige tabelværker og er kun i ringe udstrækning konfereret med originallitteraturen. Skal et datum anvendes til noget "vigtigt", fx til patientbehandling eller til en publikation, bør man kontrollere værdien ved hjælp af originallitteraturen. Det er tilstræbt, at internationale betegnelser rekommanderet af International Union of Pure and Applied Chemistry er anvendt, men der kan forekomme afvigelser. I forhold til Kemiske Data 5. udgave er oversigterne og stikordsregistret udvidet såvel inden for almen kemi som organisk kemi. Dette skyldes, at faget Medicinsk Kemi nu fokuserer mere på forståelse end på udenadslære. Oversigterne følger traditioner inden for faget med en mindre afvigelse i afsnittet om ph-beregning. Her er det tilstræbt, at man let kommer til en rimelig vurdering af ph i en given opløsning. Ud fra betragtning af protolysegraden tilnærmes phberegninger til simple formler uden brug af ligninger af højere end 1. grad. Herved begås generelt ikke større fejl end de, der skyldes, at man ikke skelner mellem aktivitet og aktuel koncentration. Det forventes, at bogen også kan anvendes ved undervisningen i dele af de efterfølgende fag i uddannelserne i medicin og odontologi samt ved en del andre uddannelser, der bygger på en basal viden i almen og organisk kemi. Bogen kan med fordel anvendes sammen med netudgivelsen, "Basal almen kemi for biologer", Vi står i taknemlighedsgæld til afdøde professor, dr.phil. Arne E. Nielsen for inspiration og godt samarbejde gennem mange år. Vi takker Mette Kjær Schou for uvurderlig hjælp med renskrivning af bogen. Endvidere takker vi Erland Demant og Jørgen W. Ulrich for deres væsentlige bidrag til oversigterne i organisk kemi og Per Hellung Larsen for tilladelse til at inkludere Human metabolismeoversigten. Endelig takker vi lærere og studenter, der har medvirket og deltaget i undervisningen i Medicinsk Kemi, for rettelser og forslag til forbedringer af bogen. Det kan næppe undgås, at der er skrive- og andre fejl. Vi modtager gerne skriftlige informationer om fejl og mangler ved bogen. December 2002 Jørgen Christoffersen Margaret R. Christoffersen
3 5 Indhold Tabel eller afsnit side Fundamentale data 1 Atomvægte 7 2 Grundstoffernes periodiske system og atomernes elektronkonfiguration 8 3 Fundamentale konstanter 10 Luft og vand 4 Sammensætningen af atmosfærisk luft 11 5 Vand og is 11 6 Vand og damp, afhængighed af temperaturen 12 Energetik 7 Termodynamiske data, standardværdier, smelte- og kogepunkt, opløselighed 13 8 Bindingsenthalpi 31 9 Atomiseringsenthalpi Stofskifteenthalpi Saltes opløselighed i vand Gassers opløselighed i vand Opløselighedsprodukter Kompleksitetskonstanter og ionparkonstanter Kolligative egenskaber 36 Protolyse 16 Oversigt over protolytter Eksempler på ph-værdier Syrekonstanter Syrekonstanter for aminosyrer Konstitutionsformler for 20 humane α-aminosyrer Autoprotolysekonstanter Vands ionprodukt Buffere Phosphat og Tris buffere, ph og bufferkapacitet ved 25 C Indikatorer 56 Elektrokemi 26 Nernstfaktoren Referenceelektroder Standardpotentialer Ledningsevne i vandige opløsninger Overføringstal 62
4 6 Molekylære data 31 Elektronegativitet Covalente og van der Waals-radier Afstande og vinkler i molekyler Atom- og ionradier 65 Organisk kemi, oversigter 35 Organiske grupper, deres prioritering og betegnelser Isomeri blandt enkle carbonforbindelser Organiske ringsystemer Syrestyrke og induktiv effekt Nukleofile og elektrofile reagenser Opløselighed af lavmolekylære organiske stoffer Eksempler på grundtyper af organiske forbindelser Nogle radikalbetegnelser samt vigtige trivialnavne Vigtige organisk kemiske reaktionstyper Udvalgte additions-/kondensationsreaktioner Carbohydrater Lipider Nucleinsyrer 94 Almen kemi, oversigter 48 Energetik Aktiviteter og aktivitetskoefficienter Biokemisk enthalpi og gibbsenergi Gasser Kolligative egenskaber Syrer og baser Elektrokemi Reaktionskinetik Enzymkinetik Lysabsorption og radioaktivitet 125 Diverse 58 Fysiske og kemiske symboler Enheder og omregningsfaktorer Regneregler Matematiske symboler Matematiske konstanter Store tals benævnelse Metriske forstavelser Det kemiske talsystem Det græske alfabet 142 Appendiks 143 Stikordsregister 146 Human metabolisme bagest
5 7 Tabel 1. Atomvægte (relative atommasser), IUPAC 2001 Symbol Num- Navn Atomvægt Sym- Num- Navn Atomvægt mer bol mer Ac 89 Actinium [227] Mt 109 Meitnerium [268] Ag 47 Sølv (argentum) 107,868 N 7 Nitrogen/kvælstof 14,007 Al 13 Aluminium 26,982 Na 11 Natrium 22,990 Am 95 Americium [243] Nb 41 Niobium 92,906 Ar 18 Argon 39,948 Nd 60 Neodym 144,24 As 33 Arsen 74,922 Ne 10 Neon 20,180 At 85 Astat [210] Ni 28 Nikkel 58,69 Au 79 Guld (aurum) 196,967 No 102 Nobelium [259] B 5 Bor 10,811 Np 93 Neptunium [237] Ba 56 Barium 137,327 O 8 Oxygen/ilt 15,999 Be 4 Beryllium 9,012 Os 76 Osmium 190,2 Bh 107 Bohrium [264] P 15 Phosphor/fosfor 30,974 Bi 83 Bismuth 208,980 Pa 91 Protactinium 231,036 Bk 97 Berkelium [247] Pb 82 Bly (plumbum) 207,2 Br 35 Brom 79,904 Pd 46 Palladium 106,42 C 6 Carbon/kulstof 12,011 Pm 61 Promethium [145] Ca 20 Calcium 40,078 Po 84 Polonium [209] Cd 48 Cadmium 112,411 Pr 59 Praseodym 140,908 Ce 58 Cerium 140,116 Pt 78 Platin 195,08 Cf 98 Californium [251] Pu 94 Plutonium [244] Cl 17 Chlor 35,453 Ra 88 Radium [226] Cm 96 Curium [247] Rb 37 Rubidium 85,468 Co 27 Cobalt 58,933 Re 75 Rhenium 186,207 Cr 24 Chrom 51,996 Rf 104 Rutherfordium [261] Cs 55 Caesium 132,905 Rh 45 Rhodium 102,906 Cu 29 Kobber (cuprum) 63,546 Rn 86 Radon [222] Db 105 Dubnium [262] Ru 44 Ruthenium 101,07 Dy 66 Dysprosium 162,50 S 16 Svovl (sulfur) 32,065 Er 68 Erbium 167,26 Sb 51 Antimon (stibium) 121,76 Es 99 Einsteinium [252] Sc 21 Scandium 44,956 Eu 63 Europium 151,964 Se 34 Selen 78,96 F 9 Fluor 18,998 Sg 106 Seaborgium [266] Fe 26 Jern (ferrum) 55,845 Si 14 Silicium 28,086 Fm 100 Fermium [257] Sm 62 Samarium 150,36 Fr 87 Francium [223] Sn 50 Tin (stannum) 118,710 Ga 31 Gallium 69,723 Sr 38 Strontium 87,62 Gd 64 Gadolinium 157,25 Ta 73 Tantal 180,948 Ge 32 Germanium 72,64 Tb 65 Terbium 158,925 H 1 Hydrogen/brint 1,008 Tc 43 Technetium [98] He 2 Helium 4,003 Te 52 Tellur 127,60 Hf 72 Hafnium 178,49 Th 90 Thorium 232,038 Hg 80 Kviksølv (hydrargyrum, Ti 22 Titan 47,87 mercurium) 200,59 Tl 81 Thallium 204,383 Ho 67 Holmium 164,930 Tm 69 Thulium 168,934 Hs 108 Hassium [277] Uub 112 Ununbium [285] I 53 Iod 126,904 Uuh 116 Ununhexium In 49 Indium 114,82 Uun 110 Ununnilium [281] Ir 77 Iridium 192,22 Uuo 118 Ununoctium K 19 Kalium 39,098 Uuq 114 Ununquadium [289] Kr 36 Krypton 83,80 Uuu 111 Unununium [272] La 57 Lanthan 138,906 U 92 Uran 238,029 Li 3 Lithium 6,941 V 23 Vanadium 50,942 Lr 103 Lawrencium [262] W 74 Wolfram (eng. tungsten) 183,84 Lu 71 Lutetium 174,967 Xe 54 Xenon 131,29 Md 101 Mendelevium [258] Y 39 Yttrium 88,906 Mg 12 Magnesium 24,305 Yb 70 Ytterbium 173,04 Mn 25 Mangan 54,938 Zn 30 Zink 65,41 Mo 42 Molybden 95,94 Zr 40 Zirconium 91,224 [ ] Massetal, mest stabile isotop. Geologisk variation: 6,939-6,996. / Ældre dansk navn eller stavemåde. ( ) Latin.
6 8 Tabel 2. Grundstoffernes periodiske system med atomernes elektronkonfigurationer i gasfase G g I II IIIa IVa Va VIa VIIa VIIIa 1H P 1 1s 1 Ikke-metaller 2 3Li (He)2s 1 4Be (He)2s 2 Metaller 3 11Na (Ne)3s 1 12Mg (Ne)3s K (Ar)4s 1 20Ca (Ar)4s 2 21Sc (Ar)4s 2 3d 1 22Ti (Ar)4s 2 3d 2 23V (Ar)4s 2 3d 3 24Cr (Ar)4s 1 3d 5 25Mn (Ar)4s 2 3d 5 26Fe (Ar)4s 2 3d 6 27Co (Ar)4s 2 3d Rb (Kr)5s 1 38Sr (Kr)5s 2 39Y (Kr)5s 2 4d 1 40Zr (Kr)5s 2 4d 2 41Nb (Kr)5s 1 4d 4 42Mo (Kr)5s 1 4d 5 43Tc (Kr)5s 2 4d 5 44Ru (Kr)5s 1 4d 7 45Rh (Kr)5s 1 4d Cs (Xe)6s 1 87Fr (Rn)7s 1 56Ba (Xe)6s 2 88Ra (Rn)7s 2 Alkalimetaller Jordalkalimetaller 57La (Xe)6s 2 5d 1 89Ac (Rn)7s 2 72Hf 73Ta 75Re 76Os 77Ir 74W 5d 2 5d 3 5d 4 5d 5 5d 6 5d 7 104Rf 105Db 106Sg 107Bh 108Hs 109Mt (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 6d 2 6d 3 6d 4 6d 5 6d 6 6d 7 Overgangsmetaller 6 7 Lanthanider Actinider 58Ce (Xe)6s 2 4f 2 90Th (Rn)7s 2 6d 2 59Pr (Xe)6s 2 4f 3 91Pa (Rn)7s 2 5f 2 60Nd (Xe)6s 2 4f 4 92U (Rn)7s 2 5f 3 61Pm (Xe)6s 2 4f 5 93Np (Rn)7s 2 5f 4 62Sm (Xe)6s 2 4f 6 94Pu (Rn)7s 2 5f 6 63Eu (Xe)6s 2 4f 7 95Am (Rn)7s 2 5f 7 64Gd (Xe)6s 2 4f 7 5d 1 96Cm (Rn)7s 2 5f 7 Sjældne jordarters metaller G = Nye gruppenumre g = Gamle gruppenumre (også fx 1a, 2a, 3b, 4b, 8b, 1b, 2b, 3a, 8a har været brugt) P = Periodenumre (He) = 1s 2 (Ne) = (He)2s 2 2p 6 = 1s 2 2s 2 2p 6, osv.
7 Ia IIa III IV V VI VII VIII 2He 1s 2 5B (He)2s 2 2p 1 6C (He)2s 2 2p 2 7N (He)2s 2 2p 3 8O (He)2s 2 2p 4 9F (He)2s 2 2p 5 10Ne (He)2s 2 2p 6 13Al (Ne)3s 2 3p 1 14Si (Ne)3s 2 3p 2 15P (Ne)3s 2 3p 3 16S (Ne)3s 2 3p 4 17Cl (Ne)3s 2 3p 5 18Ar (Ne)3s 2 3p 6 28Ni (Ar)4s 2 3d 8 46Pd (Kr)4d 10 78Pt (Xe)6s 1 4f 14 5d 9 29Cu (Ar)4s 1 3d 10 47Ag (Kr)5s 1 4d 10 79Au (Xe)6s 1 4f 14 5d 10 30Zn 48Cd 80Hg 5d 10 31Ga 4p 1 49In 5p 1 81Tl 5d 10 6p 1 32Ge 4p 2 50Sn 5p 2 82Pb 5d 10 6p 2 33As 4p 3 51Sb 5p 3 83Bi 5d 10 6p 3 34Se 4p 4 52Te 5p 4 84Po 5d 10 6p 4 35Br 4p 5 53I 5p 5 85At 5d 10 6p 5 (Møntmetaller) Zinkgruppen Borgruppen Carbongruppen Kvælstofgruppen Chalkogener (Svovl/ Halogener iltgruppen) 36Kr 4p 6 54Xe 5p 6 86Rn 5d 10 6p 6 Ædelgasser Tb (Xe)6s 2 4f 9 97Bk (Rn)7s 2 5f 9 66Dy (Xe)6s 2 4f 10 98Cf (Rn)7s 2 5f 10 67Ho (Xe)6s 2 4f 11 99Es (Rn)7s 2 5f 11 68Er (Xe)6s 2 4f 12 69Tm (Xe)6s 2 4f 13 70Yb 71Lu 5d 1 100Fm 101Md 102No 103Lr (Rn)7s 2 5f 12 (Rn)7s 2 5f 13 (Rn)7s 2 5f 14 (Rn)7s 2 5f 14 "Sidste-elektron-blokke": Gruppe 3: jordartsmetaller; gruppe 4-7: syredannende metaller; Fe, Co, Ni: jernmetaller; Ru, Rh, Pd, Os, Ir, Pt: platinmetaller
8 10 Tabel 3. Fundamentale konstanter Standard tyngdeacceleration g n 9,80665 m s 2 = 9,80665 N kg 1 Normal atmosfæretryk atm Pa Vands tripelpunkt T trp 273,16 K Celsiusskalaens nulpunkt (0 C) T 0 273,15 K "Standardtemperaturen" (25 C) T ,15 K Normalrumfanget (1 atm, 0 C) V 0 22,414 L mol 1 Standardrumfanget (100 kpa, 25 C) V 25 24,790 L mol 1 Avogadrokonstanten N A = L 6, mol 1 Boltzmannkonstanten k 1, J K 1 Planckkonstanten h 6, J s Faradaykonstanten F 96485,3 C mol 1 Elementarladningen F/L = e 1, C Lyshastigheden i vakuum c 2, m s 1 Permittiviteten i vakuum ε 0 8, C V 1 m 1 Atommasseenheden 1 u = 1 Da = m u 1, kg Protonmassen m p 1, kg Elektronmassen m e 9, kg Gaskonstanten R 8,31451 J K 1 mol 1 RT 25 = 2478,97 J mol 1 = 24,4655 L atm mol 1 kt 25 = 4, J = 8,31451 L kpa K 1 mol 1 = 0, L bar K 1 mol 1 = 0, L atm K 1 mol 1
Opgaver i atomer. c) Aflæs atommassen for Mg i det periodiske system eller på de udskrevne ark, og skriv det ned.
 Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
DET PERIODISKE SYSTEM
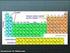 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Kemisk Reaktionslære ELO HARALD HANSEN. Polyteknisk Forlag. 2.udgave
 Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
Naturfag. Supplerende materiale. 5. udgave
 Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Sporgrundstof definition:
 Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Røntgenstråling. Baggrund. Atomers struktur og Røntgenstråling
 Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
Vikar-Guide. Den elektriske ladning af en elektron er -1 elementarladning, og den elektriske ladning af protonen er +1 elementarladning.
 Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold
 Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 UORGANISK KEMI Torsdag den 22. maj 2014
 Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Forelæsning 8. Stabile isotoper. Iltisotoper anvendt i paleoklimastudier, magmadannelse, termometri, vand-bjergart reaktion.
 Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Geokemisk differentiation af Jorden oversigt
 Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Den kosmiske kalender
 Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 UORGANISK KEMI Tirsdag den 18. december 2012
 Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Platin komplekser i kampen mod kræft. Koordinationskemi i aktion. cis-ptcl 2 (NH 3 ) 2. Essentiel, nyttig eller toxisk. Hvad der faktisk skete
 Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Dagens program TIL GAVN FOR GARTNERE
 Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering
 Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor
 Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Sølvsmedeteknik. Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie.
 Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Nr. 6-2007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 2008
 Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Skriftlig prøve i kursus 26173/E14 Side 1 af 16 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 16 pgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for, Al, e 3+ og Br. : [He]2s 2 2p 4 Al: [Ne]3s 2 3p 1 e 3+ : [Ar]3d 5 Br : [Kr] 1.2 Molekylorbitalteori.
Skriftlig prøve i kursus 26173/E14 Side 1 af 16 pgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for, Al, e 3+ og Br. : [He]2s 2 2p 4 Al: [Ne]3s 2 3p 1 e 3+ : [Ar]3d 5 Br : [Kr] 1.2 Molekylorbitalteori.
Gruppe 2 Læsestof : Kap. 11.
 ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Opgave: Du skal udfylde de manglende felter ud fra den information der er givet
 pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Bio- Den lille kemitime. - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt
 Bio- Den lille kemitime - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt Søren Husted, Institut for Plante- og Miljøvidenskab, Det Natur- og Biovidenskablige Fakultet, Københavns Universitet
Bio- Den lille kemitime - Hvordan optages næringsstofferne i busk-, sten- og kernefrugt Søren Husted, Institut for Plante- og Miljøvidenskab, Det Natur- og Biovidenskablige Fakultet, Københavns Universitet
Opgaver til: 9. Radioaktivitet
 Opgaver til: 9. Radioaktivitet 1. Opskriv henfaldskemaet for α-henfaldet af: 229 90 Th 92 U 86 Rn 2. Opskriv henfaldskemaet for β - -henfaldet af: 209 82 Pb 10 4 Be 79 Au 3. Opskriv henfaldskemaet for
Opgaver til: 9. Radioaktivitet 1. Opskriv henfaldskemaet for α-henfaldet af: 229 90 Th 92 U 86 Rn 2. Opskriv henfaldskemaet for β - -henfaldet af: 209 82 Pb 10 4 Be 79 Au 3. Opskriv henfaldskemaet for
OPGAVER OM DANNELSE AF IONER. OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal.
 OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
Liste over affald, der er omfattet af de generelle oplysningskrav i artikel 18 -Bilag III (»Grøn«liste) (1)
 Side 1 af 14 Liste over affald, der er omfattet af de generelle oplysningskrav i artikel 18 -Bilag III (»Grøn«liste) (1) Uanset om affald står på denne liste eller ej, må det ikke underlægges de generelle
Side 1 af 14 Liste over affald, der er omfattet af de generelle oplysningskrav i artikel 18 -Bilag III (»Grøn«liste) (1) Uanset om affald står på denne liste eller ej, må det ikke underlægges de generelle
Danmarks Tekniske Universitet
 Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Danmarks Tekniske Universitet Skriftlig prøve, tirsdag den 17. december 2013 Side 1 af 17 sider Kursus navn: Uorganisk Kemi Kursus nr. 26173 Varighed: Hjælpemidler: 4 timer pgave 1, 2, 3, 4 og 5: Ingen
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund.
 Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Del 2 Klassificering ADR 2005
 2.2.7 Klasse 7 - Radioaktive stoffer 2.2.7.1 Definition af klasse 7 2.2.7.1.1 Radioaktive stoffer er stoffer, som indeholder radionuklider, for hvilke såvel aktivitetskoncentrationen som den samlede aktivitet
2.2.7 Klasse 7 - Radioaktive stoffer 2.2.7.1 Definition af klasse 7 2.2.7.1.1 Radioaktive stoffer er stoffer, som indeholder radionuklider, for hvilke såvel aktivitetskoncentrationen som den samlede aktivitet
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Kortlægning af kemiske stoffer i kohl- og hennaprodukter
 Kortlægning af kemiske stoffer i kohl- og hennaprodukter Nils Bernth, Ole Christian Hansen, Steen Færgemann Hansen og Eva Pedersen Teknologisk Institut Kortlægning af kemiske stoffer i forbrugerprodukter,
Kortlægning af kemiske stoffer i kohl- og hennaprodukter Nils Bernth, Ole Christian Hansen, Steen Færgemann Hansen og Eva Pedersen Teknologisk Institut Kortlægning af kemiske stoffer i forbrugerprodukter,
Del 2 Klassificering ADR et ikke-dispersibelt fast radioaktivt stof, eller. en lukket kapsel, der indeholder radioaktive stoffer.
 Radioaktivt stof i speciel form: Enten: (a) (b) et ikke-dispersibelt fast radioaktivt stof, eller en lukket kapsel, der indeholder radioaktive stoffer. 2.2.7.2 Klassificering Specifik aktivitet af et radionuklid:
Radioaktivt stof i speciel form: Enten: (a) (b) et ikke-dispersibelt fast radioaktivt stof, eller en lukket kapsel, der indeholder radioaktive stoffer. 2.2.7.2 Klassificering Specifik aktivitet af et radionuklid:
Slibning af værktøjer til træindustrien
 Slibning af værktøjer til træindustrien Stållegeringer Stållegeringer, der anvendes i træindustrien: VS = værktøjsstål CV = krom-vanadiumstål HSS = hurtigstål HSSE = højlegeret hurtigstål HM = hårdmetal
Slibning af værktøjer til træindustrien Stållegeringer Stållegeringer, der anvendes i træindustrien: VS = værktøjsstål CV = krom-vanadiumstål HSS = hurtigstål HSSE = højlegeret hurtigstål HM = hårdmetal
1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas
 Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Atomets bestanddele. Indledning. Atomer. Atomets bestanddele
 Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Analyserapport. Prøvemærke: Lab prøvenr: Prøve ID: Min. Max.
 Udtagningsadresse: Raffinaderivej 2 Prøveudtagning: kl. 11:50 Analyseperiode: - 14.03.2013 AR-13-CA-00053773-01 EUDKVE-00053773 05377301 Enhed Kravværdier Prøve ID: 001999-30 Min. Max. Prøvens farve Farveløs
Udtagningsadresse: Raffinaderivej 2 Prøveudtagning: kl. 11:50 Analyseperiode: - 14.03.2013 AR-13-CA-00053773-01 EUDKVE-00053773 05377301 Enhed Kravværdier Prøve ID: 001999-30 Min. Max. Prøvens farve Farveløs
Lim mellem atomerne Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
m: masse i masseprocent : indhold i volumenprocent : indhold
 Kemisk formelsamling (C-niveau s kernestof samt en del formler, der hører hjemme på Kemi B ) Mængdeberegninger m: masse M: molar masse n : stofmængde : volumen ρ : densitet (massetæthed) c : koncentration
Kemisk formelsamling (C-niveau s kernestof samt en del formler, der hører hjemme på Kemi B ) Mængdeberegninger m: masse M: molar masse n : stofmængde : volumen ρ : densitet (massetæthed) c : koncentration
Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk
 Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk Billedkunst 47 1g bi Biologi 10 41 2a BI Biologi 45 95 2c
Holdelementnavn XPRS fagbetegnelse (kort) Norm. elevtid (skoleår) Lektioner (antal) 1g ap Almen sprogfors 0 28 totalt 3g as Astronomi 44 1g bk Billedkunst 47 1g bi Biologi 10 41 2a BI Biologi 45 95 2c
Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes?
 Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes? Af Carsten Jensen, FORCE Technology, Afdelingen for Korrosion & Metallurgi Risø-DTU, Roskilde, 24.
Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes? Af Carsten Jensen, FORCE Technology, Afdelingen for Korrosion & Metallurgi Risø-DTU, Roskilde, 24.
Fysikforløb nr. 6. Atomfysik
 Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fremtidens flyveaske - fra samfyring af kul og biomasse/affald
 Fremtidens flyveaske - fra samfyring af kul og biomasse/affald VELKOMMEN TIL TEKNOLOGISK INSTITUT Hvorfor samfyring? Hvad er samfyringsaske og hvilke asker er testet? Kan man anvende samfyringsaske på
Fremtidens flyveaske - fra samfyring af kul og biomasse/affald VELKOMMEN TIL TEKNOLOGISK INSTITUT Hvorfor samfyring? Hvad er samfyringsaske og hvilke asker er testet? Kan man anvende samfyringsaske på
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Metallernes atomare struktur og tilstandsformer
 Metallernes atomare struktur og tilstandsformer Metallernes struktur, opbygning og tilstandsformer For at få en forståelse af metallernes særlige måde at opføre sig på i forhold til andre materialer, er
Metallernes atomare struktur og tilstandsformer Metallernes struktur, opbygning og tilstandsformer For at få en forståelse af metallernes særlige måde at opføre sig på i forhold til andre materialer, er
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
HVAD ER RADIOAKTIV STRÅLING
 16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
Notat vedrørende resultat af undersøgelse af drikkevands- eller boringskontrol.
 Forsyning Ballerup Tlf. 4483 6000 [email protected] www.forsyningballerup.dk Notat vedrørende resultat af undersøgelse af drikkevands- eller boringskontrol. Forsyning Ballerup har bemærkninger
Forsyning Ballerup Tlf. 4483 6000 [email protected] www.forsyningballerup.dk Notat vedrørende resultat af undersøgelse af drikkevands- eller boringskontrol. Forsyning Ballerup har bemærkninger
Råstofferens kritikalitet og dynamik Arktiske udfordringer. Karen Hanghøj, Statsgeolog Afdeling for Petrologi og Malmgeologi
 Råstofferens kritikalitet og dynamik Arktiske udfordringer Karen Hanghøj, Statsgeolog Afdeling for Petrologi og Malmgeologi De Nationale Geologiske Undersøgelser for Danmark og Grønland Vand Energi Mineraler
Råstofferens kritikalitet og dynamik Arktiske udfordringer Karen Hanghøj, Statsgeolog Afdeling for Petrologi og Malmgeologi De Nationale Geologiske Undersøgelser for Danmark og Grønland Vand Energi Mineraler
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014
 Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Kortlægning af ressourcepotentialet i WEEE 4.juni 2014
 Kortlægning af ressourcepotentialet i WEEE 4.juni 2014 B.Malmgren-Hansen Formål: Screening af produkttyper hvor danske virksomheder har størst potentiale for udvikling/overførsel af teknologi til genanvendelse
Kortlægning af ressourcepotentialet i WEEE 4.juni 2014 B.Malmgren-Hansen Formål: Screening af produkttyper hvor danske virksomheder har størst potentiale for udvikling/overførsel af teknologi til genanvendelse
PSO 3141 Kortlægning af emissioner fra decentrale kraftvarmeværker Anlæg A4 April 2002
 PSO 3141 Kortlægning af emissioner fra decentrale kraftvarmeværker Anlæg A4 April 2002 Gladsaxe Møllevej 15, 2860 Søborg Tlf.: 39 555 999 Fax: 39 696 002 23-01-2003 Projektnr.: Udarbejdet af: 18.254/A4
PSO 3141 Kortlægning af emissioner fra decentrale kraftvarmeværker Anlæg A4 April 2002 Gladsaxe Møllevej 15, 2860 Søborg Tlf.: 39 555 999 Fax: 39 696 002 23-01-2003 Projektnr.: Udarbejdet af: 18.254/A4
Side 1 Færøsk-Kapitel 72-141863 30/9/08
 Kapitel 72 JERN OG STÅL Bestemmelser 1. I dette kapitel og for så vidt angår nedenstående punkt d, e og f overalt i nomenklaturen forstås ved nedenstående betegnelser følgende: a»råjern«legeringer af jern
Kapitel 72 JERN OG STÅL Bestemmelser 1. I dette kapitel og for så vidt angår nedenstående punkt d, e og f overalt i nomenklaturen forstås ved nedenstående betegnelser følgende: a»råjern«legeringer af jern
DONG ENERGY POWER A/S. Grønt regnskab for 2010
 DONG ENERGY POWER A/S Grønt regnskab for 2010 Dokument oprettet d. 01 06 2011. Side 1 / 7 Dette grønne regnskab er udarbejdet efter bekendtgørelse om visse virksomheders afgivelse af miljøoplysninger,
DONG ENERGY POWER A/S Grønt regnskab for 2010 Dokument oprettet d. 01 06 2011. Side 1 / 7 Dette grønne regnskab er udarbejdet efter bekendtgørelse om visse virksomheders afgivelse af miljøoplysninger,
Gødningslære A. Faglærer Karin Juul Hesselsøe
 Faglærer Karin Juul Hesselsøe Gødningslære er enkelt Gødningslære er enkelt For lidt Gødningslære er enkelt Alt for meget Det kan være svært at finde balancen Planter består mest af sukkerstoffer Kulhydrater
Faglærer Karin Juul Hesselsøe Gødningslære er enkelt Gødningslære er enkelt For lidt Gødningslære er enkelt Alt for meget Det kan være svært at finde balancen Planter består mest af sukkerstoffer Kulhydrater
HISTORIEN OM GRUNDSTOFFERNE. Illustrationer og tekst af Lars Kristensen
 HISTORIEN OM GRUNDSTOFFERNE Illustrationer og tekst af Lars Kristensen 1 H Hydrogen Englænderen Henry Cavendish betegnes som opdageren af hydrogen i 1766. Franskmanden Jacques Charles fremstillede den
HISTORIEN OM GRUNDSTOFFERNE Illustrationer og tekst af Lars Kristensen 1 H Hydrogen Englænderen Henry Cavendish betegnes som opdageren af hydrogen i 1766. Franskmanden Jacques Charles fremstillede den
 D Referat af ekstraordinær generalforsamling i Å T O F T E N S G RU N D E J E RF O RE N I N G tirsdag den 23. marts 2004 kl. 19.30 i fælleshuset a g s o r d e n 1. V a l g a f d i r i g e n t 2. K ø b
D Referat af ekstraordinær generalforsamling i Å T O F T E N S G RU N D E J E RF O RE N I N G tirsdag den 23. marts 2004 kl. 19.30 i fælleshuset a g s o r d e n 1. V a l g a f d i r i g e n t 2. K ø b
Gødningslære B. Find hjemmesiden: Vælg student login øverst til højre. Skriv koden: WXMITP5PS. og derefter dit navn
 En lille quiz.for de nye og de gamle Find hjemmesiden: www.socrative.com Vælg student login øverst til højre Skriv koden: WXMITP5PS og derefter dit navn Gødningstyper: Grundgødning Højt indhold af et eller
En lille quiz.for de nye og de gamle Find hjemmesiden: www.socrative.com Vælg student login øverst til højre Skriv koden: WXMITP5PS og derefter dit navn Gødningstyper: Grundgødning Højt indhold af et eller
