Naturfag. Supplerende materiale. 5. udgave
|
|
|
- Arnold Nøhr
- 10 år siden
- Visninger:
Transkript
1 Naturfag Supplerende materiale 5. udgave
2 Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke ses, hverken med det blotte øje eller med mikroskop. Disse partikler hedder atomer. Opbygningen af et atom ligner opbygningen af vores solsystem, hvor solen befinder sig i midten, og planeterne kredser rundt om. Alle atomer består af tre forskellige dele: Protoner. Neutroner (gælder ikke for hydrogenatomet). Elektroner. Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. Midten af atomet hedder kernen. Her befinder protonerne og neutronerne sig. Elektronerne kredser i baner rundt om kernen. Vores solsystem. Kun to af planetbanerne er vist. Der findes ca. 0 forskellige atomer. Det er antallet af protoner, der bestemmer, hvilket atom det er. Kernen og elektronerne bliver holdt sammen af elektriske kræfter. Protonerne er positivt ladede, og elektronerne er negativt ladede. En proton har en positiv ladning, en positiv elementarladning: +. En elektron har en negativ ladning, en negativ elementarladning:. 7
3 Naturfag I et atom er der lige mange protoner og elektroner. Derfor er et atom elektrisk neutralt. Det har lige mange positive og negative ladninger. Neutronen har ingen ladning. Den er neutral. Et atom fra helium med kerne og elektroner. Et atom er en utrolig lille partikel. Massen af atomets dele er tilsvarende meget lille. En proton vejer cirka 0, gram. Det er alt for besværligt at skrive tal med så mange decimaler, derfor har man indført enheden: unit. unit er lig med / af massen af et kulstof atom. Det svarer cirka til 0, gram. I daglig tale siger man, at massen af en proton er unit, og at en neutron har samme masse som en proton. Massen af en elektron er cirka 0,00055 unit. Elektronerne kredser i bestemte baner rundt om kernen. Disse baner kaldes for skaller. Hvor mange skaller, et atom har, afhænger af, hvilket atom det er. Skallen nærmest kernen hedder K-skallen. Her kan der højst være to elektroner. I helium er K-skallen helt udfyldt med elektroner. Nummer to hedder L-skallen. Her kan der højst være otte elektroner. I grundstoffet Neon er både K- og L-skallen helt udfyldt. Neon anvendets bl.a. til lysskilte. 3
4 Uorganisk kemi Den tredje i rækken hedder M-skallen. Her kan der maksimalt være elektroner - men der findes også N-, O-, P- og Q-skaller - i alt syv. Der kan maksimalt være otte elektroner i yderste skal. Dette gælder dog ikke for hydrogen-atomet og helium-atomet. De har kun en k- skal. På figuren kan man se, hvor mange elektroner der højst kan være i skallerne (K-L-M-N- og den yderste skal, i dette tilfælde O). Model af elektronfordeling i skaller. Eksempler:. Helium-atomet har kun én skal, K. Her befinder sig elektroner. Helium-atomet. Kulstof-atomet. Antallet af elektroner, der højst kan være i skallerne, kan også beregnes med formlen: n. n er lig skallens nummer: K =, L =, M = 3, N = Kulstof-atomet har to skaller, K og L. I K-skallen er der to, og i L-skallen er der fire elektroner. Eksempler: K-skal = = M-skal 3 = = 4
5 Naturfag Grundstoffer Når et stof kun består af samme slags atomer, hedder det et grundstof. Eksempler på grundstoffer er guld, sølv og diamant. Calcium findes i tænderne, og hvis man skal passe på dem, skal man anvende tandpasta med fluor! Alfabetisk oversigt over grundstoffer Navn Kemisk symbol Atomnr. Atomvægt i unit Aluminium Al 3 7 Argon Ar 40 Beryllium Be 4 Bor B 5 Brom Br 35 0 Calcium Ca 0 40 Klor Cl 7 35,5 Fluor F Hydrogen H Helium He 4 Kalium K 3 Krypton Kr 36 Lithium Li 3 7 Magnesium Mg 4 Mangan Mn 5 55 Nitrogen N 7 4 Neon Ne 0 0 Fosfor P 5 3 Oxygen O 6 Selen Se 34 7 Silicium Si 4 Svovl S 6 Udsnit af grundstoftabel fra side 4-5 med atomvægten afrundet. Det periodiske system De 0 forskellige grundstoffer er ordnet i et skema, der kaldes det periodiske system. Heri er hvert grundstof opført efter sit atomnummer, der er lig med stoffets antal af protoner. I skemaet kan man slå op, hvor mange protoner, neutroner, elektroner og skaller et atom har, og hvor meget det vejer. Betegnelsen for et grundstof er altid et stort bogstav, evt. efterfulgt af et eller to små bogstaver. 0 Eksempler. Hydrogen: H. Oxygen: O 3. Natrium: Na 4. Klor: Cl 5. Unnilhexium: Unh 5
6 VIII Grundstoffernes periodesystem He Helium 4,006 H Brint (Hydrogen) 7 VII,007, 3 Li Lithium 6,4,0 Na Natrium,0 0, 4 Be Beryllium II,0,6 Mg Magnesium 4,305,3 3 IIIa 4 IVa VIIIa VIIIa 7 VIIa 6 VIa 5 Va K Kalium 0 Ca Calcium Sc Scandium Ti Titanium 6 VI 7 Co Cobalt 6 Fe Jern (Ferrum) 5 Mn Mangan 4 Cr Chrom 3 V Vanadium 3,0 0, 40,07,0 44,56 5 V,4 47,67 0,5 4 IV 5,33 55,45 54,3 5,6 50,4 5, 4, 3,6 3,7,6 37 Rb Rubidium 3 Sr Strontium 3 Y Yttrium 40 Zr Zirkonium 45 Rh Rhodium 44 Ru Ruthenium 43 Tc* Technetium 4 Mo Molybdæn 4 Nb Niobium 5,46 0, 7,6,0 3 III,06, 0 Ne Neon,4,3 0 0, 0,07,06 5,4,07,3 6, 5, 3, 3,6 55 Cs Cæsium 56 Ba Barium Hf Hafnium 77 Ir Iridium 76 Os Osmium 75 Re Rhenium 74 W Wolfram 73 Ta Tantal, 0, 37,33 F Fluor 0, Lanthaniderne 7,4,3 0 O Ilt (Oxygen), 0,3 6, 3,4 0,5, 4, 4, 3,4,5 7 Fr* Francium Ra* Radium Rf* Rutherfordium 0 Mt* Meitnerium 0 Hs* Hassium 07 Bh* Bohrium 06 Sg* Seaborgium 05 Db* Dubnium 3 0,7 6,03 0, 7 N Kvælstof (Nitrogen) Actiniderne (6) 0 6 C Kulstof (Carbon) 5 B Bor Kemisk symbol Grundstofnavn dansk (latin) Molarmasse Elektronegativitet 47 Ag Sølv (Argentum) 3 (65) (6) (66) (6) La Lanthan Atomnummer 5 Ce Cerium 63 Eu Europium 6 Sm Samarium 6 Pm* Promethium fast 60 Nd Neodym 5 Pr Praseodym 3,, 40,, 07,7 0,0, 5,6 50,36 46, 44,4 40,, 5, 4, 3,, Ac* Actinium 0 Th Thorium 5, 5 Am* Americium 4 Pu* Plutonium 3 Np* Neptunium U* Uran Pa* Protactinium væske 7,,04 4,007,3 0,007 0, ,0 3,5 3,0,5,0 Ar Argon 7 Cl Chlor 6 S Svovl (Sulphur) 5 P Phosphor 4 Si Silicium 3 Al Aluminium 3,4 35,453,066 30,74,06 6, 7 3, 6,6 5, 4, 3,6 IIa Ia 0 VIIIa 36 Kr Krypton 35 Br Brom 34 Se Selen 33 As Arsen Ge Germanium 3 Ga Gallium 30 Zn Zink Cu Kobber (Cuprum) Ni Nikkel 3,7 7,04 7,6 74, 7,64 6,73 65,3 63,546 5,63 3,0,6,,0,,7, 6, Xe Xenon 53 I Iod 5 Te Tellur 5 Sb Antimon 50 Sn Tin (Stannum) 4 In Indium 4 Cd Cadmium 47 Ag Sølv (Argentum) 46 Pd Palladium 3, 6,0 7,6,76,7 4,,4 07,7 06,4,7,,0,0,,7,, Rn* Radon 5 At* Astat 4 Po* Polonium 3 Bi Bismuth Pb Bly (Plumbum) Tl Thallium 0 Hg Kviksølv 7 Au Guld (Aurum) 7 Pt Platin () (0) (0) 0, 07, 04,3 00,5 6,7 5,0,,0,0,3,6,0,5, Cn* Copernicium Rg* Røntgenium 0 Ds* Darmstadtium (3) () () (7) (5) (3) (77) (7) (6) 7 7 Lu Lutetium 70 Yb Ytterbium 6 Tm Thulium 6 Er Erbium 67 Ho Holmium 66 Dy Dysprosium 65 Tb Terbium 64 Gd Gadolinium 74,7 73,04 6,3 67,6 64,3 6,5 5,3 57,5,,, 3, 30,,, 7, 5 03 Lr* Lawrencium 0 No* Nobelium 0 Md* Mendelevium 00 Fm* Fermium Es* Einsteinium Cf* Californium 7 Bk* Berkelium 6 Cm* Curium (6) (5) (5) (57) (54) (5) (47) (47) (43) (44) (37) 3,03 (3),3,3,3,3 7,3 5, 5,3 4,4,4 gas,5 0 *,3,3 3,3 30 radioaktiv I, Elektronfordeling i skallerne :36:50 Kilde: webelements.com 6
7 Uorganisk kemi Udsnit af det periodiske system, hovedgrupperne. Hele skemaet kan ses side 6-7. Som det fremgår oven over, er systemet opdelt i lodrette og vandrette inddelinger. De lodrette inddelinger betegnes hovedgrupper, og de vandrette betegnes perioder. Lodret Hovedgrupperne er de lodrette søjler benævnt med tallene:.-,.-, 3.-, 4.-, 5.-, 6.-, 7.- og. hovedgruppe. Hovedgruppenummeret angiver, hvor mange elektroner atomet har i den yderste skal. Det er i høj grad disse elektroner, der bestemmer stoffets kemiske egenskaber. Eksempler fra hovedgruppe. Stofferne i hovedgruppe, der starter med H, har alle elektron i yderste skal. De andre er: Li, Na, K, Rb, Cs og Fr. Hovedgruppe stofferne har alle to elektroner i yderste skal. Det er: Be, Mg, Ca, Sr, Ba og Ra. Eksempler fra hovedgruppe. Vandret De vandrette rækker hedder perioder og benævnes: Periodenummeret angiver, hvor mange elektronskaller atomet har. - Kulstof har elektroner i to skaller, derfor står det i. periode. - Natrium har elektroner i tre skaller, derfor står det i 3. periode. 7
8 Naturfag NATURFAG Når man bevæger sig en gang mod højre i en periode, stiger atomnummeret, og dermed protonantallet, med en. - Bevæger man sig fra N, nitrogen med atomnummer 7, en gang mod højre til O, oxygen med atomnummer. Helium er en ædelgas, der bl.a. anvendes i balloner. Nitrogen har syv protoner, og oxygen har otte protoner. Oktetreglen (hovedgruppe ) Grundstofferne i hovedgruppe bliver kaldt ædelgasserne, fordi de ikke reagerer med andre stoffer. De har otte elektroner i yderste skal (dog ikke He, der kun har to). Dette antal gør, at de er meget stabile. Stofferne i de andre hovedgrupper prøver at opnå en tilstand, der ligner ædelgasserne; det kaldes oktetreglen (oktet=). Atommassen er den samlede vægt af protoner, neutroner og elektroner målt i unit. Antallet af neutroner finder man ved at tage atommassen, afrundet til helt tal og trække protonantallet fra. Den samlede masse af elektronerne er så lille, at den ikke har nogen betydning. på et grundstof fra det periodiske system. Kulstof, med atomnr. 6, har atomvægten:,0 unit Kulstofs atommasse afrundet til helt tal: unit Kulstofs seks protoner vejer: unit 6: 6 unit Difference: 6 unit Differencen på seks unit kan kun stamme fra neutroner, da elektronerne vejer så lidt, at vi ikke regner med dem. En neutron vejer en unit. Derfor må seks unit være lig med 6 neutroner. Opgaver. I hvilken hovedgruppe og periode hører følgende stoffer til: N, Cl, Al, Rb og As?. Find proton- og neutronantallet for følgende stoffer: O, Na, Ar, Be og K. 3. Tegn elektronerne i deres skaller for følgende stoffer: Ca, Li, P, Kr, og S. naturfag_007.indd :4:
9 Uorganisk kemi Isotoper I et grundstof har atomerne ikke altid den samme atommasse. Der er nogle få af atomerne, der har en eller flere neutroner ekstra i kernen. Atomer af samme grundstof, men med forskellig neutronantal, hedder isotoper. Der findes tre isotoper af hydrogen: - Den normale hydrogen med én proton og én elektron. - Isotopen med én neutron hedder deuterium. - Den tredje hedder tritium og har to neutroner i kernen. Der findes meget lidt af deuterium og tritium i forhold til normal hydrogen. Atommassen i det periodiske system for hydrogen er gennemsnitsmassen af de tre isotoper. Derfor værdien på.007 unit. De kemiske egenskaber for isotoperne er de samme, da de har samme antal protoner. Hydrogen-isotoper. Molekyler Den mindste del af et stof, der kan eksistere, hedder et molekyle. Molekyler består normalt af mindst to atomer. Det er kun grundstofferne i hovedgruppe, ædelgasserne, hvor et molekyle kun består af ét atom. Mange af stofferne i det periodiske system stræber efter at nå en tilstand, der ligner ædelgasserne. Det vil sige, at de prøver at opnå en tilstand med otte elektroner i yderste skal. En måde kan være at dele sine yderste elektroner med andre atomer. En anden måde kan være, at atomer stjæler elektroner fra hinanden (fx NaCl). Valens Valens er et tal for, hvor mange elektroner et atom er i stand til at optage eller afgive for at opnå en ædelgaslignende struktur. 3
10 Naturfag Eksempler. Natrium står i hovedgruppe og har dermed en elektron i yderste skal (M-skallen). I den næstyderste skal (L-skallen) har natrium otte elektroner. Eksempler på valens. Afgiver natrium sin enlige elektron i M-skallen, bliver L-skallen med otte elektroner, den yderste skal. Natrium har derved opnået en struktur, der ligner ædelgassen neon. Da det er en elektron, som natrium afgiver, har natrium valensen. Dette er normalt for hovedgruppe I.. Klor står i hovedgruppe 7 og har derfor syv elektroner i yderste skal. Klor mangler en elektron i at opnå en struktur, der ligner ædelgassen argon. Klor har derfor også valensen. H H H For hovedgruppe,, 3 og 4 er valensen normalt lig med hovedgruppenummeret. For hovedgruppe 5, 6, 7 og er valensen normalt lig med otte minus hovedgruppenummeret. O O N N Eksempler på molekyler med to ens atomer. (Kun elektroner i de yderste skaller er medtaget.) O N Derfor: - H, Na og K har valensen (hovedgruppe ). - Be, Mg og Ca har valensen (hovedgruppe ). - B og Al har valensen 3 (hovedgruppe 3). - C har valensen 4 (hovedgruppe 4). - N og P har valensen 3 (hovedgruppe 5). - O og S har valensen (hovedgruppe 6). - F og Cl har valensen (hovedgruppe 7). - Ædelgasserne har valensen 0 (hovedgruppe ). Elektronerne i atomets yderste skal kaldes valenselektroner. Kemisk tegnsætning I kemien er det nødvendigt at have klare regler for, hvordan man bruger de kemiske symboler. Et molekyle består normalt af mindst to atomer. Dette beskrives med de kemiske symboler for de grundstoffer, der indgår i molekylet. Antallet af de pågældende atomer angives med et tal efter det kemiske symbol. Eksempler på molekyler med flere slags atomer. (Kun elektroner i de yderste skaller er medtaget.) 4 Hydrogenmolekylet består af hydrogenatomer og skrives derfor H. Indgår der kun ét atom af det ene grundstof, skriver man ikke noget tal bagefter. Et vandmolekyle består af to hydrogenatomer, men kun et oxygenatom og skrives derfor H O. 0
11 Naturfag NATURFAG 4 Grundstoftabel, sorteret alfabetisk efter symbol Kemisk navn Nr. Symbol Atommasse Actinium Ac Sølv 47 Ag 07,6 Aluminium 3 Al 6, Americum 5 Am Argon Ar 3,4 Arsen 33 As 74, Astat 5 At Guld 7 Au 6,67 Bor 5 B 0, Barium 56 Ba 37,33 Beryllium 4 Be,0 Bismuth/Vismuth 3 Bi 0, Berkelium 7 Bk Brom 35 Br 7,04 Carbon/Kul 6 C,0 Calcium 0 Ca 40,0 Cadmium 4 Cd,4 Cerium 5 Ce 40, Californium Cf Chlor 7 Cl 35,453 Curium 6 Cm Cobalt 7 Co 5,33 Chrom 4 Cr 5,66 Cæsium 55 Cs,05 Kobber Cu 63,55 Dysprosium 66 Dy 6,55 Erbium 6 Er 67,6 Einsteinium Es Europium 63 Eu 5,6 Fluor F, Jern 6 Fe 55,5 Fermium 00 Fm Francium 7 Fr Gallium 3 Ga 6,7 Gadolium 64 Gd 57,3 Germanium Ge 75,5 Hydrogen/brint H,007 Helium He 4,006 Hafnium 7 Hf 7,4 Kviksølv 0 Hg 00,5 Holmium 67 Ho 64,3 Jod 53 I 6,045 Indium 4 In 4, Iridium 77 Ir, Kalium K 3,0 Krypton 36 Kr 3,0 Lanthan 57 La 3, Lithium 3 Li 6,4 naturfag_007.indd :3
12 Tabeller Lawrencium 03 Lr Luthetium 7 Lu 74,7 Mendelevium 0 Md Magnesium Mg 4,305 Mangan 5 Mn 54,3 Molybdæn 4 Mo 5,4 Nitrogen/kvælstof 7 N 4,007 Natrium Na,0 Niobium 4 Nb,06 Neodym 60 Nd 44,4 Neon 0 Ne 0, Nikkel Ni 5,70 Nobelium 0 No Neptunium 3 Np Oxygen/ilt O 5,4 Osmium 76 Os 0, Fosfor 5 P 30,74 Protactinium Pa Bly Pb 07, Palladium 46 Pd 06,4 Promethium 6 Pm Polonium 4 Po Præseodynium 5 Pr 40,0 Platin 7 Pt 5,0 Plutonium 4 Pu Radium Ra Rubidium 37 Rb 5,467 Rhenium 75 Re 6, Rhodium 45 Rh 0,06 Radon 6 Rn Ruthenium 44 Ru 0,07 Svovl 6 S,06 Antimon 5 Sb,75 Scandium Sc 44,56 Selen 34 Se 7,6 Silicium 4 Si,06 Samarium 6 Sm 50,4 Tin 50 Sn,6 Strontium 3 Sr 7,6 Tantal 73 Ta 0,5 Terbium 65 Tb 5,5 Tachnetium 43 Tc Tellur 5 Te 7,60 Thorium 0 Th,03 Titan Ti 47,0 Thallium Tl 04,37 Thulium 6 Tm 6,43 Uran U 3,0 Vanadium 3 V 50,4 Wolfram 74 W 3,5 Xenon 54 Xe 3, Yttrium 3 Y,06 Ytterbium 70 Yb 73,04 Zink 30 Zn 65,3 Zirkonium 40 Zr, 5
13 Uorganisk kemi Ioner En ion er et atom eller en kemisk forbindelse med elektrisk ladning. I stedet for kovalente bindinger kan atomer opnå en ædelgaslignende struktur ved iondannelse. Ved iondannelse sker der en elektronoverførsel mellem to atomer. I vandig opløsning optræder NaCl på ionform. Cl står i hovedgruppe 7, og mangler derfor kun én elektron i yderste skal for at opnå en ædelgaslignende struktur. Na står i hovedgruppe I og har derfor én elektron i yderste skal, M-skallen. Afgiver Na den enlige elektron, er det nu L-skallen, der er den yderste, og her har Na otte elektroner. Cl stjæler den enlige elektron fra Na. Herved har Cl fået én ekstra negativ ladning i form af elektronen. Cl-atomet får dermed et overskud på én negativ ladning og skrives nu: Cl- Salt anvendes også meget til konservering, fx saltning af kød. Cl havde før 7 protoner og 7 elektroner, lige mange positive og negative ladninger. Nu har Cl 7 protoner og elektroner, altså én negativ ladning i overskud. Na-atomet har mistet én negativ ladning og har derfor et overskud på én positiv ladning og skrives derfor: Na + Na havde før protoner og elektroner. Nu har Na protoner, men kun 0 elektroner. Der er én positiv ladning i overskud. Elektronoverførsel fra Na til C. Reaktionsligningen: NaCl Na + + Cl - En ion er derfor et atom, der enten har mistet eller fået tilført en eller flere elektroner. Herved er atomet blevet elektrisk ladet, enten positivt eller negativt. Et neutralt atom har jo lige mange positive og elektriske ladninger. For at der kan skabes ioner, skal der både være et atom til at afgive og et atom til at modtage elektroner. 3
14 Naturfag Hvis Cl danner ioner med Ca fra hovedgruppe, er situationen lidt anderledes. Ca skal af med to elektroner for at opnå en ædelgaslignende struktur. Cl kan jo kun optage en elektron (fra syv til otte). Derfor skal der to Cl-atomer til at optage Ca s to elektroner. Elektronoverførsel fra Ca til Cl. Ca har mistet to negative ladninger og har nu et overskud på to positive ladninger. CaCl Ca ++ + Cl Navngivning af ioner De positive ioner navngives ved at tilføje endelsen: ion efter grundstoffets navn. Eksempler Na + Natrium-ion Calcium-ion Ca ++ Navnet for negative ioner dannes af hele eller dele af grundstofnavnet med endelsen -id efterfulgt af -ion. Eksempler Cl Klorid-ion O Oxid-ion S Sulfid-ion N Nitrid-ion P Fosfid-ion Sammensatte ioner Mange ioner består af flere atomer. Her er det hele atomgruppen, der modtager eller afgiver en eller flere elektroner. Eksempler. SO 4 har som gruppe fået tilført to elektroner. Derfor ladningen på hele gruppen.. NH 4 + har afgivet en elektron. Derfor er ladningen +. De fleste sammensatte ioner er negative, dog er NH 4 + positiv. Den findes i en hel del salte. 4
15 Uorganisk kemi Navngivning af sammensatte ioner NO 3 Nitrat-ion SO 4 Sulfat-ion PO 4 Fosfat-ion CO 3 Carbonat-ion OH Hydroxid-ion Ammonium-ion NH 4 + De fleste af ion-forbindelserne hører til gruppen af salte (se side 30), der kan adskilles i negative og positive ioner i en opløsning. Eksempler NaCl Na + + Cl NH 4 Cl + NH 4 + Cl Man skriver altid den positive ion først i den kemiske formel. Den kemiske forbindelse navngives med grundstofnavnet for den positive ion efterfulgt af navnet for den negative ion. Eksempler NaCl Natrium-klorid KNO 3 Kalium-nitrat CaSO 4 Calcium-sulfat Na 3 PO 4 Natrium-fosfat NH 4 Cl Ammonium-klorid Opgaver. Navngiv følgende ion-forbindelser: AlPO 4, LiCl, NaOH og K SO 4.. Færdiggør reaktionsligningerne: LiCl Na 3 PO 4 NH 4 NO 3 35
16 Naturfag Organisk kemi Organisk kemi! En organisk forbindelse er en forbindelse, der indeholder kulstof. Livet på jorden er afhængigt af grundstoffet kulstof (karbon), som findes i alle levende organismer. Organisk kemi er den del af kemien, der omhandler alt det, der er levende og det, der har været levende. Stort set alt, hvad vi spiser, kommer fra levende organismer. Derfor tilhører vore levnedsmidler, som er opbygget af kulhydrater, fedtstoffer, protein og alkohol, den organiske kemi. Vi kalder disse kemiske forbindelser for kulstofforbindelser, fordi de altid indeholder kulstof. Forenklet kan organiske stoffer forklares ved, at de er opbygget af et kulstofskelet. Den eneste gruppe, der ændrer sig, er enden, som er forskellig alt afhængig af, om det er en alkan, en alkohol eller en organisk syre. Alkaner (C n H n+ ) Vi vil her starte med at kigge på opbygningen af alkaner, fordi de kemisk set er de simpleste af de organiske stoffer. 34 Alkaner er en organisk forbindelse, der er opbygget af C og H. 6
17 Organisk kemi Brændstoffer som gas, benzin, petroleum og olie kaldes kulbrinter, fordi de er kemiske forbindelser af kul og brint. De første alkaner Navn Formel Navn Formel C Methan CH 4 C 5 Pentan C 5 H C Ethan C H 6 C 6 Hexan C 6 H 4 C 3 Propan C 3 H C 7 Heptan C 7 H 6 C 4 Butan C 4 H 0 C Oktan C H Generelt gælder De fire første alkaner (kulbrinter) er gasser (methan, ethan, propan og butan). De fire næste er benziner (pentan, hexan, heptan og oktan). De næste syv er forskellige olier og dieselolie. Fra C6, C7 og opefter er det faste former som paraffiner, steariner og asfalt. CH 4, methan findes i naturgas. C 3 H, propan findes i campinggas. C 4 H 0, butangas findes i flaskegas. C 7 H 6, heptan findes i benzin. Alkener (C n H n ) Alkener er organiske forbindelser, der er opbygget af C og H, men hvor der er én dobbeltbinding mellem to C-atomer. Alkenernes navne fremkommer ved, at endelsen i det tilsvarende alkan-navn ændres til -en. Ethen er det vigtigste stof til fremstilling af plastik. Flere ethenmolekyler sættes sammen ved, at dobbeltbindingen i ethen åbnes og reagerer med andre ethenmolekyler. Ethenmolekyler kan sættes sammen i lange kæder - polyethen. En anden form for plast er PVC. Den dannes, hvis et af H-atomerne i ethen erstattes med Cl, og den i øvrigt polymeriseres. Alkyner (C n H n- ) Alkyner er organiske stoffer, der indeholder en trippelbinding mellem to C-atomer. Den simpleste alkyn hedder ethyn og har formlen C H. Alkynernes navne fremkommer ved, at endelsen i det tilsvarende alkan-navn ændres til -yn. Ethyn er en gas, der brænder ved meget høj temperatur, og som bruges til svejsning (skærebrænder). 35 7
Opgaver i atomer. c) Aflæs atommassen for Mg i det periodiske system eller på de udskrevne ark, og skriv det ned.
 Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
DET PERIODISKE SYSTEM
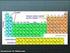 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Vikar-Guide. Den elektriske ladning af en elektron er -1 elementarladning, og den elektriske ladning af protonen er +1 elementarladning.
 Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Kemisk Reaktionslære ELO HARALD HANSEN. Polyteknisk Forlag. 2.udgave
 Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Forord 3. Udgave. Januar 2012 Jørgen Christoffersen
 Forord 3. Udgave Denne udgave er en lettere revidering af 2. udgave. Afsnittet om radioaktivitet er forbedret ved indsættelse af et appendiks. Jeg takker lektor, dr.phil. Niels Grunnet for hjælp til udarbejdelsen
Forord 3. Udgave Denne udgave er en lettere revidering af 2. udgave. Afsnittet om radioaktivitet er forbedret ved indsættelse af et appendiks. Jeg takker lektor, dr.phil. Niels Grunnet for hjælp til udarbejdelsen
Røntgenstråling. Baggrund. Atomers struktur og Røntgenstråling
 Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Opgave: Du skal udfylde de manglende felter ud fra den information der er givet
 pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomets bestanddele. Indledning. Atomer. Atomets bestanddele
 Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Lim mellem atomerne Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Den kosmiske kalender
 Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold
 Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Sporgrundstof definition:
 Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 UORGANISK KEMI Torsdag den 22. maj 2014
 Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Forelæsning 8. Stabile isotoper. Iltisotoper anvendt i paleoklimastudier, magmadannelse, termometri, vand-bjergart reaktion.
 Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Fysikforløb nr. 6. Atomfysik
 Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
OPGAVER OM DANNELSE AF IONER. OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal.
 OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
OPGAVE 3.1 OPGAVER OM DANNELSE AF IONER OPGAVE 3.1.A a. For hvert af grundstofferne herunder, skal du angive fordelingen af elektroner i hver skal. b. Angiv derefter hvor mange elektroner atomet skal optage
Nr. 6-2007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 2008
 Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Jordens salte Ny Prisma Fysik og kemi 9 - kapitel 2 Skole: Navn: Klasse:
 Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Atomets opbygning. Keminote 2010
 Atomets opbygning Oprindelig forestillede man sig, at atomet var en lille kugle, som ikke kunne deles i mindre dele. Ordet atom kommer af det græske ord atomos, som betyder udelelig. Fra slutningen af
Atomets opbygning Oprindelig forestillede man sig, at atomet var en lille kugle, som ikke kunne deles i mindre dele. Ordet atom kommer af det græske ord atomos, som betyder udelelig. Fra slutningen af
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Platin komplekser i kampen mod kræft. Koordinationskemi i aktion. cis-ptcl 2 (NH 3 ) 2. Essentiel, nyttig eller toxisk. Hvad der faktisk skete
 Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation
 Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas
 Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Relativ massefylde. H3bli0102 Aalborg tekniske skole. Relativ massefylde H3bli0102 1
 Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 UORGANISK KEMI Tirsdag den 18. december 2012
 Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
Torben Rosenørn. Aalborg Universitet. Campus Esbjerg
 Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor
 Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Fyldt med energi Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Fyldt med energi Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Grønne planter bruger vand og kuldioxid til at producere oxygen og opbygge organiske stoffer ved fotosyntese. Sæt kryds ved det
Fyldt med energi Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Grønne planter bruger vand og kuldioxid til at producere oxygen og opbygge organiske stoffer ved fotosyntese. Sæt kryds ved det
Geokemisk differentiation af Jorden oversigt
 Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014
 Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Eksamensspørgsmål til kecu eksamen tirsdag d. 3. juni og onsdag d. 4. juni 2014 Spørgsmål 1. og 15. Ionforbindelser og fældningsreaktioner, herunder øvelsen Saltes opløselighed i vand 2. og 16. Det periodiske
Opgaver til: 3. Kemiske bindingstyper
 Opgaver til: 3. Kemiske bindingstyper 1. Udfyld følgende skema ved afkrydsning (du må gerne bruge Det Periodiske System som hjælp). STOF SALT MOLE- STOF SALT MOLE- H 2 O NH 3 HBr H 2 KBr NO 2 Na CaO CO
Opgaver til: 3. Kemiske bindingstyper 1. Udfyld følgende skema ved afkrydsning (du må gerne bruge Det Periodiske System som hjælp). STOF SALT MOLE- STOF SALT MOLE- H 2 O NH 3 HBr H 2 KBr NO 2 Na CaO CO
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
 Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse:
 Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse: Opgave 1 Gasserne nitrogen, oxygen og kuldioxid er de gasser i Jordens atmosfære, der er vigtigst for livet. Angiv hvilke
Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse: Opgave 1 Gasserne nitrogen, oxygen og kuldioxid er de gasser i Jordens atmosfære, der er vigtigst for livet. Angiv hvilke
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund.
 Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse:
 Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse: Opgave 1 Et atom har oftest to slags partikler i atomkernen. Hvad hedder partiklerne? Der er 6 linjer. Sæt et kryds ud for hver linje.
Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse: Opgave 1 Et atom har oftest to slags partikler i atomkernen. Hvad hedder partiklerne? Der er 6 linjer. Sæt et kryds ud for hver linje.
Folkeskolens afgangsprøve Maj-juni 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering
 Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
1. Skalmodellen, periodesystemet og kemisk binding. Øvelse: Kaliumnitrats opløselighed i vand
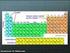 Mundtlig eksamen kemi C, 10. juni 2016 Hold: 2f ke. Antal elever til eksamen: 1 Lærer: Jørgen Mogensen 1. Skalmodellen, periodesystemet og kemisk binding. Øvelse: Kaliumnitrats opløselighed i vand Gør
Mundtlig eksamen kemi C, 10. juni 2016 Hold: 2f ke. Antal elever til eksamen: 1 Lærer: Jørgen Mogensen 1. Skalmodellen, periodesystemet og kemisk binding. Øvelse: Kaliumnitrats opløselighed i vand Gør
Spørgsmål 1 Carbonhydrider
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Carbonhydrider Der ønskes en gennemgang af udvalgte carbonhydriders opbygning og kemiske egenskaber. Du skal inddrage øvelsen:
Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole)
 Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole) Har du nogensinde tænkt på, hvordan jorden, solen og hele universet er skabt? Det er måske et af de vigtigste spørgsmål, man forsøger
Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole) Har du nogensinde tænkt på, hvordan jorden, solen og hele universet er skabt? Det er måske et af de vigtigste spørgsmål, man forsøger
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10
 NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
BASISKEMI C. Facit HELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN HAASE & SØNS FORLAG
 BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
BASISKEMI C ELGE MYGIND OLE VESTERLUND NIEL SEN VIBEKE A XEL SEN Facit AASE & SØNS FORLAG elge Mygind, Ole Vesterlund Nielsen og Vibeke Axelsen: Basiskemi C. Facit forfatterne og aase & Søns Forlag as
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Forord. Undervisere kan bruge arket ved først at kontakte [email protected] og få et skriftligt tilsagn.
 Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Efterår 2015 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfagshold Kemi C Monikka
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Efterår 2015 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfagshold Kemi C Monikka
Atomers opbygning og øvelsen: Spændingsrækken. Atomer og øvelsen: Spændingsrækken
 Kristiansen og Cederberg Aurum Kemi for gymnasiet 1 1. udgave - 2006 pensum sider # Kemi C 2 gange 16 spørgsmål Atomers opbygning og øvelsen: Spændingsrækken Kapitel 1 5-38 1 Det periodiske system, hvilke
Kristiansen og Cederberg Aurum Kemi for gymnasiet 1 1. udgave - 2006 pensum sider # Kemi C 2 gange 16 spørgsmål Atomers opbygning og øvelsen: Spændingsrækken Kapitel 1 5-38 1 Det periodiske system, hvilke
En lille verden Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Eksamensopgaverne offentliggøres selvfølgelig med det forbehold, at censor kan komme med ændringsforslag.
 VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
Afleveringsopgaver i fysik
 Afleveringsopgaver i fysik Opgavesættet skal regnes i grupper på 2-3 personer, helst i par. Hver gruppe afleverer et sæt. Du kan finde noget af stoffet i Orbit C side 165-175. Opgave 1 Tegn atomerne af
Afleveringsopgaver i fysik Opgavesættet skal regnes i grupper på 2-3 personer, helst i par. Hver gruppe afleverer et sæt. Du kan finde noget af stoffet i Orbit C side 165-175. Opgave 1 Tegn atomerne af
Eksamensopgaver. NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL
 Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Dagens program TIL GAVN FOR GARTNERE
 Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Dagens program Planteernæring og plantekvalitet - Inge ph styring Anne Pause Nye on site analysemetoder - Nauja Analysemetoder og laboratorier Inge 4-kar program Anne Planteernæring og plantekvalitet Inge
Eksamensspørgsmål 2c ke, juni Fag: Kemi C-niveau. Censor: Andreas Andersen, Skanderborg Gymnasium
 Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Eksamensspørgsmål 2c ke, juni 2016 Fag: Kemi C-niveau Censor: Andreas Andersen, Skanderborg Gymnasium Eksaminator: Jeanette Olofsson, Ikast-Brande Gymnasium 1. Bindingstyper og tilstandsformer under inddragelse
Syrer, baser og salte:
 Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
HVAD ER RADIOAKTIV STRÅLING
 16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017
 EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Fredericia HF og VUC Uddannelse Fag og niveau Lærer(e) Hold HF Kemi C Thomas Nielsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Fredericia HF og VUC Uddannelse Fag og niveau Lærer(e) Hold HF Kemi C Thomas Nielsen
Kemiske bindinger. Præsentation: Niveau: 8. klasse. Varighed: 7 lektioner
 Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Atomer, Elektroner & Andet Godt Kemi
 Atomer, Elektroner & Andet Godt Kemi Det Periodiske System Kemiske Forbindelser Reaktionsskemaer Alt levende og den materielle verden udgøres af stof, som kan omdannes ved kemiske reaktioner. Kemikeren
Atomer, Elektroner & Andet Godt Kemi Det Periodiske System Kemiske Forbindelser Reaktionsskemaer Alt levende og den materielle verden udgøres af stof, som kan omdannes ved kemiske reaktioner. Kemikeren
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Sølvsmedeteknik. Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie.
 Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE
 Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års hold Termin: Juni 2014 Uddannelse: HF-enkeltfag
Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års hold Termin: Juni 2014 Uddannelse: HF-enkeltfag
Hvor mange neutroner og protoner er der i plutonium-isotopen
 Atomet Tjek din viden om atomet. 3.1 4.1 Atommasse måles i Skriv navnene på partiklerne i atomet. Hvad angiver tallene i den kernefysiske skrivemåde? 4 2 He 13 6 Tegn atomkernen til kulstof-isotopen C.
Atomet Tjek din viden om atomet. 3.1 4.1 Atommasse måles i Skriv navnene på partiklerne i atomet. Hvad angiver tallene i den kernefysiske skrivemåde? 4 2 He 13 6 Tegn atomkernen til kulstof-isotopen C.
