Daniells element Louise Regitze Skotte Andersen
|
|
|
- Philip Jørgensen
- 10 år siden
- Visninger:
Transkript
1 Louise Regitze Skotte Andersen Fysikrapport. Morten Stoklund Larsen - Lærer K l a s s e 1. 4 G r u p p e m e d l e m m e r : N i k i F r i b e r t A n d r e a s D a h l
2 2 Indhold Indledning... 3 Materialer... 4 Metode... 5 Resultater... 6 Skema over måleresultater... 6 Graf over resistans... 6 Opsummering af resultater... 6 Teori... 7 Fremstilling af opløsningerne... 7 Hvorfor der opstår en strøm... 7 Elektronvandringen... 7 Modellen af en spændingskilde... 8 Diskussion... 9 Polspændning og strømstyrke ud fra forskrift... 9 Daniell elementets indre modstand Hvilespændningen for Daniell elementet Kortslutningssstrømmen for Daniell elementet Konklusion... 12
3 3 Indledning Denne rapport er en rapport skrevet over et forsøg lavet i samspil mellem kemi og fysik. Forsøget er lavet på basis af vores tema med redoxreaktioner i kemi, samt vores tema om ellære og elementer i fysik. Formålet med denne rapport var at skabe en Daniella element, altså et galvanisk element der producerer en strøm; et batteri. Ud fra vores forsøg skulle vi fine frem til formler der kunne bruges til udregning af hhv. polspænding, strømstyrke, indre resistans, hvilespænding og kortslutningsstrøm.
4 4 Materialer 0,1 M ZnSO 4 0,1 M CuSO 4 Salt bro. Filterpapir mættet med en opløsning af NH 4 NO 3 Amperemeter Voltmeter Kobberelektrode Zinkelektrode Ledninger Strømforsyning ml bægerglas
5 5 Metode 1. De tre opløsninger fremstilles. Zinksulfatopløsningen og kobbersulfatopløsningen hældes i hver sit bægerglas. 2. Saltbroen gøres klar ved at man dypper sin strimmel af filterpapir i ammoniumnitrat og placerer hver ende i hvert af bægerglassene 3. Det hele sættes op i følgende kredsløb, hvor komponenten er zinksulfatopløsningen, kobbersulfatopløsningen og saltbroen imellem. For at forbinde komponenten med resten af kredsløbet sætter man en zink elektrode, og en kobberelektrode for enden af ledningerne, og sætter dem i hhv. zinksulfatopløsningen og kobbersulfatopløsningen. 4. Tag kobber- og zinkelektroden ud mellem hver afmåling. Og stil strømforsyningen rigtigt imens. Sørg for at elektroder sidder nogenlunde lige langt nede i opløsningerne ved hver afmåling.
6 6 Resultater Skema over måleresultater R y - KΩ U p - mv I - μa , , , , Graf over resistans U p Indre resistans Lineær (Indre resistans) I Forskrift for tendenslinje: f(x)= * x Opsummering af resultater I forsøget afmålte vi polspændingen (U p ) og den strømstyrken (I). I Skemaet over måleresultater, kan man se de forskellige afmålte resultater ved forskellig indre resistans (R i ). R y måles I kω, U p måles i mv og I måles i μa. Grafen viser polspænding pr. strømstyrke, hvilket er den indre resistans.
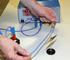
7 7 Teori Fremstilling af opløsningerne Opløsningerne fremstilles ved at blande et salt med vand. For at få den helt rigtige opløsning og M kigger man på pakken med saltet og finder molarmassen. Molarmassen ganges så med 0,1 og derefter ganger man med volumenet af opløsningen man vil have. 0,1 Hvorfor der opstår en strøm Der opstår en strøm fordi en del af elementets bundne kemiske energi bliver omsat til elektrisk energi. Når vi aflader vores element vil der blive dannet kemiske forbindelser med lavere indhold af kemisk energi end før, og det betyder at den energiforskel bliver frigjort under processen, som så udgører den indre energi i elementet, hvilken vi vil have lavest mulig, og den elektriske energi afsat i det ydre kredsløb. Elektronvandringen På ovenstående billede kan man se en model af elementets opstilling. Vi har stukket 1 stykke kobber og et stykke zink i hhv. ZnSO 4 og ZnSO 4. Når vi gør dette putter vi metaller i opløsninger med ioner, og får herved to halvceller der kan sættes sammen til en elektrokemisk celle, i dette tilfælde en galvanisk celle. I en galvanisk celle er reaktionen spontant og derfor afgiver cellen elektrisk energi. Havde cellen derimod været en elektrolysecelle ville reaktionen kun forløbe under energitilførsel. I den galvaniske celle er de to halvceller forbundet via et voltmeter hvor elektronerne kan passere frit. Saltbroen har vi for at udligne ladningerne og sørge for at ionerne fra opløsningerne ikke blandes. Elektrodepotentialet er fastlagt af en hydrogenelektrode der har elektrodepotentialet 0. Idet kobber har en højere elektronegativitet end zink er det bedre til at hive elektroner til sig en zinken er, og derfor vil der
8 8 være en forskel mellem de to elektrodepotentialer. Forskellen kalder vi hvilespændingen, og ligger på 1,10 V og kan måles under standardbetingelser for et sådan element. Standartelektrodepotentialet for de to redoxpar: Modellen af en spændingskilde = 0,76 =0,34 Hvilespænding Hvilespændingen er spændingskildens spændingsforskel og betegnes U 0. Polspænding Polspændingen er spændingsforskellen mellem ledningerne fra batteriet og betegnes U p. Indre og ydre modstand/resistans Elementet har to modstande; en indre og en ydre. Den indre modstand sidder i selve elementet, mens den ydre modstand er i vores strømforsyning. Den ydre modstand er mængden af strøm strømforsyningen giver, og den vil vi normalt gerne have så høj som muligt uden at nå maksimalspændingen. Den indre modstand er den strøm der bliver udnyttet i selve elementet og derfor ønsker vi den så lav som muligt. Modellen Et element med en perfekt spændingskilde, fast indre modstand og spændingsforskel, belastes og der trækkes en strøm. Når dette sker, vil spændingsforskellen falde over elementets poler. Spændingsforskellen her kaldes hvilespændingen (U 0 ) Polspændingen (U p ) er spændingen mellem ledningerne fra batteriet. Polspændingen er faktisk den samme som spændingsfaldet over den ydre modstand. I en sådan model for et element kan man bruge formlen: =
9 9 Diskussion Polspænding og strømstyrke ud fra forskrift Hvis vi skulle finde polspænding eller strømstyrken ved andre værdier af I, uden at lave forsøget endnu en gang, kan vi bruge forskriften for tendenslinjen til at udlede en formel for hvordan det skulle beregnes. Ud fra vores graf over måleresultater, kan vi via den opsatte tendenslinjes forskrift beregne den indre modstand. Tendenslinjens forskrift passer på modellen Forskrift for tendenslinje: = 43, ,1359 Formel: = = + Fra det kan vi udlede at modellen for tendenslinjen passer på vores formel, idet faktorernes orden er ligegyldig. Vi kan herved omskrive formlen så den passer på modellen for tendenslinjen. = + Her kan vi så udlede at svarer til funktionen for x, svarer til a og svarer til b. Når vi så skal beregne en formel hvor vi frit kan ændre på x-værdierne alt efter hvad vores strømstyrke skal være, og så finde polspændingen skal vi gøre således = 43, ,1359 For at få det lettere at overskue kan vi ændre vores minusparantes til en positiv værdi. =43, ,1359 Dette vil så være vores endelige formel for beregning af polspændingen. Hvis vi så derimod skal bruge strømstyrken skal vi have den inverse funktion til vores funktionsforskrift af tendenslinjen. Det gør vi ved at isolere x, og sætte f(y) i -1. = + = Denne funktion kan vi så, ligesom den foregående, benytte til at lave en forskrift for strømstyrken. Dette gør vi ved at sætte som I, og x som værende polspændingen.
10 10 = 1210, ,6795 Daniell elementets indre modstand Punkterne på vores graf viser i teorien R i for Daniella elementet. For at beregne dette skal vi benytte følgende formel. = = Du skal så bruge mindst to punkter for at finde den indre resistans, men da der er variation for hver afmåling, grundet forskellige fejlkilder, så som placering af metallet i væsken, og andre ting, kan man bruge forskriften for tendenslinjen. Vi kan så her bruge den formel vi tidligere opsatte for at finde hhv. polspænding og strømstyrke. Jeg vælger at bruge nogle af de værdier af I vi målte i forsøget. =43, μA+1210,1359 =221,476 =43, μA+1210,1359 =225,844 Vi skal nu beregne den indre resistans og til det bruger vi før benævne formel = 225, ,476 24μA 23μA =4,368 Ω Hvilespændingen for Daniell elementet Vi skal nu finde hvilespændingen for Daniella elementet, og til det vil vi bruge en form af ohms lov: = + Jeg vælger her at sætte I som værende 23μA og den ydre modstand som værende 9KΩ, da disse er sammenhængende ved vores målinger. Samtidigt vil jeg bruge den indre modstand hvilken vi udregnede før. = 0,4368 Ω+9.000Ω 23μA=20mV
11 11 Kortslutningssstrømmen for Daniella elementet Jeg skal nu beregne kortslutningsstrømmen for Daniella elementet, og til den vil jeg benytte forskriften for tendenslinjen Jeg vil nu benytte mig af formlen = 43, ,1 = = = 1210,1 43,68 = 43,68 43,68 =27,7038
12 12 Konklusion Formålet med denne rapport var at skabe en Daniella element, altså et galvanisk element der producerer en strøm; et batteri. Ud fra vores forsøg skulle vi fine frem til formler der kunne bruges til udregning af hhv. polspænding, strømstyrke, indre resistans, hvilespænding og kortslutningsstrøm. Mine resultater behandlet ud fra den tegnede graf, og funktionen for tendenslinjen, passer i fleste tilfælde meget godt med de målte resultater for, dog er der nogle usikkerheder mht. det afmålte resultater, dels da det ikke er helt muligt at lave en perfekt strømkilde, og da der undervejs har været noget tab af energi flere steder. Da vores eget forsøg ikke virkede, var vi nødt til at bruge forsøgsresultater fra andre grupper som basis for vores rapport, dette betød blandt andet at vi ikke kunne få fat i en måling af hvilestrømmen og derfor var det svært at sammenligne.
Indre modstand og energiindhold i et batteri
 Indre modstand og energiindhold i et batteri Side 1 af 10 Indre modstand og energiindhold i et batteri... 1 Formål... 3 Teori... 3 Ohms lov... 3 Forsøgsopstilling... 5 Batteriets indre modstand... 5 Afladning
Indre modstand og energiindhold i et batteri Side 1 af 10 Indre modstand og energiindhold i et batteri... 1 Formål... 3 Teori... 3 Ohms lov... 3 Forsøgsopstilling... 5 Batteriets indre modstand... 5 Afladning
MODUL 5 ELLÆRE: INTRONOTE. 1 Basisbegreber
 1 Basisbegreber ellæren er de mest grundlæggende størrelser strøm, spænding og resistans Strøm er ladningsbevægelse, og som det fremgår af bogen, er strømmens retning modsat de bevægende elektroners retning
1 Basisbegreber ellæren er de mest grundlæggende størrelser strøm, spænding og resistans Strøm er ladningsbevægelse, og som det fremgår af bogen, er strømmens retning modsat de bevægende elektroners retning
Opgaver i fysik - ellære
 Opgaver i fysik - ellære Indhold E1 Strømstyrke... 1 E2 Strømstyrke... 2 E3 Strømforgrening... 2 E4 Strømforbrug... 2 E5 Elementarpartikler og elektrisk ladning... 3 E6 Elektriske kræfter (kræver kendskab
Opgaver i fysik - ellære Indhold E1 Strømstyrke... 1 E2 Strømstyrke... 2 E3 Strømforgrening... 2 E4 Strømforbrug... 2 E5 Elementarpartikler og elektrisk ladning... 3 E6 Elektriske kræfter (kræver kendskab
Formålet med dette forsøg er at lave en karakteristik af et 4,5 V batteri og undersøge dets effektforhold.
 Formål Formålet med dette forsøg er at lave en karakteristik af et 4,5 V batteri og undersøge dets effektforhold. Teori Et batteri opfører sig som en model bestående af en ideel spændingskilde og en indre
Formål Formålet med dette forsøg er at lave en karakteristik af et 4,5 V batteri og undersøge dets effektforhold. Teori Et batteri opfører sig som en model bestående af en ideel spændingskilde og en indre
Fysikrapport Joules lov. Gruppe Nr. 232 Udarbejdet af Nicolai og Martin
 Fysikrapport Joules lov Gruppe Nr. 232 Udarbejdet af Nicolai og Martin 1 Indholdsfortegnelse Formål 3 Teori 3 Materialer 4 Fremgangsmåde 4-5 Måleresultater 5 Databehandling 5-6 Usikkerheder 6 Fejlkilder
Fysikrapport Joules lov Gruppe Nr. 232 Udarbejdet af Nicolai og Martin 1 Indholdsfortegnelse Formål 3 Teori 3 Materialer 4 Fremgangsmåde 4-5 Måleresultater 5 Databehandling 5-6 Usikkerheder 6 Fejlkilder
Ohms lov. Formål. Princip. Apparatur. Brug af multimetre. Vi undersøger sammenhængen mellem spænding og strøm for en metaltråd.
 Ohms lov Nummer 136050 Emne Ellære Version 2017-02-14 / HS Type Elevøvelse Foreslås til 7-8, (gymc) p. 1/5 Formål Vi undersøger sammenhængen mellem spænding og strøm for en metaltråd. Princip Et stykke
Ohms lov Nummer 136050 Emne Ellære Version 2017-02-14 / HS Type Elevøvelse Foreslås til 7-8, (gymc) p. 1/5 Formål Vi undersøger sammenhængen mellem spænding og strøm for en metaltråd. Princip Et stykke
Fysikrapport Kogepladen. Gruppe Nr. 232 Udarbejdet af Nicolai & Martin
 Fysikrapport Kogepladen Gruppe Nr. 232 Udarbejdet af Nicolai & Martin 1 Indholdsfortegnelse Formål 3 Teori 3 Materialer 4 Fremgangsmåde 4 Måleresultater 4 Databehandling 5 Usikkerheder 5 Fejlkilder 5 Diskussion
Fysikrapport Kogepladen Gruppe Nr. 232 Udarbejdet af Nicolai & Martin 1 Indholdsfortegnelse Formål 3 Teori 3 Materialer 4 Fremgangsmåde 4 Måleresultater 4 Databehandling 5 Usikkerheder 5 Fejlkilder 5 Diskussion
ELEKTRISKE KREDSLØB (DC)
 ELEKTRISKE KREDSLØB (DC) Kredsløbstyper: Serieforbindelser Parallelforbindelser Blandede forbindelser Central lovmæssigheder Ohms lov, effektformel, Kirchhoffs 1. & 2. lov DC kredsløb DC står for direct
ELEKTRISKE KREDSLØB (DC) Kredsløbstyper: Serieforbindelser Parallelforbindelser Blandede forbindelser Central lovmæssigheder Ohms lov, effektformel, Kirchhoffs 1. & 2. lov DC kredsløb DC står for direct
El-Teknik A. Rasmus Kibsgaard Riehn-Kristensen & Jonas Pedersen. Klasse 3.4
 El-Teknik A Rasmus Kibsgaard Riehn-Kristensen & Jonas Pedersen Klasse 3.4 12-08-2011 Strømstyrke i kredsløbet. Til at måle strømstyrken vil jeg bruge Ohms lov. I kredsløbet kender vi resistansen og spændingen.
El-Teknik A Rasmus Kibsgaard Riehn-Kristensen & Jonas Pedersen Klasse 3.4 12-08-2011 Strømstyrke i kredsløbet. Til at måle strømstyrken vil jeg bruge Ohms lov. I kredsløbet kender vi resistansen og spændingen.
Øvelse 1.5: Spændingsdeler med belastning Udført af: Kari Bjerke Sørensen, Hjalte Sylvest Jacobsen og Toke Lynæs Larsen.
 Øvelse 1.5: Spændingsdeler med belastning Udført af: Kari jerke Sørensen, Hjalte Sylvest Jacobsen og Toke Lynæs Larsen. Formål: Formålet med denne øvelse er at anvende Ohms lov på en såkaldt spændingsdeler,
Øvelse 1.5: Spændingsdeler med belastning Udført af: Kari jerke Sørensen, Hjalte Sylvest Jacobsen og Toke Lynæs Larsen. Formål: Formålet med denne øvelse er at anvende Ohms lov på en såkaldt spændingsdeler,
Når enderne af en kobbertråd forbindes til en strømforsyning, bevæger elektronerne i kobbertråden sig (fortrinsvis) i samme retning.
 E2 Elektrodynamik 1. Strømstyrke Det meste af vores moderne teknologi bygger på virkningerne af elektriske ladninger, som bevæger sig. Elektriske ladninger i bevægelse kalder vi elektrisk strøm. Når enderne
E2 Elektrodynamik 1. Strømstyrke Det meste af vores moderne teknologi bygger på virkningerne af elektriske ladninger, som bevæger sig. Elektriske ladninger i bevægelse kalder vi elektrisk strøm. Når enderne
NOGLE OPGAVER OM ELEKTRICITET
 NOGLE OPGAVER OM ELEKTRICITET I det følgende er der 12 opgaver om elektriske kredsløb, og du skal nok bruge 1 time til at besvare dem. I nogle af opgaverne er der forskellige svarmuligheder der hver er
NOGLE OPGAVER OM ELEKTRICITET I det følgende er der 12 opgaver om elektriske kredsløb, og du skal nok bruge 1 time til at besvare dem. I nogle af opgaverne er der forskellige svarmuligheder der hver er
Fysik rapport. Elektricitet. Emil, Tim, Lasse og Kim
 Fysik rapport Elektricitet Emil, Tim, Lasse og Kim Indhold Fysikøvelse: Ohms lov... 2 Opgave 1... 2 Opgave 2... 2 Opgave 3... 2 Opgave 4... 3 Opgave 5... 3 Opgave 6... 3 Opgave 7... 4 Opgave 8... 4 Opgave
Fysik rapport Elektricitet Emil, Tim, Lasse og Kim Indhold Fysikøvelse: Ohms lov... 2 Opgave 1... 2 Opgave 2... 2 Opgave 3... 2 Opgave 4... 3 Opgave 5... 3 Opgave 6... 3 Opgave 7... 4 Opgave 8... 4 Opgave
ELLÆRENS KERNE- BEGREBER (DC) Hvad er elektrisk: Ladning Strømstyrke Spændingsforskel Resistans Energi og effekt
 ELLÆRENS KERNE- BEGREBER (DC) Hvad er elektrisk: Ladning Strømstyrke Spændingsforskel Resistans Energi og effekt Atomets partikler: Elektrisk ladning Lad os se på et fysisk stof som kobber: Side 1 Atomets
ELLÆRENS KERNE- BEGREBER (DC) Hvad er elektrisk: Ladning Strømstyrke Spændingsforskel Resistans Energi og effekt Atomets partikler: Elektrisk ladning Lad os se på et fysisk stof som kobber: Side 1 Atomets
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2014 Institution Marie Kruses Skole Uddannelse STX Fag og niveau Fysik B (start jan. 2013) Lærer(e)
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2014 Institution Marie Kruses Skole Uddannelse STX Fag og niveau Fysik B (start jan. 2013) Lærer(e)
Figur 1 Energetisk vekselvirkning mellem to systemer.
 Energibånd Fysiske fænomener er i reglen forbundet med udveksling af energi mellem forskellige systemer. Udvekslingen af energi mellem to systemer A og B kan vi illustrere grafisk som på figur 1 med en
Energibånd Fysiske fænomener er i reglen forbundet med udveksling af energi mellem forskellige systemer. Udvekslingen af energi mellem to systemer A og B kan vi illustrere grafisk som på figur 1 med en
Højere Teknisk Eksamen maj Kemi A. - løse opgaverne korrekt. - tegne og aflæse grafer. Ved bedømmelsen vægtes alle opgaver ens.
 054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
054129 18/05/06 12:21 Side 1 Højere Teknisk Eksamen maj 2006 Kemi A Ved bedømmelsen lægges der vægt på eksaminandens evne til at - løse opgaverne korrekt - begrunde løsningerne med relevante beregninger,
Når strømstyrken ikke er for stor, kan batteriet holde spændingsforskellen konstant på 12 V.
 For at svare på nogle af spørgsmålene i dette opgavesæt kan det sagtens være, at du bliver nødt til at hente informationer på internettet. Til den ende kan oplyses, at der er anbragt relevante link på
For at svare på nogle af spørgsmålene i dette opgavesæt kan det sagtens være, at du bliver nødt til at hente informationer på internettet. Til den ende kan oplyses, at der er anbragt relevante link på
Alt om galvanisk tæring
 Alt om galvanisk tæring For de fleste har galvanisk tæring været et begreb forbundet med noget totalt uforståeligt. Vi forklarer hvorfor og hvordan galvanisk korrosion sker, hvordan du kan måle det, og
Alt om galvanisk tæring For de fleste har galvanisk tæring været et begreb forbundet med noget totalt uforståeligt. Vi forklarer hvorfor og hvordan galvanisk korrosion sker, hvordan du kan måle det, og
Benjamin Franklin Prøv ikke at gentage forsøget! hvor er den passerede ladning i tiden, og enheden 1A =
 E3 Elektricitet 1. Grundlæggende Benjamin Franklin Prøv ikke at gentage forsøget! I E1 og E2 har vi set på ladning (som måles i Coulomb C), strømstyrke I (som måles i Ampere A), energien pr. ladning, også
E3 Elektricitet 1. Grundlæggende Benjamin Franklin Prøv ikke at gentage forsøget! I E1 og E2 har vi set på ladning (som måles i Coulomb C), strømstyrke I (som måles i Ampere A), energien pr. ladning, også
Materialer: Strømforsyningen Ledninger. 2 fatninger med pære. 1 multimeter. Forsøg del 1: Serieforbindelsen. Serie forbindelse
 Formål: Vi skal undersøge de egenskaber de 2 former for elektriske forbindelser har specielt med hensyn til strømstyrken (Ampere) og spændingen (Volt). Forsøg del 1: Serieforbindelsen Materialer: Strømforsyningen
Formål: Vi skal undersøge de egenskaber de 2 former for elektriske forbindelser har specielt med hensyn til strømstyrken (Ampere) og spændingen (Volt). Forsøg del 1: Serieforbindelsen Materialer: Strømforsyningen
Øvelses journal til ELA Lab øvelse 4: Superposition
 Øvelses journal til ELA Lab øvelse 4: Navn: Thomas Duerlund Jensen, Jacob Christiansen, Kristian Krøier Øvelsesdato: 8/10-2002 Side 1 af 5 Formål: Eksperimentelt at eftervise superpositionsprincippet og
Øvelses journal til ELA Lab øvelse 4: Navn: Thomas Duerlund Jensen, Jacob Christiansen, Kristian Krøier Øvelsesdato: 8/10-2002 Side 1 af 5 Formål: Eksperimentelt at eftervise superpositionsprincippet og
Kollektor. Teknisk skole Ringsted Fysikrapport Af Kenneth René Larsen Afleveret d.26. maj 1999. Emitter
 Kollektor Teknisk skole Ringsted Fysikrapport Af Kenneth René Larsen Afleveret d.26. maj 1999 Basis Emitter 1 Indholdsfortegnelse Problemformulering 3 Transistorens opbygning 4 Transistoren DC forhold
Kollektor Teknisk skole Ringsted Fysikrapport Af Kenneth René Larsen Afleveret d.26. maj 1999 Basis Emitter 1 Indholdsfortegnelse Problemformulering 3 Transistorens opbygning 4 Transistoren DC forhold
ELEKTRISKE KREDSLØB (DC)
 ELEKTRISKE KREDSLØB (DC) Kredsløbstyper: Serieforbindelser Parallelforbindelser Blandede forbindelser Central lovmæssigheder Ohms lov, effektformel, Kirchhoffs 1. & 2. lov Serieforbindelser Men lad os
ELEKTRISKE KREDSLØB (DC) Kredsløbstyper: Serieforbindelser Parallelforbindelser Blandede forbindelser Central lovmæssigheder Ohms lov, effektformel, Kirchhoffs 1. & 2. lov Serieforbindelser Men lad os
Den eksperimentelle delprøve ved mundtlig prøve fysik B og fysik A, htx
 Den eksperimentelle delprøve ved mundtlig prøve fysik B og fysik A, htx Eksempler på forløb og tilhørende eksperimentelle delopgaver ved den mundtlige prøve i fysik Tre eksempler på undervisningsforløb
Den eksperimentelle delprøve ved mundtlig prøve fysik B og fysik A, htx Eksempler på forløb og tilhørende eksperimentelle delopgaver ved den mundtlige prøve i fysik Tre eksempler på undervisningsforløb
U = φ. R = ρ l A. Figur 1 Sammenhængen mellem potential, φ og spændingsfald, U: U = φ = φ 1 φ 2.
 Ohms lov Vi vil samle os en række byggestene, som kan bruges i modelleringen af fysiske systemer. De første to var hhv. en spændingskilde og en strømkilde. Disse elementer (sources) er aktive og kan tilføre
Ohms lov Vi vil samle os en række byggestene, som kan bruges i modelleringen af fysiske systemer. De første to var hhv. en spændingskilde og en strømkilde. Disse elementer (sources) er aktive og kan tilføre
Preben Holm - Copyright 2002
 9 > : > > Preben Holm - Copyright 2002! " $# %& Katode: minuspol Anode: pluspol ')(*+(,.-0/1*32546-728,,/1* Pilen over tegnet for spændingskilden på nedenstående tegning angiver at spændingen kan varieres.
9 > : > > Preben Holm - Copyright 2002! " $# %& Katode: minuspol Anode: pluspol ')(*+(,.-0/1*32546-728,,/1* Pilen over tegnet for spændingskilden på nedenstående tegning angiver at spændingen kan varieres.
Gruppemedlemmer gruppe 232: Forsøg udført d. 6/ Joule s lov
 Joule s lov 1 Formål I dette eksperiment vil vi eftervise Joules lov. Teori P = Watt / effekt R = Modstand /resistor Ω I = Ampere / spænding (A) Tid = Delta tid / samlet tid m = Massen c =Specifik varmekapacitet
Joule s lov 1 Formål I dette eksperiment vil vi eftervise Joules lov. Teori P = Watt / effekt R = Modstand /resistor Ω I = Ampere / spænding (A) Tid = Delta tid / samlet tid m = Massen c =Specifik varmekapacitet
Velkommen til. EDR Frederikssund Afdelings Almen elektronik kursus. Joakim Soya OZ1DUG Formand. EDR Frederikssund afdeling Almen elektronik kursus
 Velkommen til EDR Frederikssund Afdelings Joakim Soya OZ1DUG Formand 2012-09-01 OZ1DUG 1 Kursus målsætning Praksisorienteret teoretisk gennemgang af elektronik Forberedelse til Certifikatprøve A som radioamatør
Velkommen til EDR Frederikssund Afdelings Joakim Soya OZ1DUG Formand 2012-09-01 OZ1DUG 1 Kursus målsætning Praksisorienteret teoretisk gennemgang af elektronik Forberedelse til Certifikatprøve A som radioamatør
Na + -selektiv elektrode
 C.11.1 Na + -selektiv elektrode Formål: Øvelsens formål er at kalibrere en Na + -ISE (ionselektiv elektrode) finde elektrodens linearitetsområde anvende elektroden til koncentrationsbestemmelse belyse
C.11.1 Na + -selektiv elektrode Formål: Øvelsens formål er at kalibrere en Na + -ISE (ionselektiv elektrode) finde elektrodens linearitetsområde anvende elektroden til koncentrationsbestemmelse belyse
Elektronikkens grundbegreber 1
 Elektronikkens grundbegreber 1 B/D certifikatkursus 2016 Efterår 2016 OZ7SKB EDR Skanderborg afdeling Lektions overblik 1. Det mest basale stof 2. Både B- og D-stof 3. VTS side 21-28 4. Det meste B-stof
Elektronikkens grundbegreber 1 B/D certifikatkursus 2016 Efterår 2016 OZ7SKB EDR Skanderborg afdeling Lektions overblik 1. Det mest basale stof 2. Både B- og D-stof 3. VTS side 21-28 4. Det meste B-stof
Elektromagnetisme 7 Side 1 af 12 Elektrisk strøm. Elektrisk strøm
 Elektromagnetisme 7 Side 1 af 12 Med dette emne overgås fra elektrostatikken, som beskriver stationære ladninger, til elektrodynamikken, som beskriver ladninger i bevægelse (elektriske strømme, magnetfelter,
Elektromagnetisme 7 Side 1 af 12 Med dette emne overgås fra elektrostatikken, som beskriver stationære ladninger, til elektrodynamikken, som beskriver ladninger i bevægelse (elektriske strømme, magnetfelter,
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Elektromagnetisme 7 Side 1 af 12 Elektrisk strøm. Elektrisk strøm
 Elektromagnetisme 7 Side 1 af 1 Med dette emne overgås fra elektrostatikken, som beskriver stationære ladninger, til elektrodynamikken, som beskriver ladninger i bevægelse (elektriske strømme, magnetfelter,
Elektromagnetisme 7 Side 1 af 1 Med dette emne overgås fra elektrostatikken, som beskriver stationære ladninger, til elektrodynamikken, som beskriver ladninger i bevægelse (elektriske strømme, magnetfelter,
Folkeskolens afgangsprøve Maj-juni 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Det bør du vide om galvanisk tæring
 Det bør du vide om galvanisk tæring For de fleste sejlere er galvanisk tæring et begreb forbundet med noget totalt uforståeligt. Få her forklaringen på hvorfor og hvordan galvanisk tæring sker, hvordan
Det bør du vide om galvanisk tæring For de fleste sejlere er galvanisk tæring et begreb forbundet med noget totalt uforståeligt. Få her forklaringen på hvorfor og hvordan galvanisk tæring sker, hvordan
Bortset fra kendskabet til atomer, kræver forløbet ikke kendskab til andre specifikke faglige begreber, så det kan placeres tidligt i 7. klasse.
 Elektricitet Niveau: 7. klasse Varighed: 5 lektioner Præsentation: I forløbet Elektricitet arbejdes med grundlæggende begreber indenfor elektricitet herunder strømkilder, elektriske kredsløb, elektrisk
Elektricitet Niveau: 7. klasse Varighed: 5 lektioner Præsentation: I forløbet Elektricitet arbejdes med grundlæggende begreber indenfor elektricitet herunder strømkilder, elektriske kredsløb, elektrisk
Matematik A og Informationsteknologi B
 Matematik A og Informationsteknologi B Projektopgave 2 Eksponentielle modeller Benjamin Andreas Olander Christiansen Jens Werner Nielsen Klasse 2.4 6. december 2010 Vejledere: Jørn Christian Bendtsen og
Matematik A og Informationsteknologi B Projektopgave 2 Eksponentielle modeller Benjamin Andreas Olander Christiansen Jens Werner Nielsen Klasse 2.4 6. december 2010 Vejledere: Jørn Christian Bendtsen og
Lærervejledning. Lærervejledning til el-kørekortet. El-kørekortet er et lille undervisningsforløb beregnet til natur/teknikundervisningen
 Lærervejledning EVU El- og Vvs-branchens Uddannelsessekretariat 2007 Højnæsvej 71, 2610 Rødovre, tlf. 3672 6400, fax 3672 6433 www.evu.nu, e-mail: [email protected] Lærervejledning El-kørekortet
Lærervejledning EVU El- og Vvs-branchens Uddannelsessekretariat 2007 Højnæsvej 71, 2610 Rødovre, tlf. 3672 6400, fax 3672 6433 www.evu.nu, e-mail: [email protected] Lærervejledning El-kørekortet
Spørgsmål 1. Øvelse: Kobber plus dibrom. Teori: Atomers opbygning.
 Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af salte og
Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af salte og
Grätzel Solcellen. - Fremstil din egen solcelle
 Grätzel Solcellen - Fremstil din egen solcelle Find Instruktionsvideo på: http://inano.au.dk/schools/bestil-et-besoeg/ Det er relativt simpelt at fremstille sin egen Grätzel solcelle, næsten udelukkende
Grätzel Solcellen - Fremstil din egen solcelle Find Instruktionsvideo på: http://inano.au.dk/schools/bestil-et-besoeg/ Det er relativt simpelt at fremstille sin egen Grätzel solcelle, næsten udelukkende
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Mathias Rask Højen Jensen, 3MY Erhvervsskolerne Aars Fysik A Eksamensprojekt. η = Q tilført
 kalder nyttevirkningen. Carnot brugte den ideelle kredsproces til at beskrive den maksimale nyttevirkning, som en kraftvarmemaskine kunne, hvilket er hvad der kaldes carnotnyttevirkningen. Denne nyttevirkning
kalder nyttevirkningen. Carnot brugte den ideelle kredsproces til at beskrive den maksimale nyttevirkning, som en kraftvarmemaskine kunne, hvilket er hvad der kaldes carnotnyttevirkningen. Denne nyttevirkning
Forsyn dig selv med energi
 Lærervejledning Formål I denne aktivitet skal eleverne vha. en ombygget kondicykel få konkrete erfaringer med at forsyne sig selv med energi, dvs. mærke energibehovet til at dække forskellige belastninger
Lærervejledning Formål I denne aktivitet skal eleverne vha. en ombygget kondicykel få konkrete erfaringer med at forsyne sig selv med energi, dvs. mærke energibehovet til at dække forskellige belastninger
Undervisningsbeskrivelse for fysik B 2. B 2011/2012
 Undervisningsbeskrivelse for fysik B 2. B 2011/2012 Termin Undervisningen afsluttes den 16. maj 2012 Skoleåret hvor undervisningen har foregået: 2011-2012 Institution Skive Teknisk Gymnasium Uddannelse
Undervisningsbeskrivelse for fysik B 2. B 2011/2012 Termin Undervisningen afsluttes den 16. maj 2012 Skoleåret hvor undervisningen har foregået: 2011-2012 Institution Skive Teknisk Gymnasium Uddannelse
Brydningsloven og bestemmelse af brydningsindeks Fysikrapport, 5/9-2008
 ROSKILDE TEKNISKE GYMNASIUM Brydningsloven og bestemmelse af brydningsindeks Fysikrapport, 5/9-2008 Louise Regitze Skotte Andersen, Klasse 2.4 Lærer: Ashuak Jacob France 2 Indhold Indledning... 3 Materialeliste...
ROSKILDE TEKNISKE GYMNASIUM Brydningsloven og bestemmelse af brydningsindeks Fysikrapport, 5/9-2008 Louise Regitze Skotte Andersen, Klasse 2.4 Lærer: Ashuak Jacob France 2 Indhold Indledning... 3 Materialeliste...
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
KREDSLØBSTEORI 10 FORELÆSNINGER OM ELEKTRISKEKREDSLØB
 EE Basis, foråret 2010 KREDSLØBSTEORI 10 FORELÆSNINGER OM ELEKTRISKEKREDSLØB Jan H. Mikkelsen EE- Basis, Kredsløbsteori, F10, KRT1 1 Emner for idag IntrodukEon El kurset Kredsløbsteori Formål og indhold
EE Basis, foråret 2010 KREDSLØBSTEORI 10 FORELÆSNINGER OM ELEKTRISKEKREDSLØB Jan H. Mikkelsen EE- Basis, Kredsløbsteori, F10, KRT1 1 Emner for idag IntrodukEon El kurset Kredsløbsteori Formål og indhold
Impuls og kinetisk energi
 Impuls og kinetisk energi Peter Hoberg, Anton Bundgård, and Peter Kongstad Hold Mix 1 (Dated: 7. oktober 2015) [email protected] [email protected] [email protected] 2 I. INDLEDNING I denne øvelse
Impuls og kinetisk energi Peter Hoberg, Anton Bundgård, and Peter Kongstad Hold Mix 1 (Dated: 7. oktober 2015) [email protected] [email protected] [email protected] 2 I. INDLEDNING I denne øvelse
El-Fagets Uddannelsesnævn
 El-Fagets Uddannelsesnævn El-kørekort Lærervejledning El-kørekortet er et lille undervisningsforløb beregnet til natur/teknik første fase. Ved at arbejde med elementær el-lære er det vores håb, at eleverne
El-Fagets Uddannelsesnævn El-kørekort Lærervejledning El-kørekortet er et lille undervisningsforløb beregnet til natur/teknik første fase. Ved at arbejde med elementær el-lære er det vores håb, at eleverne
Kemiøvelse 2 1. Puffere
 Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
Kemiøvelse 2 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet
Teknologi & kommunikation
 Grundlæggende Side af NV Elektrotekniske grundbegreber Version.0 Spænding, strøm og modstand Elektricitet: dannet af det græske ord elektron, hvilket betyder rav, idet man tidligere iagttog gnidningselektricitet
Grundlæggende Side af NV Elektrotekniske grundbegreber Version.0 Spænding, strøm og modstand Elektricitet: dannet af det græske ord elektron, hvilket betyder rav, idet man tidligere iagttog gnidningselektricitet
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2009 juni 2010 Institution Københavns tekniske Gymnasium/Sukkertoppen Uddannelse Fag og niveau Lærer(e)
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2009 juni 2010 Institution Københavns tekniske Gymnasium/Sukkertoppen Uddannelse Fag og niveau Lærer(e)
Mini SRP. Afkøling. Klasse 2.4. Navn: Jacob Pihlkjær Hjortshøj, Jonatan Geysner Hvidberg og Kevin Høst Husted
 Mini SRP Afkøling Klasse 2.4 Navn: Jacob Pihlkjær Lærere: Jørn Christian Bendtsen og Karl G Bjarnason Roskilde Tekniske Gymnasium SO Matematik A og Informations teknologi B Dato 31/3/2014 Forord Under
Mini SRP Afkøling Klasse 2.4 Navn: Jacob Pihlkjær Lærere: Jørn Christian Bendtsen og Karl G Bjarnason Roskilde Tekniske Gymnasium SO Matematik A og Informations teknologi B Dato 31/3/2014 Forord Under
Kemiforsøg til teorihæftet Kemisk binding og elektrolyse Forsøg 1.
 Forsøg 1. At undersøge forskellen på rene stoffer og blandinger. 500 ml. bægerglas Magnet Tragt Filterpapir Kniv Stearinlys Sand Jernfilspåner Snit stearinlyset i småstykker med kniven, og bland stearin,
Forsøg 1. At undersøge forskellen på rene stoffer og blandinger. 500 ml. bægerglas Magnet Tragt Filterpapir Kniv Stearinlys Sand Jernfilspåner Snit stearinlyset i småstykker med kniven, og bland stearin,
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Studenterkurset
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Termin hvori undervisningen afsluttes: maj-juni 2014 Studenterkurset
Metallernes kemi. Præsentation: Niveau: 8. klasse. Varighed: 6 lektioner
 Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
FULD SKRUE PÅ BATTERI-INDSAMLING, LÆRING OG LÆKRE PRÆMIER. Kampagne i Haderslev Kommune uge For klassetrin
 FULD SKRUE PÅ BATTERI-INDSAMLING, LÆRING OG LÆKRE PRÆMIER Kampagne i Haderslev Kommune uge 37-40. For 4.-6. klassetrin Kære lærer! Vi vil gerne invitere dig og dine elever til at deltage i Batterier i
FULD SKRUE PÅ BATTERI-INDSAMLING, LÆRING OG LÆKRE PRÆMIER Kampagne i Haderslev Kommune uge 37-40. For 4.-6. klassetrin Kære lærer! Vi vil gerne invitere dig og dine elever til at deltage i Batterier i
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2018 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2018 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Teknologi & kommunikation
 Elektricitet Elektricitet, ordet stammer fra det græske ord elektron, der betyder rav. Elektricitet er et fysisk fænomen, der knytter sig til elektriske ladninger i hvile (elektrostatik) eller i bevægelse
Elektricitet Elektricitet, ordet stammer fra det græske ord elektron, der betyder rav. Elektricitet er et fysisk fænomen, der knytter sig til elektriske ladninger i hvile (elektrostatik) eller i bevægelse
1 Lysets energi undersøgt med lysdioder (LED)
 Solceller og Spektre Øvelsesvejledning til brug i Nanoteket Udarbejdet i Nanoteket, Institut for Fysik, DTU Rettelser sendes til [email protected] 26. august 2010 Formål Formålet med øvelsen
Solceller og Spektre Øvelsesvejledning til brug i Nanoteket Udarbejdet i Nanoteket, Institut for Fysik, DTU Rettelser sendes til [email protected] 26. august 2010 Formål Formålet med øvelsen
Fysikrapport: Rapportøvelse med kalorimetri. Maila Walmod, 1.3 HTX, Rosklide. I gruppe med Ulrik Stig Hansen og Jonas Broager
 Fysikrapport: Rapportøvelse med kalorimetri Maila Walmod, 1.3 HTX, Rosklide I gruppe med Ulrik Stig Hansen og Jonas Broager Afleveringsdato: 30. oktober 2007* *Ny afleveringsdato: 13. november 2007 1 Kalorimetri
Fysikrapport: Rapportøvelse med kalorimetri Maila Walmod, 1.3 HTX, Rosklide I gruppe med Ulrik Stig Hansen og Jonas Broager Afleveringsdato: 30. oktober 2007* *Ny afleveringsdato: 13. november 2007 1 Kalorimetri
Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT. Litteratur: Klasse: Dato: Ark 1 af. Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV
 Fag: KEMI Journal nr. Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT Navn: Litteratur: Klasse: Dato: Ark 1 af Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV Formålet er at bestemme opløseligheden
Fag: KEMI Journal nr. Titel: OPLØSELIGHEDEN AF KOBBER(II)SULFAT Navn: Litteratur: Klasse: Dato: Ark 1 af Helge Mygind, Kemi 2000 A-niveau 1, s. 290-292 8/9-2008/OV Formålet er at bestemme opløseligheden
Preview from Notesale.co.uk Page 11 of 51
 Centrifugalpumpe: Den kan flytte større mængder vand. Den kan ikke selv suge vandet til sig. (ikke selvansugende). Den skal spædes med vand for, at kunne køre. Hvis man får en større løftehøjde kan man
Centrifugalpumpe: Den kan flytte større mængder vand. Den kan ikke selv suge vandet til sig. (ikke selvansugende). Den skal spædes med vand for, at kunne køre. Hvis man får en større løftehøjde kan man
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2017 Institution Herning Hf og VUC Uddannelse Fag og niveau Lærer(e) Hold HFe Kemi C Nis Bærentsen
Alt om galvanisk tæring
 Alt om galvanisk tæring For de fleste har galvanisk tæring været et begreb forbundet med noget totalt uforståeligt. Vi forklarer hvorfor og hvordan galvanisk korrosion sker, hvordan du kan måle det, og
Alt om galvanisk tæring For de fleste har galvanisk tæring været et begreb forbundet med noget totalt uforståeligt. Vi forklarer hvorfor og hvordan galvanisk korrosion sker, hvordan du kan måle det, og
Eksamen i fysik 2016
 Eksamen i fysik 2016 NB: Jeg gør brug af DATABOG fysik kemi, 11. udgave, 4. oplag & Fysik i overblik, 1. oplag. Opgave 1 Proptrækker Vi kender vinens volumen og masse. Enheden liter omregnes til kubikmeter.
Eksamen i fysik 2016 NB: Jeg gør brug af DATABOG fysik kemi, 11. udgave, 4. oplag & Fysik i overblik, 1. oplag. Opgave 1 Proptrækker Vi kender vinens volumen og masse. Enheden liter omregnes til kubikmeter.
Eksamensopgaver. NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL
 Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Salt 2. ovenfor. x = Tid (minutter) y = gram salt i vandet
 Projekt om medicindosering Fra http://www.ruc.dk/imfufa/matematik/deltidsudd_mat/sidefagssupplering_mat/rap_medicinering.pdf/ Lav mindst side 1-4 t.o.m. Med 7 Ar b ejd ssed d el 0 Salt 1 Forestil Jer at
Projekt om medicindosering Fra http://www.ruc.dk/imfufa/matematik/deltidsudd_mat/sidefagssupplering_mat/rap_medicinering.pdf/ Lav mindst side 1-4 t.o.m. Med 7 Ar b ejd ssed d el 0 Salt 1 Forestil Jer at
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Sommer 2015 Institution 414 Københavns VUC Uddannelse Fag og niveau Lærer(e) Hold stx Fysik B Kristian Gårdhus
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Sommer 2015 Institution 414 Københavns VUC Uddannelse Fag og niveau Lærer(e) Hold stx Fysik B Kristian Gårdhus
AFKØLING Forsøgskompendium
 AFKØLING Forsøgskompendium IBSE-forløb 2012 1 KULDEBLANDING Formålet med forsøget er at undersøge, hvorfor sneen smelter, når vi strøer salt. Og derefter at finde frysepunktet for forskellige væsker. Hvad
AFKØLING Forsøgskompendium IBSE-forløb 2012 1 KULDEBLANDING Formålet med forsøget er at undersøge, hvorfor sneen smelter, når vi strøer salt. Og derefter at finde frysepunktet for forskellige væsker. Hvad
Er dit reaktionsskema afstemt? Dvs. undersøg for hvert grundstof, om der er lige mange atomer af grundstoffet før reaktionen som efter reaktionen.
 7.12 Bagning med hjortetaksalt I skal undersøge, hvilke egenskaber bagepulveret hjortetaksalt har. Hjortetaksalt bruges i bagværk som kiks, klejner, brunkager m.m. Saltet giver en sprødhed i bagværket.
7.12 Bagning med hjortetaksalt I skal undersøge, hvilke egenskaber bagepulveret hjortetaksalt har. Hjortetaksalt bruges i bagværk som kiks, klejner, brunkager m.m. Saltet giver en sprødhed i bagværket.
E l - Fagets Uddannelsesnævn
 E l - Fagets Uddannelsesnævn El-kørekort Lærervejledning El-kørekortet er et lille undervisningsforløb beregnet til natur/teknik første fase. Ved at arbejde med elementær el-lære er det vores håb, at eleverne
E l - Fagets Uddannelsesnævn El-kørekort Lærervejledning El-kørekortet er et lille undervisningsforløb beregnet til natur/teknik første fase. Ved at arbejde med elementær el-lære er det vores håb, at eleverne
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Puffere. Øvelsens pædagogiske rammer. Sammenhæng. Formål. Arbejdsform: Evaluering
 1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
1 Puffere Øvelsens pædagogiske rammer Sammenhæng Denne øvelse er tilpasset kemiundervisningen på modul 3 ved bioanalytikeruddannelsen. Kemiundervisningen i dette modul indeholder blandt andet syrebaseteori
Stamoplysninger til brug ved prøver til gymnasiale uddannelser
 Undervisningsbeskrivelse for Fag, Fysik B, 1c. 2012-2013 Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2013 Institution Uddannelse Fag og niveau Lærer(e) Hold Teknisk Gymnasium
Undervisningsbeskrivelse for Fag, Fysik B, 1c. 2012-2013 Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Juni 2013 Institution Uddannelse Fag og niveau Lærer(e) Hold Teknisk Gymnasium
Modellering af elektroniske komponenter
 Modellering af elektroniske komponenter Formålet er at give studerende indblik i hvordan matematik som fag kan bruges i forbindelse med at modellere fysiske fænomener. Herunder anvendelse af Grafregner(TI-89)
Modellering af elektroniske komponenter Formålet er at give studerende indblik i hvordan matematik som fag kan bruges i forbindelse med at modellere fysiske fænomener. Herunder anvendelse af Grafregner(TI-89)
Transienter og RC-kredsløb
 Transienter og RC-kredsløb Fysik 6 Elektrodynamiske bølger Joachim Mortensen, Edin Ikanovic, Daniel Lawther 4. december 2008 (genafleveret 4. januar 2009) 1. Formål med eksperimentet og den teoretiske
Transienter og RC-kredsløb Fysik 6 Elektrodynamiske bølger Joachim Mortensen, Edin Ikanovic, Daniel Lawther 4. december 2008 (genafleveret 4. januar 2009) 1. Formål med eksperimentet og den teoretiske
3HCl + Al AlCl3 + 3H
 For at du kan løse denne opgave, og få helt styr på det med reaktionsligninger, er du nødt til at lave forløbet om Ion-bindinger først. Hvis du er færdig med det forløb, så kan du bare fortsætte. Har du
For at du kan løse denne opgave, og få helt styr på det med reaktionsligninger, er du nødt til at lave forløbet om Ion-bindinger først. Hvis du er færdig med det forløb, så kan du bare fortsætte. Har du
KEMI C. Videooversigt
 KEMI C Videooversigt Afstemning og mængdeberegning... 2 Atomer og det periodiske system... 2 Forsøgsfilm... 2 Ioner og salte... 3 Molekyler... 3 Opløsninger og tilstandsformer... 3 Organisk kemi... 3 Redoxreaktioner...
KEMI C Videooversigt Afstemning og mængdeberegning... 2 Atomer og det periodiske system... 2 Forsøgsfilm... 2 Ioner og salte... 3 Molekyler... 3 Opløsninger og tilstandsformer... 3 Organisk kemi... 3 Redoxreaktioner...
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin August 2011-maj 2013 Institution Københavns tekniske Skole - Vibenhus Uddannelse Fag og niveau Lærer(e) Hold
BROMBÆRSOLCELLEN. Øvelsesvejledning. nano-science center
 BROMBÆRSOLCELLEN Øvelsesvejledning nano-science center kø b e n h av n s u n i v e r s i t e t Farvning af titandioxid Fremstilling af kulelektroden Først skal I lave et farvestof, som titandioxidlaget
BROMBÆRSOLCELLEN Øvelsesvejledning nano-science center kø b e n h av n s u n i v e r s i t e t Farvning af titandioxid Fremstilling af kulelektroden Først skal I lave et farvestof, som titandioxidlaget
Byg selv en solcellemobiloplader
 Byg selv en solcellemobiloplader Byggevejledning til solcelle-mobilopladeren Formålet med denne aktivitet er på en lærerig, pædagogisk og kreativ måde at vise spejderne, hvordan de selv kan lave nyttige
Byg selv en solcellemobiloplader Byggevejledning til solcelle-mobilopladeren Formålet med denne aktivitet er på en lærerig, pædagogisk og kreativ måde at vise spejderne, hvordan de selv kan lave nyttige
