Plast Teknologi. Udvalgt sektion
|
|
|
- Gustav Steffensen
- 5 år siden
- Visninger:
Transkript
1 Plast Teknologi Udvalgt sektion
2 Kemisk opbygning af plast Grundstoffer, atomer, molekyler og ioner Grundstoffer Alt stof i universet er sammensat af blot ganske få elementære bestanddele. Sådanne bestanddele kaldes grundstoffer. Man kender 107 grundstoffer, som formentlig udgør hele universet, i hvert fald den kendte del af det. De 92 grundstoffer er naturligt forekommende, mens de øvrige er kunstigt fremstillet. Et grundstof er et stof, som ikke ved almindelige kemiske metoder kan spaltes og ej heller kan fremstilles ved kemiske reaktioner. Oxygen (ilt) er det grundstof, der forekommer hyppigst på Jorden. Reg net efter vægt udgør oxygen ca. 50 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af jordskorpen. Den atmosfæriske luft omkring os indeholder ca. 20 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} oxygen. Oxygen forekommer i mange kemiske forbindelser med andre grundstoffer. Vand er den mest udbredte kemiske forbindelse; i vand indgår oxygen i kemisk forbindelse med hy drogen (brint). Oxygen udgør omkring 89 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af vand. Silicium er det næsthyppigste grundstof med en andel på omkring 25 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924}. Det forekommer fx i kemisk forbindelse med oxygen i mineralet kvarts, som udgør størsteparten af strandsand. Efter hyppighed kommer dernæst metallerne aluminium med ca. 7,5 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} og jern med ca. 4,7 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924}. Hovedparten af grundstofferne er metaller; jern, kobber, zink, tin, magnesium, calcium, chrom, bly, nikkel, kviksølv, natrium og kalium er blandt de mest kendte. Guld, sølv og platin kaldes ædel metaller; de er også grundstoffer. Bronze og messing er derimod legeringer, dvs. de er sammensat af metalliske grund stoffer. Af grundstoffer, som ikke er metaller, kendes fx luftarterne helium, neon og argon. De kaldes ædelgasser, fordi de ikke kan indgå i kemisk forbindelse med andre grundstoffer. Desuden er grundstoffer som chlor, brom og jod almindeligt kendte, ligesom svovl og phosphor er det. Grundstoffet carbon (kul stof), som indgår i alt plante- og dyremateriale, udgør kun 0,1 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af jordskorpen. Nitrogen (kvælstof) udgør en forsvindende lille del af jordskorpen, selv om ca. 79 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af atmosfærisk luft er nitrogen. Størsteparten af grundstofferne forekommer kun i meget ringe mængde i naturen en gruppe kaldes ligefrem for de sjældne jordarter. 99,2 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af jord skorpen udgøres af kun 10 grundstoffer, og de resterende 0,8 {ed57bccf0ce5f844f6ce277d4451bfd9eed34e f90da10ae08f91924} af de øv rige 82. 2
3 Atomer Den mindste del af et grundstof, man kan have, kaldes et atom. Ordet er græsk og betyder udelelig, idet man dengang troede, at atomerne var udele lige. Sidenhen har man dog fundet ud af at spalte atomer, hvorved der op står andre atomer. Et atom er den mindste del af et grundstof, der kan indgå i en kemisk forbindelse. Alle kemiske forbindelser er sammensat af atomer. Forskel len mellem kemiske forbindelser er netop de deltagende atomers natur, antal og arrangement. For nemheds skyld bruger kemikerne enkelte bogstaver eller kom bina tioner af to bogstaver som symboler for de enkelte grundstoffer. Man an vender forbogstavet alene eller forbogstavet efterfulgt af et andet, karakteristisk bogstav i grundstoffets latinske navn. H, C, N, O og F er kemiske symboler for hydrogen, carbon, nitrogen, oxygen og fluor, og Na, Mg, Al, Cl, Ca, Fe, As og Pb for natrium, magnesium, aluminium, chlor, calcium, jern (latin: ferrum), arsen og bly (latin: plumbum). Molekyler Når et atom indgår i kemisk forbindelse med et andet eller andre atomer, opstår molekyler. Molekyler er sammensat af atomer, som kan være ens eller forskellige. Et molekyle er den mindste enhed af et stof, som kan eksistere alene og bevare alle stoffets egenskaber. Kemiske forbindelser Hvis der indgår forskellige atomer i et molekyle, har man en ke misk forbindelse. En kemisk forbindelse er altså et stof, der indeholder flere end ét grundstof, og som har egenskaber, der i det store og hele er forskellige fra de indgående bestanddeles egenskaber. For eksempel er oxygen og hy drogen begge luftarter, mens vand, som er en kemisk forbindelse mellem oxygen og hydrogen, er en væske. Atommodel Den traditionelle model af atomers opbygning er den såkaldte planetmodel. Pla ne terne bevæger sig om kring solen, hvis masse er mange, mange gange større end planeternes. Et atom kan på lignende måde opfattes som bestående af en kerne, hvori langt hoved parten af atomets masse er samlet, og en eller flere, meget små og meget lette partikler, der bevæger sig i én bestemt eller i flere bestemte baner uden om kernen. 3
4 Klassisk atommodel De negativt elektrisk ladede elektroner tænkes at bevæge sig i bestemte baner uden om den positivt ladede kerne. Der findes to slags kernepartikler, som er stort set lige store og med lige stor masse. Protonen har en positiv, elektrisk elementarladning og har mas sen 1 AMU (AMU = Atomic Mass Unit = atommasseenhed). Den anden kernepartikel, neutronen, har også massen 1 AMU, men er elektrisk neutral. De lette partikler, der bevæger sig omkring atomkernen, har en negativ, elektrisk elementarladning (af nøjagtig samme størrelse som protonens positive ladning); de kaldes derfor elektroner. Kemiske bindinger Når atomer forbinder sig med hinanden til molekyler eller på an den måde, sker det, ved at elektronerne arrangerer sig på særlige måder. Man kender tre forskellige typer af kemiske bindinger. Ionbindingen er baseret på elektronoverførsel, idet en eller flere elektroner skifter plads fra et atom til et andet. Derved opstår elektrisk ladede atomer, som kaldes ioner. Da positivt og negativt ladede partikler tiltrækker hinanden, vil det også ske med positive og negative ioner. De lejrer sig i velordnede gitterstrukturer og danner krystaller. Et kendt eksempel er køkkensalt, som er natriumchlorid. Ionernes placering i natrium chlorids krystalgitter 4
5 Natriumchloridskrystal Sådan udfyldes rummet af ionerne i en natriumchlorid- krystal. Alle saltene danner krystaller, som er opbygget af ioner. Metalbindingen er baseret på elektronfrigø relse, idet nogle af elek tro nerne i metallernes atomer er så løst knyttet til atomets kerne, at de i en metalkrystal ikke kan siges at tilhøre et bestemt atom. Man må snarere fore stille sig en metalkrystal som en samling tæt pakkede metalioner, hvorimellem elektronerne befinder sig overalt og på grund af deres løse tilknytning til bestemte atomer er frit bevægelige. Denne model kan forklare stoffernes metal karakter, først og fremmest deres store elektriske ledningsevne. Metalgitter Ladningstyngde punkter af ionerne i en natrium krystal. Den principielle opbygning af et metalgitter, i dette tilfælde af metallet natrium. Det ses, at metallerne danner krystaller ligesom saltene. Den tredje bindingstype kaldes den covalente binding eller atombindingen. Den covalente binding baseres på elektronfælles skab, idet et eller flere elektronpar er fælles mellem to nabo atomers kerner. 5
6 Der ved dan nes molekyler. Luftarterne oxygen (O2), hydrogen (H2), nitro gen (N2) og chlor (Cl2) består i virkeligheden ikke af atomer, men af toatomige molekyler, hvori atomerne er holdt sammen af covalente bindinger. Vand (H2O) og ammoniak (NH3) er eksempler på kemiske forbindelser af covalent bundne atomer. I polymererne er det covalente bindinger, der dominerer. Vandmolekyle Dannelsen af et vand molekyle, H2O, ud fra to hydrogenatomer og et oxygenatom Bindingskræfter De tre beskrevne bindingstyper har nogenlunde samme styrke og repræsen terer de stærkeste bindingskræfter i kemien, de såkaldte primære bindingskræfter. De virker, som det fremgår af det foregående, mellem atomer og ioner ved at holde dem sammen i molekyler, atomgitre og iongitre. Der optræder imidlertid også bindingskræfter mellem de enkelte mo lekyler. Det er fx dem, der ved en temperatur under 100 C holder vand molekyler sammen til flydende vand og under 0 C til is. De er meget sva gere end de primære bindinger og kaldes sekundære bindingskræfter. De primære bindinger er ca. 30 gange så stærke som de sekundære bindinger. Organiske stoffers opbygning Carbon er et karakteristisk ek sempel på et grundstof, der danner covalente bindinger. Fire af carbonatomets elektroner kan ved par ring med elektroner fra op til fire andre atomer indgå i covalente bindinger. Ved forbindelse med fire hydrogenatomer opstår stoffet methan (CH4), som er en luftart og udgør hoved parten af naturgas. Carbonatomer har en sær lig evne til at forbinde sig med hinanden i lange rækker. Til stoffet methan svarer en række stoffer med 2, 3 osv. carbonatomer i række. De fire første stoffer er luftarter, de næste er væsker ved stue tem peratur. Derefter bliver stofferne mere og mere tungtflygtige og til sidst faste, jo længere molekylerne bliver. Når der bliver rigtigt mange carbonatomer i række, fx 1.000, har vi stoffet polyethylen, den plast, der har den enkleste opbygning. 6
7 Methan, ethan, propan osv. Afhængig af hvor mange carbonatomer, der sidder i række fås en mængde forskellige stoffer hvor det simpleste er gassen methan og hvor polyethylen er en polymer (plast) Der består således et nært slægtskab mellem plastpolymererne dog især poly ethylen og polypropylen og stoffer i ovennævnte række. Bindingerne mellem carbonatomerne i stofferne i denne række er en keltbindinger. Der findes imidlertid også lignende stoffer, hvori der forekommer dobbeltbindinger mellem carbonatomer. Enkeltbindin ger dannes af ét par elektroner, én elektron fra hvert af naboatomerne; mens dob belt bindinger dannes af to elektronpar, to elektroner fra hvert af naboatomerne. Carbon-carbon dobbeltbindinger Det enkleste stof med en carbon-carbon-dobbeltbinding er ethylen. Også med en dobbeltbinding i molekylet kan der hægtes flere carbonatomer i række. 7
8 Forbindelser med flere dobbeltbindinger forekommer også, fx butadien. Tredobbelt bin dinger dannet af tre elektronpar forekommer også. Det enkleste stof med en tredobbeltbinding mellem to carbon atomer er acetylen. Acetylen Det her beskrevne er grundlaget for hele den organiske kemi og dermed også for polymer- og plastkemien. Forbindelser, der udelukkende indeholder enkeltbindinger mel lem carbonatomerne, kaldes mættede, mens blot en en-kelt dobbelt- eller tredobbeltbinding gør stoffet til en umættet forbindelse. Højmolekylære stoffer Adskillige af de højmolekylære stoffer er desuden polymerer eller højpolymerer. Ordet er græsk og kommer af poly (= mange) og mer (= del). Beteg nel sen bruges om stoffer, hvis molekyler er sammensat af et stort antal ens dele eller enheder. 8
9 Polyethylen Polyethylen er opbygget ved sammen sætning af et stort antal ethylenmolekyler. Ethylgruppen Repetitionsenheden i polyethylen er ethylgruppen. Hvis der fx går ethylenmolekyler til et polyethylen-molekyle, er polymerisationsgraden De stoffer, som polymerer fremstilles af, benævnes monomerer. Til en bestemt polymer svarer altså en bestemt monomer eller eventuelt flere be stemte monomerer. Den monomer, der svarer til polyethylen, er ethylen. Den enhed, der gentages i et polymermolekyle, kaldes en repetitionsenhed, og antallet af repetitionsenheder i et molekyle kaldes molekylets polymerisationsgrad. Repetitionsenheden i polyethylen er ethylgruppen. Hvis der fx går ethylenmolekyler til et polyethylen-molekyle, er polymerisationsgraden Højpolymerers molekyler kaldes ofte for kædemolekyler, fordi de kan minde om lange kæder med ens led. Adskillige af de højmolekylære stoffer, der forekommer i natu ren, er også højpolymere, fx plantefibre, uld, silke og cellulose. Højpolymerer Polymerisation Processer, hvorved der, som beskrevet i det foregående, dannes polymerer ud fra én eller flere monomerer, kaldes polymerisations processer. 9
10 Hvorledes de i naturen forekommende højpolymere forbindel ser dannes, har man ofte kun en vag formodning om. Derimod er mekanismerne i de syntetiske polymerisationsprocesser veldokumenteret. Kun nogle få plastmaterialer er baseret på polymerer, der fore kommer i naturen, fx celluloseplast og kaseinplast. De øvrige er polymeriseret syntetisk, dvs. af mennesket. Polymerisation kan foregå med én eller flere forskellige mono merer som udgangsstoffer og med eller uden dannelse af biprodukter foruden den polymere, som er hovedproduktet. For at en monomer kan polymerisere, må dens kemiske natur være sådan, at molekylet kan reagere med mindst to andre mole kyler. Hermed er der mulighed for, at molekylvæksten kan ske i mindst to retninger principielt i det uendelige. Polymerisationsprocesserne falder naturligt i to hovedgrupper: additions polymerisation eller polyaddition, hvor der ikke dannes biprodukter, og kondensationspolymerisation eller polykondensation, hvor der fraspaltes biprodukter. Additionspolymerisation Additionspolymerisation eller polyaddition baseres på det forhold, at visse stoffer blot ved tilførsel af tilstrækkelig mængde energi kan bringes i en tilstand, hvor stoffets molekyler indgår kemisk forbindelse med hinanden under dannelse af polymere molekyler uden dannelse af biprodukter. Umættede forbindelser, altså forbindelser med mindst én dob beltbin ding, vil have en almindelig tendens til at polymerisere ved polyaddition. Dannelsen af polyethylen er et typisk eksempel. 10
11 Dannelse af polyethylen ved additionspolymerisation Ved tilførsel af energi kan monomeren bringes i en tilstand, hvor stoffets molekyler indgår kemisk forbindelse med hinanden og danner polymere Af de almindelige plastmaterialer er også polypropylen, polyvinyl chlorid (PVC), polystyren, acrylplast og polyoxymethylen produkter af en polyadditionsproces. Hvis to eller flere forskellige, umættede monomerer blandes sammen, kan de undertiden indgå forbindelse med hinanden, således at molekyler af begge monomerer indgår i det polymere produkt. Sådanne produkter kaldes copolymerer, og processen kaldes copolymerisation. Slagfast polystyren er et sådant eksempel, hvor styren og butadien begge indgår i det polymere produkt. Slagfast polystyren Copolymerisation af to umættede monomerer, her, styren og butadien. Slagfast polystyren er et sådant eksempel, hvor butadiengruppen gør materialet slagfast. Styren-acrylnitril-copolymer (SAN) og ABS er andre eksempler. 11
12 Polyaddition kan også foregå mellem to stoffer, der ikke begge har dobbeltbindinger, hvis det ene fx indeholder to dobbeltbindinger, som begge kan brydes under processen under reak tion med atomgrupper i det andet stof. Herved kan der ske overflytning af et hydrogenatom fra det ene stof til det andet under dannelse af en polymer uden fraspalt ning af biprodukter. Dannelse af polyurethan ud fra en di-isocyanat og en glykol er et eksempel herpå. Dannelsen af polyurethan ved polyaddition Her sker overflytning af et hydrogenatom fra di-isocyanaten til glykolen under dannelse af en polymer uden fraspaltning af biprodukter. Desuden kan en række ringformede molekyler polymerisere ved addition, selvom de ingen dobbeltbinding indeholder. Ved brud af en enkeltbinding åbnes ringen, uden at der derved sker et fuld stændigt brud af molekylets indre sammenhæng. Der dannes to frie bindinger, således at molekylet i begge ender kan reagere med et andet molekyle af samme slags. Polya mid 6 er et eksempel på et polyadditionsprodukt, der er dannet ud fra en ringformet monomer, nemlig stoffet ε-caprolactam (ε = epsilon). 12
13 Polya mid 6 Polyamid 6 er dannet ud fra en ringformet monomer, nemlig stoffet ε-caprolactam Kondensationspolymerisation Kondensationspolymerisation eller polykondensation er den anden type polymerisationsproces. Den bygger på almindelig kemisk reaktion mellem to kemiske forbindelser. Fx vil en hvilken som helst syre og en hvilken som helst alkohol reagere med hinanden under dannelse af en ester og samtidig fraspaltning af vand. Kondensationspolymerisation I sin simpleste form er kondensationspolymerisation reaktionen mellem syre og alkohol. Det danner en ester og fraspalter vand. Hvis man blander en dibasisk syre, dvs. en syre, som indeholder to syregrupper, med en divalent alkohol, dvs. en alkohol med to alkoholgrupper, kan der som en kædereaktion dannes esterbindinger i begge 13
14 ender af begge mono mer molekyler. For hver ester binding, der dannes, dannes samtidig et molekyle vand. Den række af polyamider, der betegnes med to tal, fx PA 6.6 og PA 6.10, dannes på tilsvarende måde ud fra en dibasisk syre og en diamin (et stof med to amingrupper: NH2). Kondensationpolymerisation af polyester Polyester dannes ved kondensationpolymerisation af dibasisk syre og divalent alkohol under fraspaltning af vand Fremstilling af polyamider Polyamider dannes ud fra en dibasisk syre og en diamin (et stof med to amingrupper: NH2). Ved polykondensation kan der ud fra en trifunktionel forbindelse, dvs. stof med tre reaktive atomgrupper, dannes tredimensionale polymerer med en netværksstruktur, som er karakteristisk for de såkaldte hærde plast. Dannel sen af phenolplast ud fra phenol og formaldehyd er et eksempel (se formel nederst på siden). 14
15 15
16 Dannelse af Phenolplast Dannelsen af phenolplast ud fra phenol og formaldehyd I phenolmolekylet er de tre markerede hydrogenatomer meget reaktionsvillige. Det fraspaltede vandmolekyle dannes ud fra oxygenatomet fra formaldehydmolekylet og et hydrogenatom fra hvert af to phenolmolekyler. Flere bindinger vil dannes ved de øvrige, markerede hydrogenatomer med en netværksstruktur til følge. Phenolplast struktur Principiel strukturformel for phenolplast 16
17 161717
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Atomets bestanddele. Indledning. Atomer. Atomets bestanddele
 Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Plast Teknologi. Hele bogen
 Plast Teknologi Hele bogen Plastmaterialernes historie De første plasttyper En plastfabrik i 1947 Arteka Formstof A/S Det første plastmateriale, der fik kommerciel betydning, var cellu loid, som er cellulosenitrat,
Plast Teknologi Hele bogen Plastmaterialernes historie De første plasttyper En plastfabrik i 1947 Arteka Formstof A/S Det første plastmateriale, der fik kommerciel betydning, var cellu loid, som er cellulosenitrat,
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Vikar-Guide. Den elektriske ladning af en elektron er -1 elementarladning, og den elektriske ladning af protonen er +1 elementarladning.
 Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Opgave: Du skal udfylde de manglende felter ud fra den information der er givet
 pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
Kemiske bindinger. Præsentation: Niveau: 8. klasse. Varighed: 7 lektioner
 Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Lim mellem atomerne Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør. Spørgsmål 1. Grundstoffer og det periodiske system
 EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
EKSAMENSSPØRGSMÅL Kemi C december 2016 Helsingør Øvelse: Opløsningsmidlers egenskaber Spørgsmål 1 Grundstoffer og det periodiske system Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Oxidationstal og elektronparbindinger December 2015
 idationstal og elektronparbindinger December 2015 idationstal og elektronparbindinger I redokemi findes en række simple regler, som gør det muligt at bestemme oidationstal for et atom i en kemisk forbindelse,
idationstal og elektronparbindinger December 2015 idationstal og elektronparbindinger I redokemi findes en række simple regler, som gør det muligt at bestemme oidationstal for et atom i en kemisk forbindelse,
Nr. 6-2007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 2008
 Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
VEUD ekstraopgave Opgave nr. 60-10
 Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 45 spørgsmål til termoplast. Introduktion til termoplast. 4 lektioner Niveau, sammenlignet med uddannelsen: Henvisning til hjælpemidler:
Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 45 spørgsmål til termoplast. Introduktion til termoplast. 4 lektioner Niveau, sammenlignet med uddannelsen: Henvisning til hjælpemidler:
Eksamensopgaverne offentliggøres selvfølgelig med det forbehold, at censor kan komme med ændringsforslag.
 VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
VUC Århus, 17. maj. 2011 Kære alle kursister på holdene ke02da1c (kemi C flex, helårsholdet) og ke05da1c (kemi C flex, halvårsholdet) På de næste mange sider vil I kunne se Jeres kommende eksamensopgaver
Jordens salte Ny Prisma Fysik og kemi 9 - kapitel 2 Skole: Navn: Klasse:
 Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Torben Rosenørn. Aalborg Universitet. Campus Esbjerg
 Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
6.3 Polyvinylchlorid (PVC) 145. 6.4 Polyvinylidenchlorid (PVDC) 151. 6.5 Polymethylmethacrylat (PMMA) 152. 6.8 Polyoxymethylen (POM) 161
 6.2 Styrenplast........................................... 13: 6.2.1 Polystyren (PS) 13: 6.2.2 Slagfast polystyren (SB) 137 6.2.3 Polystyrenacrylnitril (SAN) 139 6.2.4 ABS 141 6.2.5 Andre styrenbaserede
6.2 Styrenplast........................................... 13: 6.2.1 Polystyren (PS) 13: 6.2.2 Slagfast polystyren (SB) 137 6.2.3 Polystyrenacrylnitril (SAN) 139 6.2.4 ABS 141 6.2.5 Andre styrenbaserede
Fysik og kemi i 8. klasse
 Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Med forbehold for censors kommentarer. Eksamensspørgsmål Kemi C, 2014, Kec223 (NB).
 Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
Med forbehold for censors kommentarer Eksamensspørgsmål Kemi C, 2014, Kec223 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017
 EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
EKSAMENSSPØRGSMÅL Kemi C maj/juni 2017 Titler på eksamensspørgsmål 1. Grundstoffer og det periodiske system 2. Spændingsrækken 3. Elektronparbindinger 4. Bindingstyper 5. Saltes opløselighed i vand 6.
VEUD ekstraopgave Opgave nr. 61-10
 Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 50 spørgsmål til materialelære. Termoplast, materialelære. 4 lektioner Niveau, sammenlignet med uddannelsen: envisning til hjælpemidler:
Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 50 spørgsmål til materialelære. Termoplast, materialelære. 4 lektioner Niveau, sammenlignet med uddannelsen: envisning til hjælpemidler:
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10
 NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
Oversigt med forklaring over forskellige begreber
 Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Oversigt med forklaring over forskellige begreber fra www.michaelfynsk.dk Til dette dokument tilhører en mappe med filer bl.a..exe-,.pdf- og.jpg-filer. Side 1 af 19 Indholdsfortegnelse Brintbinding (hydrogenbinding)
Folkeskolens afgangsprøve Maj-juni 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2017, Kec126 (NB). Med forbehold for censors godkendelse 1 Stoffers blandbarhed og det periodiske system 2 Stoffers blandbarhed og elektronparbindingen 3 Redoxreaktioner, spændingsrækken
Atomets opbygning. Keminote 2010
 Atomets opbygning Oprindelig forestillede man sig, at atomet var en lille kugle, som ikke kunne deles i mindre dele. Ordet atom kommer af det græske ord atomos, som betyder udelelig. Fra slutningen af
Atomets opbygning Oprindelig forestillede man sig, at atomet var en lille kugle, som ikke kunne deles i mindre dele. Ordet atom kommer af det græske ord atomos, som betyder udelelig. Fra slutningen af
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB).
 Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensspørgsmål Kemi C, 2015, Kec124 (NB). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, spændingsrækken
Eksamensopgaver. NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL
 Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Eksamensopgaver NF Kemi C DER KAN OPSTÅ ÆNDRINGER I DE ENDELIGE SPØRGSMÅL Liste over eksamensøvelser 1. Opløsningsmidlers egenskaber 2. Fældningsreaktioner 3. Påvisning af proteiner 4. Fremstilling af
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole)
 Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole) Har du nogensinde tænkt på, hvordan jorden, solen og hele universet er skabt? Det er måske et af de vigtigste spørgsmål, man forsøger
Big Bang og universets skabelse (af Jeanette Hansen, Toftlund Skole) Har du nogensinde tænkt på, hvordan jorden, solen og hele universet er skabt? Det er måske et af de vigtigste spørgsmål, man forsøger
Intra- og intermolekylære bindinger.
 Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse
 Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Eksamensspørgsmål Kemi C, 2017, Kec196 (NB). Med forbehold for censors godkendelse Da nogle har deltaget i laboratoriekursus i Aarhus og andre i Esbjerg, er der henvist til øvelser de to steder fra. Man
Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse:
 Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse: Opgave 1 Gasserne nitrogen, oxygen og kuldioxid er de gasser i Jordens atmosfære, der er vigtigst for livet. Angiv hvilke
Der er noget i luften Ny Prisma Fysik og kemi 9 - kapitel 6 Skole: Navn: Klasse: Opgave 1 Gasserne nitrogen, oxygen og kuldioxid er de gasser i Jordens atmosfære, der er vigtigst for livet. Angiv hvilke
Relativ massefylde. H3bli0102 Aalborg tekniske skole. Relativ massefylde H3bli0102 1
 Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
 Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Elevens uni-login: Skolens navn: Tilsynsførendes underskrift: FP9. 9.-klasseprøven FYSIK/KEMI
 Elevens uni-login: Skolens navn: Tilsynsførendes underskrift: FP9 9.-klasseprøven FYSIK/KEMI December 2016 Indledning Plast Fotoet viser genstande fra hverdagen, der indeholder plast. Foto: Lars Henrik
Elevens uni-login: Skolens navn: Tilsynsførendes underskrift: FP9 9.-klasseprøven FYSIK/KEMI December 2016 Indledning Plast Fotoet viser genstande fra hverdagen, der indeholder plast. Foto: Lars Henrik
DET PERIODISKE SYSTEM
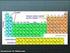 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Mundtlige eksamensopgaver
 Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
Mundtlige eksamensopgaver Kemi C 3ckecmh11308 Grundstoffer og det periodiske system Øvelse: Kobber + dibrom Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Grundstofferne er ordnet
En lille verden Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD).
 Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
Eksamensspørgsmål Kemi C, 2016, Kec225 (KSD). 1 Molekylmodeller og det periodiske system 2 Molekylmodeller og elektronparbindingen 3 Molekylmodeller og organiske stoffer 4 Redoxreaktioner, ph 5 Redoxreaktioner,
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug 2014- dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold Flex-kemi C Kemi C Mohammed
Fyldt med energi Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Fyldt med energi Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Grønne planter bruger vand og kuldioxid til at producere oxygen og opbygge organiske stoffer ved fotosyntese. Sæt kryds ved det
Fyldt med energi Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Grønne planter bruger vand og kuldioxid til at producere oxygen og opbygge organiske stoffer ved fotosyntese. Sæt kryds ved det
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Sommereksamen 2013 VUF - Voksenuddannelsescenter Frederiksberg
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Hold Sommereksamen 2013 VUF - Voksenuddannelsescenter Frederiksberg
1 Atomets opbygning. Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom.
 1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
1 Atomets opbygning Du skal fortælle om det periodiske system og atomets opbygning. Inddrag eksperimentet Reaktionen mellem kobber og dibrom. Kernepartikler og elektronstruktur Periodisk system - hovedgrupper
Lokalenhed Storstrøm (STO). Bilagsoversigt.
 Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Midtjylland (MJL). Bilagsoversigt.
 Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen
 Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
Nedenstående spørgsmål er med forbehold for censors godkendelse Spørgsmål 1 Molekyler Eksempler fra hverdagen Der ønskes en gennemgang af udvalgte molekylers opbygning, samt deres betydning i hverdagen.
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Fyn (FYN). Bilagsoversigt.
 Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Eksamensspørgsma l kemi C, 2015, kec324 (CHT)
 Oversigt Sp. 1 og 2 Ioner og Ionforbindelser Sp. 3, 4 og 5 Molekylforbindelser Sp. 6 Kemisk mængdeberegning Sp. 7 Koncentration i en opløsning Sp. 8 og 9 Organisk kemi Sp. 10 og 11 Syrer og baser Sp. 12
Oversigt Sp. 1 og 2 Ioner og Ionforbindelser Sp. 3, 4 og 5 Molekylforbindelser Sp. 6 Kemisk mængdeberegning Sp. 7 Koncentration i en opløsning Sp. 8 og 9 Organisk kemi Sp. 10 og 11 Syrer og baser Sp. 12
Lokalenhed Sjælland (SJL). Bilagsoversigt.
 Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Læringsmål i fysik - 9. Klasse
 Læringsmål i fysik - 9. Klasse Salte, syrer og baser Jeg ved salt er et stof der er opbygget af ioner. Jeg ved at Ioner i salt sidder i et fast mønster, et iongitter Jeg kan vise og forklare at salt, der
Læringsmål i fysik - 9. Klasse Salte, syrer og baser Jeg ved salt er et stof der er opbygget af ioner. Jeg ved at Ioner i salt sidder i et fast mønster, et iongitter Jeg kan vise og forklare at salt, der
1 Ioner og ionforbindelser
 1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1 Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes, så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin jan 2019 juni 2019 Institution Rybners tekniske skole Uddannelse Fag og niveau Lærer(e) Hold EUX elektrikere
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin jan 2019 juni 2019 Institution Rybners tekniske skole Uddannelse Fag og niveau Lærer(e) Hold EUX elektrikere
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Forløbet består af 7 fagtekster, 12 opgaver, tip en 12 er, 5 praktiske aktiviteter, flere kemi-sudokuer og en mindre skriftlig elevopgave.
 Atomer og molekyler Niveau: 7. klasse Varighed: 7 lektioner Præsentation: I forløbet Atomer og molekyler arbejdes der med helt grundlæggende kemiske begreber omkring stofopbygning, derfor bør temaet placeres
Atomer og molekyler Niveau: 7. klasse Varighed: 7 lektioner Præsentation: I forløbet Atomer og molekyler arbejdes der med helt grundlæggende kemiske begreber omkring stofopbygning, derfor bør temaet placeres
m: masse i masseprocent : indhold i volumenprocent : indhold
 Kemisk formelsamling (C-niveau s kernestof samt en del formler, der hører hjemme på Kemi B ) Mængdeberegninger m: masse M: molar masse n : stofmængde : volumen ρ : densitet (massetæthed) c : koncentration
Kemisk formelsamling (C-niveau s kernestof samt en del formler, der hører hjemme på Kemi B ) Mængdeberegninger m: masse M: molar masse n : stofmængde : volumen ρ : densitet (massetæthed) c : koncentration
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin januar 2017 Institution HF & VUC København Syd Uddannelse Fag og niveau Lærer(e) Hold e-learningskemi C Kemi
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Hvilket salt i hvilken beholder Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen
Fysikforløb nr. 6. Atomfysik
 Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Aug-dec 2014 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfag Kemi C Mohammed
Opgave 13 Neutraliser en syre/base + dannelse af køkkensalt
 Emne: Syrer og baser Hvad er en syre: En syrer vil altid have en PH værdi på 7 og nedefter. Altså er 1 stærkest og 6 svagest. Ph- værdi 7 er neutral. Syre kan ikke ætse gennem hud, men igennem materielle
Emne: Syrer og baser Hvad er en syre: En syrer vil altid have en PH værdi på 7 og nedefter. Altså er 1 stærkest og 6 svagest. Ph- værdi 7 er neutral. Syre kan ikke ætse gennem hud, men igennem materielle
1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation
 Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Overskrifter til kemispørgsmål, Kemi C 2012 1. Grundstoffer i mennesket og opbygningen af grundstoffernes periodesystem, herunder gennemgang af eksperimentet: Neutralisation 2. Grundstoffer i mennesket
Forord. Undervisere kan bruge arket ved først at kontakte pierre@naae.dk og få et skriftligt tilsagn.
 Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Forord Dette hjælpeark til mol og molberegninger er lavet af til brug på Nørre Åby Efterskole. Man er som studerende/elev meget velkommen til at hente og bruge arket. Undervisere kan bruge arket ved først
Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på:
 1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
1. Molekyler Redegør for opbygningen af uorganiske molekyler. Kom bl.a. ind på: Elektronparbinding (= kovalent binding) Oktetreglen/ædelgasreglen Polaritet Hydrofile og hydrofobe grupper Navngivning af
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Folkeskolens afgangsprøve Maj 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj 2006 1/26 Fk4 Opgave 1 / 20 (Opgaven tæller 5 %) I sin kemibog ser Per denne tegning, som er en model. Hvad forestiller tegningen? Der er 6 svarmuligheder. Sæt 1 kryds Et
Folkeskolens afgangsprøve Maj 2006 1/26 Fk4 Opgave 1 / 20 (Opgaven tæller 5 %) I sin kemibog ser Per denne tegning, som er en model. Hvad forestiller tegningen? Der er 6 svarmuligheder. Sæt 1 kryds Et
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Termin hvori undervisningen afsluttes: maj-juni 2011 Københavns Tekniske
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Grundstoffer og det periodiske system
 Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Spørgsmål 1 Grundstoffer og det periodiske system Øvelse: Flammefarver Gør rede for inddelingen i grupper (hovedgrupperne) og perioder i det periodiske system. Kom herunder ind på opbygningen af et atom
Molekyler & Mere Godt Kemi
 Molekyler & Mere Godt Kemi Elektronparbindinger Molekylgeometri Elektronegativitet Ethanol Buchminster Fulleren Carbondioid Asbest influenza vaccine Diamant Indhold. 1. Molekyler og Kovalente Bindinger....
Molekyler & Mere Godt Kemi Elektronparbindinger Molekylgeometri Elektronegativitet Ethanol Buchminster Fulleren Carbondioid Asbest influenza vaccine Diamant Indhold. 1. Molekyler og Kovalente Bindinger....
Syrer, baser og salte
 Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Molekyler Atomer danner molekyler (kovalente bindinger) ved at dele deres elektroner i yderste elektronskal. Dette sker for at opnå en stabil tilstand. En stabil tilstand er når molekylerne på nogle tidspunkter
Du skal også komme ind på øvelsen Saltes opløselighed i vand.
 1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
1. Ioner og ionforbindelser Du skal fortælle om, hvordan ioner kan dannes så de får samme elektronstruktur som ædelgasser, og hvordan ionforbindelser (salte) dannes ud fra positive og negative ioner. Du
Naturfag. Supplerende materiale. 5. udgave
 Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Brombærsolcellen - introduktion
 #0 Brombærsolcellen - introduktion Solceller i lommeregneren, solceller på hustagene, solceller til mobiltelefonen eller solceller til den bærbare computer midt ude i regnskoven- Solcellen har i mange
#0 Brombærsolcellen - introduktion Solceller i lommeregneren, solceller på hustagene, solceller til mobiltelefonen eller solceller til den bærbare computer midt ude i regnskoven- Solcellen har i mange
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE
 Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års hold Termin: Juni 2014 Uddannelse: HF-enkeltfag
Undervisningsbeskrivelse for: 1kec14J 0813 Kemi C, HFE Fag: Kemi C, HFE Niveau: C Institution: HF og VUC Fredericia (607247) Hold: Kemi C enkeltfag ½ års hold Termin: Juni 2014 Uddannelse: HF-enkeltfag
Årsplan i Fysik 7.klasse. 2018/2019 Abdiaziz Farah
 Årsplan i Fysik 7.klasse. 2018/2019 Abdiaziz Farah Klassen arbejder med 7 hovedemner: 1) Vi arbejder med fysik og kemi 2) Stofs egenskaber 3) Grundstoffer og kemiske forbindelser 4) luft 5) Lyd og Lys
Årsplan i Fysik 7.klasse. 2018/2019 Abdiaziz Farah Klassen arbejder med 7 hovedemner: 1) Vi arbejder med fysik og kemi 2) Stofs egenskaber 3) Grundstoffer og kemiske forbindelser 4) luft 5) Lyd og Lys
A.1. FORORD... 3 A.2. MOLEKYLER OG ATOMER A.2.1. Blandinger og rene stoffer A.2.2. Molekyler A.2.3. Atomer... 3
 Indholdsfortegnelse A.1. FORORD.... 3 A.2. MOLEKYLER OG ATOMER.... 3 A.2.1. Blandinger og rene stoffer.... 3 A.2.2. Molekyler.... 3 A.2.3. Atomer.... 3 A.3. ATOMETS OPBYGNING.... 5 A.3.1. Elementarpartikler....
Indholdsfortegnelse A.1. FORORD.... 3 A.2. MOLEKYLER OG ATOMER.... 3 A.2.1. Blandinger og rene stoffer.... 3 A.2.2. Molekyler.... 3 A.2.3. Atomer.... 3 A.3. ATOMETS OPBYGNING.... 5 A.3.1. Elementarpartikler....
KORT SUMMARISK GENNEMGANG AF KEMIEN 2013.
 COPYRIGHT NIELS NORDHOLT 2000-2013 S. 1 KORT SUMMARISK GENNEMGANG AF KEMIEN 2013. Sætning, reaktion eller kort forsøgsbeskrivelse Ved en fysisk forandring omdannes stoffer ikke til andre stoffer. Ved en
COPYRIGHT NIELS NORDHOLT 2000-2013 S. 1 KORT SUMMARISK GENNEMGANG AF KEMIEN 2013. Sætning, reaktion eller kort forsøgsbeskrivelse Ved en fysisk forandring omdannes stoffer ikke til andre stoffer. Ved en
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Efterår 2015 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfagshold Kemi C Monikka
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Efterår 2015 Institution VUC Hvidovre Uddannelse Fag og niveau Lærer(e) Hold HF enkeltfagshold Kemi C Monikka
Årsplan Fysik/kemi 8. kl.
 Årsplan Fysik/kemi 8. kl. Undervisningen foregår som en vekselvirkning mellem teori og praksis. Undervisningen knytter an ved de iagttagelser eleverne har gjort, eller kan gøre sig, i deres dagligdag.
Årsplan Fysik/kemi 8. kl. Undervisningen foregår som en vekselvirkning mellem teori og praksis. Undervisningen knytter an ved de iagttagelser eleverne har gjort, eller kan gøre sig, i deres dagligdag.
VEUD ekstraopgave Opgave nr. 62-20
 Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 41 spørgsmål til maskiner & udstyr, materialelære og 6 regneopgaver. Sprøjtestøbning. 4 lektioner Niveau, sammenlignet med uddannelsen:
Opgavens art: Opgaveformulering: Fagområde: Opgavens varighed: Teoretisk. 41 spørgsmål til maskiner & udstyr, materialelære og 6 regneopgaver. Sprøjtestøbning. 4 lektioner Niveau, sammenlignet med uddannelsen:
Syrer, baser og salte:
 Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Spørgsmål 1. Øvelse: Kobber plus dibrom. Teori: Atomers opbygning.
 Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af ioner og
Spørgsmål 1. Øvelse: Kobber plus dibrom. Atomers opbygning. Atomets struktur. Det periodiske system. Betydning af hovedgrupperne. Ædelgassernes elektronstruktur i den yderste skal. Dannelse af ioner og
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Fredericia HF og VUC Uddannelse Fag og niveau Lærer(e) Hold HF Kemi C Thomas Nielsen
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Maj-juni 2015 Institution Fredericia HF og VUC Uddannelse Fag og niveau Lærer(e) Hold HF Kemi C Thomas Nielsen
1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas
 Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Eksamensspørgsmål revideret 7/6 NW 1. Atomteorien - samt øvelsen: Best af molarmasse for lightergas Bilag: Det periodisk system. Du skal fortælle om atomets opbygning, om isotoper og naturligvis om begrebet
Metallernes kemi. Præsentation: Niveau: 8. klasse. Varighed: 6 lektioner
 Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
Undervisningsbeskrivelse
 Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Undervisningsbeskrivelse Stamoplysninger til brug ved prøver til gymnasiale uddannelser Termin Institution Uddannelse Fag og niveau Lærer(e) Termin hvori undervisningen afsluttes: maj-juni 2010 Københavns
Opgave 2a.01 Cellers opbygning. Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten
 Opgave 2a.01 Cellers opbygning Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten Vakuole - Lager-rum med energi Grønkorn Cellekerne (DNA) Cellemembran Cellevæg Mitokondrier 1. Hvad
Opgave 2a.01 Cellers opbygning Spørgsmålene her kan besvares ved at læse teksten Cellen livets byggesten Vakuole - Lager-rum med energi Grønkorn Cellekerne (DNA) Cellemembran Cellevæg Mitokondrier 1. Hvad
KEMI Vigtig baggrundsviden for biologer
 KEMI Vigtig baggrundsviden for biologer af Niels Roholt Århus Akademi 1994 For at forstå, hvordan en levende organisme fungerer, må man vide noget om sammensætningen af stofferne i protoplasma og de ændringer,
KEMI Vigtig baggrundsviden for biologer af Niels Roholt Århus Akademi 1994 For at forstå, hvordan en levende organisme fungerer, må man vide noget om sammensætningen af stofferne i protoplasma og de ændringer,
Stofegenskaber. Tryk og opdrift Elektricitet. Start på kemi
 KOSMOS A KOSMOS B Færdigheds- og vidensmål Start på fysik Stofegenskaber Tryk og opdrift Elektricitet Start på kemi Stoffer i hverdagen Grundstoffer og kemiske forbindelser Ild Sol, Måne og stjerner Magnetisme
KOSMOS A KOSMOS B Færdigheds- og vidensmål Start på fysik Stofegenskaber Tryk og opdrift Elektricitet Start på kemi Stoffer i hverdagen Grundstoffer og kemiske forbindelser Ild Sol, Måne og stjerner Magnetisme
