MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
|
|
|
- Clara Hald
- 7 år siden
- Visninger:
Transkript
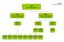
1 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S Lægemiddelstyrelsen Den 15. juni Axel Heides Gade København S Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A04, Antiemetika og midler mod kvalme, samt A03FA, Peristaltikfremmende midler Baggrund og indhold Lægemiddelstyrelsen har som led i revurderingsprocessen anmodet Medicintilskudsnævnet om at revurdere tilskudsstatus for lægemidler i ATC-gruppe A04, Antiemetika og midler mod kvalme. Nævnet finder det hensigtsmæssigt samtidig at revudere tilskudsstatus for lægemidler i ATC-gruppe A03FA, Peristaltikfremmende midler, da disse lægemidler også anvendes mod kvalme og opkastning. Indstillingen omfatter alle lægemidler i de nævnte ATC-grupper, der er godkendt til markedsføring i Danmark og for hvilke, der per den 4. maj 2009 er eller har været anmeldt en pris til Lægemiddelstyrelsen. Indstillingen omfatter dog ikke lægemidler godkendt med begrænset udlevering ( BEGR og AP4BG ), naturlægemidler, stærke vitamin- og mineralpræparater og radioaktive lægemidler. Bilag A er en grafisk oversigt over stofferne i de nævnte ATC-grupper. Fosaprepitant (A04A) og palonosatron (A04AA05) er begrænset til udlevering til sygehuse og er derfor ikke medtaget i indstillingen. Scopolamin (A04AD01) anvendes mod transportsyge og er heller ikke medtaget her. Scopolamins tilskudsstatus vil blive revurderet sammen med midler mod transportsyge, R06A. Nedenfor følger først Medicintilskudsnævnets indstilling til lægemidlernes fremtidige tilskudsstatus, derefter en kort gennemgang af revurderingsforløbet, lægemidlernes indikationer og anvendelse, forbrug samt nævnets synspunkter og begrundelser i relation til lægemidlerne og indstillingen. Bilag B er en oversigt over lægemiddelstoffer og lægemidler i ATC-gruppe A04, Antiemetika og midler mod kvalme, samt A03FA, Peristaltikfremmende midler med angivelse af den godkendte indikation for det lægemiddel med indhold af det pågældende stof, der har været godkendt længst, udleveringsgruppe, gældende tilskudsstatus, behandlingspris per døgn, forbrug og oplysninger om enkelttilskud (1). Medicintilskudsnævnets indstilling Medicintilskudsnævnet indstiller følgende til Lægemiddelstyrelsen: 1
2 1. Samtlige lægemidler i ATC-gruppe A04 (Antiemetika og midler mod kvalme) med indhold af enkeltstofferne: ondansetron (A04AA01), granisetron (A04AA02), tropisetron (A04AA03), aprepitant (A04AD12) bevarer gældende tilskudsstatus - ikke generelt tilskud. 2. Perorale lægemidler i ATC-gruppe A03FA (Peristaltikfremmende midler) med indhold af enkeltstofferne: metoclopramid (A03FA01) i lægemiddelformerne tabletter og hårde depotkapsler, og domperidon (A03FA03) i lægemiddelformen tabletter ændrer tilskudsstatus fra ikke generelt tilskud til generelt tilskud. 3. Perorale lægemidler i ATC-gruppe A03FA (Peristaltikfremmende midler) med indhold af enkeltstoffet: metoclopramid (A03FA01)i lægemiddelformen oral opløsning bevarer gældende tilskudsstatus - ikke generelt tilskud. 4. Samtlige ikke perorale lægemidler i ATC-gruppe A03FA (Peristaltikfremmende midler) med indhold af enkeltstofferne: metoclopramid (A03FA01) i lægemiddelformerne suppositorier og injektionsvæske, og domperidon (A03FA03) i lægemiddelformen suppositorier. bevarer gældende tilskudsstatus - generelt tilskud. Revurderingsforløb Lægemiddelstyrelsen orienterede i brev af 13. juni 2005 samtlige virksomheder med markedsføringstilladelse til humane lægemidler 1 om, at man ville indlede revurderingsprocessen med at revurdere tilskudsstatus for lægemidler i ATC-grupperne A, C og J. Den 29. november 2006 orienterede Lægemiddelstyrelsen om, at man i starten af 2007 ville begynde revurderingen af ATC-gruppe A, Fordøjelsesorganer og stofskifte, herunder ATC-grupperne A04 og A03. Medicintilskudsnævnet har drøftet tilskudsstatus for lægemidler i ATC-gruppe A04 på sine møder den 16. januar 2007, den 20. november 2007 og den 19. maj Med undtagelse af virksomheder med markedsføringstilladelse til lægemidler med begrænset udlevering, naturlægemidler, stærke vitamin- og mineralpræparater og radioaktive lægemidler. 2
3 Indikationer og anvendelse Behandlingskrævende kvalme kan bl.a. skyldes nylig operation, kemoterapi, stråleterapi, migræne, graviditet og forskellige lægemiddelbehandlinger. Uden for sygehussektoren er det først og fremmest sidstnævnte problemstillinger, der tages stilling til. Antiemetisk effekt opnås i de fleste tilfælde bedst ved forebyggende behandling. Det gælder både postoperativ kvalme og kvalme og opkastning udløst af cytostatika eller stråleterapi. Der findes ikke et antiemetisk præparat, der kan forebygge al slags kvalme og opkastning. Nogle patienter lader sig vanskeligt behandle, og en større dosis kan øge bivirkningsgraden til et uacceptabelt niveau. Derfor er der i nogle tilfælde brug for kombinationsbehandling for at opnå synergieffekt (2, 3). Serotoninantagonister - A04AA Ondansetron, granisetron og tropisetron virker som serotoninantagonister ved at blokere brækrefleksen med virkningsmekanisme på perifere og centrale 5-HT3 receptorer. Indikationerne er nogenlunde enslydende for de 3 stoffer: kvalme og opkastning i relation til kemoterapi eller strålebehandling. Disse stoffer anvendes derfor hovedsagelig i hospitalsregi. Der er ingen væsentlig forskel i antiemetisk effekt eller toksisitet af de forskellige 5-HT3 antagonister. De vigtigste bivirkninger er obstipation og hovedpine (4). Effekten af de forskellige 5-HT3 antagonister på akut kvalme og opkastning er nok større end for metoclopramid, og de er uden de ekstrapyramidale bivirkninger, som er associeret med metoclopramids dopaminbindende egenskaber. 5-HT3-receptorantagonister har i flere undersøgelser ikke vist sig effektive til forebyggelse af sen kvalme og opkastning. Neurokininantagonsiter A04AD Aprepitant er en non-peptid neurokinin-1 receptor antagonist, som blokerer brækrefleksen med virkning på centrale NK1-receptorer. Aprepitant anvendes til forebyggelse af kemoterapi induceret akut og sen kvalme og opkastninger. Aprepitant benyttes som tillæg til standardbehandlingen ondansetron og kortikosteroid, hvorved effekten på kemoterapiinduceret kvalme og opkastninger øges. Af bivirkninger er der bl.a. set anoreksi, hovedpine, hikke, konstipation, diarré, dyspepsi og træthed (4). Motilitetsstimulerende midler - A03FA Metoclopramid og domperidon er indicerede til kvalme og opkastninger metoclopramid injektionsvæske dog specifikt til kvalme og opkastninger ved brug af cytostatika. Den antiemetiske effekt er betinget af en accelereret ventrikeltømning til duodenum, hvorved impulsaktiviteten i de afferente nerver fra pylorus til brækcentret nedsættes, svarende til det velkendte fænomen, at ventrikeltømning via brækning ofte letter på kvalme. Metoclopramid - og i mindre grad domperidon - har tillige en antidopaminvirkning, som giver en antiemetisk effekt, og metoclopramid er derfor også førstevalg. Bivirkninger som ekstrapyramidale symptomer (dystoni), indre uro, angst, depression, træthed og konfusion er mest udtalte for metoclopramid. Domperidon anvendes ved risiko for disse bivirkninger, da stoffet kun i ringe grad passerer blodhjernebarrieren. Metoclopramid er meget veldokumenteret i kombinationsbehandling. Det forbedrer effekten af ondansetron i forebyggelse af akut kvalme og forbedrer effekten af steroider i forebyggelsen af forsinket kvalme (2, 3). 3
4 Forbrug Ifølge Lægemiddelstyrelsens Lægemiddelstatistikregister (5) har anvendelsen af serotoninantagonisterne ondansetron, granisetron og tropisetron i primærsektoren været jævnt stigende fra ca personer i 2003 til ca personer i Forbruget i sygehussektoren kendes ikke som antal patienter i behandling men kun som DDD/1.000 indbyggere/døgn. Ifølge Lægemiddelstyrelsens Lægemiddelstatistikregister blev der af serotoninantagonister i 2008 i sygehussektoren anvendt 0,17 DDD/1.000 indbyggere/døgn og i primærsektoren 0,05 DDD/1.000 indbyggere/døgn. De tilsvarende tal for 2007 var 0,17 og 0,04. For gruppen af andre antiemetika (A04AD) er antallet af aprepitantbrugere få, 2-4 personer om året. Der har gennem årene været et meget konstant antal brugere af det peristaltikfremmende metoclopramid - godt personer per år. Af disse var ca i behandling med tabletter eller depotkapsler, og ca i rektal behandling, mens knap 400 var i behandling med oral opløsning og ca patienter har fået metoclopramid i form af injektion. De generelt billigere perorale former (tabletter og depotkapsler) udgjorde 68 pct. af forbruget af metoclopramid. For domperidon er der årligt omkring 3000 personer i behandling med tabletter og 500 i suppositoriebehandling. Data for forbrug og omsætning af de enkelte lægemiddelstoffer og lægemiddelstofgrupper samt antal personer i behandling med disse lægemidler kan ses på Lægemiddelstyrelsens netsted, Medicintilskudsnævnets bemærkninger og begrundelser Medicintilskudsnævnet har baseret sine drøftelser på Lægemiddelstyrelsens vejledning af 8. juni 2005 om procedure for revurderinger af lægemidlers tilskudsstatus og Lægemiddelstyrelsens retningslinjer af 4. juli 2006 for vurdering og sammenligning af lægemidler ved revurdering af lægemidlers tilskudsstatus. Nævnets vurdering af behandlingspris per døgn for de enkelte lægemiddelstoffer er foretaget i overensstemmelse med ovennævnte retningslinjer for vurdering og sammenligning af lægemidler ved revurdering af tilskudsstatus. Beregningerne er baseret på de fastsatte DDD-værdier. Nævnets indstilling er baseret på priserne i 6 prisperioder med første periodestart den 23. februar 2009 og sidste periodestart den 4. maj Nævnet har drøftet lægemidlernes tilskudsstatus på flere møder, jf. ovenfor, og har derfor fulgt lægemidlernes prisudvikling i dette tidsrum. Priserne har været nærmest uændrede i dette tidsrum. Endvidere baserer nævnets indstilling sig på oplysninger om forbruget og forbrugsudviklingen. Selvom udlevering af ondansetron, granisetron, tropisetron og apipretant formelt ikke er begrænset til sygehuse, er den faktiske anvendelse af stofferne i overensstemmelse med de godkendte indikationer overvejende på sygehuse. Anvendelsen i primærsektoren ser dog ud til at være stigende, jf. tallene for fordeling mellem de to sektorer. Til andre patienter med kvalme bør disse stoffer generelt ikke være førstevalg, primært fordi indikationen er begrænset til kvalme og opkastning i relation til kemoterapi eller strålebehandling, men også fordi prisen er høj i sammenligning med øvrige lægemidler mod kvalme (A03FA). Medicintilskudsnævnet vurderer, at der er risiko for, at disse stoffer anvendes uden for den godkendte indikation og som førstevalg, hvor dette ikke burde være tilfældet fx til cancerpatienter, som ikke er i kemoterapi eller strålebe- 4
5 handling eller til andre patienter med kvalme. Ansøgninger om enkeltilskud, som Lægemiddelstyrelsen modtager på disse lægemidler, understøtter, at der er en sådan risiko. Samlet set finder Medicintilskudsnævnet, at lægemidler med indhold af ondansetron, granisetron, tropisetron og apipretant fortsat ikke bør have generelt tilskud. For de peristaltikfremmende lægemidler metoclopramid og domperidon ligger det største forbrug på de perorale former, tabletter og depotkapsler. De perorale former af metoclopramid og domperidon er generelt lettere at administrere for patienten og er velegnede i de tilfælde, hvor patienten kan indtage stofferne på denne måde. Med undtagelse af metoclopramid oral opløsning, er de perorale lægemidler væsentligt billigere end de i dag generelt tilskudsberettigede lægemidler til rektal anvendelse. Det er nævnets vurdering, at den behandlingsmæssige værdi af de perorale lægemidelformer står mål med prisen. Af denne grund indstiller nævnet, at de perorale former af metoclopramid og domperidon (oral opløsning undtaget) bør have generelt uklausuleret tilskud. Nogle patienter vil fx som følge af kvalme - være nødsaget til at anvende suppositorierne, og det er nævnets vurdering, at den behandlingsmæssige værdi i disse tilfælde står mål med prisen, også når der sammenlignes med tabletter og depotkapsler. Det er vanskeligt at foretage et skøn over, om forholdet mellem antal patienter i peroral og rektal behandling er rationelt, men en ændring af tilskud til de perorale former tabletter og depotkapsler kan tænkes at medvirke til, at nogle patienter vil overgå til peroral behandling. Prisstrukturen for de to former vil her være et incitament til at foretage et sådant skift. Nævnet finder derfor ikke anledning til at foreslå ændringer i tilskudsstatus for suppositorieformerne. Metoclopramid oral opløsning er 5-6 gange så dyr som tabletter og depotkapsler og dobbelt så dyr som suppositorierne. Medicintilskudsnævnet finder derfor generelt ikke, at den behandlingsmæssige værdi står mål med prisen for denne lægemiddelform. Der kan være patienter for hvilke denne specielle lægemiddelform er nødvendig eller hensigtsmæssig, men uanset, at antallet af patienter er faldende, tyder forbruget på, at der er risiko for anvendelse som førstevalg til patienter, for hvilke denne specielle form ikke er nødvendig. Disse patienter har mulighed for at få bevilget enkelttilskud. Metoclopramid injektionsvæske anvendes specifikt til kvalme og opkastninger ved brug af cytostatika, og nævnet finder, at den behandlingsmæssige værdi af denne lægemiddelform står mål med prisen. Antallet af patienter har været stort set konstant gennem årene Den bedre effekt af metoclopramid kombineret med domperidons højere pris gør det til et rimeligt valg at anvende metoclopramid (peroralt eller rektalt) som førstevalg og kun anvende domperidon som alternativ i de tilfælde, hvor patienten ikke kan behandles med metoclopramid på grund af fx ekstrapyramidale bivirkninger. Nævnet skønner, at antallet af personer i behandling med domperidon er rationelt i sammenligning med det antal personer, der er i behandling med metoclopramid, og at antallet afspejler den gruppe, som ikke har kunnet behandles med metoclopramid på grund af bivirkninger. Medicintilskudsnævnet anbefaler Lægemiddelstyrelsen at følge forbruget af metoclopramid og domperidon, herunder forbruget af lægemidler til peroral henholdsvis rektal administration. 5
6 På nævnets vegne Mogens Laue Friis Formand Referencer 1. Lægemiddelstyrelsen. Produktresumeer for de enkelte lægemidler Postoperativ kvalme og opkastning, Ugeskr Læger 2006;168(1):40 3. Medikamentel behandling af kemoterapiinduceret kvalme og opkastning, Ugeskr Læger 2007;169(9): Infomatum A/S. Medicin.dk Lægemiddelstyrelsen. Forbrug og statistik. Bilag A. Grafisk oversigt over ATC-gruppe A04, Antiemetika og midler mod kvalme, og A03FA, Peristaltikfremmende midler. B. Oversigt over lægemiddelstoffer og lægemidler i i ATC-gruppe A04, Antiemetika og midler mod kvalme, og A03FA, Peristaltikfremmende midler med angivelse af den godkendte indikation for det lægemiddel med indhold af det pågældende stof, der har været godkendt længst, udleveringsgruppe, gældende tilskudsstatus, behandlingspris per døgn, forbrug og oplysninger om enkelttilskud. 6
7 Bilag A A04A Fosaprepitant A04 Antiemetica og midler mod kvalme A03 (udsnit) Midler mod funktionelle gastrointestinale forstyrrelser A04AA Serotonin (5ht3) antagonister A04AD Andre antiemetica A03FA Peristaltikfremmende midler A04AA01 Ondansetron A04AA02 Granisetron A04AA03 Tropisetron A04AA05 Palonosetron A04AD01 Scopolamin A04AD12 Aprepitant A03FA01 Metolopramid A03FA03 Domperidon 15. juni 2008
8 Bilag B 15. juni 2009 i ATC-gruppe A04, antiemetica og midler mod kvalme, samt A03FA, peristaltikfremmende midler Læsevejledning til skemaer nedenfor : Det eller de lægemidler, med indhold af indholdsstoffet, der er omfattet af denne revurdering af tilskudsstatus for ATC-gruppe i ATC-gruppe A04, antiemetica og midler mod kvalme, samt A03FA, peristaltikfremmende midler. Revurderingen omfatter alle styrker og pakningsstørrelser af lægemidlet for hvilke, der per den 4. maj 2009 er eller har været anmeldt en pris til Lægemiddelstyrelsen. : Den eller de angivne indikationer for et lægemiddelstof og lægemiddelform/administrationsvej for det lægemiddel, som har været godkendt længst 1. : Beskrivelse af betydningen af de forskellige udleveringsgrupper A, B etc. fremgår af 64 i bekendtgørelse om recepter nr. 155 af den 20. februar : Lægemidlets gældende tilskudsstatus. : De angivne behandlingspriser per døgn er baseret på laveste tilskudspriser og beregnet i overensstemmelse med Lægemiddelstyrelsens retningslinjer af den 4. juli 2006 for vurdering og sammenligning af lægemidler ved revurdering af lægemidlers tilskudsstatus 3. Beregningerne er foretaget på baggrund af de af WHO fastsatte definerede døgndoser 4. Forbrug: Antallet af personer i behandling er fra Lægemiddelstyrelsens Lægemiddelstatistikregister, jf. og omfatter patienter i primærsektoren. * angiver, at tallet omfatter alle lægemiddelformer og administrationsveje for det pågældende stof. Enkelttilskud: Oplysninger om antallet af ansøgninger om enkelttilskud og bevillingsprocent. Lægemiddelstyrelsen har ikke fastsat vejledende kriterier for enkelttilskud til disse lægemidler. Alle lægemidler, der indgår i denne revurdering, er omfattet af aftalen om vederlagsfri udlevering til særlige patientgrupper i fortsat sygehusbehandling, jf. Medicintilskudsnævnets indstilling. Serotoninantagonister, 5-HT3-antagonister (A04AA) A04AA01 Ondansetron (perorale lægemidler) Ondansetron "1A Farma", filmovertrukne tabletter, 4 mg. Ondansetron "Stada" 'filmovertrukne tabletter, 8 mg. Zofran oral opløsning, 0,8 mg/ml. Zofran smeltetabletter, 4 og 8 mg. Kvalme og opkastninger forårsaget af kemoterapi eller strålebehandling. Profylakse mod postoperativ kvalme og opkastning hos risikopatienter, fx patienter, der ved tidligere anæstesi har haft udtalt postoperativ kvalme og opkastning. 1 Lægemiddelstyrelsen. Produktresumeer for de enkelte lægemidler full&q=recepter&activesolution=http%3a%2f%2fdatabases.tarius.com
9 Bilag B 15. juni 2009 A Ikke generelt tilskud Tabl.(4 mg /8 mg): 24,04/11,74 kr. Oral opl. (0,8 mg/ml): 257,20 kr. Smeltetabl.(4/8 mg): 285,40/ 230,40 kr. Forbrug personer i behandling i 2006* personer i behandling i 2007* personer i behandling i 2008* Enkelttilskud 2006: 96 ansøgninger, heraf 70 bevilget (73%) 2007: 96 ansøgninger, heraf 82 bevilget (85%) 2008: 92 ansøgninger, heraf 71 beviliget (77%) A04AA01 Ondansetron (lægemidler til rektal anvendelse) Zofran suppositorier, 16 mg. Kvalme og opkastninger forårsaget af kemoterapi eller strålebehandling. A Sup.(16 mg): 218,09 kr. Forbrug personer i behandling i 2006* personer i behandling i 2007* 4002 personer i behandling i 2008* Enkelttilskud 2006: 26 ansøgninger, heraf 25 bevilget (96%) 2007: 23 ansøgninger, heraf 21 bevilget (91%) 2008: 18 ansøgninger, heraf 15 bevilget (83%) A04AA01 Ondansetron (lægemidler til injektion) Ondansetron (Zofran ) inj. væske, opl., 2 mg/ml. Zofran Konserveret inj. væske, opl., 2 mg/ml. Ondansetron "Vian" inj.-/inf.vsk.,opl., 2 mg/ml. Ondansetron (Zotrix ) inj. væske, opl., 2 mg/ml. Ondansetron "Nycomed" inj. væske, opl., 2 mg/ml. Ondansetron "B. Braun" inj. væske, opl., 2 mg/ml. Kvalme og opkastninger forårsaget af kemoterapi eller strålebehandling. Profylakse mod postoperativ kvalme og opkastning hos risikopatienter, fx patienter, der ved tidligere anæstesi har haft udtalt postoperativ kvalme og opkastning. A Inj. (2 mg/ml): 77,76 kr. Forbrug personer i behandling i 2006* personer i behandling i 2007* 4002 personer i behandling i 2008* Enkelttilskud 2006: 0 ansøgninger. 2007: 7 ansøgninger, heraf 4 bevilget (57%) 2008: 1 ansøgning, heraf 1 bevilget (100%) 2
10 Bilag B 15. juni 2009 A04AA02 Granisetron (perorale lægemidler) Granisetron "Actavis" tabletter, 1 og 2 mg Kvalme og opkastning forårsaget af cancerkemoterapi. Forebyggelse af kvalme og opkastning forårsaget af stråleterapi. A Tabl.(1 mg /2 mg): 83,72/ 85,07 kr. Forbrug 40 personer i behandling i 2006* 24 personer i behandling i 2007* 27 personer i behandling * Enkelttilskud 2006: 3 ansøgninger, heraf 3 bevilget (100%) 2007: 3 ansøgninger, heraf 2 bevilget (67%) 2008: 1 ansøgning, heraf 1 bevilget (100%) A04AA02 Granisetron (lægemidler til injektion) Kytril inj.væske,1 mg/ml. Granisetron "Hameln" konc.inj.inf.vsk.opl., 1 mg/ml. Kvalme og opkastning forårsaget af cancerkemoterapi og strålebehandling omfattende større dele af kroppen. Behandling af postoperativ kvalme og opkastning samt profylakse mod postoperativ kvalme og opkastning hos risikopatienter, f.eks. patienter, der ved tidligere anæstesi har haft udtalt postoperativ kvalme og opkastning. A Inj.(1 mg/ml): 160,44 kr. Forbrug 40 personer i behandling i 2006* 24 personer i behandling i 2007* 27 personer i behandling * Enkelttilskud 2006: 0 ansøgninger. 2007: 0 ansøgninger. 2008: 0 ansøgninger. A04AA03 Tropisetron (perorale lægemidler) Navoban kapsler, 5 mg. Kvalme og opkastninger forårsaget af cancerkemoterapi. A Kaps.(5 mg): 181, 75 kr. Forbrug 3 personer i behandling i 2006* 1 person i behandling i 2007* 0 personer i behandling * Enkelttilskud 2006: 0 ansøgninger. 2007: 0 ansøgninger. 2008: 0 ansøgninger. 3
11 Bilag B 15. juni 2009 A04AA03 Tropisetron (lægemidler til injektion) Navoban inj. væske, opl. 1 mg/ml. Kvalme og opkastninger forårsaget af cancerkemoterapi. Behandling af post-operativ kvalme og opkastning i forbindelse med gynækologiske operationer. For at optimere benefit-risk forholdet, bør brug begrænses til patienter med kendt forhistorie med post-operativ kvalme og opkastning. A Inj.(1 mg/ml): 206,50 kr Forbrug 3 personer i behandling i 2006* 1 personer i behandling i 2007* 0 personer i behandling * Enkelttilskud 2006: 0 ansøgninger. 2007: 0 ansøgninger. 2008: 0 ansøgninger. Neurokininantagonister (A04AD) A04AD12 Aprepinent (perorale lægemidler) Emend kapsler hårde, 3 stk.(1x125 mg, 2x80 mg). Emend kapsler, hårde 80 mg. Forebyggelse af akut og sen kvalme og opkastning i forbindelse med højemetogen cisplatinbaseret cancerkemoterapi hos voksne. Forebyggelse af kvalme og opkastning i forbindelse med moderat emetogen cancerkemoterapi hos voksne. EMEND 125 mg/80 mg gives som en del af en kombinationsbehandling. A Komb.pakke125/80 mg: 247,00 kr. 80 mg: 297,41 kr. Forbrug 2 personer i behandling i personer i behandling i personer i behandling i 2008 Enkelttilskud 2006: 0 ansøgninger. 2007: 0 ansøgninger. 2008: 0 ansøgninger. Peristaltikfremmende midler (A03FA) A03FA01 Metoclopramid (perorale lægemidler) 4
12 Bilag B 15. juni 2009 lægemidler Forbrug Emperal tabletter, 10 mg. Gastro-Timelets depotkapsler, 30 mg. Primperan oral opløsning, 1 mg/ml. Kvalme og opkastninger. B Tabl. (10 mg): 2,10 kr. Depot kapsl.(30 mg): 2,77 kr. Oral opl. (1 mg/ml): 17,10 kr. Tabletter/depotkapsler: personer i behandling i personer i behandling i personer i behandling i 2008 Oral opløsning: 416 personer i behandling i personer i behandling i personer i behandling i 2008 Enkelttilskud 2006: 42 ansøgninger, heraf 35 bevilget (83%) 2007: 42 ansøgninger, heraf 31 bevilget (74%) 2008: 33 ansøgninger, heraf 32 bevilget (97%) A03FA01 Metoclopramid (lægemidler til rektal anvendelse) Primperan suppositorier, 20 mg. Kvalme og opkastninger. B Generelt tilskud Sup (20 mg): 5,87 kr. Forbrug personer i behandling i personer i behandling i personer i behandling i 2008 A03FA01 Metoclopramid (lægemidler til injektion) Primperan Injektion, 5 mg/ml. Forebyggelse af kvalme og opkastninger ved brug af cytostatika. B Generelt tilskud Inj.(5 mg/ml): 16,44 kr. Forbrug 898 personer i behandling i personer i behandling i personer i behandling i 2008 A03FA03 Domperidon (perorale lægemidler) 5
13 Bilag B 15. juni 2009 Domperidon "Alternova" tabletter, 10 mg. Voksne: - Lindring af symptomerne ved kvalme og opkastning, epigastrisk oppressions fornemmelse, ubehag i øvre del af abdomem, tilbagestrømning af maveindhold. Børn: - Lindring af symptomerne ved kvalme og opkastning. B Tabl.(10 mg): 5,70 kr. Forbrug personer i behandling i personer i behandling i personer i behandling i 2008 Enkelttilskud 2006: 44 ansøgninger, heraf 36 bevilget (82%) 2007: 78 ansøgninger, heraf 61 bevilget (78%) ansøninger, heraf 72 bevilget (99%) A03FA03 Domperidon (lægemidler til rektal anvendelse) Motilium suppositorier, 30 mg. Voksne: Lindring af symptomerne ved kvalme og opkastning, epigastrisk oppressions fornemmelse, ubehag i øvre del af abdomem, tilbagestrømning af maveindhold. Børn: Lindring af symptomerne ved kvalme og opkastning. B Generelt tilskud Suppositorier (30 mg): 33,28 kr. Forbrug 589 personer i behandling i personer i behandling i personer i behandling i
Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA
 Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A04 og A03FA
Til virksomheder der per 16. november 2009 eller tidligere har markedsført et eller flere lægemidler i ATC-gruppe A04 og A03FA Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A04 og A03FA
Medicintilskudsnævnet
 Medicintilskudsnævnet Sagsnr: 2013111155 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A03, midler mod funktionelle gastrointestinale forstyrrelser Baggrund og indhold
Medicintilskudsnævnet Sagsnr: 2013111155 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A03, midler mod funktionelle gastrointestinale forstyrrelser Baggrund og indhold
Revurdering af tilskudsstatus for lægemidler i ATC-gruppe A08, midler mod fedme, ekskl. diætmidler
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 14. april 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 14. april 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
C02 Antihypertensiva
 C02 Antihypertensiva Bilag A1 C02A Antiadrenerge midler, centralt virkende C02C Antiadrenerge midler, perifert virkende C02K Andre antihypertensiva C02AB C02AC Imidazolin-receptor Agonister C02CA Alfa-adrenoceptor
C02 Antihypertensiva Bilag A1 C02A Antiadrenerge midler, centralt virkende C02C Antiadrenerge midler, perifert virkende C02K Andre antihypertensiva C02AB C02AC Imidazolin-receptor Agonister C02CA Alfa-adrenoceptor
Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
 Medicintilskudsnævnet Den 4. november 205 Sagsnr: 20505674 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed Baggrund Sundhedsstyrelsen
Medicintilskudsnævnet Den 4. november 205 Sagsnr: 20505674 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed Baggrund Sundhedsstyrelsen
Revurdering af tilskudsstatus for lægemidler mod demens
 Den 4. november 2015 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at revurdere tilskudsstatus for lægemidler
Den 4. november 2015 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at revurdere tilskudsstatus for lægemidler
Revurdering af tilskudsstatus for lægemidler mod demens
 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 14. april 2016 Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at
Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 14. april 2016 Revurdering af tilskudsstatus for lægemidler mod demens Baggrund Sundhedsstyrelsen (nu Lægemiddelstyrelsen) har anmodet om at
Medicintilskudsnævnet
 Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen i ATC-gruppe A01 og A07AA02 Baggrund
Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen i ATC-gruppe A01 og A07AA02 Baggrund
Vejledning til ansøgning om generelt tilskud. Lovgrundlag
 Vejledning til ansøgning om generelt tilskud Lovgrundlag Lægemiddelstyrelsen træffer i henhold til sundhedslovens 144, stk. 1-3, samt sundhedslovens 152, stk. 2 og 4, afgørelse om, hvorvidt Regionsrådet
Vejledning til ansøgning om generelt tilskud Lovgrundlag Lægemiddelstyrelsen træffer i henhold til sundhedslovens 144, stk. 1-3, samt sundhedslovens 152, stk. 2 og 4, afgørelse om, hvorvidt Regionsrådet
Medicintilskudsnævnet
 30. maj 2012 Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Sundhedsstyrelsen har
30. maj 2012 Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Sundhedsstyrelsen har
ikke kan tolereres eller i helt særlige tilfælde efter lægens samlede kliniske vurdering af patientens tilstand ikke er hensigtsmæssig.
 Virksomhed Partshøring - Revurdering af tilskudsstatus for dihydropyridincalciumantagonister - ATC-gruppe C08CA Lægemiddelstyrelsen har foretaget vurdering af spørgsmålet om fremtidig tilskudsstatus for
Virksomhed Partshøring - Revurdering af tilskudsstatus for dihydropyridincalciumantagonister - ATC-gruppe C08CA Lægemiddelstyrelsen har foretaget vurdering af spørgsmålet om fremtidig tilskudsstatus for
Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud
 22. marts 2019 Sagsnr. : 2019032928 T +45 44889386 E mss@dkma.dk Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud Vi har vurderet tilskudsstatus for kapsler og depotplastre med indhold
22. marts 2019 Sagsnr. : 2019032928 T +45 44889386 E mss@dkma.dk Rivastigmin kapsler og depotplastre får generelt klausuleret tilskud Vi har vurderet tilskudsstatus for kapsler og depotplastre med indhold
Generelt tilskud til tabletter med indhold af ezetimib
 Til virksomheden 0. september 018 Sagsnr. 018089 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af ezetimib Vi har revurderet tilskudsstatus for tabletter med indhold af ezetimib,
Til virksomheden 0. september 018 Sagsnr. 018089 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af ezetimib Vi har revurderet tilskudsstatus for tabletter med indhold af ezetimib,
Til virksomheden 21. juni 2016 Sagsnr Reference usk T E
 Til virksomheden 21. juni 2016 Sagsnr. 20160228 Reference usk T +4 4488930 E usk@dkma.dk Ændring af tilskudsklausul for duloxetin 30 og 60 mg Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Til virksomheden 21. juni 2016 Sagsnr. 20160228 Reference usk T +4 4488930 E usk@dkma.dk Ændring af tilskudsklausul for duloxetin 30 og 60 mg Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Patienter, hvor behandling med antipsykotisk lægemiddel med generelt tilskud
 Til virksomheder, der per 31. marts 2016 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe N05AX12 med indhold af aripiprazol som smeltetabletter 31. marts 2016 Sagsnr.
Til virksomheder, der per 31. marts 2016 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe N05AX12 med indhold af aripiprazol som smeltetabletter 31. marts 2016 Sagsnr.
Generelt tilskud til tabletter med indhold af rosuvastatin
 Til virksomheden 0. september 018 Sagsnr. 0180894 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af rosuvastatin Vi har revurderet tilskudsstatus for tabletter med indhold af rosuvastatin,
Til virksomheden 0. september 018 Sagsnr. 0180894 T +454488986 E mss@dkma.dk Generelt tilskud til tabletter med indhold af rosuvastatin Vi har revurderet tilskudsstatus for tabletter med indhold af rosuvastatin,
C08 Calciumantagonister
 C08 Calciumantagonister Bilag A4 C08C Selektive calciumantagonister m. overv. vaskulær effekt C08D Selektive calciumantagonister m. direkte cardiel effekt C08CA Dihydropyridinderivater C08DA Phenylalkylaminderivater
C08 Calciumantagonister Bilag A4 C08C Selektive calciumantagonister m. overv. vaskulær effekt C08D Selektive calciumantagonister m. direkte cardiel effekt C08CA Dihydropyridinderivater C08DA Phenylalkylaminderivater
Til virksomheden 1. november 2017 Sagsnr Reference usk T E
 Til virksomheden 1. november 2017 Sagsnr. 2017011413 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod migræne Vi har revurderet tilskudsstatus for lægemidler
Til virksomheden 1. november 2017 Sagsnr. 2017011413 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod migræne Vi har revurderet tilskudsstatus for lægemidler
Revurdering af tilskudsstatus for lægemidler mod migræne
 Medicintilskudsnævnet Den 12. oktober 2016 2. forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet om at revurdere
Medicintilskudsnævnet Den 12. oktober 2016 2. forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet om at revurdere
N02 Analgetika. N02A Opioider. N02AB Phenylpiperidinderivater. N02AF Morfinanderivater. N02AG Opioider i komb. med antispasmodika
 N02 Analgetika Bilag A N02A Opioider N02AA Naturlige opiumalkaloider N02AB Phenylpiperidinderivater N02AE Oripavinederivater N02AF Morfinanderivater N02AG Opioider i komb. med antispasmodika N02AX Andre
N02 Analgetika Bilag A N02A Opioider N02AA Naturlige opiumalkaloider N02AB Phenylpiperidinderivater N02AE Oripavinederivater N02AF Morfinanderivater N02AG Opioider i komb. med antispasmodika N02AX Andre
Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus
 Dato 9. november 2017 Sagsnr. 2017103730 PFR Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus Indledning Formålet med denne vejledning er at orientere om proceduren for den periodiske
Dato 9. november 2017 Sagsnr. 2017103730 PFR Vejledning om den periodiske revurdering af lægemidlers tilskudsstatus Indledning Formålet med denne vejledning er at orientere om proceduren for den periodiske
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 7. september 2006 Axel Heides Gade 1 2300 København S Indstilling til tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 7. september 2006 Axel Heides Gade 1 2300 København S Indstilling til tilskudsstatus for
Generelt tilskud til flere lægemidler med indhold af angiotensin-ii antagonister
 Til virksomheder, der per 18. juni 2018 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe C09CA07, C09DA04 og C09DA07. 28. juni 2018 Sagsnr. 2018063702 T +45 4488
Til virksomheder, der per 18. juni 2018 eller tidligere har markedsført et eller flere aktuelt godkendte lægemidler i ATC-gruppe C09CA07, C09DA04 og C09DA07. 28. juni 2018 Sagsnr. 2018063702 T +45 4488
C07. Beta-blokerende midler, Beta-blokerende midler, C07CB Beta-blokkere, selektive, og andre diuretica. C07BB Beta-blokkere, selektive, og thiazider
 C07 Beta-blokerende midler Bilag A3 C07A Beta-blokerende midler, usammensatte C07B Beta-blokerende midler og thiazider C07C Beta-blokkere og andre diuretica C07F Beta-blokkere og andre antihypertensiva
C07 Beta-blokerende midler Bilag A3 C07A Beta-blokerende midler, usammensatte C07B Beta-blokerende midler og thiazider C07C Beta-blokkere og andre diuretica C07F Beta-blokkere og andre antihypertensiva
Revurdering af tilskudsstatus for lægemidler mod migræne
 Medicintilskudsnævnet Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 10. januar 2017 Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet
Medicintilskudsnævnet Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 10. januar 2017 Revurdering af tilskudsstatus for lægemidler mod migræne aggrund Lægemiddelstyrelsen har anmodet Medicintilskudsnævnet
Til virksomheden 16. januar 2017 Sagsnr Reference usk T E
 Til virksomheden 16. januar 2017 Sagsnr. 2015122548 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Vi har revurderet tilskudsstatus for
Til virksomheden 16. januar 2017 Sagsnr. 2015122548 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Vi har revurderet tilskudsstatus for
Til Medicintilskudsnævnets medlemmer Den 16. august Revurdering af lægemidlers tilskudsstatus
 Til Medicintilskudsnævnets medlemmer Den 16. august 2011 Hermed indkaldes til møde i Medicintilskudsnævnet om Revurdering af lægemidlers tilskudsstatus Mødet er nr. 358 og finder sted tirsdag den 23. august
Til Medicintilskudsnævnets medlemmer Den 16. august 2011 Hermed indkaldes til møde i Medicintilskudsnævnet om Revurdering af lægemidlers tilskudsstatus Mødet er nr. 358 og finder sted tirsdag den 23. august
VEJLEDNING I FOREBYGGELSE OG BEHANDLING af kvalme og opkastning hos børn og unge i kemoterapi og stråleterapi
 Titel: FOREBYGGELSE OG BEHANDLING af kvalme og opkastning hos børn og unge i kemoterapi og stråleterapi Udarbejdet af : catherine rechnitzer, Henrik Schrøder, Mimi Kjærsgaard Drøftet under: 4. DAPHOs samarbejdssymposium
Titel: FOREBYGGELSE OG BEHANDLING af kvalme og opkastning hos børn og unge i kemoterapi og stråleterapi Udarbejdet af : catherine rechnitzer, Henrik Schrøder, Mimi Kjærsgaard Drøftet under: 4. DAPHOs samarbejdssymposium
Medicintilskudsnævnet
 Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi har revurderet tilskudsstatus
Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi har revurderet tilskudsstatus
BILAG II VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF PRODUKTRESUMÉ, ETIKETTERING OG INDLÆGSSEDDEL FREMLAGT AF EMA
 BILAG II VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF PRODUKTRESUMÉ, ETIKETTERING OG INDLÆGSSEDDEL FREMLAGT AF EMA 11 Videnskabelige konklusioner Samlet resumé af den videnskabelige vurdering
BILAG II VIDENSKABELIGE KONKLUSIONER OG BEGRUNDELSER FOR ÆNDRING AF PRODUKTRESUMÉ, ETIKETTERING OG INDLÆGSSEDDEL FREMLAGT AF EMA 11 Videnskabelige konklusioner Samlet resumé af den videnskabelige vurdering
Bilag Journalnummer Kontor C.2-0 EUK 2. marts 2005
 Europaudvalget (2. samling) EUU alm. del - Bilag 43 Offentligt Medlemmerne af Folketingets Europaudvalg og deres stedfortrædere Bilag Journalnummer Kontor 1 400.C.2-0 EUK 2. marts 2005 KOMITÉSAG Til underretning
Europaudvalget (2. samling) EUU alm. del - Bilag 43 Offentligt Medlemmerne af Folketingets Europaudvalg og deres stedfortrædere Bilag Journalnummer Kontor 1 400.C.2-0 EUK 2. marts 2005 KOMITÉSAG Til underretning
Medicintilskudsnævnet
 23. december 2011 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Baggrund og indhold
23. december 2011 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for stærke smertestillende lægemidler (opioider) i ATCgruppe N02A, N07BC og R05DA Baggrund og indhold
Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter
 Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 20. december 2016 Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Baggrund Lægemiddelstyrelsen har anmodet om at revurdere
Lægemiddelstyrelsen Axel Heides Gade 1 2300 København S Den 20. december 2016 Revurdering af tilskudsstatus for lægemidler mod neuropatiske smerter Baggrund Lægemiddelstyrelsen har anmodet om at revurdere
Til virksomheden 21. juni 2016 Sagsnr Reference usk T E
 Til virksomheden 21. juni 2016 Sagsnr. 20160221 Reference usk T +4 4488930 E usk@dkma.dk Generelt tilskud til nogle pregabalin kapsler Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Til virksomheden 21. juni 2016 Sagsnr. 20160221 Reference usk T +4 4488930 E usk@dkma.dk Generelt tilskud til nogle pregabalin kapsler Den 30. september 2011 afsluttede vi revurdering af tilskudsstatus
Medicintilskudsnævnet
 Lægemiddelstyrelsen Axel Heides Gade 2300 København S Den 0. september 208 Sagsnr.: 208080020 Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Baggrund Lægemiddelstyrelsen
Lægemiddelstyrelsen Axel Heides Gade 2300 København S Den 0. september 208 Sagsnr.: 208080020 Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Baggrund Lægemiddelstyrelsen
Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens
 Til virksomheden 15. juni 2018 Sagsnr. 2018051042 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens Vi har revurderet tilskudsstatus for
Til virksomheden 15. juni 2018 Sagsnr. 2018051042 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens Vi har revurderet tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 1. september 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 1. september 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 MEDLEMMER UDPEGET AF MINISTEREN FOR SUNDHED OG FOREBYGGELSE 20 MØDER I 2014
 ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 Medicintilskudsnævnet rådgiver Sundhedsstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
ÅRSRAPPORT FRA MEDICINTILSKUDSNÆVNET 2014 Medicintilskudsnævnet rådgiver Sundhedsstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Sagsfremstilling Medicintilskudsnævnet har afgivet indstilling om lægemidlernes fremtidige tilskudsstatus den 26. januar 2015.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for NSAID er og lægemidler mod svage smerter i ATC-gruppe M01A (ekskl. glucosamin), M02A, N02BA, N02BB og N02BE Vi afslutter
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for NSAID er og lægemidler mod svage smerter i ATC-gruppe M01A (ekskl. glucosamin), M02A, N02BA, N02BB og N02BE Vi afslutter
Det Europæiske Lægemiddelagentur anbefaler ændringer i anvendelsen af metoclopramid
 Den 20. december 2013 EMA/13239/2014 Corr. 1 Det Europæiske Lægemiddelagentur anbefaler ændringer i anvendelsen af Ændringerne har hovedsagelig til formål at nedsætte risikoen for neurologiske bivirkninger
Den 20. december 2013 EMA/13239/2014 Corr. 1 Det Europæiske Lægemiddelagentur anbefaler ændringer i anvendelsen af Ændringerne har hovedsagelig til formål at nedsætte risikoen for neurologiske bivirkninger
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Zofran 0,8 mg/ml oral opløsning ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Zofran 0,8 mg/ml oral opløsning ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Antallet af ansøgninger om generelt tilskud, som nævnet behandlede på de månedlige møder, fremgår af figur 1.
 Årsrapport fra Medicintilskudsnævnet 2010 Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Årsrapport fra Medicintilskudsnævnet 2010 Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra
Medicintilskudsnævnet
 Medicintilskudsnævnet Den. juni 205 Sagsnr: 20505674 Sundhedsstyrelsen Axel Heides Gade 2300 København S Forslag til indstilling Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
Medicintilskudsnævnet Den. juni 205 Sagsnr: 20505674 Sundhedsstyrelsen Axel Heides Gade 2300 København S Forslag til indstilling Ad hoc revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed
Medicinpriser. Priser for den Uge 12/13
 Medicinpriser 2010 Priser for den 19.03.2010 Uge 12/13 LÆSEVEJLEDNING Medicinpriser indeholder priser på alle markedsførte apoteksforbeholdte lægemidler i. Desuden indeholder den det markedsførte sortiment
Medicinpriser 2010 Priser for den 19.03.2010 Uge 12/13 LÆSEVEJLEDNING Medicinpriser indeholder priser på alle markedsførte apoteksforbeholdte lægemidler i. Desuden indeholder den det markedsførte sortiment
KLINISKE RETNINGSLINJER
 KLINISKE RETNINGSLINJER for behandling af kvalme og opkastninger hos palliative patienter juni 2008 Torben Ishøy, virksomhedsansvarlig lægelig chef VII Kvalme og opkastninger forekommer hos mange palliative
KLINISKE RETNINGSLINJER for behandling af kvalme og opkastninger hos palliative patienter juni 2008 Torben Ishøy, virksomhedsansvarlig lægelig chef VII Kvalme og opkastninger forekommer hos mange palliative
Medicintilskud I MEDICINTILSKUDSSYSTEMET. Lægemiddelstyrelsen. Generelt om medicintilskud
 MEDICINTILSKUDSSYSTEMET 169 Medicintilskud I Lægemiddelstyrelsen Det danske medicintilskudssystem er bygget op af en række elementer, som tilsammen skal sørge for, at ingen patienter af økonomiske grunde
MEDICINTILSKUDSSYSTEMET 169 Medicintilskud I Lægemiddelstyrelsen Det danske medicintilskudssystem er bygget op af en række elementer, som tilsammen skal sørge for, at ingen patienter af økonomiske grunde
Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG
 Til virksomheden 4. juli 2017 Sagsnr. 2015122546 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG Vi har revurderet tilskudsstatus
Til virksomheden 4. juli 2017 Sagsnr. 2015122546 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler i ATC-grupperne N07A, N07CA01, N07X + N02BG Vi har revurderet tilskudsstatus
Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler
 Dato 9. november 2017 Sagsnr. 2017103730 UDKAST Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler Indledning Denne vejledning uddyber reglerne i sundhedslovens
Dato 9. november 2017 Sagsnr. 2017103730 UDKAST Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler Indledning Denne vejledning uddyber reglerne i sundhedslovens
C09 Midler med virkning på renin-angiotensin systemet
 C09 Midler med virkning på renin-angiotensin systemet ilag A C09C Angiotensin-II antagonister C09D Angiotensin-II antagonister, kombinationer C09X Andre midler med virkning på renin-angiotensinsyst. C09CA
C09 Midler med virkning på renin-angiotensin systemet ilag A C09C Angiotensin-II antagonister C09D Angiotensin-II antagonister, kombinationer C09X Andre midler med virkning på renin-angiotensinsyst. C09CA
Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB
 Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB Vi har revurderet tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB, der per
Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB Vi har revurderet tilskudsstatus for lægemidler mod alkoholafhængighed i ATC-gruppe N07BB, der per
Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"7."Lægemiddelstyrelsens"afgørelse"april"2010" " " " Bilag"8."IRF" "skift"fra"a2a"til"ace" " " " "
 Sundheds- og Forebyggelsesudvalget 2013-14 SUU Alm.del Bilag 436 Offentligt Oversigt-over-bilag- " Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"2."Medicintilskudsnævnets"indstilling"januar"2008"
Sundheds- og Forebyggelsesudvalget 2013-14 SUU Alm.del Bilag 436 Offentligt Oversigt-over-bilag- " Bilag"1."Spørgsmål"og"svar"på"S"2849" " " " " Bilag"2."Medicintilskudsnævnets"indstilling"januar"2008"
Indlægsseddel: Information til brugeren
 Indlægsseddel: Information til brugeren Zofran 4 mg og 8 mg frysetørrede tabletter ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Indlægsseddel: Information til brugeren Zofran 4 mg og 8 mg frysetørrede tabletter ondansetron Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
Nedenfor følger sagsfremstilling, lovgrundlag, afgørelse, begrundelse, klagevejledning samt information om ændringerne.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A09- digestiva, inkl. enzymer, A11-vitaminer, A12- mineralpræparater og A16 - andre midler
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler i ATC-gruppe A09- digestiva, inkl. enzymer, A11-vitaminer, A12- mineralpræparater og A16 - andre midler
Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion Vi afslutter med denne afgørelse revurdering af tilskudsstatus
KVALMEBEHANDLING. Kvalme forekommer hos op mod 40 % i de sidste 6 uger af alvorligt syge menneskers levetid.
 Udarbejdet af:lsi,vst dato: sept. 2010 Revideret af: VSt dato: okt.2014 Godkendt af:lan,san dato: okt.2014 2010 Revideres igen: om max 2 år KVALMEBEHANDLING Kvalme er en subjektiv oplevelse, som ofte ledsages
Udarbejdet af:lsi,vst dato: sept. 2010 Revideret af: VSt dato: okt.2014 Godkendt af:lan,san dato: okt.2014 2010 Revideres igen: om max 2 år KVALMEBEHANDLING Kvalme er en subjektiv oplevelse, som ofte ledsages
Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske
 Til virksomheden 7. december 2018 Sagsnr. 2018092970 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Vi har revurderet tilskudsstatus
Til virksomheden 7. december 2018 Sagsnr. 2018092970 T +45 93518614 E dila@dkma.dk Revurdering af tilskudsstatus for lægemidler til lokalbehandling af gynækologiske infektioner Vi har revurderet tilskudsstatus
Besvarelse af spørgsmål nr. 265 (Alm. del), som Folketingets Sundhedsudvalg har stillet til indenrigs- og sundhedsministeren den 16.
 Sundhedsudvalget SUU alm. del - Svar på Spørgsmål 265 Offentligt Indenrigs- og Sundhedsministeriet Dato: 18. april 2006 Kontor: Lægemiddelkontoret J.nr.: 2006-13009-331 Sagsbeh.: TBA Fil-navn: Dokument
Sundhedsudvalget SUU alm. del - Svar på Spørgsmål 265 Offentligt Indenrigs- og Sundhedsministeriet Dato: 18. april 2006 Kontor: Lægemiddelkontoret J.nr.: 2006-13009-331 Sagsbeh.: TBA Fil-navn: Dokument
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 413, tirsdag den 27. maj 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 27. maj 2014. I mødet deltog:
Referat af Medicintilskudsnævnets møde nr. 413, tirsdag den 27. maj 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 27. maj 2014. I mødet deltog:
Medicintilskudsnævnet
 2. februar 2011 Referat af s møde nr. 347, tirsdag den 25. januar 2011 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 25. januar 2011. I mødet deltog:
2. februar 2011 Referat af s møde nr. 347, tirsdag den 25. januar 2011 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 25. januar 2011. I mødet deltog:
Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud til lægemidler
 Sundheds- og Ældreministeriet Enhed: MEDINT Sagsbeh.: DEPRHH Koordineret med: Sagsnr.: 1807871 Dok. nr.: 716616 Dato: 22-10-2018 Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud
Sundheds- og Ældreministeriet Enhed: MEDINT Sagsbeh.: DEPRHH Koordineret med: Sagsnr.: 1807871 Dok. nr.: 716616 Dato: 22-10-2018 Vejledning om ansøgning om generelt tilskud eller generelt klausuleret tilskud
Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe
 Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe C10 16. marts 2007 Indledning Folketinget besluttede ved udgangen af 2004 1, at afgørelser om generelt tilskud til lægemidler skal
Revurdering af tilskudsstatus for lipidsænkende lægemidler, ATCgruppe C10 16. marts 2007 Indledning Folketinget besluttede ved udgangen af 2004 1, at afgørelser om generelt tilskud til lægemidler skal
Kvalme og opkastning ved medicinsk kræftbehandling. Symptombehandling
 Kvalme og opkastning ved medicinsk kræftbehandling Symptombehandling Maj 2011 Definitioner Akut kvalme og opkastning Sen kvalme og opkastning Forventningskvalme og opkastning Første 24 timer efter start
Kvalme og opkastning ved medicinsk kræftbehandling Symptombehandling Maj 2011 Definitioner Akut kvalme og opkastning Sen kvalme og opkastning Forventningskvalme og opkastning Første 24 timer efter start
PRODUKTRESUMÉ. for. Metomotyl, injektionsvæske, opløsning
 12. december 2017 PRODUKTRESUMÉ for Metomotyl, injektionsvæske, opløsning 0. D.SP.NR. 28870 1. VETERINÆRLÆGEMIDLETS NAVN Metomotyl 2. KVALITATIV OG KVANTITATIV SAMMENSÆTNING Hver ml i 2,5 mg/ml opløsning
12. december 2017 PRODUKTRESUMÉ for Metomotyl, injektionsvæske, opløsning 0. D.SP.NR. 28870 1. VETERINÆRLÆGEMIDLETS NAVN Metomotyl 2. KVALITATIV OG KVANTITATIV SAMMENSÆTNING Hver ml i 2,5 mg/ml opløsning
Vi har modtaget høringssvar fra følgende: Bristol-Myers Squibb Danmarks Apotekerforening Lægeforeningen Tandlægeforeningen UCB Pharma AS
 Svar på Medicintilskudsnævnets høring over nævnets 4 forslag til indstillinger af 22. november 2013 til tilskudsstatus for lægemidler i ATC-gruppe A01, A03, A07, A09, A11, A12 og A16 Vi har modtaget høringssvar
Svar på Medicintilskudsnævnets høring over nævnets 4 forslag til indstillinger af 22. november 2013 til tilskudsstatus for lægemidler i ATC-gruppe A01, A03, A07, A09, A11, A12 og A16 Vi har modtaget høringssvar
Medicintilskudsnævnet
 Den 21. august 2019 Sagsnr: 2019033133 FORSLAG Revurdering af tilskudsstatus for centralt virkende muskelrelaksantia (ATC-gruppe M03) Baggrund Lægemiddelstyrelsen har anmodet om at revurdere tilskudsstatus
Den 21. august 2019 Sagsnr: 2019033133 FORSLAG Revurdering af tilskudsstatus for centralt virkende muskelrelaksantia (ATC-gruppe M03) Baggrund Lægemiddelstyrelsen har anmodet om at revurdere tilskudsstatus
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 417, tirsdag den 23. september 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 23. september 2014.
Referat af Medicintilskudsnævnets møde nr. 417, tirsdag den 23. september 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 23. september 2014.
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 434, tirsdag den 29. september 2015. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 29. september 2015.
Referat af Medicintilskudsnævnets møde nr. 434, tirsdag den 29. september 2015. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 29. september 2015.
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 442, tirsdag den 19. januar 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. januar 2016. I mødet
Referat af Medicintilskudsnævnets møde nr. 442, tirsdag den 19. januar 2016. Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. januar 2016. I mødet
Her er oversigt over de af jeres virksomheds lægemidler, der er omfattet af afgørelsen. Afgørelsen følger på de næste sider.
 1. november 2017 Sagsnr. 2015030614 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod Parkinsons sygdom Vi har revurderet tilskudsstatus for lægemidler mod Parkinsons
1. november 2017 Sagsnr. 2015030614 Reference usk T +45 44889350 E usk@dkma.dk Revurdering af tilskudsstatus for lægemidler mod Parkinsons sygdom Vi har revurderet tilskudsstatus for lægemidler mod Parkinsons
Nedenfor følger sagsfremstilling, lovgrundlag, afgørelse, begrundelse, klagevejledning samt information om ændringerne.
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for lægemidler til lokal behandling af sygdomme i mundhulen Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus og er startet med at se på hypertensionsmidlerne.
 Dansk Hypertensionsselskab Fællessekretariatet Esplanaden 8C, 3. 1263 København K. Hypertensionsbehandling i Danmark 6. marts 2006 Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus
Dansk Hypertensionsselskab Fællessekretariatet Esplanaden 8C, 3. 1263 København K. Hypertensionsbehandling i Danmark 6. marts 2006 Lægemiddelstyrelsen har påbegyndt en gennemgang af alle lægemidlers tilskudsstatus
Til Virksomheden. Revurdering af tilskudsstatus for lægemidler mod diabetes
 Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod diabetes Sundhedsstyrelsen har revurderet tilskudsstatus for lægemidler i ATCgruppe A10, der per 3. juni 2013 er godkendt til markedsføring
Til Virksomheden Revurdering af tilskudsstatus for lægemidler mod diabetes Sundhedsstyrelsen har revurderet tilskudsstatus for lægemidler i ATCgruppe A10, der per 3. juni 2013 er godkendt til markedsføring
Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsførings-tilladelse for lægemidlet Eucreas
 Sundhedsudvalget SUU alm. del - Bilag 76 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsførings-tilladelse for lægemidlet Eucreas Resumé
Sundhedsudvalget SUU alm. del - Bilag 76 Offentligt Grundnotat til Folketingets Europaudvalg om forslag til kommissionsbeslutning om udstedelse af markedsførings-tilladelse for lægemidlet Eucreas Resumé
INFORMATION TIL HJEMMEPLEJEN KVALMEBEHANDLING TIL PATIENTER I KEMOTERAPI
 INFORMATION TIL HJEMMEPLEJEN KVALMEBEHANDLING TIL PATIENTER I KEMOTERAPI Udarbejdet af: SIG EMESIS 2013 Forord Denne information er udarbejdet af SIG Emesis, en landsdækkende gruppe af sygeplejersker,
INFORMATION TIL HJEMMEPLEJEN KVALMEBEHANDLING TIL PATIENTER I KEMOTERAPI Udarbejdet af: SIG EMESIS 2013 Forord Denne information er udarbejdet af SIG Emesis, en landsdækkende gruppe af sygeplejersker,
Medicintilskudsnævnet
 Referat af s møde nr. 481 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 20. marts 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Referat af s møde nr. 481 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 20. marts 2018. I mødet deltog: Nævnsmedlemmer: Frank Ingemann Jensen (Danske Regioner) Janne Unkerskov John Teilmann
Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07
 Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi
Medicintilskudsnævnet Sundhedsstyrelsen Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler mod diarré og tarminflammation/infektion i ATC-gruppe A07 Baggrund og indhold Vi
Medicinpriser. Priser for den 22.10.2015. Uge 42/43
 Medicinpriser 2015 Priser for den 22.10.2015 Uge 42/43 LÆSEVEJLEDNING Medicinpriser indeholder priser på alle markedsførte apoteksforbeholdte lægemidler i Danmark. Desuden indeholder den det markedsførte
Medicinpriser 2015 Priser for den 22.10.2015 Uge 42/43 LÆSEVEJLEDNING Medicinpriser indeholder priser på alle markedsførte apoteksforbeholdte lægemidler i Danmark. Desuden indeholder den det markedsførte
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf AXEL HEIDES GADE KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 29. januar 2008 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 29. januar 2008 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for lægemidler
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 415, tirsdag den 19. august 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. august 2014. I mødet
Referat af Medicintilskudsnævnets møde nr. 415, tirsdag den 19. august 2014. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 19. august 2014. I mødet
Bilag II. Videnskabelige konklusioner
 Bilag II Videnskabelige konklusioner 14 Videnskabelige konklusioner Haldol, der indeholder det aktive stof haloperidol, er et antipsykotisk lægemiddel, der tilhører butyrophenon-gruppen. Det er en potent,
Bilag II Videnskabelige konklusioner 14 Videnskabelige konklusioner Haldol, der indeholder det aktive stof haloperidol, er et antipsykotisk lægemiddel, der tilhører butyrophenon-gruppen. Det er en potent,
Medicintilskudsnævnet
 Sundheds- og Forebyggelsesudvalget 2011-12 SUU alm. del, supplerende svar på spørgsmål 799 Offentligt Medicintilskudsnævnet Den 28. september 2012 Revurdering af lægemidlers tilskudsstatus Referat af Medicintilskudsnævnets
Sundheds- og Forebyggelsesudvalget 2011-12 SUU alm. del, supplerende svar på spørgsmål 799 Offentligt Medicintilskudsnævnet Den 28. september 2012 Revurdering af lægemidlers tilskudsstatus Referat af Medicintilskudsnævnets
BRUGERE AF OG INDBERETTEDE BIVIRKNINGER VED LÆGEMIDLER MED DESMOPRESSIN
 AUGUST 2015 BRUGERE AF OG INDBERETTEDE BIVIRKNINGER VED LÆGEMIDLER MED DESMOPRESSIN Med fokus på ældre brugere og hyponatriæmi BRUGERE AF OG INDBERETTEDE BIVIRKNINGER VED LÆGEMIDLER MED DESMOPRESSIN Med
AUGUST 2015 BRUGERE AF OG INDBERETTEDE BIVIRKNINGER VED LÆGEMIDLER MED DESMOPRESSIN Med fokus på ældre brugere og hyponatriæmi BRUGERE AF OG INDBERETTEDE BIVIRKNINGER VED LÆGEMIDLER MED DESMOPRESSIN Med
Udviklingen i forbruget af lægemidler mod depression og angst. Fra januar 2011 til december 2012. Notat
 Udviklingen i forbruget af lægemidler mod depression og angst Fra januar 2011 til december 2012 Notat Udviklingen i forbruget af lægemidler mod depression og angst Fra januar 2011 til december 2012 Sundhedsstyrelsen,
Udviklingen i forbruget af lægemidler mod depression og angst Fra januar 2011 til december 2012 Notat Udviklingen i forbruget af lægemidler mod depression og angst Fra januar 2011 til december 2012 Sundhedsstyrelsen,
INFORMATION TIL HJEMMEPLEJEN. KVALMEBEHANDLING TIL PATIENTER I MEDICINSK KRÆFTBEHANDLING
 INFORMATION TIL HJEMMEPLEJEN. KVALMEBEHANDLING TIL PATIENTER I MEDICINSK KRÆFTBEHANDLING 1 Forord Denne information er udarbejdet af SIG Emesis, en landsdækkende gruppe af sygeplejersker, der beskæftiger
INFORMATION TIL HJEMMEPLEJEN. KVALMEBEHANDLING TIL PATIENTER I MEDICINSK KRÆFTBEHANDLING 1 Forord Denne information er udarbejdet af SIG Emesis, en landsdækkende gruppe af sygeplejersker, der beskæftiger
Medicintilskudsnævnet, den 7. december Vi har modtaget høringssvar fra følgende:
 Svar på Medicintilskudsnævnets høring over nævnets forslag til indstillinger af 11 august 2016 om tilskudsstatus for lægemidler i ATC-gruppe N01 (anæstetika), N05C (mod søvnløshed) samt N07A, N07CA01,
Svar på Medicintilskudsnævnets høring over nævnets forslag til indstillinger af 11 august 2016 om tilskudsstatus for lægemidler i ATC-gruppe N01 (anæstetika), N05C (mod søvnløshed) samt N07A, N07CA01,
Afgørelse om fremtidig tilskudsstatus for midler mod funktionelle gastrointestinale forstyrrelser
 Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for midler mod funktionelle gastrointestinale forstyrrelser Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Til de på vedlagte liste anførte virksomheder Afgørelse om fremtidig tilskudsstatus for midler mod funktionelle gastrointestinale forstyrrelser Vi afslutter med denne afgørelse revurdering af tilskudsstatus
Aripiprazol. Sundhedspersonale. FAQ-brochure (ofte stillede spørgsmål)
 Aripiprazol Sundhedspersonale FAQ-brochure (ofte stillede spørgsmål) Aripiprazol er indiceret til behandling i op til 12 uger af moderate til svære maniske episoder ved bipolar lidelse type I hos unge
Aripiprazol Sundhedspersonale FAQ-brochure (ofte stillede spørgsmål) Aripiprazol er indiceret til behandling i op til 12 uger af moderate til svære maniske episoder ved bipolar lidelse type I hos unge
MEDICINFORBRUG - MONITORERING Medicinsk cannabis monitorering af brugen 1. kvartal 2018
 1 MEDICINFORBRUG - MONITORERING 2018 Medicinsk cannabis monitorering af brugen 1. kvartal 2018 Brug af medicinsk cannabis i 1. kvartal 2018 Som led i implementering af den 4-årige forsøgsordning med medicinsk
1 MEDICINFORBRUG - MONITORERING 2018 Medicinsk cannabis monitorering af brugen 1. kvartal 2018 Brug af medicinsk cannabis i 1. kvartal 2018 Som led i implementering af den 4-årige forsøgsordning med medicinsk
Medicintilskudsnævnet
 29. oktober 2013 Sagsnr: 2013034167 Forslag til indstilling Revurdering af tilskudsstatus for antipsykotiske lægemidler i ATC-gruppe N05A, N03AG01 og N03AX09 Baggrund og indhold Vi har revurderet tilskudsstatus
29. oktober 2013 Sagsnr: 2013034167 Forslag til indstilling Revurdering af tilskudsstatus for antipsykotiske lægemidler i ATC-gruppe N05A, N03AG01 og N03AX09 Baggrund og indhold Vi har revurderet tilskudsstatus
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S
 MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 10. december 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
MEDICINTILSKUDSNÆVNET SEKRETARIATET Tlf. 44 88 95 95 AXEL HEIDES GADE 1 2300 KØBENHAVN S Lægemiddelstyrelsen Den 10. december 2009 Axel Heides Gade 1 2300 København S Revurdering af tilskudsstatus for
BILAG III ÆNDRINGER TIL RELEVANTE AFSNIT AF PRODUKTRESUME, ETIKETTERING OG INDLÆGSSEDDEL
 BILAG III ÆNDRINGER TIL RELEVANTE AFSNIT AF PRODUKTRESUME, ETIKETTERING OG INDLÆGSSEDDEL Note: Produktresume og indlægsseddel vil muligvis blive ændret efterfølgende af den nationale myndighed, evt. i
BILAG III ÆNDRINGER TIL RELEVANTE AFSNIT AF PRODUKTRESUME, ETIKETTERING OG INDLÆGSSEDDEL Note: Produktresume og indlægsseddel vil muligvis blive ændret efterfølgende af den nationale myndighed, evt. i
Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens
 Medicintilskudsnævnet Den 25. oktober 207 Sagsnr: 20700643 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens aggrund Lægemiddelstyrelsen har
Medicintilskudsnævnet Den 25. oktober 207 Sagsnr: 20700643 Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod overaktiv blæresyndrom og inkontinens aggrund Lægemiddelstyrelsen har
Medicintilskudsnævnet
 Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
Medicintilskudsnævnet Forslag til indstilling Revurdering af tilskudsstatus for lægemidler mod epilepsi i ATC-gruppe N03, N05BA og N05CD Baggrund og indhold Vi har revurderet tilskudsstatus for lægemidler
Medicintilskudsnævnet
 Referat af s møde nr. 480 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 27. februar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Palle Mark
Referat af s møde nr. 480 Tid og sted: Mødet fandt sted i Lægemiddelstyrelsen, tirsdag den 27. februar 2018. I mødet deltog: Nævnsmedlemmer: Janne Unkerskov John Teilmann Larsen Michael Røder Palle Mark
Jordemoderuddannelsen Aalborg. EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00
 Jordemoderuddannelsen Aalborg EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00 1 DEL I - ingen hjælpemidler tilladt Varighed 2 timer (65 point kan opnås) 1. Beskriv de 3 faser som farmakokinetikken
Jordemoderuddannelsen Aalborg EKSTERN PRØVE FARMAKOLOGI J07S D. 14. november 2008 kl. 9.00 12.00 1 DEL I - ingen hjælpemidler tilladt Varighed 2 timer (65 point kan opnås) 1. Beskriv de 3 faser som farmakokinetikken
Medicintilskudsnævnet
 Referat af Medicintilskudsnævnets møde nr. 389, tirsdag den 26. februar 2013. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 26. februar 2013. I mødet
Referat af Medicintilskudsnævnets møde nr. 389, tirsdag den 26. februar 2013. Tid og sted: Mødet fandt sted i Sundhedsstyrelsen, Axel Heides Gade 1, 2300 København S, tirsdag den 26. februar 2013. I mødet
Til virksomheden 5. oktober 2018 Sagsnr T E
 Til virksomheden 5. oktober 2018 Sagsnr. 2018080284 T +45 93518614 E dila@dkma.dk Afgørelse om fremtidig tilskudsstatus for lægemidler til behandling af symptomer ved overgangsalder Vi afslutter med denne
Til virksomheden 5. oktober 2018 Sagsnr. 2018080284 T +45 93518614 E dila@dkma.dk Afgørelse om fremtidig tilskudsstatus for lægemidler til behandling af symptomer ved overgangsalder Vi afslutter med denne
Postoperativ kvalme og opkastning (PONV) - kan det forebygges (hvordan og hvornår)?
 Postoperativ kvalme og opkastning (PONV) - kan det forebygges (hvordan og hvornår)? Berit Ahlmann Thomsen Ortopædkirurgisk afdeling T Herlev Hospital FSOS Landskonferencen 2013 1 Postoperativ kvalme og
Postoperativ kvalme og opkastning (PONV) - kan det forebygges (hvordan og hvornår)? Berit Ahlmann Thomsen Ortopædkirurgisk afdeling T Herlev Hospital FSOS Landskonferencen 2013 1 Postoperativ kvalme og
Indlægsseddel: Information til brugeren. Unixan 200 mg depottabletter Unixan 300 mg depottabletter Unixan 400 mg depottabletter theophyllin
 Indlægsseddel: Information til brugeren Unixan 200 mg depottabletter Unixan 300 mg depottabletter Unixan 400 mg depottabletter theophyllin Læs hele denne indlægsseddel grundigt, inden du begynder at tage
Indlægsseddel: Information til brugeren Unixan 200 mg depottabletter Unixan 300 mg depottabletter Unixan 400 mg depottabletter theophyllin Læs hele denne indlægsseddel grundigt, inden du begynder at tage
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN. Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml. glyceryltrinitrat
 INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
INDLÆGSSEDDEL: INFORMATION TIL BRUGEREN Glycerylnitrat SAD, koncentrat til infusionsvæske, opløsning 5 mg/ml glyceryltrinitrat Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel,
