Forord. Januar Maria Rasmussen
|
|
|
- Helle Andrea Schmidt
- 10 år siden
- Visninger:
Transkript
1 Forord Denne specialerapport er resultatet af et eksperimentelt og et teoretisk arbejde, udført i perioden fra Oktober 2005 til Januar 2007 på Biokemisk Afdeling, Institut for Molekylær Biologi. Jeg vil gerne rette en stor tak til min vejleder Stine Falsig Pedersen for uvurderlig hjælp og vejledning i forsøgene og under rapportskrivningen. Ligeledes vil jeg gerne takke alle de studerende for en fantastisk tid igennem speciale, det har været en fornøjelse at være blandt jer. En stor del af mine resultater er præsenteret i posterform til den årlige Experimental Biology konference i Washington DC, April 2007 og er derfor publiceret i abstrakt form. Desuden er en del af resultaterne submitted til publikation i December. Januar 2007 Maria Rasmussen 1
2 Abstract Ezrin, radixin, and moesin (ERM proteins) are plasma membrane-cytoskeleton linkers coupling F-actin with integral membrane proteins, including NHE1. I therefore hypothesized that ERM proteins might be early sensors of cell volume changes and play a role in shrinkage-induced activation of NHE1. The aim of this study was to investigate the effect of osmotic cell shrinkage on ERM proteins, and to investigate the possible causal relationship between ERM proteins, NHE1 activity, Rho activity, and F-actin organization, and to address whether ezrin is involved in regulating cell survival during osmotic shrinkage. A second aim was to investigate the mechanisms involved in NHE1-mediated regulation of MAP kinases after osmotic shrinkage, specifically whether this effect could be mediated through changes in ph or in MEK1/2 and/or MKK3/6 activity. PCR analyses demonstrated the presence of ezrin, radixin, moesin and the related protein merlin in Ehrlich Lettre Ascites (ELA) cells. Osmotic shrinkage resulted in a rapid ( 1 min) phosphorylation of ERM proteins (T 558 in moesin, T 567 in ezrin, T 564 in radixin), indicative of activation. Immunocytochemical studies in ELA cells indicated that ERM protein activation was associated with translocation to the cortical region. Ezrin knockdown in ELA cells by sirna caused a % decrease in ezrin protein levels, and increased the rate of shrinkage-induced intracellular alkalinization by about 20 %. Thus, ezrin is not responsible for the shrinkageinduced NHE1 activation, but rather appears to act as a negative regulator of NHE1 activity. Shrinkage-induced ERM protein activation was not NHE1-dependent, since it was similar in AP1 cells lacking functional NHE1 versus AP1 cells overexpressing human NHE1. RhoA was activated by osmotic shrinkage of ELA cells, in a manner partially dependent on ezrin, and ezrin also appeared to be involved in the shrinkage-induced formation of ezrin- and F-actin containing microvillus-like protrusions. Ezrin was not involved in regulation of cell survival, as ezrin knock-down was not associated with changes in shrinkage-induced loss of cell viability. Elevation of ph o and ph i significantly stimulated basal JNK1/2 activity, and, to a lesser extent, p38 MAPK activity, while ERK1/2 seem to be independent of ph i. MEK1/2, the upstream kinase activating ERK1/2, was inhibited by osmotic cell shrinkage in an NHE1-dependent manner. Neither shrinkage nor NHE1 inhibition affected the activity of MKK3/6, the upstream kinase activating p38 MAPK. This indicates that shrinkageinhibition of ERK1/2 occurs at or above the MEK1/2 level, while p38 MAPK is activated independently of NHE1. MTT assays revealed that inhibition of NHE1, JNK1/2, or ERK1/2 exacerbated, while inhibition of p38 MAPK attenuated, shrinkage-induced cell death. In conclusion, ERM proteins are activated by osmotic cell shrinkage in an NHE1-independent manner. Ezrin negatively regulates NHE1, and is an important regulator of Rho activation and formation of mikrovillus-like protrusions during osmotic shrinkage, yet does not regulate shrinkage-induced cell death. The NHE1-dependent inhibition of ERK1/2 during cell shrinkage involves NHE1-dependent inhibition of MEK1/2, apparently in a ph-independent manner, while NHE1-dependent stimulation of JNK1/2 during cell shrinkage appears to reflect the alkaline optimum for JNK1/2 activity. NHE1, JNK1/2, and ERK1/2 activity favors cell survival during osmotic shrinkage, while p38 MAPK activity contributes to shrinkage-induced cell death. 2
3 Resumé Ezrin, radixin og moesin (ERM proteiner) er plasmamembran-cytoskelet kædere, der kobler F-aktin med integral membrane proteiner, inklusiv NHE1. Jeg har derfor testet om ERM proteiner kan være tidlige sensorer for cellevolumen ændringer og om de har en vigtig funktion i skrumpnings-induceret aktivering af NHE1. Formålet med dette speciale var at undersøge effekter af osmotisk skrumpning på ERM proteiner og at undersøge de mulige causale sammenhænge mellem ERM proteiner, NHE1 aktivitet, Rho aktivitet og F-aktin organisering. Jeg har også undersøgt om ezrin er involveret i regulering af celleoverlevelse under osmotisk skrumpning. Et andet formål var at undersøge de mekanismer der er involveret i NHE1-medieret regulering af MAP-kinaser efter osmotisk skrumpning, specielt om denne effekt kan være medieret gennem ændringer i ph eller i MEK1/2 og/eller MKK3/6 aktivitet. PCR analyse har demonstreret tilstedeværelse af ezrin, radixin, moesin og det relaterede protein merlin i Ehrlich Lettre Ascites (ELA) celler. Osmotisk skrumpning resulterede i hurtig ( 1 min) fosforylering af ERM proteiner (T 558 i moesin, T 567 i ezrin, T 564 i radixin) hvilket indikerer at de aktiveres. Immunocytokemi studier i ELA celler, har indikeret at ERM protein aktivering er associeret med translokering til den kortikale region. Ezrin knock-down i ELA celler vha. sirna forårsagede et % fald i ezrin protein niveau og øgede raten af skrumpnings-induceret intracellulær alkalinisering med omkring 20 %. Derved er ezrin ikke ansvarlig for den skrumpnings-inducerede NHE1 aktivering, men ser i stedet ud til at virke som en negativ regulator, for NHE1 aktivitet. Skrumpnings-induceret ERM protein aktivering var ikke NHE1 afhængig, idet den var ens i AP1 celler, der mangler funktionel NHE1, versus AP1 celler der har overekspresseret human NHE1. RhoA blev aktiveret af osmotisk skrumpning i ELA celler, på en måde der delvist er afhængig af ezrin. Ezrin ser også ud til at være involveret i skrumpnings-induceret dannelse af ezrin- og F-aktin indeholdende mikrovillus-lignende protrusioner. Ezrin var ikke involveret i regulering af celleoverlevelse, idet ezrin knock-down ikke var associeret med ændringer i skrumpnings-induceret tab af celle viabilitet. Øget ph o og ph i stimulerede significant basal JNK1/2 aktivitet og i mindre grad p38 MAPK aktivitet, mens ERK1/2 ser ud til at være uafhængig af ph i. MEK1/2, opstrøms kinasen der aktiverer ERK1/2 blev hæmmet af osmotisk skrumpning, på en NHE1-afhængig måde. Mens hverken osmotisk skrumpning eller NHE1 hæmning påvirkede aktiviteten af MKK3/6, opstrøms kinasen der aktiverer p38 MAPK. Dette indikerer at osmotisk skrumpning hæmmer ERK1/2, på et niveau over MEK1/2, mens p38 MAPK aktiveres uafhængigt af NHE1. MTT assays har vist, at hæmning af NHE, JNK1/2, eller ERK1/2 forværrer celledød, mens hæmning af p38 MAPK fremmer skrumpningsinduceret celledød. Konklusion: ERM proteiner bliver aktiveret af osmotisk celleskrumpning, på en NHE1 uafhængig måde. Ezrin regulerer negativt NHE1 og er en vigtig regulator af Rho aktivering og dannelse af mikrovillus-lignende protrusioner, under osmotisk skrumpning, men regulerer ikke skrumpnings-induceret celledød. Den NHE1-afhængige hæmning af ERK1/2 under celleskrumpning involverer NHE1-afhængig hæmning af MEK1/2, tilsyneladenede på en ph uafhængig måde, mens NHE1 afhængig stimulering af JNK1/2 under celleskrumpning, ser ud til at afspejle et alkalisk optimum for JNK1/2 aktivitet. NHE1, JNK1/2 og ERK1/2 aktivitet stimulerer celleoverlevelse under osmotisk skrumpning, mens p38 MAPK aktivitet medvirker til skrumpnings-induceret celledød. 3
4 Ordliste BCECF 2,7 -bis-(2-carboxyethyl)-5,6-carboxyflourescein BSA Bovin Serum Albumin CaM Calmodulin Caspase Cysteine-dependent aspartate specific protease DTT DiThioThreitol EATC Ehrlisch Ascites Tumor Cells EIPA EthylIsoPropylAmilorid ELA Ehrlisch Lettre Ascites ERK Extracellular Signal Regulated Kinase ERM Ezrin/Radixin/Moesin FITC Flourescein IsoThioCyanat JNK C-Jun NH 2 -terminal Kinase LALS Large Angle Light Scatter MAPK Mitogen Activated Protein Kinase MLCK Myosin Ligth Chain Kinase Moesin Membrane-Organizing Extension Spike protein MOPS 3-(N-MOrpholino) PropaneSulfonic MTT 3,[4,5-dimethylthiazol-2-yl]-2,5-difenyltetrazolium bromide NHE Na + /H + exchanger NIK NF- κb Inducing Kinase NKCC Na + /K + /2Cl - Cotransportør p38 Protein 38 p53 Protein 53 PBS Phosphate Buffered Saline PDGF Platelet-Derived Growth Factor PKA Protein Kinase A PKC Protein Kinase C PCD Programed Cell Death ROCK Rho-activated kinase RNAi RNA-interference RVI Regulatory Volume Increase SAPK Stress Activated Protein Kinase SDS-PAGE Sodium- Dodecyl- Sulfat- Poly- Acrylamide-Gel-Electroforese S.E.M. Standard Error of the Mean sirna Small Interference RNA Ste-20 Sterile-20 TBS Tris Buffered Saline 4
5 1 Formål Introduktion Volumen sensorer Aktin cytoskelettet ERM Proteiner ERM protein familien ERM protein familiens fysiologiske funktioner ERM proteins lokalisering Struktur af Ezrin ERM proteiners funktionsmekanisme Regulering af ERM proteiner Regulering af ERM proteiner via PIP Regulering af ERM proteiner gennem fosforylering Inaktivering af ERM proteiner Rho GTPaser Små GTP bindende proteiner Rho som molecular switches Aktivering og effektorer af Rho GTPaser Reciprok regulering imellem Rho og ERM proteiner ERM protein regulering gennem NHE Cellevolumen regulering Steady state volumen Regulering efter akutte cellevolumen ændringer RVD RVI Langtids- cellevolumen regulering NHE - isoformer NHE NHE1 drivkraft og struktur Regulering af NHE1 aktivitet Regulering af NHE1 under hyperton skrumpning Hæmning af NHE Mitogen aktiverede protein kinaser (MAPK) ERK, JNK og p38 MAPK ERK JNK P
6 MAP-kinaser og celleskrumpning Regulering af MAPKs og NHE Skrumpnings-induceret NHE1 aktivering regulerer MAP-kinase aktivitet MAP-kinaser regulerer NHE1 aktivering Død og overlevelses-signalering Mulige arbejdsmodeler Metoder Celler og celledyrkning ELA celler AP-1 celler og S5 celler Celledyrkning Osmotisk skrumpning Hel-celle RNA oprensning fra ELA celler Teori bag RNA oprensning vha. RNeasy teknologi Praktisk udførelse af RNA oprensning Beregning af RNA indhold Verificering af RNA indhold i ekstrakter RT og PCR Praktisk udførelse af RT PCR Praktisk udførelse af PCR Teoretiske betragtninger bag brug af fluorescerende prober Måling af ændringer i intracellulær ph Teoretiske betragtninger bag måling af intracellulær ph (ph i ) BCECF Ratio-metoden Bestemmelse af ph i ved kalibrering Beskrivelse af apparatur Praktisk udførelse af ph i bestemmelser Databehandling Bestemmelse af cellevolumen Teori Praktisk udførelse af LALS CLSM Teori Praktisk udførelse af præparater til CLSM Western blotting
7 Fremstilling af helcelleekstrakt Proteinbestemmelse Udregning SDS-PAGE teori Praktisk udførelse af SDS-PAGE Western blotting- og immunodetektions teori Praktisk udførelse af Immunodetektion Kvantitativ analyse RNA interference (RNA i ) Kontrol for sirna forsøg Praktisk udførelse af sirna forsøg MTT viabilitets-assay Praktisk udførelse af MTT forsøg ELA cellers dødelighed ved tilstedeværelse af MAPK hæmmere ELA cellers dødelighed ved tilstedeværelse af ezrin sirna, samt kontrol sirna Rho aktiverings assay Teori Praktisk udførelse af Rho aktiverings assay SDS PAGE og Western Blot analyse F-aktin kvantificering Teori Praktisk udførelse af F-aktin kvantificering Statestik Resultater NHE1 aktiveres ved celleskrumpning NHE isoformer i ELA celler Effekt af skrumpning på NHE1 og dens rolle i volumen regulering ERM proteiner aktiveres ved celleskrumpning ERM proteiners tilstedeværelse i ELA celler Lokalisering og skrumpnings-induceret translokation af ezrin i ELA celler Co-lokalisering af fosforylerede ERM proteiner med F-aktin i kortex og i mikrovilli-lignende protrusioner Rho aktiveres ved celleskrumpning NHE1s mulige roller i skrumpnings-induceret aktivering af ERM Ezrins roller ved hyperosmotisk celleskrumpning Effekten af ezrin sirna knockdown Effekten af ezrin sirna knockdown på NHE1 protein niveau
8 4.5.3 Ezrins effekt på skrumpnings-induceret NHE1 aktivering Ezrins rolle i skrumpnings-induceret Rho aktivering Ezrins rolle i regulering af F-aktin indhold og organisering under celleskrumpning i ELAceller Roller for NHE1, ezrin og PI3-kinasen i skrumpnings-induceret celledød Rho-ROCK vejens rolle i skrumpnings-induceret aktivering af NHE NHE1, MAPKs og celledød efter osmotisk skrumpning af ELA-celler phs betydning for basal aktivitet af MAPK (ERK, p38 og JNK) MEK1/2, MKK3/6 og NHE1s effekt i skrumpnings-induceret aktivering af ERK og p38 MAPK Effekt af hæmning af de tre MAPKs (ERK, JNK og p38 MAPK) på ELA celler viabilitet94 5 Diskusion Del A ERM proteiner NHE Den causale sammenhæng mellem NHE1 og ERM proteiner under hyperton skrumpning i ELA celler Aktivering af Rho-ROCK vejen efter osmotisk skrumpning og mulige causale sammenhænge med NHE1 aktivering Causale sammenhænge mellem ezrin og Rho aktivering Skrumpnings-inducerede F-aktin ændringer i ELA-celler Ezrins rolle i balancen mellem død og overlevelse efter hyperton skrumpning Del B phis betydning for fosforylering af MAP-kinaser (ERK1/2, p38 MAPK og JNK1/2) NHE1s mulige rolle i skrumpnings-induceret regulering af MEK1/2 og MKK3/ Effekt af NHE1, samt effekten af hæmning af de tre MAPKs (ERK1/2, JNK1/2 og p38 MAPK) på celledød og celleoverlevelser, efter hyperton skrumpning Konklusion Perspektivering Stjerneartikler Appendiks Materialer Opløsninger Antistoffer Hæmmere sirna Primere
9 Figur liste Figur 1. ERM familie medlemmer. 10 Figur 2. En strukturel model for ezrins opbygning 11 Figur 3. En model for ERM protein familiens kædning til plasmamembranen 12 Figur 4. Aktivering af ERM proteiner ved hyperosmotisk stress. 13 Figur 5. Regulering af Rho-GTPase cyclen.. 16 Figur 6. Rho aktivering og effektorer 18 Figur 7. En model for Rho-afhængig regulering af ERM proteiner. 19 Figur 8. En model for aktivering af ERM og Rho proteiner 20 Figur 9. Foreslået model for aktivering af NHE1 og ERM proteiner.. 20 Figur 10. Ion-transport systemer i cellevolumen regulering 23 Figur 11. En model for transportere der er involveret i RVI respons.. 24 Figur 12. Model af NHE1 proteinet. 27 Figur 13. EIPA struktur 29 Figur14. MAPK tre-trins modulet 30 Figur 15. En skematisk model for mamalian MAPK signalerings transduktionsveje. 32 Figur 16. En model for overlevelses- og dødssignaleringsveje 37 Figur 17. Arbejdsmodel for projekt A.. 38 Figur 18. Arbejdsmodel for projekt B.. 38 Figur 19. PCR metoden består af tre trin. 42 Figur 20. Fluorescens stadier.. 45 Figur 21. Stokes shift 45 Figur 22. Loadning af BCECF-AM indi celler 46 Figur 23. Excitation og emission spectra for BCECF.. 47 Figur nm/495 nm fluorescens ratio som funktion af ph i 49 Figur 25. Princippet bag CLSM Figur 26. Mekanismen bag RNA interference medieret silencing.. 60 Figur 27. OD signal som funktion af antallet af celler 63 Figur 28. OD signal som funktion af inkubationstid med MTT.. 64 Figur 13. Ekspression af NHE isoformer i ELA celler 69 Figur 30. Aktivering af NHE1 under celleskrumpning og volumen regulering.. 70 Figur 31. Ekspression af ERM og merlin proteiner i ELA celler 71 Figur 32. Lokalisering af ezrin proteiner og F-aktin under hyperton skrumpning.. 72 Figur 33. Co-lokalisering og fosforylering af ERM proteiner og F-aktin under osmotisk skrumpning. 73 Figur 34. Rho aktivering under hyperton skrumpning 74 Figur 35. Fosforylering af ERM proteiner sker uafhængigt af NHE1 tilstedeværelse 75 Figur 36. Knock down af ezrin 76 Figur 37. Knock down af ezrins betydning for NHE protein niveau i ELA celler. 77 Figur 38. Ezrins effekt på NHE1 aktivitet og volumenregulering.. 78 Figur 39. Ezrin knock-downs effekt på Rho aktivering.. 79 Figur 40. Effekten af hyperton skrumpning på cellulært indhold af F-aktin 80 9
10 Figur 41. Ezrins rolle i reorganisering af F-aktin under hyperosmotisk skrumpning.. 81 Figur 42. Effekten af osmotisk skrumpning på ELA cellers viabilitet i nærvær og fravær af EIPA Figur 43. Ezrin knock-down og hæmning af PI3Ks betydning for celle viabilitet Figur 44. Rho-ROCK vejens rolle i skrumpnings-induceret aktivering af NHE1 84 Figur 45. phs betydning for fosforylering af MAPKs.. 86 Figur 46. NHE1s effekt på skrumpnings-induceret aktivering af ERK og p38 MAPKs.. 88 Figur 47. Effekt af MAPKs hæmning på ELA cellers viabilitet 89 Figur 48. Arbejdsmodel for hypotese 1 og Figur 49. Model for projekt A 98 Figur 50. Arbejdsmodel for hypotese 3 og Figur 51. Model for projekt B
11 1 Formål Kort inden jeg påbegyndte specialearbejdet, havde man i Stine Falsig Pedersens laboratorium fundet, at ERM proteiner aktiveres af celleskrumpning i Ehrlich Lettre Ascites (ELA) celler. I dette speciale har hovedformålet været at klarlægge signaltransduktionsveje op- og nedstrøms for ERM proteiner efter celleskrumpning. Specifikt har jeg ønsket at teste følgende hypoteser: At skrumpnings-induceret aktivering af ERM proteiner, specielt ezrin, er et tidligt signal om celleskrumpning, og derved fungerer opstrøms for skrumpningsinduceret aktivering af volumenregulatoriske og celle-beskyttende mekanismer. Specifikt ønskede jeg at undersøge ezrins roller i (i) aktivering af Na + /H + exchangeren NHE1, (ii) skrumpningsinduceret F-aktin reorganisering, herunder Rho aktivering, og (iii) regulering af celleoverlevelse efter skrumpning via aktivering af en NHE1-Ezrin-PI3K-Akt/PKB overlevelsesvej. At skrumpningsinduceret aktivering af ERM proteiner er nedstrøms for aktivering af Rho-Rho kinase vejen. Desuden tydede tidligere studier i gruppen på, at aktivering af NHE1 kan lede til regulering af MAP kinase aktivitet, og i denne forbindelse ønskede jeg at teste følgende hypoteser: At skrumpnings-induceret aktivering af NHE1 kan være et opstrøms signal for regulering af MAP kinaserne ERK1/2, JNK1/2, og p38 MAPK, muligvis igennem effekter på intracellulær ph og/eller MEK1/2 eller MKK3/6 aktivitet. At disse MAP kinaser regulerer celleoverlevelse efter hyperosmotisk skrumpning 11
12 2 Introduktion Da hyperosmotisk skrumpning inducerer flere cellulære respons, inklusiv aktivering af volumenregulatoriske iontransport proteiner, cytoskeletal re-organisering og celledød, har jeg i dette speciale ønsket at klarlægge, de mulige mekanismer der fører til disse begivenheder og derved ønsket at finde eventuelle volumen sensorer, der fører til aktivering af de førnævnte begivenheder, samt undersøge de signaler der fører til de/dens aktivering. Jeg har især arbejdet udfra at ezrin/radixin/moesin (ERM) proteiner, kan være involveret i disse begivenheder, idet det tidligere er vist, at ERM proteiner aktiveres under hyperosmotisk skrumpning (Di Ciano et al., 2002)(se afsnit 2.3). Min indledning er delt op således, at der først kort beskrives om begrebet bag en volumen sensor og derefter er mulige volumensensorer diskuteret, især er ERM proteiner og cytoskelettet vigtige effektorer i volumen sensing. Til sidst findes en generel beskrivelse af cellevolumen, samt dets regulering bl.a. gennem iontransporter proteinet Na + /H + exchangeren, isoform 1 (NHE1) og de mitogen aktiverede protein kinaser (MAPK). Desuden er enkelte aspekter af skrumpnings-induceret celledød undersøgt. 2.1 Volumen sensorer Ændringer i volumen-følsomme transportveje, som respons overfor cellevolumen ændringer, bliver medieret gennem følgende mekanismer; 1) en/flere volumen sensor(er), der opfanger volumen ændringen, 2) et signal dannet af volumesensoren, der viderebringer signalet om volumenændring, 3) transduktionsveje der fører signalet videre til de rette effektorer og 4) et antal effektorer, som f.eks. volumen-følsomme ion kanaler (Hoffmann EK & Dunham PB, 1995;Hoffmann EK & Pedersen SF, 1998). Disse er forsøgt beskrevet i den nedenstående teori. Deciderede volumen-sensorer er fundet i lavere organismer som f.eks. gær (Burg et al., 1996), mens en/flere egentlig(e) volumen sensor(er) i mammale celler endnu ikke er defineret (Hoffmann EK., 1997;Pedersen SF., 2006;S.F.Pedersen C.Varming, 2002). Mulige sensorer omfatter bl.a. cytosoliske mekanismer, der f.eks. kan være baseret på ændringer i ion-styrke. Ion-styrke kan påvirke volumen sensor(er), idet ani-isotonisk svulmning eller skrumpning ændrer den intracellulære koncentration af uorganiske ioner, hvilket påvirker ion-styrken i cellens cytoplasma, som derved aktiverer effektorer (f.eks. iontransport proteiner), der registrerer volumen ændringer (se afsnit 2.7) (Mongin AA & Orlov SN, 2001). Interaktioner mellem plasmamembran proteiner og cytoskelet komponenter, f.eks. ved osmotisk stress, kan også fungere som en evt. volumen-sensor, muligevis gennem ERM proteiner (se afsnit 2.3) (Hoffmann EK., 1997;Pedersen SF., 2006;S.F.Pedersen C.Varming, 2002). I dette speciale arbejdes der kun med cytoskelettet og dets interaktioner med 12
13 plasmamembranen og derfor er det kun dem, der beskrives nærmere, som værende en del af en eventuel volumensensor. 2.2 Aktin cytoskelettet Aktin cytoskelettet består af aktin filamenter, der dannes af polymeriserede globulære aktin molekyler, der sammen med et stort antal aktin bindende og associerede proteiner, danner det såkaldte aktin cytoskelet (Schmidt A & Hall MN, 1998). Aktin cytoskelettet associerer med plasmamembranen og denne association giver mekanisk stabilitet, opretholder cellens form og adhæsion og regulerer overflade protusioner, som lamellipodier og filopodier, der er fundamentale i cellens bevægelse (Denker SP og Barber, 2002). Aktin cytoskelettet er ligeledes essentielt for regulering af ionkanal og transport protein aktivitet, opretholdelse af cellevolumen, samt fordeling af integral-membran proteiner (Cantiello HF., 1997;Papakonstanti EA et al., 2000). En familie af vigtige proteiner, der kæder det aktin-baserede cytoskelet med plasmamembranen er ERM protein familien, der danner et reguleret netværk fra filamentøs aktin (F-aktin) i kortex til membran-proteiner på celleoverfladen (afsnit 2.3). Flere integrale membranproteiner, ankrer ligeledes aktin filamenter og det kortikale cytoskelet til plasmamembranen, bl.a. gennem ion-transport proteiner som Na + /K + -ATPasen, NKCC og NHE (Cantiello HF., 1997;Denker SP og Barber, 2002) (afsnit 2.6). Cytoskelettet er involveret i volumen regulering på flere niveauer. Det kan fungere som den instans, der genererer volumen ændringssignaler, det kan være en del af en hypotetisk volumen sensor, eller det kan aktivere effektorer, enten ved vesikel medieret indsætning i plasmamembranen, eller ved direkte interaktion med effektor proteiner ved plasmamembranen, f.eks. aktivering af iontransportere, der er involveret i RVI og RVD processer (Hoffmann EK & Pedersen SF, 1998;Mongin AA & Orlov SN, 2001). Når celler ændrer volumen ændrer de også form og derfor er volumen ændringer associeret med bevægelser af cytoskelettet (Sarkadi B & Parker JC, 1991). Pedersen og kollegaer fandt i 1998, at volumen ændringer fører til ændringer i EAT-cellers F-aktin indhold og/eller organisering (ved hhv. et fald og en stigning ved RVD og RVI respons) (Pedersen et al., 1999). Den osmotiske effekt på F-aktin kan derved påvirke det kortikale cytoskelet, ved at inducere mekaniske ændringer, der ændrer cytoskelettets organisering (Mills & Mandel, 1994;Hoffmann EK & Pedersen SF, 1998), således at F- aktin ændringer kan være et vigtigt led i kæden af events, der fører fra opfangning af cellevolumen ændring, til aktivering af volumen-regulatorisk osmolyt-transport (se(henson JH., 1999;Pedersen SF & Hoffmann EK, 2002). Aktin cytoskelettet er således vigtig ved signalering fra overfladen til det indre i cellen og er herved en integreret del af cellers signal-transduktionssystem. Celleoverflade receptorer kan aktivere aktin organisering, f.eks. gennem virkning fra de små Ras-relaterede GTPaser, Rac, Cdc42 og Rho (Rho familien), der er nøgleregulatorer i signaleringsveje der kæder ekstracellulære vækstsignaler til 13
14 samling og organisering af aktin cytoskelettet (Di Ciano et al., 2002;Hall A., 1994;Schmidt A & Hall MN, 1998), (se afsnit 2.4). 2.3 ERM Proteiner ERM protein familien ERM protein familien består af 3 tæt relaterede proteiner, ezrin, radixin og moesin (se figur 1) (Sato et al., 1992). I vertebrater har ERM protein familien et højt niveau af aminosyre identitet (70-85 %), hvilket peger på at de kan stamme fra et fælles gen i lavere eukaryoter. Da ERM proteiner ikke findes i gær, tyder det på at de er udviklet specifikt i multicellulære organismer (Bretscher A et al., 2002). ERM proteiners N-terminale del er især højt konserveret (figur 1) og disse sekvenser findes ligeledes i aminoterminale ender af flere andre kortikale proteiner, inkl. human erythrocyte membranprotein bånd 4.1 protein (ca. 85 % identitet), hvilket indikerer at ERM protein familien er et medlem af bånd 4.1 superfamilien (Tsukita et al., 1994). Superfamilien af bånd 4.1 består af proteiner der deler homologi med et domæne, kaldet FERM domænet (four point one protein ezrin, radixin moesin, (Louvet-Vallee S., 2000;Tsukita S & Yonemura S, 1997), der findes i det N-terminale domæne af de fleste proteiner i superfamilien (Mangeat P et al., 1999). Der findes et ERM lignende protein, der er blevet identificeret som et tumorsupressor gen, (neurofibromatosis type 2) kaldet Merlin (moesin/ezrin/radixin-lignende protein) eller schwannomin. Merlin har høj sekvenshomologi (60 % aminosyre identitet i N-terminal, 49 % over hele proteinet) med de 3 ERM proteiner (Sato et al., 1992). Merlin har delvis overlappende funktioner med ERM proteinerne (Bretscher A et al., 2002;Vaheri A et al., 1997). Merlin proteiner har intet F-aktin bindingsdomæne i C- terminalen, men domænet kan stadig binde til FERM. Dette sker gennem Merlins interaktion med F- aktin, via aktin-bindende steder indenfor FERM domænet (Bretscher A et al., 2002;Gusella JF et al., 1999). At Merlins aminoterminale del er så homolog med ERM proteinernes, kan tyde på at Merlin kan konkurrere med ERM proteiner for deres membranbindingssted (Tsukita et al., 1994). Nedenfor ses en illustreret model, for ERM protein familien, samt Merlin og bånd 4.1 superfamilien procentvise aminosyre sekvens identitet mellem ezrin: 14
15 Figur 14. ERM protein familie medlemmer (ezrin, radixin og moesin), merlin og bånd 4.1 protein. ERM proteiner består af 3 domæner, et globulært N-terminalt membran bindingsdomæne (FERM domæne eller N-ERMAD), efterfulgt af et forlænget a-helix domæne og et positivt ladet C-term aktin bindingsdomæne (C-ERMAD). Øverst i figuren ses bindings-partnere til ERM proteiner, nogle af disse er diskuteret i nedenstående afsnit. Den procentvise aminosyre sekvens identitet i forhold til ezrin er vist for hver N- og C terminale ende, indikeret på aminosyre niveau (Tsukita & Yonemura, 1999). I dette speciale fokuseres der på ERM protein familien, især ezrin. Ezrin er det mest studerede medlem af ERM protein familien og deler ca. 75 % primær sekvens identitet med de andre medlemmer af familien (Sato et al., 1992). Da der er så høj grad af homologi mellem ERM protein familie medlemmer, vil mange af de egenskaber der karakteriserer ezrin også være gældende for radixin og moesin (Bretscher et al., 1997) ERM protein familiens fysiologiske funktioner Ezrin-radixin-moesin (ERM) proteiner er en familie af udbredte membranassocierede proteiner, der udfører en reguleret kædning mellem plasmamembran proteiner og (F-) aktin cytoskelet. ERM protein familiens sammenkædning mellem F-aktin og integrale membranproteiner ved celleoverfladen, er vigtig for cellers fundamentale funktioner, som bestemmelse af celleform, membranprotein lokalisering, membrantransport og signaltransduktion, hvilket betyder at ERM proteiner er essentielle i regulering af flere kortikale funktioner (Bretscher A et al., 2002;Bretscher A et al., 2000;Tsukita S & Yonemura S, 1997). Funktionel inaktivering af ERM proteiner har givet en idé om deres funktionelle roller. Eksperimenter med antisense oligonukleotider der er komplementære til ERM protein sekvenser, har vist at ERM protein familien har essentielle funktioner in vivo og in vitro, i celle-celle og celle-substrat adhæssion og mikrovilli dannelse, samt dannelse af andre F-aktin holdige strukturer (Saotome I et al., 2004), (Shaw et al., 1998). I celler (muse-epithel celler og thymoma celler) hvor et eller to ERM proteiner er undertrykt, er der ikke fundet nogle fænotypiske ændringer, hvilket tyder på at proteinerne kan komplementere hinanden (Bretscher A et al., 2000;Mangeat P et al., 1999;Tsukita S & Yonemura S, 1997;Tsukita et al., 1994). 15
16 2.3.3 ERM proteins lokalisering Immunoblotting og immunofluorescence microskopi har afsløret, at i de fleste dyrkede epithel- og fibroblastceller er alle tre ERM proteiner co-ekspresseret og co-lokaliseret i specialiserede regioner, hvor aktin filamenter er tæt associeret med plasmamembraner, som f.eks. i mikrovilli, i filopodier og ved cellecelle/celle-matrix adhæsionssteder (Bretscher A et al., 2002;Sato et al., 1992;Tsukita & Yonemura, 1999;Vaheri A et al., 1997). Ezrin er blevet oprenset fra cytoskelettet af intestinal mikrovilli og er til stede i aktinindeholdende overfladestrukturer i flere celletyper (Bretscher, 1983). Radixin findes ligeledes i mikrovilli i hepatocytter og i aktin indeholdende celleoverfladestrukturer. Moesin er blevet identificeret gennem dens evne til at binde heparin og findes ligeledes i celleoverfladestrukturer i dyrkede celler. Selvom mange dyrkede celler udtrykker alle 3 ERM proteiner er situationen anderledes i native væv (Bretscher A et al., 2000), idet ERM proteinerne udviser en vævsspecifik ekspression. Ezrin findes især i tarm, mave, lunger og nyrer, moesin findes i lunger og milt, mens radixin findes i lever og tarm (Louvet-Vallee S., 2000;Mangeat P et al., 1999) Struktur af Ezrin ERM proteinerne indeholder et ca. 300 residue NH 2 terminalt domæne, der direkte kan interagere med cytoplasmatiske domæner af transmembran proteiner, som CD44, CD43, EBP50, ICAM I, II og III. N- terminalen kan ligeledes binde signaleringsmolekylet PIP 2 og Rho-GDI (en regulator af Rho). Efter dette domæne findes der en α-helix region, der er efterfulgt af en F-aktin bindende region (se figur 2), (Turunen et al., 1994;Reczek & Bretscher, 1998) Figur 15. En strukturel model for ezrins opbygning. I figuren er C- og N-terminale bindingssteder illustreret. * markerer de bindingssteder, der menes at være masket, når ezrin ikke er aktiveret. Øverst er de forskellige domæners længde angivet som aminosyre-længde. Området fra indeholder et polyprolin område, hvis funktion stadig er ukendt. (figuren er modificeret fra (Bretscher et al., 1997). 16
17 2.3.5 ERM proteiners funktionsmekanisme At der findes både plasmamembran-binding og aktin-bindingsdomæner i ERM proteinerne, tillader dem at fungere som plasmamembran/aktin filament krydsbindere (Tsukita et al., 1994;Turunen et al., 1994). Association mellem aktin filamenter og plasmamembran giver strukturel support til plasmamembranen og er en nøgle komponent i opretholdelse af celleform og regulering af dynamiske aktin remodelerings processer (Denker SP et al., 2000;Bretscher A et al., 2000). ERM proteiner bliver konformationelt reguleret, således at de i deres inaktive stadie har masket deres NH 2 - og COOH-ERM associations-domæner (N- og C-ERMADs) og derved findes i en auto-hæmningskonformation (Ivetic A & Ridley AJ, 2004;Reczek & Bretscher, 1998). Et eller flere signaler kan aktivere ERM proteiner, der herved eksponerer sine bindingsteder ved begge terminale ender, hvorved de bliver i stand til at fungere som crosslinkere lige under plasmamembranen (Bretscher A et al., 2002;Louvet-Vallee S., 2000;Tsukita S & Yonemura S, 1997;Tsukita et al., 1994). Inaktiv ERM findes i cytosolet, mens aktiveret ERM er membran-associeret og binder med integral membranproteiner via deres N terminale FERM domæne og med F-aktin via deres C- terminal, hvilket er illustreret i figur 3 (Ivetic A & Ridley AJ, 2004;Reczek & Bretscher, 1998;Tsukita et al., 1994). ERM protein familiens kædning til plasmamembranen gennem FERM domænet, sker på flere måder, enten direkte via deres kædning til den cytoplasmatiske hale af membranproteiner med enkelt transmembran domæner, som CD43, CD44 og I-CAM 1-3 (Barret et al., 2000), eller indirekte gennem adaptor molekyler, som EBP50 (ERM-Binding phosphoprotein 50)/NHE-RF (Na + /H + exchangeregulatorisk faktor) med flere transmembrane domæner (Bretscher A et al., 2000;Mangeat P et al., 1999). Nedenstående figur illustrerer den direkte og den indirekte aktiveringsmekanismen for ezrin. Figur 16. En model for ERM protein familiens kædning til plasmamembranen. ERM proteiner findes i et hvilende, monomerisk form hvori FERM/N-ERMAD domæner er associerede med C-ERMAD. a) Et eller flere signaler aktiverer ERM, løsner den auto-hæmmende konformation og rekrutterer dem til plasmamembranen b) Aktiveret ERM kan herefter være en del af mikrofilament-membran kædning ved direkte association med membran proteiner, eller c) indirekte gennem scaffolding molekyler som EBP50/NHE-RF (Modificeret fra (Bretscher A et al., 2002). 17
18 At ERM proteiner translokeres til plasmamembranen/det kortiakle cytoskelet under hyperosmotisk skrumpning, er yderligere bekræftet via CLSM billeder med antistof rettet mod ERM og fosforyleret ERM i ELA celler, udført af Barbera Darborg og Stine Falsig Pedesen (Barbara Vasek Darborg et al., 2005), se figur 4. Isoton 1 min hyp 5 min hyp ERM Fosforyleret ERM Figur 17. Aktivering af ERM proteiner ved hyperosmotisk stress. I forsøget har de udsat ELA celler for isoton eller hyperton ringer og derefter mærket for hhv. ERM og fosforyleret ERM proteiner. Som det ses findes ERM proteiner både i cytosol og i kortikale regioner under isotonicitet, mens de translokeres ERM proteiner til cellens periferi under skrumpning (Rasmussen M et al., 2007) Regulering af ERM proteiner Aktivering af ERM proteiner, resulterer i unmasking af deres funktionelle bindingssteder og sker som tidligere nævnt gennem konformationelle ændringer, udløst af et eller flere signaler. 2 signaleringsveje menes at medvirke til aktivering af ERM proteiner in vivo og in vitro; fosforylering af et konserveret threonin residue i aktin bindingsstedet (Thr 567 (ezrin)/thr 564 (radixin)/thr 558 (moesin)) i C-terminalen (Matsui T et al., 1999) og interaktion af fosfatidyl-inositol(4,5)bisfosfat med FERM domænet (Hirao et al., 1996;Niggli V et al., 1995). Tilstedeværelse af fosfolipider unmasker generelt membranprotein og F-aktin bindingstederne, mens fosforylering svækker FERM/hale interaktioner, således at de to domæner ikke kan interagere igen, når proteinet først er aktiveret, mens (Pearson MA et al., 2000). Se nedenstående afsnit for yderligere forklaring. 18
19 Regulering af ERM proteiner via PIP 2 I 1994 fandt Tsukita og kollegaer, at moesin co-precipiteres sammen med CD44 i Baby Hamster Kidney celler (BHK), samt at ERM proteiner generelt co-lokaliserer med CD44 i mikrovilli i BHK- og i L celler fra mus (Tsukita et al., 1994). Hirao og kollegaer (1996) fandt yderligere, at den N-terminale del af ERM binder direkte til det cytoplasmatiske domæne af CD44, mens fuldlængde (inaktiv) ERM kun binder, under lave salt koncentrationer eller ved tilstedeværelse af fosfoinositider, specielt PIP 2 (Hirao et al., 1996). ERM proteiner indeholder bindingssteder for PIP 2 (Niggli V et al., 1995), hvilket kan forklare deres afhængighed af PIP 2 tilstedeværelse for deres aktivering. PIP 2 er en vigtig second messenger i regulering af flere aktin-cytoskeletale dynamiker, idet PIP 2 binder og regulerer funktionen af mange aktin-bindende proteiner (Aspenstrom P., 1999;Hirao et al., 1996). Andre studier har fundet, at det cellulære nivaeu af PIP 2 stiger under osmotisk skrumpning i flere celletyper, samt at den skrumpningsinducerede translokation af ezrin til plasmamembranen ikke ses, når plasmamembranen er depleteret for PIP 2, hvilket indikerer at den skrumpnings-inducerede stigning i PIP 2 er det signal, der initierer skrumpnings-induceret ERM protein fosforylering (Barret et al., 2000;Fievet et al., 2004;Hirao et al., 1996;Rasmussen M et al., 2007) Regulering af ERM proteiner gennem fosforylering Fosforylering af det konserverede threonin residue i ERM proteinernes C-terminal, er vigtig for ERM proteinernes krydsbindingsaktivitet, idet det generelt menes, at fosforylering af dette threonin residue, stabiliserer den aktive konformation af ERM proteiner, ved at hindre interaktion mellem deres N- og C terminale domæner, efter deres aktivering (Fievet et al., 2004;Hayashi et al., 1999;Tsukita S & Yonemura S, 1997). Flere Ser/Thr protein kinaser er ligeledes impliceret i regulering af ERM protein funktion gennem fosforylering af C terminalens konserverede threonin residue. Disse inkluderer bl.a. protein kinase C (PKC) og den ste20 relaterede Nck-interacting kinase (NIK), der fosforylerer ERM proteiner in vitro og/eller in vivo. Rho kinase medierer også ERM protein fosforylering in vitro (Matsui T et al., 1999;Tsukita S & Yonemura S, 1997), men det er kontroversielt om den spiller en rolle in vivo (Ivetic A & Ridley AJ, 2004;Nakamura N et al., 2000), eller om involvering af Rho i ERM protein aktivering sker gennem en anden Rho effektor nemlig fosfatidyl-inositol 4-fosfat-5 kinase (PI4P5K), der hæver det cellulære niveau af PIP 2 (Rasmussen M et al., 2007;Matsui T et al., 1999). Rhos rolle i fosforylering/aktivering af ERM er yderligere diskuteret i afsnit
20 2.3.7 Inaktivering af ERM proteiner ERM protein inaktiveres ved defosforylering og resulterer i translokation af proteinet til cytoplasmaet (se (Louvet-Vallee S., 2000). ERM proteinerne inaktiveres ligeledes ved nedregulering af aktiveringssignaler (Tsukita & Yonemura, 1999), samt af myosin fosfatase der er en del af myosin-bindings subuniten af myosin fosfatasen. Denne fosfatase kan interagere med moesin og derved de-fosforylere moesin ved T558 in vitro (Ivetic A & Ridley AJ, 2004). 2.4 Rho GTPaser Små GTP bindende proteiner Små GTP-bindende proteiner er monomere G proteiner, med en molekylær vægt på ml 20 og 40 kda. Der er blevet identificeret mere end 100 forskellige små G proteiner i eukaryote celler, fra gær til mennesker. Proteinerne kan inddeles i underfamilier, der strukturelt kan klassificeres i mindst 5 familier: Ras, Rho, Rab, Sar1/Arf og Ran, (Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Generelt regulerer Ras familien af GTPaser signaleringsevents, der fører til ændringer i gen-transkription, Rab og Arf familien kontrollerer dannelse, fusion og bevægelse af vesikel transport mellem membranafdelinger i cellen, mens Ran GTPaser regulerer både mikrotubuli organisering og nucleocytoplasmatisk protein transport (Sasaki T & Takai Y, 1998;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). I dette speciale er der kun arbejdet med Rho og det er derfor kun den, der nærmere vil blive beskrevet. Rho GTPaser inkluderer 14 forskellige familie medlemmer i mammale celler (Rac 1-3, Cdc42, TC10, RhoA-E, G, H og Rnd1 og 2), hvoraf de bedst karakteriserede er Cdc42, Rac og RhoA (Aspenstrom P., 1999). Rho/Rac/Cdc42 underfamilien (Rho familien) regulerer både cytoskelet reorganisering og gen ekspression. Rac regulerer lamellipodie dannelse og membran ruffling og cdc42 regulerer filopodium dannelse (Hall A., 1994), mens Rho fungerer som centrale regulatorer af organisering af aktin cytoskelettet i mange celletyper og er vigtige regulatorer af aktin polymerisering og myosin aktivitet, to vigtige drivende kræfter for det aktin-baserede cytoskelets bevægelse (Ridley AJ & HallA, 1994). Specifikt ser det ud til at Rho spiller en vigtig rolle i at styrke det kortikale cytoskelet, ved at facilitere perifer de novo F-aktin samling og ved at inducere translokation af kortaktin, et protein der fremmer aktin polymerisering og stabiliserer nyligt genereret aktin netværk (Ciano-Oliveira et al., 2003;Lewis et al., 2002). De fleste små G proteiner findes spredt i mammale celler og næsten alle celler har Ras, Rho, Rab, Sar1/Arf og Ran familier ekspresseret, selvom ekspressions niveauer af deres 20
21 medlemmer kan variere fra en celletype til en anden (Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001) Rho som molecular switches Som andre G proteiner cycler små G-proteiner mellem et GDP-bundet inaktivt og et GTP-bundet aktivt stadie. Et opstrømssignal stimulerer dissociation af GDP fra den GDP bundne form, hvilket er efterfulgt af binding af GTP, der fører til en konformationel ændring af en effektor-bindingsregion, således at denne region interagerer med nedstrøms effektorer (Sasaki T & Takai Y, 1998;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Denne mekanisme tilader GTPaser at cycle mellem en aktivt GTP bundet og en inaktivt GDP bundet konformation. Der findes mindst 3 typer af regulatorer for små G-proteiner (se figur 5). 1) GDP/GTP exchange protein (GEP), der stimulerer omdannelse fra den GDP-bundne form til den GTP-bundne form, 2) Guanine nucleotid dissociation inhibitorer (GDIs), der hæmmer denne reaktion og 3) GTPaseaktiverende proteiner (GAPs), der stimulerer omdannelse af den GTP-bundne form til den GDP-bundne form. I cytosolet danner Rho/Rac/Cdc42 protein et komplex med GDI og opretholder derved en GDPbunden inaktiv form. Den GDP bundne form bliver frigivet fra GDI ved en endnu ukendt mekanisme og bliver derefter omdannet til den GTP bundne form vha. GEP. Den GTP bundne interagerer herefter med nedstrøms effektorer, hvirefter den GTP bundne form omdannes til den GDP-bundne form, hvilket fører til dannelsen af et kompleks med GDI og det returnerer til cytosolen (Lewis et al., 2002;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Gennem denne cyclus af aktivering og inaktivering, vil små G proteiner fungere som molecular switches, der transducerer opstrøms signaler til nedstrøms effektorer (Aspenstrom P., 1999;Ciano-Oliveira et al., 2003;Ivetic A & Ridley AJ, 2004;Sasaki T & Takai Y, 1998;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Figur 18. Regulering af Rho-GTPase cyclen. 3 klasser af proteiner regulerer denne cycel. I ustimulerede celler er Rho- GTPaser opretholdt i et inaktivt stadie i cytoplasmaet, via binding til Rho-GDI. Flere RhoGDIs regulerer cyclingen af rho mellem membranen og cytoplasmaet (Yixian Zheng, 2004). Dissociation af Rho-GDI fra Rho, kan f.eks. ske gennem fosforylering eller interaktion med aktiverede og udfoldede ERM proteiner. Membran rekrutering og interaktion med RhoGEFs inducerer exchange af GDP for GTP på RhoGTPaserne. Når Rho-GTPaser er bundet til GTP kan den interagere og derved aktivere nedstrøms effektorer (f.eks. ROCK eller Rho-kinase). RhoGAPs inaktiverer RhoGTPaser ved at øge deres GTPase aktivitet, hvilket resulterer i accelereret hydrolyse af GTP til GDP (Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). 21
22 Det hastighedsbegrænsende trin i GDP/GTP udvekslings reaktionen er dissociation af GDP fra den GDP bundne form (Bhattacharya M et al., 2004;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Denne reaktion er langsom og stimuleres derfor af en regulator, kaldet GEP eller GEF (guanine nucleotide releasing factor), hvis aktivitet ofte er reguleret af et opstrøms signal. GEP interagerer først med den GDP bundne form og frigiver bunden GDP, hvilket danner et kompleks mellem små-g proteiner og GEP. GEP udskiftes herefter af GTP og danner derved den GTP bundne form. GDP/GTP udvekslings reaktioner fra Rho/Rac/Cdc42 proteiner bliver yderligere reguleret af en anden type af regulator, kaldet Rho-GDI. Denne type regulator hæmmer både basal og GEP-stimuleret dissociation af GDP fra den GDP-bundne form og opretholder små-g proteinet i den GDP bundne form. Rho GDI har større substrat specificitet end GEPs og GTPase aktiverings proteiner (GAPs) og de er aktive i alle Rho/Rac/Cdc42 proteiner (Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001) Aktivering og effektorer af Rho GTPaser Signalering fra celleoverfladereceptorer til Rho proteiner, sker gennem f.eks. tyrosinreceptor kinaser og G-protein koblede proteiner (Hall A., 1994). Aktiveringen af Rho proteiner kan ligeledes ske gennem LPA, mitogener, integrin aktivering (Bishop AL & Hall A, 2000), (Pedersen et al., 2002), eller gennem vækstfaktorer som PDGF, EGF og insulin (Burridge K & Wennerberg K, 2004;Pedersen et al., 2002). Rho familien af GTPaser bliver stimuleret/aktiveret af hyperosmotisk stress (Tilly BC et al., 1996) (hvilket jeg også finder i dette speciale, se afsnit 4.3), samt ved en stigning i den intracellulære ion-styrke (i kidney proximal tubule (LLC-PK1) celler) (Ciano-Oliveira et al., 2003;Lewis et al., 2002). Osmotisk stress kan virke ved at ændre konformationen af overfladereceptorer for vækst faktorer og cytokiner og derigennem subverte deres tilknyttede signaleringsveje. Derved kan disse receptorer, som er kendte regulatorer af Rho familien af GTPaser, virke som potentielle osmosensorer (C.Di Ciano-Oliveira et al., 2006;DeMali KA et al., 2003). Der findes et hav af formodede nedstrøms effektorer for Rho (se figur 6). Blandt disse er Rho kinase (p164rokα og p160rokβ/rock isoformer), myosin light chain kinase (MLCK), protein kinase C (PKC) og p38 MAPK, der alle aktiveres af osmotisk stress og alle er vigtige modulatorer af organisering af det aktin-baserede cytoskelet (Pedersen SF & Hoffmann EK, 2002). ROCK (en serine/threonin protein kinase), også kaldet ROKa/Rho-kinase regulerer dannelse af stress fibre og fokale adhæsioner. Den fosforylerer mange substrat proteiner, som MLC fosfatase, LIM-kinase og ERM familien(takaishi K et al., 2000;Yoshimi Takai & Takuya Sasaki and Takashi Matozaki, 2001). Andre Rho effektorer inkluderer Phosphatidylinositol 3-kinase (PI3K) og Phosphatinositol-4-phosphat 5 kinase (PI4P5 kinase), der er en del af den Rho-medierede F-aktin reorganisering (Pedersen et al., 2002). PI4P5 kinase fører til dannelse af PIP 2, der er en særlig vigtig regulator af den Rho inducerede aktin re- 22
23 organisering, idet den binder til GEFs af Rho familien og derved påvirker aktiviteten af flere aktinbindende proteiner in vitro, derfor er det muligt, at ved at øge niveauet af PIP 2, kan Rho inducere aktin polymerisering in vivo (Ridley AJ & HallA, 1994;Stossel, 1989;Zigmond SH., 1996). Det er ligeledes vist at p160 Rho-associeret kinase (p160rock) kan være involveret i aktivering af NHE1 (Tominaga T et al., 1998). Andre studier har dog fundet det modsatte, at NHE1 aktivitet sker uafhængigt af Rho-kinase (C.Di Ciano-Oliveira et al., 2006). Figur 19. Rho aktivering og effektorer. Signalering fra celleoverfladereceptorer til Rho proteiner, sker gennem f.eks. tyrosinreceptor kinaser og G-protein koblede proteiner. Nedstrøms for Rho findes et hav af effektorer, der kan regulere organiseringen af det aktin baserede cytoskelet. Figuren illustrerer nogle enkelte eksempler. 2.5 Reciprok regulering imellem Rho og ERM proteiner Rho aktivering regulerer ERM protein aktivering Flere studier har peget på, at Rho aktiverer ERM proteiner. Det er bl.a. fundet at Rho-GDI co-lokaliseres sammen med ERM/CD44 komplekser i MDCK, Cos7- og i BHK celler in vitro. Da ERM proteiner ikke kan danne kompleks med CD44 før de er aktiveret, indikerer fundet af Rho-GDI i komplekset at Rho er involveret i aktiveringen af ERM proteinerne (Hirao et al., 1996;Tsukita et al., 1994). Ligeledes har forsøg med permeabiliserede BHK celler in vivo vist, at ERM proteiners association med CD44 (og derved deres aktivering) svækkes, når der ikke er Rho tilstede, mens associationen blev fremmes af tilstedeværelse af Rho, hvilket yderligere indikerer, at Rho er involveret i aktivering af ERM proteiner (Hirao et al., 1996;Takahashi K et al., 1998). Selvom Rho aktivering kan inducere ERM protein aktivering in vivo, kan aktiveringsmekanismer muligvis også være moduleret gennem andre Rho effektor 23
24 proteiner, som f.eks. PI4P5K der øger den cellulære mængde af PIP 2 (Matsui T et al., 1999), hvilket er beskrevet yderligere i afsnit Da ERM proteiner, som tidligere nævnt indeholder et bindingssted for PIP 2 (Niggli V et al., 1995) og det at deres kompleksdannelse med CD44 in vitro, er afhængig af PIP 2 (Hirao et al., 1996), kan tyde på at PIP 2 binding og RhoA afhængig fosforylering, er de signaler der aktiverer ERM (Shaw et al., 1998). Matsui og kollegaer har yderligere fundet, at ved overekspression af fosfatidylinositol 4-fosfate 5-kinase, øges niveauet af CPERMs og derved ses en stigning i mikrovilli dannelse (Matsui T et al., 1999) og som tidligere nævnt har Barret og kollegaer fundet, at mutationer i PIP 2 stedet i ezrin, påvirker ERM proteinernes lokalisering ved plasmamembranen og derved deres aktivering (Yonemura et al., 2002). Da PIP 2 bliver produceret på en Rho-afhængig måde og direkte aktiverer ERM proteiner, kan den Rho-afhængige aktiveringsmekanisme for ERM proteiner, beskrives udfra følgende figur: Figur 20. En model for Rho-afhængig regulering af ERM proteiner. Ekstracellulære stimuli, som f.eks. LPA aktiverer Rho. Flere signaleringsveje der kommer fra aktiveret Rho, regulerer organisering af aktin cytoskelettet. Rho afhængig aktivering af PI4P5K resulterer i et øget niveau af PIP 2, hvilket kan åbne inaktiv ERM protein og derved kan ERM blive fosforyleret ved deres C-terminal af kinaser som f.eks. PKC. ERM proteinernes åbne konformation krydsbinder til aktin filamenter og plasmamembran og kan derved f.eks. danne mikrovilli. Aktiverede ERM proteiner danner et positivt feedback loop til Rho aktivering. aminoterminalen af ERM binder til Rho-GDI, der er i kompleks med Rho-GDP. Ved denne binding bliver Rho-GDI hæmmet og det fører til aktivering af Rho- GTP (Figuren er fra (Matsui T et al., 1999). Ligeledes har studier med ELA og LLC-PK1-celler, hvor man transient har udtrykt konstitutivt aktivt Rho, vist at ERM protein fosforylering øges kraftigt (Rasmussen M et al., 2007) ERM protein aktivering regulerer Rho aktivitet I modsætning til at Rho aktiverer ERM proteiner, er det også blevet fundet, at Rho proteiners aktivering sker gennem regulering fra ERM proteiner, idet det er vist, at ERM kan displacere den GDP-bundne form af Rho proteiner fra Rho-GDI (Takahashi et al., 1997). RhoGDI kan binde til den aminotermiale del af 24
25 ERM proteiner, men ikke til inaktive ERM proteiner, hvilket indikerer at ERM proteinerne er aktive før, de interagerer med RhoGDI. Derfor kan aktivering af ERM proteiner, der binder til Rho-GDI være en forudsætning for aktivering af Rho signaleringsveje (Bretscher A., 1999;Bretscher et al., 1997;Mackay et al., 1997;Takahashi et al., 1997). Derfor kan en anden mulig signaleringsvej for aktivering af Rho være følgende: Figur 21. En model for aktivering af ERM og Rho proteiner. Den GDP-bundne form af Rho danner kompleks med Rho-GDI. ERM proteiner kan frigive Rho-GDI fra dette kompleks, således at Rho proteinet herefter kan aktiveres af Rho- GEPs. Figuren er fra (Sasaki T & Takai Y, 1998). Ud fra disse studier ser det ud til at ERM proteiner kan virke både opstrøms og nedstrøms for Rho GTPaser, hvilket tyder på eksistens af et positivt feedback loop mellem de to typer af proteiner (Bretscher et al., 1997;Hirao et al., 1996;Ivetic A & Ridley AJ, 2004). 2.6 ERM protein regulering gennem NHE1 ERM protein regulering kan muligvis ske gennem NHE1, idet Denker og kollegaer har fundet, at ezrin associerer med NHE1. Direkte association mellem NHE1 og ezrin spiller en vigtig rolle i celle migration og organisering af det kortikale cytoskelet (Denker SP et al., 2000;Denker SP og Barber, 2002). Denker og kollegaer har ud fra deres studier foreslået en model, hvori NHE1 ankrer aktin filamenter til plasmamembranen gennem en direkte interaktion med ERM proteiner, hvilket betyder at NHE1 virker som et anker for aktin filamenter til at kontrollere integriteten af det kortikale cytoskelet. Figur 22. Foreslået model for aktivering af NHE1 og ERM proteiner. Aktivering af NHE1 faciliterer binding af ERM proteiner til det cytoplasmatiske domæne af NHE1. Figuren er modificeret fra (Denker SP et al., 2000) 25
26 Aharonovitz og kollegaer har vist, at både NHE1 og ERM proteiner kan interagere med PIP 2 og at PIP 2 s tilstedeværelse er nødvendig for ERM proteinernes evne til at interagere med andre proteiner og derved nødvendig for associationen mellem NHE1 og ERM proteiner. De har derfor foreslået en model, hvorved binding af PIP 2 til ion transport proteiner, kan inducere en konformationel ændring, der unmasker steder for binding af cytoskeletale linkere og derved stimulerer transport aktivitet (Aharonovitz et al., 2000). 2.7 Cellevolumen regulering Eukaryote celler er særlig følsomme overfor ændringer af deres volumen, idet deres plasmamembran har en høj permeabilitet overfor vand, samtidig med at deres membraner ikke er rigide og derfor ikke kan modstå hydrostatiske tryk gradienter, der opbygges når vand trænger ind i cellen (LANG et al., 1998a), (se (Mongin AA & Orlov SN, 2001). Hovedparten af vand-bevægelse over den semi-permeable membran kaldes for osmose. Trykket der kræves for at stoppe vand-flowet, kaldes for det osmotiske tryk og er defineret ud fra van t Hoff loven (Strange, 2004): Δπ = RTΔC i Hvor Δπ er den osmotiske tryk forskel, R er gaskonstanten, T er den absolute temperatur og ΔC i er forskellen i solute koncentration over membranen. Vand er generelt i termodynamisk ligevægt over plasmamembranen, hvilket betyder at den osmotiske koncentration af cytoplasmatiske og ekstracellulære væsker (hhv. π i og π o ) vil være ens under steady state omstændigheder. Ændringer i intracellulær eller ekstracellulær osmolyt indholdet, danner den transmembran osmotisk gradient (Δπ). Da cellemembraner er permeable overfor vand, vil tryk gradienter resultere i vandflow ind eller ud af cellen indtil ligevægt etableres igen og derved kan cellerne svulme eller skrumpe, som respons overfor osmotiske forstyreleser (Strange, 2004). Cellevolumen bestemmes herved af en sammenhæng mellem koncentrationen af osmolytter i den ekstracellulære væske og koncentrationen i det cellulære cytoplasma (Hoffmann EK., 1997). De fleste celler reagerer overfor svulmning eller skrumpning ved at aktivere specifikke membrantransport og/eller metaboliske processer, der fungerer ved at returnere cellen til dens normale steady-state volumen. Disse funktioner er essentielle for normale cellefunktioner og opretholdelse af cellevolumen er derfor en forudsætning for cellens overlevelse (Strange, 2004). Cellevolumen bliver udfordret af flere faktorer, der forstyrrer denne 26
27 osmotiske ligevægt. Udover ændringer i ekstracellulær ion sammensætning, kan energi depletering, ændringer i ion-transport, substrat transport og metabolisme også forstyrre cellevolumens ligevægt (Ritter M et al., 2001), (Strange, 2004). Når man diskuterer regulering af cellevolumen er det vigtigt at skelne mellem faktorer der bestemmer 1) steady-state cellevolumen, se afsnit 2.7.1, 2) mekanismer der korrigerer for akutte forstyrrelser i dette volumen, se afsnit og 3) Langtidsforstyrrelser, der fører til øget ekspression af f.eks. transportproteiner, se afsnit Disse skal betragtes som tre forskellige processer og de er nærmere beskrevet i nedenstående afsnit (O'Neill, 1999) Steady state volumen Selv under fysiologiske steady-state omstændigheder, vil celler konstant regulere deres volumen (Hoffmann EK., 1997), idet cytoplasmaet indeholder et stort antal af impermeable makromolekyler (som DNA og proteiner f.eks.), der er negativt ladede og derfor vil trække uorganiske ioner af modsat ladning ind i cellen (Mongin AA & Orlov SN, 2001;Sarkadi B & Parker JC, 1991). Det betyder at cellen har en tendens til at svulme, under steady state forhold. Plante- og bakterieceller har rigide cellevægge, der tillader et højt osmotisk turgor tryk i cellerne, uden at disse springer. I modsætning har dyreceller ikke en rigid cellevæg og kan derfor ikke modstå opbygning af intracellulært tryk (Okada Y., 2004;Sarkadi B & Parker JC, 1991). Når dyreceller skal opretholde deres cellevolumen under steady state, er de derfor nødt til at kompensere for denne ophobning af vand, ellers vil cellerne sprænges (Mongin AA & Orlov SN, 2001). Steady-state volumen regulering sker hovedsageligt gennem "pump and leak" mekanismer, hvor osmotisk tryk, der stammer fra disse ikke-permeable makromolekyler bliver modbalanceret, via den såkaldte Gibbs-Donnan ligevægt, der etableres gennem Na + /K + -pumpen, der pumper 3 Na + ud af cellen, samtidigt med at den pumper 2 K + ind i cellen (Hoffmann EK., 1997;Mongin AA & Orlov SN, 2001;Okada Y., 2004;Sarkadi B & Parker JC, 1991). Dette skaber en ubalance over membranen i fordeling af Na + og K +. Da plasmamembranen har en højere selektiv permeabilitet overfor K + i forhold til Na +, vil denne ulige fordeling, resultere i et udad K + flux og derved et negativt membranpotentiale, der driver Cl - ud af cellen. Denne evne til at uddrive Na + og Cl - ser ud til at være den pricipielle mekanisme der opretholder steady state cellevolumen (LANG et al., 1998b;O'Neill, 1999). Extrusionen af Cl - vil samtidig kompensere for cellens tilstedeværelse af makromolekyler (LANG et al., 1998b;Mongin AA & Orlov SN, 2001;Okada Y., 2004). 27
28 2.7.2 Regulering efter akutte cellevolumen ændringer Dyreceller vil, når de udsættes for akutte osmotiske forstyrrelser, svulme eller skrumpe via osmose (se afsnit 2.7). Processer hvorved svulmede og skrumpede celler kommer tilbage til deres normal stadie, kaldes hhv. regulatory volume decrease (RVD) og regulatory volume increase (RVI) (Hoffmann EK., 1997;Sasaki T & Takai Y, 1998;Strange, 2004). RVI og RVD sker gennem aktivering af specifikke ion transport proteiner i plasmamembranen der medierer netto flux af osmotisk aktive molekyler (og derfor vand) (O'Neill, 1999). Figur 10 viser en oversigt over de vigtigste iontransport processer der aktiveres ved hhv. RVI og RVD i forskellige celltyper: Figur 23. Ion-transport systemer i cellevolumen regulering. Øverst ses et typisk RVI respons, mens der nederst ses et typisk RVD respons. Aktivering af disse transportveje sker hurtigt og indenfor sekunder eller minutter efter volumen forstyrrelsen (Strange, 2004) RVD Celler der udsættes for en hypoton opløsning, eller som får en øget mængde organiske eller uorganiske osmolytter intracellulært, vil efter initiel svulmning, undergå langsommere, kompensatorisk skrumpning, gennem tab af intracellulære osmolytter og osmotisk betinget vand, en proces kaldet RVD. I Ehrlich celler og i mange andre celletyper aktiverer cellesvulmning transportveje, der resulterer i netto efflux af K +, Cl - og andre organiske osmolytter. K +, Cl - tabes fra cellen via separate K +, Cl - konduktive transportveje, således at cellen returneres til dens set-point (Grinstein S & Foskett JK, 1990;Hoffmann EK., 1997;Sasaki T & Takai Y, 1998). Elektroneutral K + /Cl co-transport kan ligeledes medvirke til RVD respons. I Amphiuma blodceller har Cala og kollegaer vist, at cellers hypotone svulmning, resulterer i aktivering af elektroneutral K + /H + exchange, der er koblet til Cl - /HCO - 3 udveksling, hvilket fører til et 28
29 netto tab af KCl, sammen med osmotisk betinget vand (Cala & Maldonado, 1994;Grinstein S & Foskett JK, 1990) RVI Ved hyperton skrumpning, vil mange celler først skrumpe og derefter svulme ved at optage osmolytter, en proces kaldet RVI. Amphiuma blodceller og Necturus galdeblære epithelceller er blandt de få celletyper, der kan udføre et RVI-respons efter direkte hypoton skrumpning. Andre celler som f.eks. lymfocytter og EATC, udviser kun et meget svagt RVI-respons, efter direkte hyperton skrumpning. Alligevel kan disse celler stadig udføre volumen gen-oprettelse efter osmotisk skrumpning. Cellerne skal dog først igennem en såkaldt RVI- efter RVD protokol (Hoffmann EK & Dunham PB, 1995), hvor cellerne først undergår et RVD respons (cellerne vil svulme, tabe ioner og derved volumen regulere). Derefter tilføres cellerne isotont medie, der nu vil være hypertont for cellerne og derved vil cellerne volumenregulere (Hoffmann EK & Dunham PB, 1995;Kenneth R.Hallows and Philip A.Knauf, 1994). Det primære RVI respons er karakteriseret ved et optag af både NaCl, KCl, samt osmotisk betinget vand (Hoffmann EK., 1997;Kenneth R.Hallows and Philip A.Knauf, 1994). Optaget af disse salte sker hovedsageligt gennem NHE og Cl - - /HCO 3 exchangere (Anion exchangeren, AE) og/eller NKCC cotransporteren (Okada Y., 2004;Strange, 2004). Aktivering af NHE er den primære event under et RVI-respons og dens aktivering fører til en stigning i ph i, der sekundært stimulerer AE (Cala, 1980;Hoffmann EK & Dunham PB, 1995). Ved celleskrumpning vil aktiviteten af disse to transportører føre til et H + efflux, der er koblet til Na + indflux, samt til efflux af HCO - 3, der er koblet til influx af Cl - (LANG et al., 1998b;Pedersen SF & Cala PM, 2004) (se figur 11). H + - og HCO 3 kombineres ekstracellulært, via H 2 CO 3 og danner derved CO 2 og H 2 O, der diffunderer ind i cellen, hvor CO 2 og H 2 O omdannes til H + og HCO - 3, vha. carbonic anhydrase (CaII) (LANG et al., 1998b;O'Neill, 1999;Pedersen SF & Cala PM, 2004) Figur 24. En model for transportere der er involveret i RVI respons. NHE aktivering sker parallelt med aktivering af AE, hvilket resulterer i et netto optag af NaCl og et netto efflux af H + og HCO - 3. Figuren er fra (Pedersen SF & Cala PM, 2004). 29
30 I EATC er det vist, at ved mangel på HCO 3 -, sker RVI primært gennem NKCC, mens RVI ved tilstedeværelse af HCO 3 - sker gennem både NHE og NKCC (Hoffmann EK., 1997;Pedersen SF et al., 1996) Langtids- cellevolumen regulering Hypertonicitet er stress-fuldt for cellerne og cellerne har derfor udviklet mekanismer, der kan overkomme eksponering til hypertont miljø, gennem længere tid (Dahl et al., 2001;Miyakawa H et al., 1999). For at undgå høje intracellulære ion koncentrationer og for at balancere ekstracellulær og intracellulær osmolaritet, kan cellerne overkomme hypertont stress ved at ophobe kompatible organiske osmolytter (Sheikh-Hamad & Gustin, 2004), bl.a. stimulering af transkription af specifikke gener, spiller vigtige roller overfor hypertonicitet. Dette fører til induktion af en gruppe af gener, der koder for transport proteiner for organiske osmolytter (bl.a. for betaine (BGT1), for inositol (SMIT) og for taurin) (se(miyakawa H et al., 1999;Sheikh-Hamad & Gustin, 2004) og herved øges transportprotein- og enzym aktivitet, der katalyserer ophobning af kompatible osmolytter (Miyakawa H et al., 1999). Måden hvorved ændringer i ionstyrke eller cellevolumen bliver transduceret som signaler, der kan regulere gen ekspression er stadig ukendte. Men flere studier har peget på, at aktivering af TonE binding protein (TonEBP) har en central rolle i cellens beskyttelse mod skadelige effekter fra hypertonicitet (se (Miyakawa H et al., 1999;Sheikh-Hamad & Gustin, 2004;Woo SK et al., 2002). Cellens eksponering til hypertonicitet aktiverer TonEBP, som herefter translokeres til cellekernen, hvor den binder til et TonE bindingssted, hvilket fører til stimulering af yderligere transkription af transportproteiner, samt af enzym aktivitet, der katalyserer ophobning af kompatible osmolytter (Miyakawa H et al., 1999). Hypertonicitet aktiverer også MAP-kinaser (se afsnit 2.9) og disse kan aktivere transkriptionsfaktorer, som c-myc, Elk-1, c-jun, ATF-2, der regulerer cellevækst og celledød (Miyakawa H et al., 1999) (se figur 21). I gær er adaptationen overfor osmotisk stress afhængig af p38 MAPK homologen high-osmolality glycerol (HOG1) kinase (Han J et al., 1994), (se (Sheikh-Hamad & Gustin, 2004) og det kan derfor tænkes, at p38 MAPK er involveret i aktivering af TonEBP (Nadkarni et al., 1999), (Miyakawa H et al., 1999). JNK og ERK ser ikke ud til, at have en rolle i TonEBP inducering, under hypertonicitet (se (Sheikh-Hamad & Gustin, 2004). Nyligt har Padda og kollegaer foreslået at osmotisk stress, aktiverer et aktin-bundet scaffold af proteiner, der inkluderer MEKK3, MKK3 og Rac GTPase, som er krævet i den hypertone-medierede p38 MAPK aktivering, hvilket indikerer at aktivering af p38 MAPK, kan være et tidligt signal i osmosensing, under hyperton skrumpning (Padda et al., 2006). 30
31 2.8 NHE - isoformer NHE familien indeholder 9 klonede mammale medlemmer (isoformerne NHE 1-9) (Brett et al., 2005;Orlowski J & Grinstein S, 2004;Pedersen SF., 2006). NHE isoformerne udviser forskellig vævs og subcellulære distributionsmønstre og forskellige fysiologiske funktioner. NHE1-5 findes hovedsageligt i plasmamembranen, NHE6, 7 og 9 findes i intracellulære membraner, mens NHE8 formentlig findes i både plasmamembran og i organeller (se(fliegel L., 2005;Pedersen SF., 2006). I dette speciale arbejdes der hovedsageligt med NHE isoform 1, og derfor er det kun den der vil blive nærmere beskrevet NHE1 NHE1 aktiveres af ændringer i steady-state ph i og af osmotisk celleskrumpning og mekanisk stress, men aktiveres også af flere hormoner og vækstfaktorer. NHE1 spiller centrale roller i regulering af ph i og cellevolumen (se afsnit 2.7) (Pedersen SF., 2006). Kontrol af ph i er en fundamental mekanisme til at bevare et passende cytoplasmatisk miljø for protein aktivitet og interaktioner. Derved er NHE1 særdeles vigtig for cellens funktion og overlevelse (Orlowski J & Grinstein S, 2004) NHE1 drivkraft og struktur NHE1 proteiner er et sekundært aktivt transport protein, der katalyserer den elektroneutrale udveksling af Na + og H + ioner (1:1). Iontransporten sker pga den nedadgående elektrokemiske gradient ( µ), der findes over membranen for de to ioner. Drivkraften for NHE proteiner, er summen af drivkraften for Na + og H + og kan beregnes ud fra følgende formel (S.F.Pedersen et al., 2006): Δ µ = RT [ Na ] [ H + + inde inde ln RT ln + + [ Na ] ude [ H ] ude Hvor R er gaskonstanten, T er temperatur i Kelvin og ln er den naturlige logaritme ] Der findes en høj indadgående gradient for Na + og typisk også en beskeden udad gående gradient for H + under normale "steady-state" omstændigheder og derfor vil der være en relativ stor drivende kraft for Na + optag og for H + efflux (S.F.Pedersen et al., 2006). Den transmembrane gradient for Na + og H + dannes af primært aktive ion transport proteiner, hovedsageligt gennem Na + /K + ATPaser, men også gennem H + ATPaser eller H + /K + ATPaser (Orlowski J & Grinstein S, 2004;Ritter M et al., 2001). 31
32 Det humane NHE1 protein (figur 12) består af mellem ~ 780 og 820 aminosyrer og har en beregnet molekylærvægt på mellem ~ 87 og 91 kda (S.F.Pedersen et al., 2006). Proteinet har en membran associeret N-terminal del og en cytoplasmatisk C-terminal del, der begge er lokaliseret intracellulært (Wakabayashi et al., 2000). Den N-terminale del er højt konserveret blandt NHE isoformer og består af 12 konserverede transmembrane segmenter (Orlowski J & Grinstein S, 2004), der indeholder områder for ion translokation, drug -binding og for allosterisk modulering af NHE1 aktivitet via intracellulære H + ioner (S.F.Pedersen et al., 2006). Den C-terminale del bærer funktionelle domæner, der er ansvarlige for regulering af NHE1 exchangeren via ph i, fosforylering, ATP og via mekaniske stimuli bl.a. gennem cellevolumen ændringer (Orlowski J & Grinstein S, 2004;Pedersen SF & Cala PM, 2004;Pedersen SF., 2006;Ritter M et al., 2001). Nedenstående figur viser den formodede topologi af NHE1 isoformen, der er bestemt vha. hydropati og protease kløvningsstudier: Figur 25. Model af NHE1 proteinet. N- terminalen af NHE1 proteinet består af 12 transmembrane segmenter. Det C terminale domæne indeholder bindingssteder for proteiner og lipider, samt protein kinase konsensussites. Disse vil blive diskuteret i nedenstående afsnit, dog kun i det omfang at det er relevant for dette speciale. (CHP = calcineurin B homologt protein, NIK = Nck-interacting kinase, CaM = Calmodulin, PP1 = protein phosphatase 1 og CaII = carbon anhydrase II). Figuren er fra (S.F.Pedersen et al., 2006) Regulering af NHE1 aktivitet Det karakteristiske for NHE1 er, at dens aktivering bliver reguleret af mange typer af celleoverfladereceptorer, inklusiv receptor tyrosin kinaser, G-protein koblede receptorer og integrin receptorer. Celleoverfladereceptorer medierer aktivering af NHE1 gennem NHE1 interagerende 32
33 proteiner, der regulerer modifikationer i exchangerens COOH regulatoriske domæne (Putney LK et al., 2002). Disse modifikationer, inkluderer proteinfosforylering, binding af regulatoriske proteiner (direkte protein-protein interaktioner) og konformationelle ændringer, der alle regulerer transport aktivitet ved, at ændre affinitettet af den transmembrane intracellulære H + transport sted (Bertrand et al., 1994;Putney LK et al., 2002). Regulering af NHE1 aktivitet gennem protein-protein interaktioner, via dens associerede proteiner sker idet NHE1 proteinets COOH terminal indeholder flere bindingssteder for regulatoriske proteiner (se figur 12). Disse inkluderer bl.a. CaM (Bertrand et al., 1994) (se afsnit ), medlemmer af bånd 4.1 familien og derfor også for ERM proteiner (Denker SP et al., 2000;Putney LK et al., 2002) (se afsnit 2.3). NHE1 interagerer ligeledes med Calcineurin homologt protein, CHP (Lin X & Barber DL, 1996), Nck-interagerende kinase, NIK (Fliegel L., 2005;Yan et al., 2001b), Protein fosfatase 1, PP1 (Misik AJ et al., 2005), og Carboanhydrase II, CaII (Li et al., 2002), men disse vil ikke blive nærmere diskuteret. Da NHE1 proteinet indeholder et PIP 2 bindingssted, har Orit Aharonovvitz og kollegaer (2000) foreslået, at binding af PIP 2 til ion transport proteiner, kan inducere en konformationel ændring, der unmasker steder for binding af cytoskeletale linkere, som f.eks. ERM proteiner og derved stimulerer transport aktivitet (Aharonovitz et al., 2000;Denker SP og Barber, 2002). Flere kinaser er ligeledes blevet foreslået som værende involveret i den direkte regulering af NHE1 efter forskellige stimuli. Især følgende tre serin/threonin kinaser er kendte; ROCK, p90 RSK og NIK. Rho kinase (ROCK) aktiveres som respons overfor integrin receptorer og G-protein koblede receptorer for trombin og LPA (Tominaga T et al., 1998), mens p90 RSK og af NIK aktiveres af vækstfaktorer (Putney LK et al., 2002;Takahashi et al., 1999) Regulering af NHE1 under hyperton skrumpning De molekylære mekanismer hvorved cellevolumen kan kontrollere aktiviteten af NHE antiporteren er stadig relativ uklare. NHE1 aktiveres under hyperosmotisk skrumpning, bl.a. som et resultet af ændringer i følsomheden overfor H + koncentration og derved ved ændringer i steady-state ph i (Grinstein et al., 1992;Pedersen SF & Cala PM, 2004). Direkte fosforylering ser også ud til at have en rolle i den skrumpnings-inducerede aktivering af NHE1, gennem mitogener og/eller vækstfaktorer (Pedersen SF., 2006). I 1982 fandt Aronson og kollegaer i bl.a. nyre mikrovilli membran vesikler, nyreceller og i lymfocytter, at intracellulær H + kan virke som en allosterisk aktivator for NHE under hyperton celleskrumpning, ved at inducere en konformationel ændring og derved flyttes et auto-inhibitorisk 33
34 domæne fra NHE. Flytning af dette auto-inhibitoriske domæne fører til en stigning i affinitet for intracellulær H +, som derved aktiverer antiporteren ved ph i ændringer (Aronson PS et al., 1982;Grinstein S & Foskett JK, 1990). NHE1 kan som tidligere nævnt, virke som et scaffolding protein, da dens C- terminal domæne indeholder flere konsensus steder for bl.a. protein kinaser (Pedersen SF., 2006). Flere protein kinaser bliver aktiveret af hypertont stress i mammale celler, inklusiv PKC, MLCK og MAPK (for beskrivelse af MAPK se afsnit 2.9). I EATC er det dog fundet, at den skrumpnings-inducerede NHE aktivering kun er afhængig af PKC og p38 MAPK og ikke af MLCK eller Erk (S.F.Pedersen C.Varming, 2002). Denker og kollegaer har som tidligere nævnt, foreslået at NHE1 associerer med aktinfilamenter ved en direkte association med aktin-bindende proteiner som ERM familien. Disse cytoskeletale associationer kan derved regulere membranens distribution af NHE1 og er en determinant i NHE1-reguleret organisering af kortikale aktin filamenter, men muligvis også i modulering af transport aktivitet under osmotisk skrumpning (Denker SP et al., 2000;Putney LK et al., 2002). NHE1s C- terminale domæne interagerer direkte med plasmamembran-cytoskeletkæderen ezrin, men det er stadig uklart om ezrin er sekundær påvirket af en stigning i NHE1 aktivitet eller om fosforylering af ezrin modulerer NHE1 aktivitet (Alexander RT & Grinstein S., 2006;Pedersen SF., 2006). PIP 2 (Hirao et al., 1996) og Rho/Rho kinase vejen (Mackay et al., 1997) er vigtige regulatorer af ERM protein familien og gennem denne vej reguleres interaktionen mellem NHE1 og ERM proteiner og/eller ERM afhængig signaleringsevents der er nedstrøms for NHE1 (Denker SP et al., 2000;Pedersen SF., 2006). Det C-terminale domæne af NHE1 indeholder to calmodulin bindingssteder (Wakabayashi et al., 1994) og det er tidligere vist, at CaM direkte interagerer med og fosforylerer NHE1, under osmotisk skrumpning (Garnovskaya et al., 2003). CaM domænet menes at have en auto-inhibitorisk effekt på ion-transport via NHE1, ved at reducere affiniteten overfor H + ioner. Derfor kan binding af CaM muligvis resulterer i en konformationel ændring, der undertrykker den auto-inhibitoriske effekt på ion-transporten (Wakabayashi et al., 1997). Deletion eller mutation af CaM stedet i PS120-fibroblaster, fører til stærk hæmning af den hypertone-inducerede aktivering af antiporteren, hvilket yderligere bekræfter at CaM er medvirkende i NHE1 aktivering (Bertrand et al., 1994;Wakabayashi et al., 1994). I EATC har Pedersen og kollegaer desuden vist calmodulin-antagonister hæmmer NHE1 aktivitet (Pedersen SF et al., 1996) Hæmning af NHE1 Der findes to klasser af farmakologiske stoffer, der bruges til at hæmme NHE1 aktivitet. Den ene klasse omfatter amilorid og dens 5 alkyl-substituerede afledte komponenter, som f.eks. ethylpropylamilorid (EIPA) (se figur 13). Den anden klasse indeholder benzoylguanidiner og afledte stoffer som HOE694 og 34
35 HOE642 (carporide) (Putney LK et al., 2002). I dette speciale er det EIPA, der er benyttet til at hæmme NHE1 aktivitet. Figur 26. EIPA struktur (Putney LK et al., 2002). 2.9 Mitogen aktiverede protein kinaser (MAPK) MAPK signal transduktionsveje er blandt de mest udbredte i eukaryote cellers regulering (Kyriakis & Avruch, 2001). Alle eukaryote celler har flere MAPK signaleringsveje, der hver især rekrutteres af forskellige stimuli og derved kan cellen reagere koordineret overfor flere forskellige indputs. MAPK aktiveres ved stimulering af flere receptor familier, bl.a. af receptortyrosin-kinaser, cytokin-receptorer og af G-protein-koblede receptorer (Kyriakis & Avruch, 2001;Widmann C.H.R.I. et al., 1999). Størstedelen af af de definerede substrater for MAPK er transkriptionsfaktorer, der regulerer genekspression, men MAPKs kan også fosforylere protein kinaser, fosfolipaser og cytoskelet-associerede proteiner (Kyriakis & Avruch, 2001;Widmann C.H.R.I. et al., 1999). Den basale samling af MAPK veje et et tre-komponnet modul, af tre kinaser, der er konserveret fra gær til mennesker (figur 14). Specifikke MKKKs kan aktiveres af fosforylering, membran translokation, ved interaktion med små GTP-bindende proteiner (Kyriakis et al, 2000) eller ved ændringer i osmolaritet (Roger et al., 1999). MKKK er en serin/threonin kinase, der aktiverer den næste kinase i modulet, en MAPKK også kaldet MKK eller MEK. MKKs er kinaser der genkender og fosforylerer et konserveret Threonin-X-Tyrosin motif i MAPK, hvilket betyder at MKKs er såkaldte dual specifikke kinaser. MAPK er den sidste kinase i modulet (Kyriakis & Avruch, 2001;Werry TD et al., 2006;Widmann C.H.R.I. et al., 1999). 35
36 Figur 27. MAPK tre-trins modulet. MAP3K aktiveres af flere ekstracellulære indputs. Deres aktivering fosforylerer MAP2K, der videre fosforylerer MAPK, der herefter medierer flere respons. Figuren er fra (Kyriakis & Avruch, 2001). MAP-kinaser kan inddeles i en lang række underfamilier udfra hvilket MAPKK de fosforyleres af, samt hvilket substrater de selv fosforylerer. Kun de mest grundigt undersøgte grupper af MAPK, vil blive beskrevet nærmere i dette speciale. Disse drejer sig om ekstracellulær signaleringsreguleret proteinkinase, (ERK), c-jun N-terminal kinase (JNK) og protein p38 (p38 MAPK) (Han et al., 1996;Kyriakis & Avruch, 2001) ERK, JNK og p38 MAPK ERK ERK-isoformerne ERK1 (44 kda) og ERK2 (42 kda), er serin/threonin kinaser, der findes ubiquitously ekpresseret i celler (Pages G et al., 1993). Den hurtig aktiveres af flere ekstracellulære signaler, bl.a. af vækstfaktorer, hormoner, neurotransmittere og af "heat shock" og har vigtige roller i integrering og transmition af transmembrane signaler, der er krævet for bl.a. vækst, differentiering og cellecyclus stop, hvilket gør dem essentielle i regulering af flere cellulære processer, men især i regulering af cellevækst (Kyriakis & Avruch, 2001;Pages G et al., 1993;Yoon S & Seger R, 2006). ERK1/2 MAPK kaskaden involverer aktivering af ERK MAPK ved direkte forsforylering af den dual-specifikke kinase MKK1 og MKK2, der selv bliver fosforyleret og aktiveret gennem en serin/threonin kinase kaldet Raf (en MAP3K). 36
37 Raf bliver rekrutteret til membranen af små GTP bindende proteiner af Ras familien, under aktivering af enten G-protein koblede receptorer eller af tyrosin kinase receptorer (Bianchini et al., 1997;Kyriakis JM et al., 1992;Sheikh-Hamad & Gustin, 2004). Flere andre MAP4K er involveret i aktivering af kaskaden, blandt disse findes PKC (Yoon S & Seger R, 2006). ERK aktivering er essentiel for cellevækst (Pages G et al., 1993), idet dens aktivering øger nukleotid syntese, aktiverer transkription af mange gener, der virker via trasnkriptionsfaktorer, som c-fos og c-myc, der fører til transkription af gener, der danner proteiner, der initierer cellecyclus. ERK stimulerer ligeledes proteinsyntese (Pouyssegur J et al., 2002), proteinkinaser/fosfataser, cytoskeletale elementer og de er medvirkende i regulering af apoptose (Morrison DK & Davis RJ, 2003;Werry TD et al., 2006;Yoon S & Seger R, 2006) JNK Der findes tre c-jun N-terminal kinase (JNK) gener; jnk1, jnk2 og jnk3. jnk1 (46 kda) og jnk2 (52 kda) er ekspresseret i de fleste væv, mens jnk3 hovedsageligt findes i hjernen (Harper SJ & LoGrasso P, 2001). JNKs blev oprindeligt fundet via deres evne til at fosforylere c-jun, som respons overfor UVstråling, men den aktiveres ligeledes af osmotisk stress (Matsuda et al., 1995) og inflammatoriske cytokiner og kendes i dag som en stress-aktiveret kinase (Karin M & Gallagher E, 2005). Opstrøms for JNK1/2 findes hhv. MMK4 og MKK7, hvoraf MKK4 også kan fosforylere/aktivere p38 MAPK (Harper SJ & LoGrasso P, 2001). JNKs er kendte, som værende kritiske regulatorer af flere aspekter af mammalian fysiologi, inklusiv celle proliferering, celle overlevelse, celledød, DNA reparering og metabolisme (Karin M & Gallagher E, 2005). Mange substrater aktiveres af JNK, inklusiv transkriptionsfaktorer som c-jun, ATF2 og tumor supressor genet p53 (p53, er et protein der hæmmer cellevækst og fremmer differentiering, samt PCD). ATF2 og c-jun er en del af AP-1 transkriptions komplekset, der påvirker apoptose (Harper SJ & LoGrasso P, 2001;Yan et al., 2001a). Dette betyder at JNKs er involveret i programmeret celledød P38 p38 MAPK (hvoraf der findes fire isoformer af p38; p38α, β, γ og δ) signal transduktionsvejen aktiveres af hypertont stress (Burg MB et al., 1997;Han J et al., 1994), proinflammatoriske cytokiner og environmental stress og er ligesom JNK en stress-aktiveret kinase (Raingeaud et al., 1996). Opstrøms for p38 MAPK findes MKK6, MKK4, MKK3 (Harper SJ & LoGrasso P, 2001). Flere substrater er fundet for p38 MAPK, heriblandt kinaser som MAPKAP og transkriptionsfaktoren ATF2, der fosforyleres og derved virker ved at regulere gen ekspression af apoptotiske signaler. Ligesom JNK bliver p38 MPAK 37
38 fosforyleret og aktiveret som respons overfor flere cellulære stress stimuli (Harper SJ & LoGrasso P, 2001). I gær er der fundet gener (p38 MAPK homologen, high-osmolality glycerol (HOG1)), der er krævet for at cellen kan opnå normal volumen igen, efter øget eksternal osmolaritet. Disse gener fungerere i gær, som en del af en osmosensing signal transduktionsvej, under hypertone forhold (Brewster JL et al., 2006). Da HOG1 og p38 MAPK deler mange af de samme karakteristika, kan der være tale om, at p38 MAPK kan være en del af en osmosensing signaleringsvej i mammale celler (Han J et al., 1994). Under aktivering vil p38 MAPK translokere til cellens kerne, hvor den aktiverer transkriptionsfaktorer, som f.eks. ATF2 og p53, hvilket betyder, at p38 MAPK aktivering ofte vil virke pro-apoptotisk på cellen, under stress situationer (Zhu et al., 2002). Nedenstående figur illustrerer en samlet model for MAPK signal transduktionsveje for hhv. ERK, p38 MAPK og JNK. Figur 28. En skematisk model for mamalian MAPK signalerings transduktionsveje. ERK MAPK aktiveres af bl.a. tyrosin kinaser, MEK1/2 aktiverer ERK1/2, som fosforylerer transkriptions-faktorerne c-fos og c-myc. P38MAPK fosforylerer og aktiverer transkriptionsfaktoren ATP2 og virker som en evt. osmosensor. MKK3/6 og til dels af MKK4 aktiverer p38 MAPK. JNK fosforylerer ligeledes ATF2, samt c-jun og p53 og bliver selv aktiveret af MKK4/7. Figuren er modificeret fra (Raingeaud et al., 1996) MAP-kinaser og celleskrumpning Aktivering af ERK, p38 MAPK og JNK moduleres af osmotisk stress i stort set alle celletyper, hvor det er undersøgt (Gillis D et al., 2001;S.F.Pedersen C.Varming, 2002;Sheikh-Hamad & Gustin, 2004). Celleskrumpning vil generelt stimulere p38 MAPK og JNK (Bianchini et al., 1997;Friis et al., 2005;Gillis D et al., 2001;S.F.Pedersen C.Varming, 2002), mens cellesvulmning stimulerer ERK (Else K.Hoffmann & Stine F.Pedersen, 2006). Ved langtidsforstyrrelser af celler via osmotisk stress, kan MAPKs aktivering, påvirke cellernes proliferering, programmeret celledød (PCD) og de kan udføre adaptive ændringer i osmolyt transpoter ekspression. Generelt er der tale om, at JNK og p38 MAPK 38
39 inducerer PCD og modvirker celle-proliferering (Harper SJ & LoGrasso P, 2001), mens ERK fremmer celleoverlevelse og vækst (Pages G et al., 1993). Dette stemmer overens med at cellesvulmning stimulerer proliferation, mens celleskrumpning blokkerer cellecycel progression og inducerer PCD, (Else K.Hoffmann & Stine F.Pedersen, 2006) Regulering af MAPKs og NHE1 NHE1 aktiveres af hyperosmotisk stress og er en stor del af cellers volumenregulerings mekanisme. Signaleringsveje der fører til aktivering af NHE er stadig uklare. MAPKs er som tidligere nævnt, involveret i flere cellulære respons overfor ændringer i cellulær osmolaritet. Den samtidige aktivering af NHE og MAPKs under hyperosmotisk skrumpning, kan tyde på, at der findes et samspil mellem MAPKs aktivering og skrumpnings-induceret NHE1 aktivering (Gillis D et al., 2001;Pedersen SF et al., 2007). MAPKs relation med NHE1 er ikke fuldt ud klarlagt og deres sammenspil (om skrumpnings-induceret NHE1 aktivering aktiverer MAPK, eller om det er omvendt) er meget kontroversielt og celletypeafhængigt. Nogle studier peger endda på, at MAP-kinaser overhoved ikke har nogen rolle i aktivering af NHE1 (U937 og Cos-7 celler) (Gillis D et al., 2001) Skrumpnings-induceret NHE1 aktivering regulerer MAP-kinase aktivitet Skrumpnings-induceret aktivering af NHE1, har en vigtig funktion i modulering af MAP-kinasers aktivitet. Darborg og kollegaer har i ELA celler fundet, at osmotisk skrumpning hæmmer ERK1/2 aktivitet i EAT-celler, hvilket tidligere også er vist af Friss MB og kollegaer i NIH3T3 celler. Ligeledes er det vist, at denne hæmning af ERK1/2 kan hindres ved hæmning af NHE1, hvilket indikerer, at NHE1 aktivering findes opstrøms for ERK1/2 MAPK inaktivering (Friis et al., 2005;Pedersen SF et al., 2007). Mekanismen hvorved NHE1 kan modulere ERK1/2 aktivitet er stadig ukendt, men flere forsøg har peget på, at afvigelser i ph i kan aktivere ERK1/2 aktivitet i flere celletyper (bl.a. neonatal rotte ventricular myocytter og COS-7 celler) (Haworth et al., 2003), derfor kan det tænkes, at den intracellulære alkalinisering, der medieres gennem skrumpnings-induceret NHE1 aktivering, er det der er ansvarlig for inaktivering af ERK1/2 (Pedersen SF et al., 2007). Muhkin og kollegaer har i RASM celler (rotte aortic smooth muskel celler) ligeledes vist, at NHE1 aktivitet spiller en vigtig rolle i ERK1/2 modulering, ved stimulering med Ang II og 5-HT (Mukhin et al., 2004). I modsætning til ERK1/2, aktiveres både JNK og p38 MAPK transient under osmotisk skrumpning i flere celltyper (Friis et al., 2005), (Gillis D et al., 39
40 2001), men i ELA celler ser det ud til, at det kun er JNK, der er afhængig af NHE1 aktivitet, idet hæmning af NHE1 delvist påvirker den skrumpnings-inducerede JNK-aktivering (Pedersen SF et al., 2007). Skrumpnings-induceret aktivering af NHE1, ser ikke ud til at have nogen funktion i aktivering af p38 MAPK (Pedersen SF et al., 2007). Opsummeret betyder dette at skrumpnings-induceret NHE1 aktivering hæmmer ERK1/2 aktivitet, hvilket indikerer at NHE findes opstrøms for ERK1/2. JNK1/2 og p38 MAPK aktiveres under osmotisk skrumpning, men kun JNK moduleres af skrumpnings-induceret NHE1 aktivitet MAP-kinaser regulerer NHE1 aktivering Det er veldokumenteret at ERK1/2 MAPK aktivering findes optrøms for NHE aktivering i mange celletyper (bl.a. Isolated primary myocytes og i rotte aortic smooth muscle (RASM) celler) (Bianchini et al., 1997;Moor & Fliegel, 1999), ved andre stimuli end osmotisk skrumpning. Den ERK medierede stimulering af NHE1 aktivitet, kan ske via direkte fosforylering af NHE1s regulatoriske domæne (Moor & Fliegel, 1999) og /eller indirekte gennem en eller flere nedstrøms effektorer (Bianchini et al., 1997). En mulig effektor er 90-kDa ribosomal S6 kinase (p90 RSK ), der aktiveres af ERK-medieret fosforylering, idet det tidligere er vist at p90 RSK fosforylerer NHE1 og derved øger NHE1s aktivitet (Haworth et al., 2003;Takahashi et al., 1999). Studier har ligeledes vist, at p38 MAPK kan virke opstrøms for NHE1 aktivering under osmotisk skrumpning, idet hæmning af p38 MAPK førte til en hæmmet skrumpningsinduceret NHE1 aktivitet i ELA- og i EAT-celler. ERK og JNK hæmning havde i disse studier ingen effekt på skrumpnings-induceret NHE1 aktivitet og ser derfor ikke ud til, at de findes opstrøms for NHE1 aktiveting (Barbara Vasek Darborg, 2005;Rentsch M et al., 2006;S.F.Pedersen C.Varming, 2002). Andre studier har dog fundet, at den hypertone aktivering af NHE i Xenopus oocytes kræver aktivering af JNK (Goss et al., 2001). Nogle forsøg modargumenterer for, at MAP-kinaser overhoved er involveret i skrumpnings-induceret NHE1 aktivering (i U937 celler) (Gillis D et al., 2001). Opsummeret betyder dette, at p38 MAPK findes opstrøms for den skrumpnings-inducerede aktivering af NHE1, mens JNK1/2s og til dels ERK1/2s roller opstrøms for NHE1 aktivering er omdiskutterede Død og overlevelses-signalering Apoptose er en konserveret mekanisme, der er udviklet til at eliminere skadede eller ødelagte celler, uden cytolytisk frigivelse af potentielle skadelige substanser, som kan udløse inflammatoriske respons i vævet (se (Jin Z & El-Deiry WS, 2005;Lang F et al., 2000;Okada Y & Maeno E, 2001). Apoptose bliver tæt 40
41 reguleret og fejl i denne regulering resulterer i udviklingsmæssige defekter, autoimmune sygdomme, neurodegeneration eller kræft. Apoptose er karakteriseret ved membran blebbing, celleskrumpning, kromatin kondensering og DNA fragmentering, som ender med at celler bliver spist af makrofager eller af naboceller, hvorved inflammatorisk respons undgås. Apoptose er forskellig fra nekrose, idet nekrose fører til tab af membran integritet, cellesvulmning og ødelæggelse af cellen. Under nekrose bliver det cellulære indhold frigivet til det omgivende miljø, hvilket resulterer i ødelæggelse af dette væv og i et inflammatorisk respons (Jin Z & El-Deiry WS, 2005;Lang F et al., 2000). I eukaryote celler er mindst to veje for apoptose beskrevet; en dødscelle receptorvej (ekstracellelære vej), f.eks. via Fas og TNF-familien af dødsreceptorer, der aktiverer caspase-8 og derved caspase-3 og en mitochondriel vej (intracellulære vej), hvor mitochondrierne aktiverer caspaser, ved at frigive cytokrom C (cytc) (Matsuyama S et al., 2000). Apoptose aktiveres ligeledes efter DNA ødelæggelse induceret af stråling eller af kemikalier, vækstfaktor mangel, osmotisk stress eller af oxidativt stress (Matsuyama S et al., 2000). Apoptose kan aktiveres i mange celletyper gennem diverse signaleringsveje, men alle apoptotiske signaler resulterer i en meget konserveret serie af morfologiske og biokemiske ændringer, hvilket tyder på, at der findes en fælles vej opstrøms for celle og/eller siganl specifikke events (Matsuyama S et al., 2000). Tab af cellevolumen er et fundamentelt træk ved apoptose. Celler kan kompensere for deres ændringer i cellevolumen via aktivering af flere volumen regulatoriske respons mekanismer. Disse mekanismer kan være yderst vigtige i cellens overlevelse under apoptose. Bevægelse af ioner kan således være en fundamental mekanisme til kontrol af volumen som respons overfor apoptose, således at ukontrollerede ændringer i cellevolumen, som respons til ion bevægelser kan være et fysiologisk signal, der aktiverer events der fører til celledød (Bortner CD & Cidlowski JA, 1998). Hughes og kollegaer har fundet, at ionstyrken af den intracellulære væske, fungerer ved at opretholde apoptotiske systemer i et inaktivt stadie (Hughes et al., 1997). Mere specifikt har Bortner og kollegaer (1998) fundet, at den intracellulære koncentration af kalium, hæmmer det apoptotiske maskineri, inklusiv den caspase-3 lignende aktivering og et signifikant fald i den generelle intracellulære ion styrke er krævet for aktivering af flere caspaser og nukleaser, der er kendte i involveringen i celledøds processer (Bortner CD & Cidlowski JA, 1998). Generelt vil det sige, at tidlige events i apoptose, involverer et fald i cytosolisk ph og at dette fald i cytosolisk ph, er krævet for aktivering af caspase kaskaden, der fører til den egentlige apoptose (Matsuyama S et al., 2000;Wu et al., 2003;Wu et al., 2004). Aktivering af NHE1 er som tidligere nævnt (se afsnit 2.8.1), en vigtig komponent i RVI respons, hvor den resulterer i Na + indflux og derved cytoplasmatisk volumen forøgelse. Samtidigt medierer NHE1 efflux af H + ioner, der fører til intracellulær alkalinisering, der således beskytter cellen mod apoptose, ved at hæmme caspase katalyse (Matsuyama S et al., 2000;Segal & Beem, 2001;Wu et al., 2004). Ligeledes er det fundet, at apoptose er associeret med en caspase-afhængig nedbrydning af NHE1 i renal tubular 41
42 celler, samt at NHE1 loss-of-function mutanter gør disse celler mere modtagelige overfor apoptose in vivo og in vitro. Når NHE1 bliver nedbrudt, forhindres RVI-respons og derved fremmes intracellulær acidose, som er optimalt for caspase aktivitet (Wu et al., 2003). Denker og kollegaer har fundet at NHE1 er koblet til plasmamembranen og cytoskelettet gennem en direkte interaktion med det aktin bindende protein ERM (Denker SP et al., 2000) (se afsnit 2.3) og derfor kan det tænkes, at NHE1s modstand overfor apoptose, kan være medieret, gennem dens kobling med ERM proteiner (Wu et al., 2003). Det er i LLC-PK1- (Gautreau A et al., 1999) og i nyre epithel celler (Wu et al., 2003) fundet, at ezrin direkte interagerer med signaleringsenzymer, som fosfoinositid 3-kinasen (PI3K) under bl.a. osmotisk skrumpning og derigennem regulerer Akt/PKB overlevelsesvejen, hvilket kan betyde at celleoverlevelse fremmes af signaleringskomplekser, der inkluderer NHE1, ERM, PI3K og Akt (Gautreau A et al., 1999;Wu et al., 2003;Wu et al., 2004). Herved kan NHE1s interaktion med aktiveret ERM proteiner have en rolle i apoptotisk stress-induceret kobling til PI3K, der nedstrøms aktiverer Akt/PKB (Wu et al., 2004), se figur 16. PI3-kinasevejen er en anti-apoptotisk vej, der aktiveres af flere faktorer, bl.a. vækstfaktorer. Akt er serin/threonin kinaser, der som nævnt aktiveres af PI3K, men mere også af fosfatidylinositol-afhængig protein kinase (PDK-1), osmotisk stress og af vækstfaktorer. Den fungerer ligesom PI3K, som en anti-apoptotisk reagent og medierer derfor celleoverlevelse (Dogra C.Changotra et al., 2006;Downward J., 2004). Aktivering af MAPK er ligeledes blevet foreslået, som værende medvirkende under cellulær apoptose, idet p38 MAPK muligvis findes som opstrøms aktivator for caspase-3 og p53, efter hyperosmotisk skrumpning i NIH3T3 celler (Friis et al., 2005), hvilet stemmer overens med at p38 MAPK fremmer celledød, under osmotisk skrumpning, mens ERK fremmer vækst og derved celleoverlevelse (se afsnit 2.9). Figur 29. En model for overlevelses- og dødssignaleringsveje. NHE aktivering via osmotisk skrumpning fører til aktivering af Akt/PKB overlevelsesvejen. Ezrin interagerer med signaleringsenzymer som PI3K og derigennem regulere dette kompleks Akt overlevelsesvejen, hvilket kan betyde at celleoverlevelse fremmes af signalerings-komplekser, der inkluderer NHE1, ERM, PI3K og Akt (Gautreau A et al., 1999;Wu et al., 2003;Wu et al., 2004). Apoptose gennem dødsreceptorer og mitochondrier er medieret gennem caspase aktivering (Matsuyama S et al., 2000). Figuren er modificeret fra (Wu et al., 2004). 42
43 Regulering af Akt/PKB via osmotisk skrumpning er kontroversiel, idet nogle studier har fundet, at osmotisk skrumpning hæmmer Akt/PKB (Barbara Vasek Darborg, 2005;Rasmussen M et al., 2007;Meier R et al., 1998), mens andre studier har fundet, at den osmotiske skrumpning aktiverer Akt/PKB vejen (Rasmussen M et al., 2007;Wu et al., 2004). Det betyder, at effekten af Akt/PKB reflekterer en reguleret balance mellem celleoverlevelse og celledød efter osmotisk skrumpning og at denne effekt i høj grad er celletype specifik (Rasmussen M et al., 2007) Mulige arbejdsmodeler Mit speciale har været opdelt i to overordnede projekter; et ezrin protein projekt A) og et MAP-kinase projekt B), derfor har jeg ud fra litteraturen og udfra hvad jeg yderligere gerne vil undersøge, opstillet følgende to arbejdsmodeller. A B Figur 30. Arbejdsmodel for projekt A. Jeg har undersøgt om ERM proteiner, specielt ezrin, kan være et signal der fører til celleskrumpning og således virker opstrøms for NHE1 og derigennem aktivering af overlevelsesvejen, NHE1, PI3K, Akt/PKB. Ligeledes har jeg undersøgt ERMs rolle i F-aktin organisering og derigennem deres rolle i Rho-protein aktivering og om Rho-Rho-kinasen findes opstrøms for ERM protein aktivering. Pilenes farver indikerer, mine forskellige opsatte hypoteser (se afsnit 5) Figur 31. Arbejdsmodel for projekt B. Jeg har undersøgt hvorledes skrumpnings-induceret aktivering af NHE1 kan være opstrøms for MAPKs, muligvis igennem effekter på intracellulær ph og/eller MEK1/2 eller MKK3/6 aktivitet. Samt om disse MAPKs kan regulere cellens overlevelse efter hyperosmotisk skrumpning. Disse arbejdsmodeler vil blive nærmere diskuteret i diskusionen, se afsnit 5. 43
44 3 Metoder 3.1 Celler og celledyrkning ELA celler Der arbejdes med Ehrlich Lettre Ascites celler (ELA-celler), som er epithel-deriverede tumorceller fra mus. Disse celler er en adherent sublinie af suspensionscellelinien Ehrlich Ascites tumor celler (EATC), hvor der er opnået mange forskningsresultater fra. ELA cellerne har en fordoblingstid på ca. 22 timer (oplyst af fabrikanten) og de splittes to gange om ugen, når en konfluens på % er opnået. Cellerne dyrkes under sterile forhold i RPMI medium, der indeholder 1 % Pen/Strep (penicillin/streptomycin opløsning bevirker, at der ikke kommer anden vækst i mediet), samt 10 % FBS (føtal bovin serum; næring så cellerne kan vokse). Cellerne inkuberes i en inkubator, som har en luftfugtighed på 100 %, er 37 o C varm og indeholder 6 % CO 2, hvorved ph stabiliseres på AP-1 celler og S5 celler AP1 celler er chinese hamster ovary celler (CHO), der ikke har NHE1 tilstede. Na + -H + exchangedeficient AP-1 celler, er opnået vha. en proton selvmords-teknik, hvor cellerne først bliver mutageniseret vha. ethylmethane sulfonate og derefter loaded med Li + ioner, der kan erstatte Na + ioner. Cellerne eksponeres herefter til lav ph (5.5) og mangel på ekstracellulære alkaliske kationer. Da NHE-antiporteren er reversibel, vil der ske en udveksling af Li + ioner for ekstracellulær H + ioner, hvilket fører til massiv cytosolisk acidifikation. Dette er dødeligt for celler der har en funktionel antiporter, mens celler der ikke har antiporteren overlever. Mutationen der medfører Na + -H + exchange-deficient er stabil i ca. 25 passager (Grinstein S et al., 1989). S5 celler er AP1 celler der mangler endogen NHE aktivitet og som er transfekteret med plasmider, der indeholder human NHE cdna konstrukter. cdna der koder for human NHE1 protein er klonet ind i en pcdna 3.1 plasmid vektor, der ligeledes indeholder et G418 resistens gen. Celler er blevet dyrket til ca. 50 % konfluens og er derefter transfekteret med plasmid DNA vektoren (for princip bag metoden se (McLean et al., 1999), hvorefter celler er blevet inkuberet i 24 timer (37 C, 5 % CO 2 ) i α-minimal essentiel medie, α-mem. Selektionsprocessen går ud på, at celler får tilført α -MEM, der indeholder 400 ug/ml G418 sulfate, et antibiotikum der er giftigt overfor normale celler. De celler der er blevet 44
45 transfekteret med plasmid vektoren og derfor indeholder G418 genet, såvel som NHE cdna, er i stand til at overleve og dele sig i α -MEM, tilført G418 (Lee Anne McLean, 1999). AP1 og S5 cellerne kommer fra prof. P.M Cala, School of medicine, University of California, Davis. Cellerne dyrkes i a-minimal essential medium, tilsat 1% Pen/Strep, 10 % FBS, G418-sulfat, samt 1% L- glutamin. Cellerne inkuberes i en inkubator, som har en luftfugtighed på 100 %, er 37 o C varm og indeholder 6 % CO 2, hvorved ph stabiliseres på Celledyrkning Cellerne splittes når de er ca. 90 % konfluente. Mediet suges fra og cellerne skylles med ca. 5 ml 37 C varm steril PBS, som umiddelbart efter suges fra. Cellerne tilsættes 1.5 ml trypsin (bestående af trypmix og PBS i forholdet 1:10) og T75-flasken anbringes få minutter i inkubator, hvorefter cellerne runder op og slipper underlaget. Der tilsættes nu 8.5 ml medie til T75-flasken, således svarer 1 ml til 10 % konfluens. Til videredyrkning af celler tilsættes til en ny T75-flaske ca. 1 ml cellesuspension, samt 15 ml medie, hvorefter cellerne er ca. 90 % konfluente efter 3-4 dage. Cellerne kan ca. dyrkes til passage 25-30, hvorefter en ny kultur optøes. Ved celle-opsætninger til forsøg i 4, 6 og 96 brøndsbakker, tælles cellerne i et hæmocytometer, hvorimod celleopsætning i petriskåle samt T75 flasker beregnes ud fra procent konfluens, idet 1 ml svarer til 10 % konfluens ved splitnig af celler. 3.2 Osmotisk skrumpning Osmotisk skrumpning er induceret af hyperton normal-ringer med en osmolaritet på 600 mosm. Denne er fremstillet udfra isoton normal-ringer (300 mosm), ved at fordoble ionstyrken og ved at bibeholde den samme koncentration af buffere. Den hypertone Ringer er brugt ved forsøg der har varet under 1 time. Ved længere varende forsøg med hypertonicitet, er der blevet anvendt RPMI medie tilsat 150 mm NaCl-opløsning, således at osmolariteten bliver 600 mosm. 3.3 Hel-celle RNA oprensning fra ELA celler For at kunne udføre PCR reaktioner, skal der oprenses RNA først. RNeasy kittet er designet til at oprense RNA fra små mængder start materiale. Kittet kan bruges til mange henseender: RT-PCR og real-time RT- PCR, Differential display, cdna syntese, Northern, dot og slot blot analyse, Primer extension, Poly A+ 45
46 RNA selection, RNase/S1 nuclease protection og microarrays. Det benyttede RNA oprensningskit er et Qiagen RNeasy protect mini Kit Teori bag RNA oprensning vha. RNeasy teknologi RNeasy proceduren er baseret på en etableret teknologi for RNA-oprensning. Et specialiseret høj-salt buffer system tillader, at op til 100 µg RNA på mere end 200 baser, kan binde til RNeasy silica membranen. Prøver (op til 1*10 7 celler, alt afhængig af celletype) lyseres og homogeniseres ved tilstedeværelse af denaturerende guanine-thiocyanat-indeholdende buffer, der frigør RNA fra proteinet og som med det samme inaktiverer RNaser, for at sikre at oprensning af intakt RNA. Ethanol tilsættes for at sikre de rigtige bindingsomgivelser, hvorefter prøverne tilføres til en RNeasy mini spin kolonne, hvor total RNA binder til membranen og kontaminanter effektivt vaskes væk. Høj kvalitets RNA elueres herefter i ul RNase frit vand. Med RNeasy proceduren, vil alle RNA molekyler der er længere end 200 nucleotider blive oprenset. Det meste RNA >200 nucleotider (som 5.8S rrna, 5S rrna og trna, der tilsammen er % af total RNA) vil derfor blive vasket væk Praktisk udførelse af RNA oprensning RNA er oprenset ud fra følgende protokol: ELA celler dyrkes i Petriskåle til ca. 80 % konfluens. På forsøgsdagen lyseres cellerne i 600 μl RTL. Lysatet overføres til et RNase frit Eppendorf rør, hvorefter det suges gennem en 21 Gauge kanyle, 10 til 15 gange. 600 μl 70 % ETOH tilsættes (fortyndet i dep H 2 O laves frisk hver gang) mix ved at pippettere op og ned. 600 μl overføres til en mini kolonne og centrifuges ved x g/15 sek, hvorefter gennemløbet fjernes. 600 μl 70 % ETOH tilsættes igen og der centrifugeres som før. Der tilsættes 700 μl RW1 til søjlen og der centrifuger x g/15 sek. Gennemløbet fjernes. Søjlen overføres til et nyt 2 ml rnasefrit eppendorf rør, hvortil der tilsættes 300 μl RPE. Der centrifugeres igen (8.000 x g/2 min). Gennemløbet fjernes. Søjlen overføres igen til nyt RNasefrit eppendorf-rør og der centrifugeres ved x g/ 1 min. Overfør søjle til nyt rnasefrit eppendorf rør og tilsæt 30 μl H 2 O (tilsat Rnase inhibitor) og centrifuger 8000 x g/1 min. Sidste punkt gentages igen Beregning af RNA indhold 2 µl RNA ekstrakt fortyndes med 110 µl Deb H 2 0 (1:55 fortynding) og RNA koncentrationen bestemmes spektrofotometrisk ved bølgelængden 260 nm og en faktor 40 (1 OD = 40 µg/ml RNA). Regneeksempel: absorbans værdi * (55*40 (1 OD = 40 ug/ml RNA)) = XX ug/ml 46
47 3.3.4 Verificering af RNA indhold i ekstrakter Elektroferese apparatet sættes i blød i 1 % H 2 O 2 24 timer før brug, for at ødelægge evt. RNaser. 0.4 g Agarose blandes med 40 ml TAE og smeltes i mikroovn (1 % gel). Blandingen afkøles til ca. 60 C, hvorefter der tilsættes 1.2 µl Ethidiumbromide (10 mg/ml). Gelen hældes i holderen og en kam placeres. Når gelen er størknet fjernes kammen og der hældes TAE i apparatet til ca. 3 mm over gelens overflade. 0.5 µg RNA og 3 µl markør (Kb plus DNA ladder (100 ng/µl, Invitrogen, kat nr ) loades. Prøver blandes med DNA loadingbuffer i forholdet 1:5 og justeres til totalt 10 µl med ddh 2 0. Gelen køres ved 70 mv i 1 time. RNA visualiseres vha. UV lys. Der fremkommer som regel bånd ved 1650 og 1000 basepar, hvilket afspejler hhv. 28 S og 18 S ribosomalt RNA. Gelen køres for at tjekke at RNA oprensningen er vellykket, dvs. at RNA båndene skal være klare og velafgrænsede. Herved tjekkes der for at RNA et ikke er blevet nedbrudt af RNaser. 3.4 RT og PCR cdna er en DNA kopi af RNA, som regel mrna. Den centrale del af cdna kloning er syntese af cdna fra en mrna template, ved brug af enzymet reverse transkriptase, der er en RNA afhængig DNA polymerase. RNA fra eukaryote organismer indeholder en polymerase A-hale, der gør det muligt at komplimentært DNA (cdna) kan syntetiseres ud fra det oprensede mrna i retningen 5 til 3 ved hjælp af enzymet reverse transkriptase. Random oligo-deoxynukleotider anvendes som primere til syntese af cdna s førstestreng og de fire deoxynukleotidtrifosfater (datp, dctp, dttp og dgtp) bruges som byggesten. Reverse transkriptase fungerer som andre DNA syntetiserende enzymer, idet den ikke kan initere DNA syntese uden en primer Praktisk udførelse af RT Til syntese af cdna anvendes 4 µg RNA. Der tilsættes 2 µl random primer (250 ng/ml), 2 µl, 10 mm dntp mix (final 0.5 mm) og H 2 O til et slutvolume på 24 µl. Dette inkuberer i 5 minutter ved 65 C, hvilket gør at random primer hybridiserer til mrna et. Herefter placeres blandingen på is og centrifugeres kort. Derefter tilsættes 8 µl 5 x first strand buffer (part. nr. Y00146), 4 µl 0,1 M DTT final 10 mm (Part. Nr. Y00147), 1 µl Rekombinant Rnasin ribonuklease inhibitor 40U/µl final 1U/µl (Promega, Kat. nr. N2511) og 1 µl H 2 O. Blandingen inkuberer ved 25 C i 2 min, hvorefter der tilsættes 2 µl SuperSript II RT (Invitrogen, Kat. nr ). Til sidst inkuberes der 10 minutter ved 25 C, 50 47
48 minutter ved 42 C, hvor enzymet aktiveres og i 15 minutter ved 70 C, hvor enzymet inaktiveres. Prøverne nedkøles på is og opbevares derefter ved 20 C. 3.5 PCR Karin Mullis opfandt I 1984 en metode kaldet polymerase chain reaction (PCR), der kunne lave kopier af specifikke DNA sekvenser. PCR kan udføres ved at tilføre følgende komponenter til en opløsning der indeholder mål sekvensen, der ønskes kopieret. 1) et primerpar der hybridiserer med de flankerende sekvenser af mål sekvensen, 2) alle fire deoxyribonukleotide trifosfat (dntps) og 3) en varmestabil DNA polymerase. PCR processen foregår automatiseret i en maskine, hvor de ønskede temperaturer, cycluslængder og antal kan indprogrammeres (Berg et al., 2002). I nedenstående figur ses princippet bag PCR teknikken Figur 32. PCR metoden består af tre trin. 1) denaturering af dobbeltstrenget DNA 2) annealing og 3) extension. Hvert af disse trin gentages gange i hver cykel. I den første cykel bliver dobbeltstrenget DNA denatureret, ved at varme reaktionen op til 90 C. Dette gør det ønskede område af DNA strengen mere tilgængelig. Temperaturen køles herefter ned til mellem 40 C og 60 C., hvorved annealing tillader hybridisering af de to oligonukleotid primere til DNA strengene. Primerne binder til deres komplementære steder, der flankerer target DNA (Berg et al., 2002). En PCR cycler består af tre trin, 1) Seperation af DNA strenge. To strenge af DNA molekyle separeres ved at varme opløsningen til 95 C i 15 sekunder, hvorved syntese af komplementær streng forekommer. 2) Hybridisering af primere. Her sænkes temperaturen til mellem 40 og 60 C, således at der kan ske en 48
49 hybridisering af forward og reverse primere til det enkeltstrengede DNA. Den anvendte hybridiseringstemperatur er primerspecifik, da primere har forskellige smeltetemperaturer (T m ). Det oprindelige DNA dupleks gendannes ikke, idet der er et stort overskud af primer. Primerne har typisk en længde på mellem 20 og 30 nukleotider lang. 3) DNA syntese. Her hæves temperaturen igen til ca. 72 C, idet Taq polymerasen ved denne temperatur har den maksimale synteseaktivitet. Taq polymerasen syntetiserer komplementær DNA streng ud fra template DNA. Polymerasen forlænger begge primere i en 5 til 3 retning. Disse tre trin fyldestgør en PCR cyclus af DNA forøgelse og kan gentages mange gange, blot ved at ændre temperaturen af reaktionsmikset (Berg et al., 2002). Der er flere fordele ved PCR metoden. For det første behøver mål sekvensen ikke at være kendt. Kun de flankerende sekvenser er nødvendige. For det andet, kan mål sekvensen være meget større end de flankerende sekvenser (Berg et al., 2002) Praktisk udførelse af PCR Der fremstilles en mastermix (20 µl reaktion) der inderholder 2.0 µl 10 x PCR buffer (promega, kat. nr. M190G), 1.60 µl 25 mm MgCl 2 (slutkonc. 2 mm) (promega, kat. nr. A351H), 1.0 µl dntp mix (slut konc. 0.5 mm), 10 mm dntp mix til final 0.5 mm, 0.4 µl DNA Taq polymerase 5U/µl (promega, kat. nr. M1865) final 2 %, 1.0 µl forward primer (100 ng/µl final 5 ng/ml), 1.0 µl 100 ng/µl reverse primer (100 ng/µl final 5 ng/ml), samt 1.0 µl Template (R1,R2 el RT-PCR). Der tilføres til sidst 12.0 µl H 2 O. De anvendte primere ses i appendix. Følgende PCR program er brugt: 95 C, 2 min 95 C 30 sek 40 C 30 sek dette trin gentages 35 x 72 C 2 min 72 C 10 min 4 C 3.6 Teoretiske betragtninger bag brug af fluorescerende prober Fluorescence er et resultat af en 3 stadie proces, der sker i bestemte molekyler, f.eks. i fluorescerende prober også kaldet fluoroforer. Flourescerende prober er molekyler, der absorberer lys energi, og derved eksiteres til et højere energistadie, der herefter vil emittere lysenergi. Processen der er ansvarlig for 49
50 fluorescensen af en fluorescerende probe og for andre fluoroforer, kan illustreres ved et enkelt elektronstadie diagram, kaldet et Jablonski diagram: Figur 33. Flourescens stadier. Fluoroforer vil I deres grundstadie, S 0, være i et relativt lavt energistadie og vil derfor ikke udsende fluorescence. Når lys af den rette bølgelængde rammer fluoroforen vil den exciteres h EX og derved opnå et højere energistadie, S 1. Da fluoreoforen i det høje energi stadie, er ustabil, vil den tabe energi og til sidst komme tilbage til sit grundstadie, hvorved fluoroforen vil udsende lys i form af emission, h EM. Kilde:143HHttp://probes.invitrogen.com/resources Fluorescerende molekyler vil når de exciteres ved lys af en bølgelængde, emittere lys ved en anden længere bølgelængde. En foton af energi h EX fra en ekstern kilde, bliver absorberet af fluoroforen, hvilket fører til et exciteret elektron stadie (S 1 '). Energien fra det indkomne lys (ekscitation) vil løfte valens elektroner i molekylet til et højere energistadie, et såkaldt exciteret stadie. Det exciterede stadie vil vare i 1-10 nanosekunder, hvorunder fluoroforen undergår konformationelle ændringer og er udsat for flere mulige interaktioner med dens molekylære miljø. Bl.a mister den elektroner i S 1 energi ved kollision med ikke-exciterede elektroner, hvilket fører til et lavere energistadie (S 1 ). Ved overgangen fra (S 1 ) til (S 0 ) opstår der fluorescens emission, hvilket returnerer fluoroforen til grundstadiet. Det emitterende lys er af lavere energi og derfor af længere bølgelængder, end den exciterende bølgelængde, hvilket betyder at det emitterede lys vil være forskelligt, fra det lys der blev absorberet. Den afstand der opstår mellem eksitationsmaksimum og emissionsmaksimum, kaldes for Stokes shift (se nedenstående figur), (Kilde: ( /resources/education.com), (Negulescu PA & Machen TE, 1990). Figur 34. Stokes shift. Stokes shift illustrerer forskellen i bølgelængde mellem exciteret og emitteret lys. Det emitterede lys er af lavere energi, end det exciterede lys og vil derfor udsende lys der er af en anden bølgelængde, end det exticeredes (142Hhttp://en.wikipedia.org/ wiki/stokes shift) Brug af flourescerende prober har flere fordele, idet fluoroforer gentagne gange kan exciteres, medmindre de bliver irreversibelt ødelagt, f.eks. ved foto-blegning. Flere fluoroscerende prober kan ligeledes benyttes samtidigt, blot der tages hensyn til probernes eksitations og emissionsspektra. 50
51 3.7 Måling af ændringer i intracellulær ph Der findes flere fluorescerende prober, der er i stand til at måle intracellulære ion aktiviteter i celler. Nogle af disse virker ved at den frie og den ion bundne form af den fluorescerende ion indikator har forskellige emission eller ekscitations spektre. Det betyder at den fluorescerende probe udviser et skift i deres ekscitations eller emissionsspektre, når de binder deres specifikke ion. Dette tillader dem at blive brugt i den såkaldte ratio metode, hvor ratioen af fluorescens-intensiteten mellem to forskellige bølgelængder bliver målt. Med denne type af indikator kan ratioen mellem de optiske signaler bruges til, at estimere ion koncentration og denne vil være uafhængig af probe koncentration. Ratiometriske målinger eliminerer forstyrrelse af data, forårsaget af foto-blegning og variationer i probe loadning og retention (Negulesen og Machen). Ratio-metoden er nærmere beskrevet i afsnit Teoretiske betragtninger bag måling af intracellulær ph (ph i ) ph i er en vigtig parameter til at studere i cellefunktioner. Da mange metaboliske reaktioner og funktioner i cellulære organeller bliver påvirket af ændringer i intracellulær H + ion koncentration, er det kritisk at kunne måle ph i præcist under fysiologiske omgivelser (Ozkan P & Mutharasan R, 2002). Fluorescerende ph indikatorer er et uundværligt redskab til måling af ændringer i intracellulær proton koncentration. For at kunne bestemme ph i så præcist som muligt, er det nødvendigt at matche pka af indikatoren til ph af det system, som undersøges. Da ph i cytosolen er tæt på neutral (generelt ml 6.5 og 7.5) er fluorescens indikatorer med en pka omkring 7 krævet for cytosoliske ph bestemmelser (Tsien RY., 1989). De oftest benyttede fluorescens indikatorer til nær-neutral ph målinger i celler, er fluorescein-afledte molekyler (Boens N et al., 2006). I dette speciale er 2 7 -bis-2-carboxyethyl-5,6 carboxy-flourescein (BCECF) brugt til målinger af ph i BCECF BCECF er et hydrofilt molekyle og kan derfor ikke krydse plasmamembranen. Derfor skal celler der loades med BCECF, først inkuberes med en acetoxymethyl ester (AM- ester) form af BCECF, der er membran-gennemtrængelig, idet at de negative ladninger bliver masked af AM- esterene. Intracellulære esteraser hydrolyserer BCECF-AM til BCECF, hvilket medfører at BCECF atter bliver hydrofil inde i cellen og bliver derved fanget i cytosolet, se nedenstående figur (Negulescu PA & Machen TE, 1990), (Bachmeier CJ et al., 2004). 51
52 Figur 35. Loadning af BCECF-AM indi celler. Modificeret fra (Bachmeier CJ et al., 2004). BCECF er en H + følsom fluorofor, hvis ekscitationsmaksimum er ca. 500 nm og emissionsmaksimum er ca. 525 nm. BCECF har et ph ufølsom punkt ved ca. 440 nm. Når BCECF eksciteres ved 440 nm påvirker ph ikke den relative fluorescens. Dette punkt kaldes det isosbestiske punkt, eller det phufølsomme punkt. Når BCECF derimod eksciteres ved ca. 450 til 530 nm udvises der ph afhængighed, idet fluorescensen af BCECF reduceres ved stigende H + koncentrationer. Det betyder at BCECFs ekscitationsspektrum, ligesom absorptionsspektrummet, flyttes mod kortere bølgelængder, når ph falder. Man kan derfor tale om at ekscitations-spektrummet for BCECF har en ph følsom og en ph ufølsom region ( nm) (Negulescu PA & Machen TE, 1990;Tsien RY., 1989). Nedenstående figur viser ekscitations og emissionsspektre for BCECF. Figur 36. Excitation og emission spectra for BCECF. Ved stigende koncentrationer af H +, bliver fluorescencen af BCECF, når den exciteres ved bølgelængder fra 450 nm til 530 nm, reduceret signifikant og derved vil excitations spektraet flyttes mod kortere bølgelængder. Pilen indikerer hvor det isobestiske punkt findes (Dissing S and Gasbjerg PK, 1993). 52
53 Fordele ved brug af BCECF I forsøgene er der brugt fluorescens proben BCECF, idet den har flere fordele og ulemper (ifølge (Negulescu PA & Machen TE, 1990): den har en pka værdi på ca. 7,0. hvilket er tæt på ph I der normalt er observeret i de fleste celler. den findes som en AM-ester, så loading af probe til cellerne er simpel. den har fluorescens- spektrum skift, der muliggør ratiometrisk måling. Ulemper ved brug af BCECF Kløvning af en BCECF-AM resulterer i dannelse af 3 formaldehyd og 2 eddike-syre molekyler, der begge er toxiske for cellerne (formaldehyd fører til ATP depletion i cellerne). Det er derfor vigtigt at inkubering med BCECF-AM ikke sker i mere end 30 min og det er vigtig at ekstracellulær probe vaskes væk, før forsøgsstart. Autofluorescence fra celler, ringere eller fra det optiske udstyr kan påvirke den totale fluorescens intensitet. Ved at fratrække den målte baggrund fra BCECF uloadede celler efter hver måling, i de forskellige Ringere, kan denne fejlkilde udelukkes. Fotoblegning. Ved belysning af BCECF vil proben langsomt miste fluorescens signal og derved blive omdannet til et kemisk non-fluorescerende molekyle. Da den anvendte probe koncentration er minimal, formindskes dannelsen af de kemiske non-fluorescerende molekyler Ratio-metoden I ratio ekscitationsmetoden, bliver fluorescensproben exciteret ved to forskellige bølgelængder, som regel 445 nm (den ph ufølsomme bølgelængde) og ved 495 nm (den ph følsomme bølgelængde) mens emissionen måles ved 525 nm (for BCECFs vedkommende). Ratioen (445nm/495nm) kalibreres herefter, således at ph i -værdier opnås (baggrundsværdier fratrækkes først de pågældende bølgelængder), se databehandling for yderligere forklaring. Metoden anvendes kun for prober som BCECF, som udviser et skift i deres ekscitationsspektrum, når en ligand bindes. Desuden afhænger metoden af en række faktorer, bl.a. at proben skal danne et 1:1 kompleks med ionen og at proben er så opløselig at fluorescens intensitet er proportionel med koncentration af fluorescens species. I forsøget skal det bemærkes, at der er brugt den reverse ratio, idet vi finder den mere illustrativ, at stigende [H + ] er lig en stigning i ratio. 53
54 3.7.3 Bestemmelse af ph i ved kalibrering Det er nødvendigt at kalibrere fluorescenssignalet i forhold til den frie ion- koncentration/aktivitet, for at kunne bestemme den intracellulære ph værdi. Dette sker ved en såkaldt in situ kalibrering, hvor cellemembranerne behandles med en ionophor, der ækvilibrerer intracellulære og ekstracelluære koncentrationer af den ion man vil have undersøgt, i dette tilfælde H +. Når den ekstracellulære opløsning bliver titreret til forskellige ion koncentrationer, vil den indre koncentration clampes til den samme værdi og fluorescens intensiteten kan måles. Herefter kan en kalibrerings kurve laves (Negulescu PA & Machen TE, 1990). Denne kalibreringskurve er i forsøget lavet vha. høj K + /nigericin-metoden, hvor ph i bliver beregnet vha. en Nigericin kalibreringsteknik, hvor cellerne i slutningen af forsøget tilføres en Na + fri Ringer (KCl Ringer, ph 7.0), samt 5 µg/ml Nigericin (for princip bag metode, se (Boyarsky et al., 1988). Nigericin er en ionofor der udveksler K + for H + over membranen. Da [K + ] i og [K + ] o er i forsøget er ens, vil dette clampe ph i ved samme værdi, som ph o, derfor er [K + ] i /[K + ] o = [H + ] i /[H + ] o, når man anvender en opløsning hvor [K + ] o er lig [K + ] i. Det betyder at når intracellulær og ekstracellulær [K + ] er ens, så vil ph i være = ekstracellulær ph og derved kan ph i kontrolleres ved at ændre ph i den Ringer der anvendes, når nigericin tilsættes. I dette speciale er der fremstillet en kalibreringskurve, hvor fluorescensratioen er bestemt ud fra funktion af 6 ph værdier fra 6.2 til 8.0 (Pedersen SF et al., 1998). Figur nm/495 nm fluorescens ratio som funktion af ph i. ELA-celler er inkuberet med KCl ringer med forskellige ph-værdier (6.2, 6.6, 7.0, 7.2, 7.4, 7.6 og 7.8) i nærvær af nigericin (5 µl/ml). ph i kalibreres til ph o efter ca. 5 min. og 445/495 nm ratioen blev målt. Ligningen for den linære del af kurven er bestemt. Data er baseret på fem uafhængige kalibreringsforsøg (Pedersen SF et al., 1998) Kalibreringskurvens data er blevet fittet i forhold til følgende ligning; (Boyarsky et al., 1988): F F ph 10 R n = 1 + b pka pka = ph pka 7.0 pka Ligning
55 Rn er ratioen mellem F445/495 normaliseret til ph 7.0. b er en konstant og pka er dissosiationskonstanten for BCECF. Disse kan bestemmes udfra kalibreringskurven, idet ligningen kan omskrives til: ph i = pk a ( Rn 1) + ( ba) + log (1 Rn) + ( b(1 a)) Ligning 1.2 a = ( pka )/( pKa ) og Rn = 445 nm/495 nm ratioen normaliseret til ratioen ved ph 7.0. Da b og pka bestemmes udfra kalibreringskurven kan ph i nu bestemmes vha. ét punkts kalibrerings med Nigericin og KCl Ringer (ph 7.0). Rn kan herefter beregnes og sættes ind i ligning 1.2 og derved udregnes ph i. pka er bestemt til 6.852, mens b er bestemt til Beskrivelse af apparatur 4 elementer er nødvendige for fluorescens detection systemer, 1) en ekscitationskilde, 2) en fluorophore, 3) bølgelængde filtre til at isolere emissions fotoner fra ekscitationsfotoner og 4) en detektor der kan registrere emissions fotoner og producere et optagebart udkom, som regel er dette et elektrisk signal eller et fotografisk image. Til måling af fluorescens anvendes et Ratio fluorescens Spektrofotometer Model C- 44 i dette speciale. Modellen er forbundet til en computer og data kontrolleres af computer programmet, software 2.1. Felix PTI spektrofotometeropstilling model C Lampehus med 75 W xenon arc lampe. 8. Filter holdere. 2. Justerbare lysspalter. 9. Excitations/emissions optik. 3. Excitations monochromator 10. Tempereret kuvetteholder 4. Optisk fiberkabel. med magnetomrarer 5. Optisk fiberadapter 11. Emissions lukker. 6. Kuvettehus Justerbare lysspalter 7. Afskaermning. 13. Emissions monochromator. 14. Fotomultiplier tube detektor 55
56 PTI ratiomaster spektrofotometeret består af en 75 W powerarc xenon arc lampe, der emitterer bredspektret lys med en høj intensitet. Excitations monochromatoren bestemmer bølgelængden af det lys der skal sendes videre ( nm). Desuden findes der i selve spektrofotometeret justerbare spalter ved monochroma-torernes ind- og udgang. Disse kan regulere båndbredden af lyset der slipper igennem denne. Et optisk kabel overfører lys fra ekscitations monochromatoren til kuvetten i kuvetteholderen, hvor den oplyser et lille område med celler nederst på dækglasset. Dækglasset med celler sidder med en vinkel på 50 til det indfaldne lys og en monochromator selekterer emissions bølgelængden (13). De spredte fotoner opfanges vha. af et analog/photon counting photomultiplier detection system (PMT) og via disse opsamlede spændingsændringer, kvantificeres volumenændringer som ændringer i PMT output. Herefter konverteres data fra analogt til digitalt signal og overføres til en computer, hvor datasporet kan følges på skærmen med Felix software version Praktisk udførelse af ph i bestemmelser ELA celler dyrkes på sterile dækglas (10*50 mm) i 4-brøndsbakke, således at de på forsøgsdagen er ca. 90 % konfluente, dvs. 7,5*10 5 celler pr. brønd. I hvert brønd placeres 2 dækglas, samt 3 ml medie (RPMI-1640) + celler og bakken sættes i 37 C steril inkubator. På forsøgsdagen vaskes dækglassene i isoton Ringer 2 gange, hvorefter de loades med 2 μm BCECF-AM, i 2 ml isoton Ringer. Dækglassene inkuberes i en ½ time i 37 C inkubator. Efter endt inkubering vaskes dækglassene 2 gange i isoton Ringer. Dette gøres for at fjerne ekstracellulært BCECF-AM. Dækglassene inkuberer herefter videre i 15 min ved 37 C og 0 % CO 2 ved tilstedeværelse af isoton Ringer, således at evt. lækket probe fjernes. Ved forsøg med Rho kinase hæmmeren, Y27632 (10 μm) inkuberes cellerne 1 time før forsøgsstart med hæmmeren. I de sidste 30 min af denne inkuberingstid, tilsættes der 2 µm BCECF-AM, hvorefter cellerne inkuberes videre i 30 min i 37 C inkubator. Cellerne behandles herefter som ovenfor beskrevet. Ved sirna transfektionsforsøg transfekteres cellerne med 20 µm ezrin sirna eller kontrol sirna 3 dage før forsøgsstart (se beskrivelse i ), hvorefter de er klar til forsøg, efter ovennævnte procedure. Ved forsøg med NHE hæmmeren EIPA, inkuberes celler efter normal procedure og 5 µm EIPA tilsættes når cellerne har stabiliseret sig efter tilsætning af hyperton Ringer. Når celler er loaded og inkuberet med BCECF placeres et dækglas med celler i spektrofotometerets kuvetteholder, sammen med 3 ml 37 C isoton Ringer og en magnet. Protokollen indstilles til at måle fluorescens ved en fast emission på 525 nm og ekscitation indstilles til en ph afhængig bølgelængde på 495 nm og en ph uafhængig bølgelængde på 445 nm. Kuvetteholderen har et ind- og et udførsels system, hvilket gør, at der kan skiftes Ringer i kuvetten under forsøget. Ind-/udførsels hastigheden sættes til (1,6 56
57 ml/min). Først tilføres der isoton Ringer (ph 7.4). Når et stabilt signal opnås (efter ca. 500 sek.), skiftes der til hyperton Ringer (ph 7.4). Når der igen indfinder sig et stabilt signal, udføres der en såkaldt étpunkts kalibrering med en isoton KCl Ringer og med 10 µm nigericin. Baggrunds fluorescens skal måles hver forsøgsdag, på celler der ikke er inkuberet med BCECF-AM, men som ellers er behandlet under samme vilkår som BCECF-AM loadede celler. Under eksperimenter med fluorescens prober er det normalt at signalet ved både 490 og 440 nm falder. En typisk rate for tabet af signal er % / time. Dette signaltab kan bl.a. forklares ved, at der sker en lækning af probe fra cellerne og der sker en blegning fra xenon lampen af den fluorescerende probe (Negulescu PA & Machen TE, 1990) Databehandling Først trækkes baggrundsværdierne fra samtlige fluorescens værdier. Derefter udregnes ratioen mellem dem (445nm/495 nm). Der tages et gennemsnit af ratioen, efter tilsætning af ionoforen nigericin (R n ). Dette gennemsnit divideres med samtlige ratioværdier, for at normalisere til værdierne ved ph 7.0. ph i kan herefter bestemmes ud fra ligning 1.2, idet pka og b kendes fra kalibreringskurven. 3.8 Bestemmelse af cellevolumen Teori Afbøjning af lys afhænger af det ramte objekts brydningsindeks. Cellers brydningsindeks og dermed deres lyssprednings-egenskaber ændres ved ændringer i cellens volumen. En celles volumenændring forårsager en målelig ændring i spredningen af lys fra cellerne, typisk således, at hvis cellen skrumper, vil den udsende et stærkere lys signal (McManus et al., 1993). Lightscatter-systemet bruges til at studere cellevolumenregulering og membranprocesser. Celler regulerer deres volumen under osmotisk stress. Det er vist, at celleskrumpning eller cellesvulmning, der er induceret af udsætning for hyper- eller hypotoniske opløsninger, kan lave hurtige stigninger eller fald i lightscatter signal (McManus et al., 1993;Negulescu PA & Machen TE, 1990). Large angle Ligth Scattering (LALS) bruges i dette speciale til, at estimere cellevolumen under osmotisk stress. 57
58 Fordele ved LALS Der er flere fordele ved at bruge ligthscatter teknikken, 1) den er non-invasiv, 2) den kan hurtigt detektere og kvantificere små cellevolumen ændringer 3) man kan undersøge cellerne i en fastholdt tilstand og derved påvirker metoden ikke cellernes evne til at opretholde naturlig celle morfologi, celle overflade kontakter og celle-celle interaktioner 4) der kan laves flere forstyrrelser i hvert forsøg og 5) den kan laves samtidig med ph i målinger i celler der kan være loaded med flere prober samtidigt (McManus et al., 1993). Ulemper ved LALS Ulemperne ved teknikken er, at data giver et relativt og ikke et absolut billede af cellevolumen ændringen. Volumeændringer og raten af volumeændringer kan kvantificeres vha. PMT output. Der er dog et problem ved denne løsning når data skal sammenlignes. Data kommer fra kulturer fra forskellige passager og med evt. forskellige vækstperioder før forsøgsstart. Den absolutte mængde af cellulært materiale, der vokser på hvert dækglas, vil direkte påvirke størrelsen af ændringer i ligthscatter signal for enhver cellevolume ændring (McManus et al., 1993) Praktisk udførelse af LALS LALS blev udført samtidigt med fluorescens målinger, på de BCECF-loadede celler. Data blev omregnet til relativ cellevolumen ved at der udregnes et gennemsnit for emissionsmålingerne, når et stabilt signal forefindes efter tilsætning af isoton Ringer. Dette gennemsnit (I 0 ) divideres op i hver enkel emissionsværdi (I) og disse værdier (I 0 /I) vil illustrere den relative volumen ændring i forsøget. Emissionsværdierne plottes som funktion af tiden. 3.9 CLSM Teori Konfokal laser scannings mikroskopet er en videreudvikling af det traditionelle lysmikroskop. Med konfokal lys mikroskopi kan man generere meget tynde optiske sektionsbilleder, gennem en tyk fluorescerende prøve, hvor der ikke er out of fokus fluorescens. Desuden kan man se prøver i flere planer og man kan få tre-dimentionelle billeder i høj opløsning på få sekunder (Shinya Inoue, 1995). 58
59 CSLM fungerer ved, at laseren sender lys ud gennem et pinhole, hvor lyset rammer et dichroisk spejl, som afbøjer lyset og sender det ned i et specifikt punkt i præparatet, kaldet fokal planet. Hvis præparatet er et fluorescens -præparat, bevirker det indkomne lys, at der udsendes fluorescerende lys fra præparatet. Dette vil ramme det dichroiske spejl, som samler og afbøjer lyset mod PMT (fotomultiplier tube). Foran denne PMT er et pinhole placeret og i dette fokuseres det afbøjede lys og sendes via PMT en videre til et computerprogram, der danner et billede. Navnet konfokal mikroskopi stammer fra, at de 2 pinholes er i fokus. Det lys der rammer uden for det fokale plan, vil ikke ramme åbningen i pinhole foran PMT en. Dette lys vil derfor blive udelukket fra PMT en (Paddock SW., 1999), (Tauer, 2002). Figur 38. Princippet bag CLSM. Confocal princippet med spot illumination og spot observation til fluorescense lys. Det exciterede lys (produceret af laseren) bliver fokuseret i en lille objektivåbning (excitations pinhole) af en linse. Stråle splitteren diregerer lyset fra objektivåbning-en mod prøven. Objektivet fokuserer lyset mod prøven. Fluorescense lyset der emitterer fra prøven passerer gennem stråle splitteren, da dens bølge-længde er længere end excitations bølgelængdens lys. Emissionen fokuseres på pinhole. Kun lys der passerer obejtivåbningen når detektoren. Dette lys kommer fra det fokale plan. Alt out of fokus undertrykkes af detektions pinholet (Tauer, 2002). Fordele ved confocal mikroskopi Confocal mikroskopi har flere fordele over almindelig lys og electron mikroskopi. For det første kan man vha. confocal mikroskopi optisk sektionere prøven man vil have undersøgt. Da optisk sektionering er non-invasiv, kan levende såvel som fikserede celler observeres med større klarhed. En anden fordel ved confocal mikroskopi er at optiske sektioner kan tages fra forskellige planer, dvs. xy planet, xz og zy planet. En tredje fordel ved confocal mikroskopi er at de optiske sektioner kan gemmes i et digitalt format (Wright SJ & Wright DJ, 2002). 59
60 Ulemper ved confocal mikroskopi CLSM er begrænset af tilgængeligheden af bølgelængder af lys produceret af lasere (Wright SJ & Wright DJ, 2002) Praktisk udførelse af præparater til CLSM 3 dage før forsøgsstart sås celler ud i 6 brøndsbakker på syrevaskede dækglas, således at de har en konfluens på ca %. Samme eftermiddag transfekteres cellerne med 20 µm ezrin sirna, kontrol sirna eller med H 2 O. Efter 3 dage vaskes cellerne en gang med isoton Ringer og der tilsættes derefter igen isoton Ringer, som efterlades på cellerne i 20 min, for at stabilisere cellerne. Den isotone Ringer udskiftes med isoton, eller hyperton Ringer, som efterlades i 1, 5 eller 15 min. Stimuleringen stoppes ved at tilføre 200 ul paraformaldehyd til en slutkoncentration på 2 %, herved fikseres cellerne. Cellerne henstår i 15 min ved stuetemperatur og derefter 30 min på is. Cellerne vaskes 3*5 min med TBS + 1 % BSA, hvorefter cellerne permeabiliseres ved tilsætning af TBS % tritonx-100 i 10 min. Dette suges væk og der tilsættes blocking buffer (TBS+5 % BSA), hvilket henstår i 30 min på cellerne. Der tilføres primært antistof (fortyndet i 5 % BSA) til brøndene og det henstår natten over på rystebord ved 4 C. Næste dag vaskes cellerne 3*5 min med TBS + 1 % BSA, hvorefter der tilsættes sekundært antistof, samt rhodamine phaloidine (der mærker cytoskelettet). De sekundære antistoffer er konjugeret med GAR eller GAM-FITC (fortyndet 1:500). Cellerne henstår i 1-2 timer og vaskes derefter i 5 min i TBS + 1 % BSA. Cellerne dækkes med DAPI (1:600 i TBS + 1 % BSA) i 5 min. Der vaskes igen 3* 5 min med TBS + 1 % BSA, hvorefter cellerne monteres på glas, vha. N-propyl-galleat antifade og neglelak. Til hvert forsøg blev der lavet der et dækglas uden primære antistoffer, til kontrol for uspecifik fluorescense. Dette dækglas blev i stedet inkuberet i TBS+5 % BSA. Selve confocal mikroskopien af præparaterne er blevet udført af Stine Falsig Pedersen. Mikroskopet der er anvendt er et Leica IRB/E-mikroskop, der er koblet til en Leica TNS confocal laserscanningsenhed (Leica Lasertechnik GmbH, Heidelberg, Tyskland). Det anvendte objektiv var 1.25/160x/1.4NA. Fluorescensen i præparaterne uden primært antistof, blev indstillet til 0 ved den relevante bølgelængde og den numeriske aperture blev sat til 1 i begge pinholes. 60
61 3.10 Western blotting Fremstilling af helcelleekstrakt Cellerne blev høstet når en konfluens på ca. 85 % var nået. Efter stimulering i x antal minutter, lyseres cellerne ved at der tilsættes 280 μl 95 C varm lysisbuffer. Cellerne skrabes herefter af Petriskålen med en rubber police man. Efter høstningen overføres cellerne til et 1.5 ml Eppendorfrør, hvorefter samtlige prøver stilles på varmeblok (95 o C) i 5 minutter. Prøverne suges op i en 27 gauge kanyle og presses ca. 15 gange igennem denne, hvorved nucleinsyrer, membraner og cytoskelet-strukturer bliver ødelagt. Cellerne centrifugeres herefter i 10 min. ved g /4 C, hvorefter supernantanten overføres til et nyt Eppendorfrør. Prøverne er nu klar til proteinbestemmelse Proteinbestemmelse Proteinkoncentration er bestemt udfra et DC Protein Assay, hvor en farvereaktion mellem protein i prøven og Reagent A og Reagent S. Protein i prøverne danner et kompleks med Cu 2+ - tartrat fra reagent A og S og reduceres herefter af folinreagens, Reagent B. Folinreagent indeholder syregrupper, der reduceres af protein-cu 2+ - komplekset, hvorved der dannes en blå farve, grundet tab af iltatomer. Farveintensiten måles spektrofotometrisk ved 595 nm (Gene Quant Pro, Amersham Pharma Biotech.). En standardrække fremstilles udfra BSA-standarder (bovin serum albumin) og lysisbuffer. Standardrækken skal indeholde 0.2, 0.4, 0.6, 0.8, 1.0 og 1.2 µg protein/ µl. 10 µl prøve og 15 µl vand tilføres til x antal 5 ml nunc rør. Til 7 andre nunc rør tilføres 25 µl af hver standard. Til alle nunc rørene tilsættes 125 μl working reagent A+S. Herefter tilsættes der 1 ml reagent B til alle rør og umiddelbart efter wortexes rørene. Prøverne henstår nu i 15 minutter under sølvpapir. Prøverne overføres til kuvetter og derefter måles deres absorbans. Proteinmængden i de enkelte prøver kan beregnes udfra en linær regression af standardkurven og OD værdierne fra prøverne, herved kan der loades lige meget protein i hver banes. Til denne mængde tilsættes loadingbuffer og 50 µm dithiolthretiol (DTT). Prøverne varmes kort ved 95 C, hvorefter de er klar til at blive kørt på en gel Udregning Standard rækkens linære regression beregnes. Prøvernes OD værdi divideres med den lineære regression, herved udregnes hvor mange µg der er af prøven. For at finde ud af mange µg/µl der er, divideres µg med antal µl cellelysat, der er tilsat prøverne. Da man gerne vil have udregnet hvor mange µl prøve, der skal tilsættes til et total volumen på 50 µl divideres 50 µl med µg/µl. For at der loades lige meget protein i 61
62 hver bane, fortyndes den udregnede mængde protein med H 2 O. Mængden af H 2 O udregnes ved at tage totalvolumen på 50 µl og trække µl prøve, samt loadingbuffer + DTT fra. Herved ved man præcist hvor meget der skal tilsættes af de forskellige ingredienser, for at der bliver loadet lige meget protein til hver bane SDS-PAGE teori Ved separation af proteiner i SDS-PAGE gel elektroforese, opnår man en adskillelse af proteiner på baggrund af deres størrelse. SDS er en negativt ladet detergent, der nedbryder proteiners kvarternære, tertiære og sekundære strukturer, ved at opløse hydrofobe områder, hvorved proteinerne bliver mere udfoldede. Desuden påføres proteinerne negative ladninger, idet SDS bindes til dem i forholdet 1.4:1 (SDS:protein). For at bryde proteinernes svovlbroer tilsættes thiolreagenten DTT (dithiothreitol) til prøverne. Proteinerne indeholder herefter kun deres primære struktur og de vil have fået en negativ ladning, svarende til deres størrelse påført. Dette medfører at proteinerne kan adskilles udelukkende på baggrund af deres størrelse og ikke deres indre ladning. Det betyder at proteinfragmenternes vandringslængde i gelen er proportional med deres molekylemasse. Gelen består af polyacrylamid, som er kæder af monomeren acrylamid krydsbundet med monomeren bisacrylamid. Gelens densitet, elasticitet og viskositet afhænger af koncentrationen af acrylamid. Jo mere acrylamid, desto mindre porer i gelen. Gelen kan opdeles i en stackinggel (den øverste del) og en seperationsgel (den resterende del). Proteinerne loades i stackinggelen, i en zone kaldet stackingzonen, som har specielle brønde til formålet. Dette gør at proteinerne koncentreres i en smal zone og at proteinerne derved vil have samme startsted Praktisk udførelse af SDS-PAGE Gelelektroforesen udføres i NOVEX system elektroferesekammer med NuPAGE precast 10% Bis-Trisgeler til kørsel under denaturerende og reducerende forhold. Detergenten SDS forårsager de denaturerende forhold, og DTT samt antioxidant de reducerende forhold. Der fremstilles 600 ml runningbuffer, 200 ml af disse overføres til et bægerglas, hvor der tilsættes 500 μl antioxidant. Til det indre kammer tilsættes de 200 ml, mens de resterende 400 ml tilsættes det ydre kammer. Prøverne varmes kort på varmeblok (95 C), hvilket har en yderligere denaturerende effekt på proteinekstrakterne. Prøverne samt en markør påsættes gelen. Der benyttes en markør, der indeholder kendte proteiners molekylvægt, for at proteinekstrakternes adskilte fragmenter kan identificeres (se appendix )). Elektroforesen startes og køres ved 140 V i ca min, eller til det blå bånd når bunden af gelen, som 62
63 stopper et lille stykke over bunden af kassetten, som gelen er støbt i. Efter endt elektroforese skæres stackinggelen af og seperationsgelen lægges i en sandwich af membran og filterpapir, begge klippet i gelens størrelse. Omkring sandwichen lægges blotting pads, dels for at holde den sammen og dels for at transferbufferen får adgang til membranen. Der elektroblottes ved 25 V i 2 timer. Efter endt blotting udtages nitrocellulose-membranen med de overførte proteiner og denne farves med Ponceau. Formålet med farvningen er, at undersøge om membranen indeholder lige store mængder protein og at undersøge om blottet er kørt korrekt. Herefter skylles membranen i ddh 2 O og markørens bånd markeres med blyant. Der tages en fotokopi af membranen. Membranen lægges herefter i blockingbuffer (5% skummetmælkepulver i trisbufret saltvand med tween og NaAzid) i 2 timer ved stuetemperatur, eller natten over i kølerum på rystebord. Blockingbuffer binder de overskydende bindingssteder på membranen og reducerer derved evt. uspecifik binding af antistoffer Western blotting- og immunodetektions teori Western blotting bruges til at detektere specifikke proteiner eller proteinfragmenter, der reagerer med et kendt antistof. De primære antistoffer er enten monoklonale eller polyklonale. Monoklonale antistoffer binder til én epitop på et antigen, mens polyklonale antistoffer kan binde til flere epitoper. Det primære antistof vil binde til det immobiliserede protein på membranen. De sekundære antistoffer genkender F c - delen på de primære antistoffer og har en alkalisk fosfatase vedhæftet. Denne fosfatase spaltes under fremkaldelse med nitroblue chlorid og 5-bromo-4-chloro-3-indoylfosfat p-toluidin salt (BCIP/NBT) og farvereaktionen der udvikles kan herefter kvantificeres Praktisk udførelse af Immunodetektion Membranen vaskes to gange med blockingbuffer og der tilsættes blockingbuffer indeholdende primært antistof. De primære antistoffer fortyndes i blockingbuffer og tilføres til membranen, som herefter skal henstå i 2 timer ved stuetemperatur, eller natten over ved 4 C. Efter inkubering med primært antistof vaskes membranen i TBST (1*15 min og 3*5 min) og sekundært antistof, fortyndet 1:600, tilsættes. Der vaskes igen med TBST (1*15 min og 3*5 min), hvorefter der fremkaldes med BCIP/NBT. Når båndene på membranerne bliver tydelige, stoppes reaktionen med tilsætning af ddh 2 O. Membranerne tørres på papir og gemmes. 63
64 Kvantitativ analyse Proteinbåndene på membranerne kvantificeres med computerprogrammet UN-SCAN-IT. Programmet sammenligner de enkelte bånds farveintensitet med hinanden og til baggrunden. Resultatet opgives som arbitrær intensitet. Farveintensiteten er et udtryk for mængden af det sekundære antistof og dermed for de proteiner der detekteres for. For at membranerne kan sammenlignes, normaliseres data til farveintensiteten i kontrolpræparatet. Dette gøres ved, at sætte kontrolprøven (isoton, 5 min.) fra hver membran til 1. Flere membraner kan sammenlignes, da der er påsat præcis den samme mængde protein til hver bane i alle forsøg RNA interference (RNA i ) Mammal gen funktion er traditionelt bestemt vha. metoder som f.eks. ødelægger gener, eller introducerer transgener. Mikroinjektion af specifikke antistoffer i dyrkede celler, eller binding af antistoffer på celleoverflade-eskponerede receptorer, kan ligeledes give information om funktionen af det udvalgte gen. Et nyere alternativ er sirna, der kan udløse RNAi i mammale celler (Elbashir SM et al., 2002). RNAi har udviklet sig til at være en af de vigtigste metoder til analysering af gen funktion, gennem de sidste 15 år og metoden har i år vundet nobelprisen i medicin. RNA interference (RNAi) er et term der bruges til at beskrive fænomenet hvorved dobbeltstrenget RNA (dsrna) fører til silencing af gener der er homologe i sekvens (Gregory RI et al., 2005), (Elbashir SM et al., 2002). dsrna er et naturligt og meget vigtigt signaleringsmolekyle i eukaryote celler, idet det er med til at udløse et forsvarssystem der er udviklet til at eliminere uvelkomment fremmede RNA molekyler, som f.eks. cytoplasmatisk replikerende RNA vira, transkipter fra transgener, transposale elementer, eller virus der prøver at blive integreret i værtsgenomet (Harborth J et al., 2003). Mens lange dsrna molekyler kan inducere RNAi i lavere eukaryoter, er sirna (21 nt) blevet udviklet til at kunne silence gener i mammale celler (Kurreck J., 2006). RNAi metoden omfatter, at lange dsrna strenge via RNase III endonukleasen, DICER, bliver omdannet til ca 22 nukleotid sirna, der indeholder 2 nukleotid 3 overhæng. sirna bliver inkorporeret i et ribonukleo-protein effektor kompleks, kendt som RNA-induced silencing complex, RISC. En streng af sirna duplekset er den respektive guide streng, der videre fungerer som den specifikke komponent i selve silencing mekanismen, den anden streng bliver smidt væk. RISC bruges guide strengen til at target komplementær mrna til nedbrydning vha. endonukleolytisk kløvning af target mrna eller til 64
65 translationel repression (Gregory RI et al., 2005), (Cheng JC et al., 2003), (Elbashir SM et al., 2002). Nedenfor er mekanismen bag RNAi vist: Figur 39. Mekanismen bag RNA interference medieret silencing. Aktivering af RNA induceret silencing kompleks (RISC) fører til komplet parring med mrna og derved hæmning ved nedbrydning af target transkriptet (Cheng JC et al., 2003). Preliminære forsøg med brug af RNAi i mammale systemer, hvor man brugte lange dsrna som udløsere til gen silencing, førte det til induction af et non-specifikt Type I interferon respons, i stedet for den sekvens specifikke silencing (Kim DH et al., 2005). Dette interferon respons resulterede i flere ændringer i protein ekspression, hvilket dækkede for enhver sekvens silencing specifik effekt og førte til sidst til apoptose. I dag er der udviklet kemisk syntetisk fremstillede sirna, som effektivt kan passere det mammale interferon respons og derved silence gen ekspression ( com/sirna/about.aspx). Designet af et sirna baseret knockdown eksperiment kræver selektion af en mål region indenfor target mrna, der er 1) unik i sekvens i genomet af den studerede organisme 2) kan kløves af sirna targeting kompleks. Desuden anbefales det, at den udvalgte region helst skal være i den kodende region, være mindst 50 nukleotider nedstrøms for start kodon og have et GC-indhold på mellem 30 og 50 %. En blast søgning er nødvendig for at sikre at sirnaet ikke har signifikant homologi med andre gener, end det egentlige mål (Kurreck J., 2006), (Cheng JC et al., 2003). Når sirna sekvenser af interesse er identificeret, kan sirnaet kemisk fremstilles, in vitro transkriberes, eller genereres gennem PCRbaserede metoder (Cheng JC et al., 2003). Transient transfektion med sirna duplekser i mammale celler kan genereres via traditionelle liposomale metoder, via f.eks. reagenter som oligofektamin eller lipofektamin, eller transfektionen kan ske via elektroporation. Transient silencing varer i flere celle genrationer og flere knockdowns af proteiner i samme celle population er muligt (Harborth J et al., 2003). Idag findes der ligeledes stabile sirna ekspressions-systemer, der bruger plasmid og viral vektorer til at opretholde sirna "knock down". 65
66 Plasmid vektorer der driver sirna ekspression i mammale celler kan genereres gennem kloning af sirna sekvenser med en RNA pol II eller III promoter. Ekspressionsvektorer kan bruges, men en mere effektiv metode er at ekspressere korte "hairpin" RNA (shrna). Når disse ekspresseres i mammale celler vil shrna bliver genkendt af dicer og derfor blive kløvet til funktionel sirna. Plasmid vektorer er stadig begrænset i deres evne til at opretholde den hæmmende effekt af genet, grundet deres afhængighed af transfektion. Dette har ført til anvendelse af viral baserede vektorer, der ekspresserer shrna. Lentiviral og andre retroviral systemer, fjerner afhængighed af transfektionen for RNAi og er derfor mere effektiv i mange celler (Cheng JC et al., 2003;Harborth J et al., 2003). Ulemper: Introduktion af sirna med det simple 21 basepar dsrna forårsager kun transient knockdown af target gener, med mindre sirna bliver klonet ind i et plasmid eller en viral vektor, hvilket er en mere kompliceret procedure (Harborth J et al., 2003). Det er ligeledes en ulempe at transfektionsreagenter kan virke toksiske på cellerne, samt at sirna er dyrt og kræver en del optimering Kontrol for sirna forsøg SiRNA medierede RNAi forsøg, skal inkludere kontrol sirna, der ikke har sekvens specifikke effekter. Ændringer i mrna eller protein niveau i celler der er behandlet med kontrol sirna, skulle gerne reflektere et ikke-specifikt cellulært respons, hvortil sirna kan sammenlignes. Kontrol sirna er designet således at de har et sammenligneligt GC-indhold (i dette speciale er der benyttet et GC-indhold på 47 %), i forhold til sirna man benytter i forsøget, men de mangler homologi med den kendte target sekvens. I dette speciale er der også benyttet H 2 O som en ekstra kontrol Praktisk udførelse af sirna forsøg Celler splittes efter normal procedure. Til sirna forsøg sættes cellerne op, således at de er ca. 30 % konfluente, 3 dage før forsøgsstart (72 timer). De 3 dage er valgt ud fra kontrolforsøg udført af Stine Falsig Pedersen, hvor cellers tæthed, samt sirna optag og funktion er undersøgt til forskellige tider. Samme eftermiddag som cellerne er blevet splittet, transfekteres de efter følgende protokol: En time før transfektion suges mediet fra cellerne og der tilsættes RPMI-1640 med 12.5 % eller 20 % serum. I en bakke eller lign. med minimum 3 rum blandes følgende: I første rum blandes Lipofektamine 2000 og RPMI-1640 medie (uden serum og pen/strep). I næste rum blandes sirna (til en slut konc. På 100 nm) og RPMI-1640 medie (uden serum og pen/strep). I tredje rum blandes kontrol sirna (med 66
67 sammenligneligt GC indhold, 47 %) (til en slut koncentration på 100 nm) og RPMI-1640 medie (uden serum og pen/strep). Lipofektamin blandingen fordeles i rum 2 og 3 og henstår i min ved stuetemperatur. Herefter tilføres X antal ul RPMI-1640 medie (uden serum og pen/strep) til hvert rum. Dette overføres til petriskålene eller bakkerne, (sirna og Ctrl sirna). Transfektionsmikset skal stå i 72 timer, hvorefter cellerne er klar til forsøg. Oversigt over sirna transfektionsforsøgsopsætninger. Petriskåle 4 brøndsbakker 6 brøndsbakker 96 brøndsbakker Tilført medie eller ul medie % 2400 ul medie + 12,5% 1600 ul medie + 20% 50 ul medie + 20 % serum % serum serum serum serum Lipofektamine + medie (-/-) 30 ul ul 7.5 ul ul 5 ul + 94 ul 0.25 ul ul Ezrin sirna + medie (-/-) 60 ul ul 15 ul ul 10 ul ul 0.5 ul ul Kontrol sirna + medie (-/-) 120 ul ul 30 ul ul 20 ul ul 1 ul ul Tilført medie (-/-) til hhv ul 300 ul 200 ul 25 ul ezrin og kontrol sirna Overføres til hver brønd 2400 ul 600 ul 400 ul 25 ul 3.12 MTT viabilitets-assay Mange biologiske assays kræver et mål for overlevelse og/eller proliferation. Dette kan opnås gennem flere metoder, f.eks. ved at tælle celler der indeholder en fluorescerende probe, eller ved måling af indbygning af radioaktive nucleotider under celle proliferering (Mosmann T., 1983). MTT assay et er blevet udviklet som et kvantitativt colorimetrisk assay for mammale cellers overlevelse og proliferering. Ideelt set skal et colorimetrisk assay for levende celler have et farveløst substrat, der bliver modificeret til et farverigt produkt i levende celler, men ikke i døde celler. Tetrazolium salte er en stor gruppe af heterocykliske organiske stoffer der danner farvet og ofte uopløselig formazan efter reduktion. MTT er et monotetrazolium salt, hvis reduktion er en af de mest brugte metoder til måling af celle proliferering og cytotoxitet (Mosmann T., 1983). 3-(4,5-Dimethylthiazolyl-2)-2,5-diphenyltetrazolium bromide (MTT) er en gul, vandopløselig tatrazolium probe, der kan krydse både plasma- og mitochondriemembran. I mitochondrierne i levende og glycolytisk aktive celler, bliver MTT reduceret vha. NADH- eller NADPH-afhængige dehydrogenaser til et blåt, hydrofobt produkt, formazan (Burton JD., 2005). Tetrazolium bliver kløvet i aktive mitochondrier og derved forgår reaktionen kun i levende celler (Mosmann T., 1983). Mængden af formazan produkt der resulterer fra denne reaktion er afhængig af antallet af celler og af deres glycolytiske aktivitet, hvilket ses af nedenstående figur (Burton JD., 2005;Mosmann T., 1983). 67
68 Figur 40. OD signal som funktion af antallet af celler. Det ses at OD værdien stiger, des større celle antallet er/ brønd (hvis MTT slutkonc. holdes på 1 mg/ml) (figur fra (Hansen MB et al., 1989). Tilsætning af en solubiliseringsbuffer bevirker, at celler lyseres, og den intracellulære formazan frigives og opløses. Det opløste formazan, der er frigivet fra de levende glycolytisk aktive celler, kan måles spektrofotometrisk (Burton JD., 2005;Hansen MB et al., 1989;Mosmann T., 1983). Fordelen ved denne metode frem for de førnævnte er at den er hurtig og præcis. Det er hurtigt at processere prøver og substrat og komponenter af medie interferer ikke med målinger af produkt. Dette tillader at assayet kan læses uden fjernelse af medie/ringer eller vaske trin, hvilket øger hastigheden af assayet og hjælper til at minimere variabiliteter mellem prøver (Burton JD., 2005;Mosmann T., 1983). Ulemper ved dette assay er, at det giver et indirekte mål for cellers viabilitet, idet det ikke kan skelne mellem celler der har undergået apoptose, frem for celler der er under nekrose. Ligeledes kan assayet heller ikke skelne, om celler har nedsat proliferering, eller om der er øget celledød Praktisk udførelse af MTT forsøg ELA cellers dødelighed ved tilstedeværelse af MAPK hæmmere ELA celler dyrkes i 96 brøndsbakker med 1640-RPMI medie, således at der ved forsøgsstart er ca celler/brønd indeholdende 200 μl medie (ca. 80% konfluens). På forsøgsdagen suges mediet fra alle brøndene og der stimuleres i 1 time med 200 µl isotont medie + 10 mm hæmmer (PD 98059, SB203580, SP600120, EIPA eller Wortmannin), (Kontrol samt baggrundsprøverne skal dog ikke have tilført hæmmer). Herefter fjernes mediet igen og der stimuleres med 200 µl hypertont (eller isotont) medie +/- hæmmer (10 mm). Stimuleringen afsluttes til tiderne 3 t, 6 t, 12 t, 24 t og 48 t. 68
69 ELA cellers dødelighed ved tilstedeværelse af ezrin sirna, samt kontrol sirna Cellerne transfekteres som tidligere nævnt, se afsnit På forsøgsdagen fjernes mediet og der tilføres 200 µl isotont medie. Efter 1 time skiftes der til hypertont medie, 200 µl til hver brønd i de hypertone 96 brøndsbakker. Dette henstår i 24 og 48 timer. Efter hver tidssituation, fjernes 100 ul medie fra hver brønd og der tilføres 25 µl MTT (3,(4,5-dimethylthiazol-2 yl)2,5-diphenyl-tetrazolium bromide) (50 mg opløst i 10 ml PBS). Efter 2 timer lyseres cellerne med 100 µl solubiliseringsvæske (10% SDS i 0.01 M HCl), hvorefter bakken rystes godt. De 2 timers inkuberingstid er valgt ifølge (Hansen MB et al., 1989), se nedenstående figur. Figur 41. OD signal som funktion af inkubationstid med MTT, (Δ) 5000 celler/brønd, ( ) celler/brønd, ( ) celler/brønd og ( ) celler/brønd. ( ) medie og MTT alene. 5 mg/ml MTT blev tilført hver brønd og der blev inkuberet i 0.5, 1, 2 og 4 timer ved 37 grader. Ud fra figuren ses det, at efter 2 timer OD signalet er mættet, med undtagelse ved 5000 celler og derfor er der i mit speciale valgt en ikuberingstid på 2 timers med solubiliseringsvæske (figur fra (Hansen MB et al., 1989). Bakken pakkes ind i parafilm, samt sølvpapir og står mellem 4 og 18 timer ved stuetemperatur. Derefter aflæses absorbansen på en Fluorestar optima pladelæser ved 592 nm (bakken rystes inden aflæsning). Absorbans-gennemsnittet beregnes og baggrundsabsorbansen trækkes fra. Levedyg-tigheden af celler bestemmes ud fra flg. formel: Viabilitet = (Abs. Prøve/ Abs. Baggrund) *
70 3.13 Rho aktiverings assay Teori Rho familien af små GTPaser består af ca. 20 medlemmer, hvoraf de bedst karakteriserede er Rac-1, RhoA og Cdc42. Rho proteiner virker, ligesom alle andre G-proteiner, som molekylære switches. De er inaktive i deres GDP bundne form og aktive i deres GTP bundne form. Familien af små GTPaser har flere funktioner i celler, bl.a. medierer de cytoskeletorganisering og de er medvirkende under apoptose. Det er derfor vigtig at forstå de mekanismer der regulerer aktivering/inaktivering af GTPaser (William T.Arthur et al., 2000). Aktiviteten af Rho GTPaser er målt vha. en metode hvor man følger aktiviteten af Rho GTPaser, baseret på det faktum, at kun aktiv GTP loadede proteiner reagerer med deres effektorer (Di Ciano et al., 2002). Man kan derfor fiske med gluthathione-s-transferase fusions proteiner, der indeholder sekvenser der specifikt interagerer med den aktive form af GTPaser og som er bundet til små kugler, der kan centrifugeres ud af opløsningen. Rho aktiverings-assayet bruger Rho Binding Domænet (RBD) af Rho effektor proteinet Rhotekin. RBD protein motifetet binder specifikt til den GTP bundne form af Rho. At RBD regionen af Rhotekin har en høj affinitet for GTP-Rho, gør den til et ideelt værktøj til affinitets oprensning af GTP-Rho fra celle-lysater. Rhotekin-RBD proteinet fra kittet indeholder aminosyrerne 7-89 af mus Rhotekin-RBD, der er ekspresseret som GST fusion i E-Coli bundet til glutathione-agarose. Dette gør at man kan udføre en såkaldt Pull down af Rhotekin-RBD/GTP-Rho komplexet med glutathione affinitets beads. Assayet er derfor meget anvendeligt til1 at måle Rho aktivitet. Mængden af aktiveret Rho bliver bestemt ved hjælp af Western blot, ved brug af et Rho specifikt antistof (Di Ciano et al., 2002),(protokol fra cytoskeleton) Praktisk udførelse af Rho aktiverings assay X antal Petriskåle sættes op til forsøg. Før stimulering skal der optøes det krævede antal Rhotekin-RBD beads, samt protease inhibitor cocktail og alle buffere og reagenter skal være klar. Mediet suges fra og der tilsættes 2-5 ml tempereret PBS for at fjerne serum protein. PBS en suges fra og der tilsættes 5 ml isoton, eller hyperton 2x Ringer. Efter inkubering ved de forskellige tidsintervaler, høstes cellerne ved at Ringeren suges fra og der tilsættes 2-5 ml tempereret PBS. PBS en suges fra og der tilsættes 500 µl 1x iskold lysisbuffer til hver Petriskål. Cellerne skrabes af og overføres til et Eppendorfrør. Cellerne centrifugeres ( xg, 4 C, 5 min) og 500 µl af supernantanten overføres til et Eppendorfrør der indeholder 20 µl aliquot (15 µg) Rhotekin-RBD beads. Der tilføres 5 ul Protease inhibitor og dette 70
71 inkuber i 1 time ved 4 C på en rotater. Den resterende mængde supernantant gemmes (total Rho), således at det vha. proteinbestemmelse kan bestemmes, at der bliver loaded lige meget protein i hver bane, under den senere elektroforese. Eppendorfrøret med Rhotekin-RBD beads centrifugeres ved x g, 4 C, 3 min, hvorefter 90 % af supernantanten fjernes. Den resterende pellet med indeholdende beads vaskes i 500 µl 1xlysisbuffer. Hvorefter der centrifugeres igen ved x g, 4 C, 3 min. 90 % af supernantanten fjernes og pellet vaskes med 500 µl vaskebuffer. Der centrifugeres igen ved xg, 4 C, 3 min, hvorved Rhotekin-RBD beads fældes. Supernantanten fjernes og pellet resuspenderes i 10 µl Laemmli buffer. Prøven er nu klar til at blive kørt på en gel SDS PAGE og Western Blot analyse Protein mængden bestemmes som beskrevet i afsnit og det udregnes hvor meget protein der skal loades (20 ug giver fine bånd). Hver gel skal også have loaded 5 nm His-tagged Rho (5 ul) og 10 nm His-tagged Rho (10 ul). Der skal bruges 12 % Nupage geler, med MES som runningbuffer. Gelen skal køre i 1.35 timer ved 140 V. Rho har en molekylær vægt på ca. 21 kda, mens His-tagged Rho vejer ca. 24 kda. Membranen vaskes kort i TBST og blokkeres herefter i 45 min med 5 % non-fat mælk i TBST ved stuetemperatur. Herefter inkuberes membranen med anti-rho (1:500 fortynding i TBST) i 1.5 timer ved stuetemperatur, eller O/N ved 4C på rystebord. Membranen vaskes 3x10 min i TBST og der inkuberes herefter med sekundært antistof (GAM) 1:500 fortynding i TBST. Membranen vaskes 6 x10 min i TBST. Tilsidst vaskes blottet i 5 min i TBS. Blottet fremkaldes herefter med BCIP/NBT og båndene bliver kvantificeret vha. Unscan-it-program F-aktin kvantificering Teori Aktin cytoskelettet er involveret i regulering af mange ion transportveje og flere beviser peger på at det har vigtige funktioner i regulering af cellevolumen. Vi har forsøgt at klarlægge F-aktins rolle i cellevolumen regulering i ELA celler, ved brug af et kvantitativt rhodamin-phalloidin assay. Idet rhodamin phalloidin mærker F-aktin, kan der ved at måle rhodamins fluorescens opnås et mål for F-aktin mængde i prøven. Rhodamin fluorescens måles ved 576 nm efter ekscitation ved 540 nm, ved hjælp af en PTI-ratiomaster (Pedersen et al., 1999). 71
72 Praktisk udførelse af F-aktin kvantificering 3 dage før forsøgsstart sås celler ud i 6 brøndsbakker, således at de har en konfluens på ca %. Samme eftermiddag transfekteres cellerne med 20 µm ezrin sirna eller med kontrol sirna. Efter 3 dage vaskes cellerne to gange med isoton Ringer og der tilsættes derefter igen isoton Ringer, som efterlades på cellerne i 20 min, for at stabilisere cellerne. Den isotone Ringer udskiftes med isoton, eller hyperton Ringer, som efterlades i 1 eller 5 min. Stimuleringen stoppes ved at tilføre 200 ul paraformaldehyd til en slutkoncentration på 2 %. Cellerne henstår i 15 min ved stuetemperatur og derefter 30 min på is, hvorefter de vaskes 3*5 min med TBS. Cellerne permeabiliseres ved tilsætning ad saponin buffer (10 mm MOPS, 5 mm EGTA, 20 mm K 2 HPO 4, og 2 mm MgSO % saponin), i 10 min. Til hver brønd tilsættes 250 ul rhodamin phalloidin opløsning (0.33 um) og bakkerne inkuberes i en 1 time på rystebord (mild rystning), dækket med parafilm og sølvpapir, hvorefter der vaskes 2 gange i MOPS buffer (10 mm MOPS, 5 mm EGTA, 20 mm K 2 HPO 4, og 2 mm MgSO 4 ). 2.5 ml methanol tilsættes og det inkuberer i 30 min på rystebord (mild rystning), dækket med parafilm og sølvpapir. Methanolen ekstraherer rhodamin-phallodin. Ekstraktet overføres til en kuvette og dækkes med parafilm. På PTI-ratiomaster måles der ved 540 ex. og ved 576 em. Som baggrundskontrol benyttes en ren metanol kontrol Statestik Der er i dette speciale benyttet Students T-test (parret T-test) for at undersøge om der er signifikant forskel, mellem prøver og kontrol situationer. T-test er udregnet ved at bruge Sigmaplot P værdier < 0.05 er betragtet som statistisk signifikante. Alle gennemsnit er beregnet ud fra uafhængige forsøg og er derfor angivet med S.E.M. error bars. Der er benyttet en Outliers test, til at undersøge om der er statistisk belæg for, at udelukke en skæv værdi, selv om der ikke har været noget galt i forsøgsproceduren. Outlier test er baseret på DixonsQ og er udregnet vha. følgende formel; (Skæve værdi nærmeste værdi)/(højeste Laveste værdi). Hvis den udregnede værdi er større end tabelværdien, ved et givent n, kan værdien forkastes. Tabelværdier fremgår af tabel 1. 72
73 n Tabelværdi Tabel 1. Outlier værdier. Hvis den udregnede værdi er større end tabelværdien, ved et givent n, kan værdien 73
74 4 Resultater Resultat afsnittet er delt op i underafsnit, der omhandler; 1) NHE1 proteiner 2) ERM proteiner og effekten af osmotisk skrumpning, samt deres mulige effektorer, 3) mekanismerne bag den skrumpningsinducerede aktivering af ERM proteiner, samt konsekvenser ved ERM protein aktivering og 4) samspillet mellem MAPK og NHE NHE1 aktiveres ved celleskrumpning NHE isoformer i ELA celler For at teste hvilke NHE isoformer, der findes udtrykt i ELA celler, har jeg udført PCR, efter isolering af total RNA fra cellerne. Figur 29 illustrerer NHE isoformerne NHE1 og NHE8s tilstedeværelse i ELA celler, men tilsyneladende ses ikke hverken NHE2, NHE3 eller NHE4 isoformerne kunne detekteres. Der er brugt specifikke forward og reverse primere, der genkender disse isoformer (se appendiks). Markør NHE1 K NHE2 K NHE3 K Markør Markør NHE4 K NHE8 K bp Figur 42. Ekspression af NHE isoformer i ELA celler. Total RNA fra ELA celler er isoleret og reverst transkriberet ved hjælp fra en random primer. RNA et amplificeredes ved brug af NHE specifikke primere og 15 µl prøve blev loaded på en 2 % agarose gel, tilsat ethidium bromid. Gelen er kørt ved 50 V i ca. en time, hvorefter DNA er visualiseret vha. UV belysning. Gelen fotograferes vha. computerprogrammet Doc- IT. Der er benyttet H 2 O som kontrolreaktioner. PCR analysen viser tilstedeværelse af isoformerne NHE1 og NHE8, men tilsyneladende ikke NHE2, NHE3 eller NHE4. Det viste forsøg er et repræsentativt for 4 uafhængige forsøg Effekt af skrumpning på NHE1 og dens rolle i volumen regulering NHE1 aktiveres som beskrevet i indledningen (se afsnit 2.8.1) af osmotisk skrumpning i mange celletyper og bidrager til cellernes volumen regulering, under hyperton skrumpning. Jeg har således undersøgt om NHE1 aktiveres af hyperton skrumpning i ELA celler og om den bidrager til volumen regulering. Intracellelulære ph målinger er udført vha. fluoroforen BCECF og ud fra en kendt 74
75 kalibreringskurve (se figur 24) er værdierne beregnet. Cellernes relative volumen er estimeret vha. LALS, som det er beskrevet i metodeafsnittet (se afsnit 3.7.1). Figur 30 A illustrerer at hypertont stress i ELA celler fører til intracellulær alkalinisering, som kan hæmmes ved tilstedeværelse af NHE1 hæmmeren EIPA (5 µm). Figur 30 B illustrerer den gennemsnitlige initielle rate af intracellulær ph ændring efter skift til hyperton ringer (målt over 90 sekunder efter tilsætning af hyperton ringer). Figur 30 C viser det relative cellevolumen (I o /I). Af figuren fremgår det, at celler der er behandlet med EIPA er dårligere til at volumenregulere efter udsætning for hyperton ringer. RVI er ikke fuldstændigt, men det kan ses at kontrolcellerne volumenregulerer efter hyperton stress. Figur 30 D illustrerer den gennemsnitlige stigning/fald i relativ cellevolumen pr. min. udregnet fra umiddelbart efter tilsætning af hyperton ringer og ca. 500 sekunder frem. A B Intracellulær ph H2O kontrol EIPA Initiel rate af intracellulær alkalinisering (-delta [H + ], i forhold til H 2 O kontrol) * Min. H2O EIPA C D delta (I o /I)/ min * H2O kontrol EIPA 75
76 Figur 43. Aktivering af NHE1 under celleskrumpning og volumen regulering. A. ELA-celler er først placeret i isoton Ringer og derefter, som pilen indikerer, blev der tilført hyperton Ringer (med 5 µm EIPA). Hyperton skrumpning bevirker at cellernes ph i stiger, hvilket ikke ses i de EIPA behandlede celler (5 µm EIPA). B. Gennemsnitlig initiel intracellulær alkalinisering/min ( H+/min), efter osmotisk skrumpning. Raten af skrumpnings-induceret intracellulær alkalinisering er signifikant højere i kontrolsituationen, sammenlignet med EIPA behandlede celler p = 3.95*10-6. C. Volumen regulering i ELA celler med og uden tilstedeværelse af EIPA (5 um). Volumen er estimeret vha. LALS og omregnet til relativ cellevolumen, som beskrevet i metodeafsnit (se afsnit 3.8.2). D. Gennemsnitlig ændring i relativ cellevolumen/min med og uden EIPA til stede. EIPA behandlede cellers relative cellevolumen er signifikant forskellig fra kontrollernes (P = 0.043). Data er repræsentativ for 4 (EIPA) og 5 (kontrol) forsøg. Gennemsnittet er angivet med S.E.M error bars, hvor * indikerer, at der er signifikant forskel fra kontrol, p < 0.05 er betragtet som signifikant. Det kan ud fra disse forsøg konkluderes, at NHE1 i høj grad aktiveres ved osmotisk skrumpning i ELA celler og at den er medvirkende under cellevolumen regulering, idet den intracellulære alkaliniseringsrate, samt cellers evne til at volumen regulere hæmmes af tilstedeværelse af EIPA. 4.2 ERM proteiner aktiveres ved celleskrumpning ERM proteiners tilstedeværelse i ELA celler For at teste om ERM proteiner og det relaterede protein merlin, findes udtrykt i ELA celler, har jeg udført PCR, efter isolering af total RNA fra cellerne. Figur 31 illustrerer ELA cellers ekspression af radixin, moesin, ezrin og merlin, idet sekvensen af disse proteiner genkendes af specifikke primere rettet mod hvert protein (se appendiks). Markør Radixin Moesin Ezrin Merlin Markør 600 bp 500 bp 400 bp 300 bp 200 bp 100 bp Figur 44. Ekspression af ERM og merlin proteiner i ELA celler. PCR analyse har vist tilstedeværelse af ezrin, radixin, moesin og det relaterede protein merlin i ELA celler. Total RNA er isoleret fra ELA celler og reverst transkriberet vha. en random primer, hvorefter RNA er blevet amplificeret ved brug af ezrin, radixin, moesin og merlin speciffik primere og 15 µl prøve er loadet på en 2 % agarose gel, tilsat ethidium bromid. Gelen er kørt ved 50 V i ca. en time, hvorefter den er fotograferet vha. computerprogrammet Doc-IT. Der er benyttet H 2 O som kontrolreaktioner, i stedet for RNA, hvilket ikke er vist i overstående figur. Data er repræsentativ for 4 uafhængige forsøg. 76
77 4.2.2 Lokalisering og skrumpnings-induceret translokation af ezrin i ELA celler Da det i vores laboratorium for nyligt blev fundet at ERM proteiner aktiveres ved celleskrumpning (Barbara Vasek Darborg et al., 2005), (Maria Rasmussen, 2006), har jeg ønsket at undersøge den skrumpnings-inducerede effekt på translokation af ezrin. Som det ses af figur 32, er ezrin mest lokaliseret cytosolisk under isotone forhold, mens de delvist translokerer mod den kortikale region under osmotisk skrumpning. F-aktin fluorescens i cellerne øges desuden ved de kortikale regioner under hyperton skrumpning. Ezrin F-aktin Mergede Isoton 5 min Hyperton 5 min Figur 45. Lokalisering af ezrin proteiner og F-aktin under hyperton skrumpning. ELA celler er dyrket på 22 mm glas coverslips, hvor de eksponeres til isoton Ringer (300 mosm, 10 min) eller til hyperton Ringer (600 mosm, i 5 minutter), hvorefter cellerne er blevet paraformaldehyd fikseret, permeabiliseret, blokeret mod uspecifik binding og mærket med primært antistof (monoclonalt ezrin antistof) og med rhodamin-conjugeret phallodin (2 U/ml) for at mærke F-aktin. Billede a og d illustrerer ezrin mærkning, c og e F-aktin mærkning (rhodamine-phalloidin), mens c og f er de mergede billeder af hhv. a/b og d/e. De øverste billeder viser de isotone omstændigheder, mens de nederste viser de hypertone omstændigheder. Fluorescensen blev analyseret vha. CLSM (40X/1.25 NA objektiv). De viste billeder er 1 µm optiske snit, der er taget ca. en tredjedel nede i cellen. Billederne er et repræsentativ for 3 uafhængige forsøg. 77
78 4.2.3 Co-lokalisering af fosforylerede ERM proteiner med F-aktin i kortex og i mikrovilli-lignende protrusioner Tilstedeværelse og lokalisering af fosforylerede ERM proteiner er undersøgt i ELA celler vha. immunocytokemi og CLSM. Af nedenstående figur fremgår det; 1) at der i ustimulerede celler (under isotone omstændigheder) findes kun en meget svag fosforylering af ERM proteiner, 2) at fosforylerede ERM proteiner primært findes i kortikale områder af cellerne og 3) efter hyperton celleskrumpning (1, 5 og 15 min) ses en kraftig øget fosforylering af ERM proteiner ved de kortikale områder nær plasmamembranen, især ses en kraftig ERM protein fosforylering i F-aktin indeholdende protrusioner, allerede efter 1 min og yderligere efter 5 min. p-erm F-aktin Merged Isoton 1 min hyp 5 min hyp 15 min hyp Figur 46. Co-lokalisering og fosforylering af ERM proteiner og F-aktin under osmotisk skrumpning. ELAceller er dyrket og behandlet, som beskrevet i figurtekst 32, bortset fra at der i dette forsøg er benyttet perm, som primært antistof. Fluorescens er målt vha. CLSM (100X/1.4 NA objektiv). Første søjle illustrerer perm, miderste søjle illustrerer F-aktin mærkning, mens sidste søjle viser de mergede billeder af hhv. perm og F-aktin. Grøn farve indikerer perm, rød farve F-aktin mærkning og Blå er kerne farvning. De fire rækker repræsenterer hhv. isotonicitet, 1, 5 og 15 minutters hyperton skrumpning. Billederne er et repræsentativ for 3 uafhængige forsøg. Disse resultater indikerer, at ERM proteiner fosforyleres hurtigt og translokeres til cellens periferi, især til lange, mikrovilli-lignende F-aktin-indeholdende protrusioner, de såkaldte mikrospikes, samt at de fosforylerede ERM proteiner co-lokaliserer sammen med F-aktin under hyperosmotisk skrumpning. 78
79 4.3 Rho aktiveres ved celleskrumpning Jeg har ønsket at undersøge aktivering og samspil mellem Rho og ERM proteiner i ELA celler under hyperton skrumpning, da tidligere studier har vist, at både Rho og ERM proteiner er vigtige i regulering af flere cellulære processer, som skrumpnings-induceret NHE1 aktivering og F-aktin organisering (Hall A., 1994;Pedersen et al., 2002). I dette afsnit beskrives Rho proteiners aktivering ved celleskrumpning. Rho aktivitet er målt under iso- og hypertone forhold, vha. et Rhotekin-baseret Rho-GTP pull down assay, (se afsnit 3.13). Af figur 34 ses det, at Rho aktiveres hurtigt og transient ved hypertont stress. Aktiveret rhoa Total rhoa Isoton 1 min hyp 5 min hyp 15 min hyp 30 min hyp Trombin Rho aktivering Bånd intensitet, relative til egen total rho * * p = iso 1 min hyp 5 min hyp 15 min hyp 30 min hyp Trombin Figur 47. Rho aktivering under hyperton skrumpning. Cellerne er først inkuberet 30 minutter i isoton ringer og derefter i isoton ringer (5 min), eller i hyperton ringer (1, 5, 15 eller 30 min). Cellelysaterne blev loaded på en 12 % bis-tris gel (MES som runningbuffer) med 25 ug pr. bane, efterfulgt af SDS-PAGE og Western blotting. Det primære antistof er et Rho specifikt antistof rettet mod RhoA (1:500). Det sekundære antistof er et alkalisk-fosfatase konjugeret ged anti-mus (1:600). Trombin er en aktivator af Rho proteiner under celleskrumpning og er benyttet som positiv kontrol for Rho proteiners aktivering. Øverst ses repræsentative blots fra Rho aktiveringsassayet. Den øverste viser aktiveret Rho, mens det nederste blot viser den totale mængde Rho i cellelysatet. Data er givet relativt til isoton kontrol, efter normalisering til egen total Rho. Data er gennemsnit for 5 uafhængige forsøg. Der er benyttet S.E.M. error bars, hvor * indikerer at der er signifikant forskel fra den isotone kontrol. P < 0.05 betragtes som signifikant. 79
80 4.4 NHE1s mulige roller i skrumpnings-induceret aktivering af ERM Denker og kollegaer (2000) tidligere har fundet, at ERM proteiner interagerer med NHE1 under hyperosmotisk skrumpning (Denker SP et al., 2000) og Wu et al. har yderligere postuleret, at ERM protein aktivering er nedstrøms for NHE1. Men da tidligere forsøg i vores laboratorium har vist, at ERM protein fosforylering er upåvirket af EIPA og derfor af NHE1 aktivitet (Barbara Vasek Darborg et al., 2005), (Maria Rasmussen, 2006), har jeg ønsket at undersøge om skrumpnings-induceret ERM protein fosforylering er afhængig af NHE1 tilstedeværelse. Jeg har undersøgt ERM protein fosforylering i AP1 celler, der mangler endogene NHE1 proteiner, i forhold til S5 celler der er transfekteret med human NHE1 og som vides at have en kraftigt NHE1 aktivering (McLean et al., 1999). Af nedenstående figur ses det, at der ikke er signifikant forskel i ERM protein fosforylering mellem de 2 celletyper, hvilket indikerer at NHE1s tilstedeværelse ikke er nødvendig for ERM protein fosforylering. S5 Celler AP1 Celler Iso 1min hyp 5 min hyp 15 min hyp 30 min hyp 45 min hyp ERM protein fosforylering Bånd intensitet, relativ til isoton kontrol AP1 celler S5 celler 5 min iso 1 min hyp * * 5 min hyp 15 min hyp 30 min hyp 45 min hyp Figur 48. Fosforylering af ERM proteiner sker uafhængigt af NHE1 tilstedeværelse. ELAcellerne er først inkuberet med isoton ringer i 30 minutter og derefter med isoton (5 minutter), eller med hyperton ringer (1, 5, 15, 30 eller 45 minutter). Cellelysaterne er loaded på en 10 % bis-tris gel med 25 ug protein pr. bane, efterfulgt af SDS-PAGE og Western blotting. Primært antistof rettet mod fosforyleret og total ezrin (Thr 567)/radixin (Thr 564)/ moesin (Thr 558) (1:1000). Sekundært antistof var et alkalisk-fosfatase konjugeret ged anti-kanin antistof (1:600). Øverst ses et repræsentativt Western blot af fosforyleringen af ERM proteiner i hhv. S5 og AP1 celler. AP1 cellers fosforylering af ERM proteiner er signifikant forskellig fra den isotone kontrol efter 15 minutters hyperton skrumpning, mens S5 cellernes fosforylering af ERM protein på intet tidspunkt er signifikant forskellig fra den isotone kontrol. Fosforyleringsgraden stiger dog i S5 cellerne. Data er gennemsnit for 7 uafhængige forsøg. Der er benyttet S.E.M error bars, hvor * indikerer at der er signifikant forskel fra den isotone kontrol. P < 0.05 betragtes som signifikant. * 80
81 4.5 Ezrins roller ved hyperosmotisk celleskrumpning Da ERM proteiner aktiveres meget hurtigt (>1 min), ønskede jeg at undersøge hvorvidt disse proteiner virker opstrøms for skrumpnings-inducerede effektor såsom, NHE1 aktivering, Rho aktivering og skrumpnings-induceret celledød Effekten af ezrin sirna knockdown Vha. short interfering RNA (sirna) kan man effektivt og specifikt hæmme ekspression af proteiner, som man ellers ikke har mulighed for specifikt at hæmme (se afsnit 3.11). For at kontrollere effekten af det anvendte ezrin sirna, er der kørt Western blots, med antistof rettet mod ezrin. Som det fremgår af figur XX, resulterer transfektion med ezrin sirna i % knock-down af ezrin i ELA-celler H 2 O Kontrol sirna ezrin sirna H 2 O Kontrol sirna ezrin sirna Ca. 80 kda A B total-ezrin, bånd intensitet, ezrin sirna i forhold til ikke-relateret sirna total-ezrin, bånd intensitet, ezrin sirna i forhold til ikke-relateret sirna brøndsbakke Petriskål * * kontrol sirna ezrin sirna 0.0 kontrol sirna ezrin sirna Figur 49. Knock down af ezrin. ELA-celler er dyrket i hhv. 6 brøndsbakker og i petriskåle, til cellerne er ca. 25 % konfluente, hvorved de transfekteres med hhv. kontrol sirna (20 µm) og ezrin sirna (20 µm). Cellerne henstod i 72 timer hvorefter de blev lyseret og høstet. De 72 timers er valgt ud fra tidligere forsøg udført af Stine Pedersen, der har vist at der til denne tid var den med optimal transfektions effektivitet. Cellelysaterne blev loaded på en 10 % bis-tris gel med 25 ug protein pr. bane, efterfulgt af SDS-PAGE og Western blotting. Proteinerne blev detekteret med ezrin antistof (1:1000), rettet mod ezrin (Thr 567). Det sekundære antistof er en alkalisk-fosfatase konjugeret ged anti-kanin antistof (1:600). Ezrin aktivering er signifikant lavere i celler der er behandlet med sirna mod ezrin, P = og 0.03 i hhv. 6 brøndsbakker og i Petriskåle. Ezrin knockdown i ELA celler vha. sirna forårsagede et ca. 69 % fald i ezrin protein niveau i 6 brøndsbakker a) og et fald på ca. 80 % i petriskåle b), i forhold til ikke relateret sirna. ELA celler er blevet transfekteret med ezrin sirna (100 nm), ikke-relateret sirna (100 nm) eller med H 2 O, vha. Lipofektamine Data er et gennemsnit for 3 uafhængige forsøg. Der er benyttet S.E.M. error bars, hvor * indikerer at der er signifikant forskel fra kontrol sirna. P < 0.05 betragtes som signifikant. 81
82 4.5.2 Effekten af ezrin sirna knockdown på NHE1 protein niveau For at kontrollere effekten af det anvendte ezrin sirna på NHE1 protein niveau, er der kørt Western blots, med antistof rettet mod NHE1. Som det fremgår af figur 37, resulterer transfektion med ezrin sirna ikke i ændringer i NHE1 på protein niveau. NHE1 protien niveau, efter ezrin sirna behandling (relativ til kontrol sirna) Kontrol sirna Ezrin sirna Figur 50. Knock down af ezrins betydning for NHE protein niveau i ELA celler. ELAceller er dyrket i petriskåle og ved ca. 25 % konfluens er de transfekteret med ezrin sirna eller kontrol sirna (20 µm). Cellerne henstod i 72 timer hvorefter de blev lyseret og høstet. Cellelysaterne blev loaded på en 10 % bis-tris gel med 25 ug protein pr. bane, efterfulgt af SDS-PAGE og Western blotting. Proteinerne blev detekteret med NHE1 antistof. Det sekundære antistof er en alkalisk-fosfatase konjugeret ged anti-mus antistof. Øverst ses et repræsentativt blot. Der observeres ingen signifikant forskel i NHE1 protein niveau ved ezrin sirna behandling, i forhold til kontrol situationen. Data er et gennemsnit for 2 uafhængige forsøg. Der er benyttet S.E.M. error bars Ezrins effekt på skrumpnings-induceret NHE1 aktivering For at undersøge om ezrin findes opstrøms for skrumpnings-induceret NHE1 aktivering, udførte jeg knock-down af ezrin vha. sirna og undersøgte derefter ELA cellernes skrumpnings-induceret NHE1 aktivering og deres evne til at volumenregulere, vha. BCECF-AM og LALS, som beskrevet i afsnit 3.7 og 3.8. Figur 38 A. Illustrerer at ezrin knock-down fører til øget intracellulær alkalinisering, efter skift til hyperton ringer. Figur 38 B. sirna medieret knock-down af ezrin i ELA celler, resulterer i en ca. 25 % stigning i raten af skrumpnings-induceret intracellulær alkalinisering, sammelignet med celler, der er transfekteret med kontrol sirna. Figur..38 C og D. Det fremgår at celler der er transfekteret med ezrin 82
83 sirna er en smule dårligere til at volumenregulere, efter udsætning for hyperton ringer. Dette er dog ikke statistisk signifikant. A B 8.0 Intracellulær ph Kontrol sirna Ezrin sirna Tid i minutter Initiel rate af intracellulær alkalinisering (-delta H + /min, ezrin sirna i forhold til ikke relateret sirna) Kontrol sirna * ezrin sirna C D Relativ cellevolume (I o /I) Kontrol sirna Ezrin sirna delta (i o /I)/ min Min Kontrol sirna P = 0.13 ezrin sirna Figur 51. Ezrins effekt på NHE1 aktivitet og volumenregulering. ELA celler er dyrket på rektangulære glas coverslips og transfekteret med ezrin sirna eller med kontrol sirna, med sammenligneligt GC-indhold, som beskrevet i metodeafsnit timer efter transfektion blev cellerne brugt til måling af ph i og cellevolumen vha. BCECF-AM og LALS, som beskrevet i afsnit 3.8. A og B. Et repræsentativt tidsforløb for ændringer i ph i og dh + /dt for hhv. ezrin sirna og kontrol sirna behandlede celler. Som det ses medfører hyperton skrumpning, at ELA celler der er transfekteret med ezrin sirna har en højere initiel stigning i intracellulær ph efter skift til hyperton ringer, i forhold til celler der er transfekteret med kontrol sirna. NHE1 aktivitet er estimeret som den initielle ΔH + /min efter osmotisk skrumpning. Raten af skrumpnings induceret intracellulær alkalinisering er signifikant højere i celler der er behandlet med ezrin sirna, i forhold til celler der er behandlet med kontrol sirna. Data er i figur B er normaliseret i forhold til kontrol sirna. C og D. Repræsentativt tidsforløb for relativ cellevolumen (I o /I) og for delta(i o /I)/dt for celler behandlet med hhv. ezrin sirna og kontrol sirna. De gennemsnitlige stigninger i relativ cellevolumen/min er beregnet for hhv. ezrin sirna og kontrol sirna behandlede celler, i ca. 500 sekunder efter tilsætning af hyperton ringer. Ezrin sirna behandlede volumen regulerer numerisk ikke lige så godt som kontrolsituationen, men der er ikke signifikant forskel. Data her er repræsentativ for ezrin sirna og 9 kontrol sirna forsøg. Der er benyttet S.E.M. error bars, hvor * indikerer at der er signifikant forskel fra kontrol sirna. P < 0.05 betragtes som signifikant. 83
84 Disse data indikerer, at ezrin har en negativ regulerende effekt på skrumpnings-induceret aktivering af NHE Ezrins rolle i skrumpnings-induceret Rho aktivering Tidligere studier har fundet, at der er et kompleks forhold mellem Rho og ezrin; Rho er en vigtig regulator af ERM protein aktivering (Hirao et al., 1996), (Hall A., 1994;Takahashi K et al., 1998), men ERM protein aktivering kan ligeledes være opstrøms for Rho aktivering (Bretscher et al., 1997), (Mackay et al., 1997). Jeg har vha. sirna medieret knock-down af ezrin, testet ezrins rolle i Rho aktivering, efter celleskrumpning. Som det er illustreret i figur 39, reducerer sirna-medieret ezrin knockdown, den skrumpnings-inducerede aktivering af Rho med ca. 50 % og hæmmer basal Rho aktivering, hvilket tyder på, at ezrin vigtig i aktivering af RhoA proteiner i ELA-celler. Isoton kontrol ezrin Hyperton kontrol ezrin Trombin sirna sirna sirna sirna Aktiveret RhoA Total RhoA RhoA aktivitet bånd intensitet, relativ til egen total rho 4 Isoton 5 min Hyperton 1 min * * ** # * * 0 Kontrol kontrol sirna ezrin sirna Trombin Figur 52. Ezrin knock-downs effekt på Rho aktivering. ELA celler er dyrket i petriskåle og ved 25 % konfluens transfekteret med ezrin sirna eller med kontrol sirna, med sammenligneligt GC-indhold, som beskrevet i metodeafsnit timer efter transfektion blev Rho aktivitet målt vha. vha. et Rhotekin-baseret Rho-GTP pull down assay, (se afsnit 3.13). Cellerne er først inkuberet 30 minutter i isoton Ringer og derefter i isoton eller i hyperton Ringer i 5 min. Cellelysaterne blev loaded på en 12 % bis-tris gel (MES som runningbuffer) med 25 ug pr. bane, efterfulgt af SDS-PAGE og Western blotting. Det primære antistof er et Rho specifikt antistof rettet mod RhoA (1:500). Det sekundære antistof er et alkalisk-fosfatase konjugeret ged anti-mus (1:600). Trombin er en aktivator af Rho proteiner under celleskrumpning og er benyttet som positiv kontrol for Rho proteiners aktivering. Øverst ses repræsentative blots fra Rho aktiveringsassayet. Den øverste viser aktiveret Rho, mens det nederste blot viser den totale mængde Rho i cellelysatet. Rho aktivitet er signifikant højere ved hyperton skrumpning for både kontrol, kontrol sirna og ezrin sirna, i forhold til den isotone kontrol (markeret med *). Yderligere ses det, at ved hyperton skrumpning er ezrin sirna transfekterede cellers aktivering af Rho signifikant lavere end kontrol sirnaet s aktivering af RhoA (markeret med #). Isoton ezrin sirna er signifikant lavere end H 2 O kontrollen (markeret med **). Data er givet relativt til isoton kontrol, efter normalisering til egen total Rho. Data er gennemsnit af 3-13 uafhængige forsøg. Der er benyttet S.E.M error bars, hvor * indikerer at der er signifikant forskel fra den isotone kontrol. P < 0.05 betragtes som signifikant. 84
85 Disse resultater tyder på, at ezrin knock-down, reducerer Rho aktivitet med ca. 50 % og derved kan det konkluderes at ERM protein aktivering er vigtig i både basal og efter skrumpnings-induceret aktivering af RhoA proteiner i ELA-celler Ezrins rolle i regulering af F-aktin indhold og organisering under celleskrumpning i ELA-celler I de fleste celletyper der er studeret, er osmotisk skrumpning associeret med en reorganisering af det aktin-baserede cytoskelet (Pedersen SF et al., 2001) og i mange tilfælde ses en netto stigning i cellulært F-aktin indhold (Pedersen et al., 1999). Da ezrin associerer med F-aktin og derved er en vigtig modulator af F-aktin organisering (Mackay et al., 1997), har jeg ønsket at teste, om ezrin indflydelse på F-aktin mængde og re-organisering i ELA celler, under hyperton skrumpning. F-aktin indhold blev målt vha. et Rhodamin-Phalloidin ekstraktionsassay (se metodeafsnit 3.14). Som det ses af figur 40 er der ingen signifikant forskel i F-aktin indhold i celler, der er behandlet med hhv. kontrol og ezrin sirna, hvilket indikerer at ezrin ikke har en direkte funktion i regulering af cellens netto F-aktin indhold, under osmotisk skrumpning i ELA celler. A B F-aktin indhold, relativ til isoton kontrol (5 min iso/hypertonicitet) Isoton Hyperton F-aktin, relativ til egen isotone kontrol (5 min iso/hypertonicitet) H2O Kontrol Kontrol sirna Ezrin sirna 0 H2O kontrol Kontrol sirna Ezrin sirna Figur 53. Effekten af hyperton skrumpning på cellulært indhold af F-aktin. 3 dage før forsøgsstart er ELA celler transfekteret med sirna. På forsøgsdagen er cellerne først vasket to gange i isoton ringer (300mOsm) og derefter inkuberet med isoton ringer i ca. 20 minutter. Til tiden 0 er cellerne stimuleret med hhv. isoton (300 mosm) eller hyperton ringer (600 mosm) i 5 minutter. Cellerne blev fikseret med paraformaldehyd og mærket med Rhodamine Phalloidin. Rhodamine Phalloidin, udsender fluorescens der måles spektrofotometrisk. A. Viser F-aktin mængden relativt til den isotone kontrol uden sirna, mens B viser F-aktin mængden relativt til hver situations respektive isotone kontrol. Der ses ingen signifikant forskel i F-aktin mængden, mellem isoton og hyperton behandling. Data er gennemsnit af seks uafhængige forsøg. Der er benyttet S.E.M error bars, hvor * indikerer at der er signifikant forskel fra den isotone kontrol. P < 0.05 betragtes som signifikant. 85
86 F-aktin organisering i ELA-celler blev undersøgt vha. mærkning af cellernes F-aktin og confokal laser scannings mikroskopi. Af figur 41 fremgår det, at den kortikale F-aktins fluorescens øges under osmotisk skrumpning. Ezrin er blevet knocked ned vha. sirna. Isoton Hyperton Figur 54. Ezrins rolle i reorganisering af F-aktin under hyperosmotisk skrumpning. 72 timer efter transfektion med kontrol sirna, ezrin sirna, eller Kontrol ddh 2 O eksponeres ELA celler til isoton eller hyperton ringer i 5 min, hvorefter de paraformaldehyd fikseret og mærket med rhodamin phalloidin og antistof rettet mod perm, som beskrevet i metodeafsnit Cellerne blev visualiseret vha. CLSM (100X/1.4 NA objektiv). Kontrol Første kolonne illustrer de isoton behandling, mens sirna anden kolonne illustrerer hyperton behandling. Billede a og b illustrerer kontrol situationen, billede c og d, kontrol sirna behandlede celler, mens billede e og f illustrerer ezrin sirna behandlede celler. Ved ezrin sirna behandling ser det ud til at den skrumpnings-inducerede dannelse af F-aktin protrusioner hæmmet. Men selvom netto perm fluorescens er reduceret, ses der stadig F-aktin Ezrin protrusioner der indeholder perm (f). De viste data sirna er et repræsentativ for fire forsøg. Ezrin sirna behandlede cellers skrumpnings-inducerede dannelse af membrane/f-aktin protrusioner er hæmmet, hvilket indikerer at ezrin proteiner har en vigtig funktion i F-aktin re-organisering ved osmotisk skrumpning. Da der stadig ses fosforyleret ERM proteiner i F-aktin indeholdende protrusioner, skyldes sandsynligvis at ezrin sirna kun er ca. 70 % effektiv og/eller at de to andre ERM proteiner, radixin og moesin ligeledes er involveret i dannelse af F-aktin-lignende strukturer. 86
87 4.6 Roller for NHE1, ezrin og PI3-kinasen i skrumpningsinduceret celledød Det er i tidligere studier fundet, at NHE1 aktivering via osmotisk skrumpning, rekrutterer og fosforylerer ezrin, hvilket resulterer i aktivering af PI3K og derigennem Akt overlevelses vejen (Wu et al., 2004). Jeg fandt, at ERM protein aktivering sker uafhængigt af NHE1, er det i umiddelbart modstrid med disse resultater og derfor har jeg forsøgt at klarlægge nogle aspekter af denne overlevelsesvej. Vha. MTTassays har jeg undersøgt hvorledes; 1) osmotisk skrumpning og hæmning af NHE1 og 2) knock-down af ezrin, samt hæmning af PI3-kinasen påvirker cellernes evne til at overleve. Jeg har således undersøgt den generelle celledødelighed under osmotisk skrumpning over 48 timer, samt hvilken rolle NHE1 har i cellernes overlevelse under denne skrumpning. Af figur 42 fremgår det, at hæmning af NHE1 forværrer det skrumpnings-inducerede tab af viabilitet. % celledød, relativ til isoton kontrol Isoton kontrol Hyperton kontrol Isoton + EIPA Hyperton + EIPA * * # * * # * timer 6 timer 12 timer 24 timer 48 timer Figur 55. Effekten af osmotisk skrumpning på ELA cellers viabilitet i nærvær og fravær af EIPA. Celleviabilitet er estimeret vha. MTT assay (se metodeafsnit ) celler/brønd er sat op dagen før forsøgsstart i 96 brøndsbakker og på forsøgsdagen er de inkuberet én time med 200 µl isotont medie (300 mosm) og derefter med 200 µl hyperton medie (600 mosm) (lavet ud fra en 3 M NaCl opløsning), hvorefter prøver er udtaget til de indikerede tider. Til forsøgets afslutningstider tilsættes 25 µl MTT og efter 2 timer er der tilsat solubiliseringsbuffer. Der inkuberes natten over, hvorefter cellernes viabilitet er bestemt vha. en fluorostar pladelæser. Til hver tidssituation er celledødeligheden undersøgt og dødeligheden ved hypertont medie tilstede, er taget relativ til den isotone kontrol til hver tidssituation. Celleskrumpning medfører en signifikant højere celledødelighed, som forstærkes ved hæmning af EIPA. Data er vist som gennemsnit af 4-6 uafhængige forsøg. hvor * indikerer at der er signifikant forskel fra den isotone kontrol og # indikerer at der er signifikant forskel mellem den hypertone kontrol og EIPA behandlede cellers viabilitet. P < 0.05 betragtes som signifikant 87
88 Med hensyn til MTT viabilitetsassay skal det fremhæves, at assayet ikke skelner mellem nedsat celleproliferering og øget celledød. Figur 43 illustrerer at knockdown af ezrin ikke påvirker cellernes viabilitet efter 24 og 48 timers hyperton skrumpning, mens figur d) viser at hæmning af PI3K fører til en signifikant højere celledød. A B Figur 56. Ezrin knock-down og hæmning af PI3Ks betydning for celle viabilitet. A. ELAceller dyrkes i 96 brøndsbakker, hvor de ved ca. 25 % konfluens transfekteres med hhv. kontrol eller ezrin sirna. Efter 72 timer startes forsøget. Data er taget i forhold til egen isoton kontrol. Der observeres ingen signifikant forskel mellem kontrol og ezrin sirnas celleviabilitet. B. Cellerne er dyrket som i de fornævnte forsøg, blot med tilstedeværelse af 10 µm wortmannin, der hæmmer PI3-kinasen. Der observeres ingen signifikant forskel mellem kontrol- og wortmannin behandlede celler. Data er vist som et gennemsnit af 4-6 uafhængige forsøg. Der er benyttet S.E.M. error bars. p < 0.05 betragtes som signifikant. Disse resultater indikerer at ELA cellers viabilitet er upåvirket af ezrin knock-down og af hæmning af PI3K, hvilket strider imod NHE1-ezrin-PI3K-Akt overlevelsesvejen, som tidligere er fundet (Wu et al., 2004). 88
89 4.7 Rho-ROCK vejens rolle i skrumpnings-induceret aktivering af NHE1 Tidligere studier har vist, at Rho-ROCK er vigtig for aktivering af NHE1 efter visse stimuli (Tominaga T et al., 1998). Jeg har derfor ønsket at teste Rho-ROCK vejens rolle i NHE1 aktivering og volumen regulering i ELA-celler, vha. Rho-kinase hæmmeren, Y Figur 44 A og B illustrerer at Y27632 behandlede- og kontrol cellers intracellulære alkalinisering er forholdsvis ens, hvilket indikerer at NHE1 ikke påvirkes af Rho-kinase hæmning. C og D. viser at celler der er behandlet med Y27632 ikke udviser forskellig volumenregulering i forhold til kontrol celler. A B 7.4 H 2 O kontrol Y27632 Intracellulær ph Min. Initiel rate of intracellulær alkalinisering (-delta [H + ] i /min, relativ til H 2 O kontrol) H2O Y27632 C D H 2 O kontrol Y Relativ cellevolume (I o /I) delta (I o /I)/ min Min H2O kontrol Y
90 Figur 57. Rho-ROCK vejens rolle i skrumpnings-induceret aktivering af NHE1. ELA celler er dyrket på rektangulære glas coverslips og på forsøgsdagen inkuberet med Rho-kinase hæmmeren, Y27632 (10 µm) i 15 min. som beskrevet i metodeafsnit 3.7.5, hvorefter cellerne blev brugt til måling af ph i og cellevolumen vha. BCECF-AM og LALS, som beskrevet i afsnit A og B. Et repræsentativt tidsforløb for ændringer i ph i og dh + /dt for hhv. kontrol og Y27632 behandlede celler. NHE1 aktivitet er estimeret som den initielle ΔH + /min efter osmotisk skrumpning. Pilen indikerer overgang fra isoton ringer til hyperton ringer. Raten af skrumpnings induceret intracellulær alkalinisering er ikke signifikant forskellig mellem Y27632 behandlede celler og kontrollen. C og D. Repræsentativt tidsforløb for relativ cellevolumen (I o /I) og for delta(i o /I)/dt for hhv. Y27632 behandledes ELA-celler og for kontrol situation. Der observeres ingen signifikant forskel i cellernes volumen regulerin mellem de to typer behandlingg. Data her er repræsentativ for 5 kontrol og 4 Y27632 uafhængige forsøg. Der er benyttet S.E.M. error Disse resultater indikerer at NHE1 aktivering, efter hyperton skrumpning ikke er afhængig af Rho-kinase aktivitet. 4.8 NHE1, MAPKs og celledød efter osmotisk skrumpning af ELA-celler phs betydning for basal aktivitet af MAPK (ERK, p38 og JNK) Data fra andre og fra vores eget laboratorium har vist, at MAPKs reguleres af celleskrumpning, således inaktiveres ERK1/2 i ELA-celler efter celleskrumpning, mens JNK1/2 og p38 MAPK aktiveres. Vi har desuden vist at NHE1 regulerer ERK1/2 og JNK1/ efter celleskrumpning (Pedersen SF., 2006). Tidligere studier har ligeledes vist, at lavere ph værdier aktiverer ERK1/2 i flere celletyper (rotte ventricular myocyteter og Cos-7 celler) (Haworth et al., 2003), derfor kunne det tænkes, at intracellulær alkalinisering via skrumpnings-induceret NHE1 aktivering kan være ansvarlig for ERK1/2 inaktivering og JNK og p38 MAPK aktivering. Jeg har derfor undersøgt hvorledes ph påvirker fosforylering af MAPkinaserne JNK, p38 og ERK. 90
91 A B ERK1 fosforylering (Relative data) ERK2 fosforylering (Relative data) ph 6.8 ph 7.4 ph ph 6.8 ph 7.4 ph 8.0 C D * JNK1 fosforylering (Relative data) JNK2 fosforylering (Relative data) * 5000 * ph 6.8 ph 7.4 ph ph 6.8 ph 7.4 ph 8.0 E p38 MAPK fosforylering (Relative data) * ph 6.8 ph 7.4 ph
92 Figur 58. phs betydning for fosforylering af MAPKs. ELA-cellerne er først inkuberet i isoton Ringer i 30 minutter og derefter inkuberet med isoton Ringer med ph værdierne 6.8, 7.4 og 8.0 i en time. Cellelysaterne blev loaded på en 10 % bis-tris gel med 25 ug protein pr. bane, efterfulgt af SDS-PAGE og Western blotting. De primære antistoffer der er brugt er p-erk, p-jnk og p-p38. Det sekundære antistof der er brugt er et alkaliskfosfatase konjugeret ged anti-kanin (1:600). A og B ERK42/44 fosforylering er upåvirket af ændringer i ph i. C og D. JNK1/2 aktiveres ved højere ph i værdier, set i forhold til aktiveringen ved neutral ph, 7.4. E. p38 aktivering er signifikant lavere ved ph 6.8, mens fosforyleringen ved 8.0 er højere, dog ikke signifikant (p = 0.21). Data er gennemsnit af 5 uafhængige forsøg. Der er benyttet S.E.M. error bars, hvor * indikerer at der er signifikant forskel fra ph 7.4. P < 0.05 betragtes som signifikant. Disse resultater indikerer, at ph i nogen grad påvirker fosforylering/aktivering af hhv. JNK og p38 MAPK, men tilsyneladende ikke i fosforyleringen af ERK1/2. Fosforyleringen af JNK og p38 MAPK stiger ved højere ph værdier, mens kun p38 MAPK fosforylering falder ved lavere ph værdier MEK1/2, MKK3/6 og NHE1s effekt i skrumpnings-induceret aktivering af ERK og p38 MAPK MEK1/2 og MKK3/6 er vigtige opstrøms regulatorer af ERK1/2 og p38 MAPK, derfor har jeg ønsket at undersøge, om osmotisk skrumpning og hæmning af NHE1, bevirker ændringer i MEK1/2 og MKK3/6 aktivitet. Det er tidligere vist at ERK1/2 aktivitet hæmmes, mens p38 aktiveres ved osmotisk skrumpning og at EIPA fuldstændigt kan hæmme denne skrumpningsinducerede disse effekter (Pedersen SF et al., 2007), Figur. 46 A illustrerer, at osmotisk skrumpning medfører en transient hæmning af MEK1/2 fosforylering, som til dels modvirkes af tilstedeværelse af EIPA (kun ved 5 min hypertonicitet). Figur 46 B illustrerer, at MKK3/6 fosforylering ikke ændres signifikant ved celleskrumpning og uafhængigt af NHE1 aktivering. 92
93 Iso iso min iso/hyp /- EIPA Iso iso p-mek1/2 Bånd intensitet, relativ til isoton kontrol EIPA + EIPA # # * p-mkk3/6 Bånd intensitet, relativ til isoton kontrol EIPA + EIPA * * * iso 5 hyp 15 hyp 30 hyp min Iso 5 min Hyp 15 min Hyp 30 min Hyp Figur 59. NHE1s effekt på skrumpnings-induceret aktivering af ERK og p38 MAPKs. ELA celler er dyrket i petriskåle, på forsøgsdagen blev cellerne først inkuberet med isoton Ringer i ca. 20 min og derefter i isoton/hyperton Ringer, hvorefter cellerne er høstes til de indikerede tider. Cellelysaterne er loaded på en 10 % bis-tris gel med 25 ug protein pr. bane, efterfulgt af SDS-PAGE og Western blotting. A. Fosforylering af MEK1/2 i fravær og nærvær af EIPA. Øverst ses en repræsentativ membran fra western blotting efter tilsætning af antistof rettet mod fosforyleret MEK1/2 (Ser 218/222 ). Nederst ses den gennemsnitlige relative fosforylering af MEK1/2, i forhold til isoton kontrol. Fosforyleringsgraden er vist som funktion af tiden i henholdsvis fravær og nærvær af EIPA. Der ses en signifikant forskel mellem (-/+ EIPA) ved 5 min isoton og ved 5 min hyperton behandling, markeret med #. Ved 5 min hyperton behandling (- EIPA), ses en signifikant forskel fra den isotone kontrol, markeret med *. Data er et gennemsnit af 4-10 uafhængige forsøg. B. Øverst ses en repræsentativ membran fra Western blotting efter tilsætning af antistoffer rettet mod fosforyleret MKK3/6 (Ser 189 /Thr 193 /Ser 207 /Thr 211 ). Nederst ses den gennemsnitlige relative fosforylering af MKK3/6, i forhold til isoton kontrol. Fosforyleringsgraden er vist som funktion af tiden i henholdsvis fravær og nærvær af EIPA. Der er ingen signifikant forskel i fosforyleringsgrad af MKK3/6 mellem (+/- EIPA), mens der ses en signifikant forskel fra den isotone kontrol ved 15 min (- EIPA) og ved 30 min (+/- EIPA), markeret med *, hvilket indikerer at p38 fosforyleres ved osmotisk skrumpning, uafhængigt af NHE1 aktivitet. Data er et gennemsnit af 4-5 uafhængige forsøg (2 for 30 minutter). Der er benyttet S.E.M. error bars, hvor p < 0.05 betragtes som signifikant. Disse resultater peger på, at MEK1/2 fosforylering hæmmes ved hypertonicitet på en NHE1 uafhængig måde, mens MKK3/6 er upåvirket af skrumpning og af NHE1 hæmning. 93
94 4.8.3 Effekt af hæmning af de tre MAPKs (ERK, JNK og p38 MAPK) på ELA celler viabilitet Ved hæmning af MAP-kinaserne ERK, JNK og p38 MAPKs har jeg undersøgt deres rolle for cellernes viabilitet under hyperosmotisk skrumpning. Af nedestående figur fremgår det, at MAPKs hæmning fører til en signifikant højere celledødelighed, i forhold til den isotone kontrol. ERK hæmmes af PD98059, JNK hæmmes af SP og p38 MAPK hæmmes af SB A B % celledød, relativ til isoton kontrol Isoton + PD98059 Hyperton + PD98059 Isoton i forhold til isoton kontrol Hyperton i forhold til isoton kontrol * * * * # * * # * % celledød, relativ til isoton kontrol Isoton + SB Hyperton + SB Isoton i forhold til isoton kontrol Hyperton i forhold til isoton kontrol * * # * * # timer 6 timer 12 timer 24 timer 48 timer timer 6 timer 12 timer 24 timer 48 timer C D Kontrol NHE1 p38 MAPK JNK1/2 ERK1/2 % celledød, relativ til isoton kontrol isoton + SP Hyperton + SP Isoton i forfold til isoton kontrol Hyperton i forhold til isoton kontrol * * # 3 timer 6 timer 12 timer 24 timer 48 timer * * # * Celleviabilitet, isoton relativ til isoton kontrol efter 48 timers isotonicitet * * Kontrol EIPA SB SP PD98059 E Celleviabilitet, hyperton relativ til egen isoton kontrol efter 48 timers hypertonicitet Kontrol NHE1 p38 MAPK JNK1/2 ERK1/2 * * F Celleviabilitet, hyperton relativ til isoton kontrol efter 48 timers hypertonicitet Kontrol NHE1 p38 MAPK JNK1/2 ERK1/2 * * * 0.0 Kontrol EIPA SB SP PD Kontrol EIPA SB SP PD
95 Figur 60. Effekt af MAPKs hæmning på ELA cellers viabilitet. ELA-celler er dyrket i 96 brøndsbakker med celler/brønd dagen før forsøgsstart. På forsføøgsdagen inkuberes cellerne først med isoton medie (300 mosm) i 1 time og derefter i hypertont medie (600 mosm) til de angivne tider, hvorefter der tilsættes solubiliseringsbuffer, MTT og celleviabiliteten aflæses på en fluorostar pladlæser, som beskrevet i metodeafsnit A. Celledødelighed ved hæmning af ERK1/2, ved isoton og hyperton behandling. B. Celledødelighed ved hæmning af p38 MAPK, ved isoton og hyperton behandling. C. Celledødelighed ved hæmning af JNK1/2, ved isoton og hyperton behandling. D. Samlet oversigt over celleviabilitet ved hæmning af NHE1 og MAPKs, isoton i forhold til isoton kontrol. E. Samlet oversigt over celleviabilitet ved hæmning af NHE1 og MAPKs, hyperton i forhold til egen tilsvarende isoton kontrol. F. Samlet oversigt over celleviabilitet ved hæmning af NHE1 og MAPKs, hyperton i forhold til isoton kontrol. Data er givet som et gennemsnit af 4-6 uafhængige forsøg. Der er benyttet S.E.M. error bars, hvor * indikerer at der er signifikant forskel fra isoton kontrol, mens # indikerer at der er signifikant forskel fra den hypertone kontrol værdi. p < 0.05 betragtes som signifikant. 95
96 5 Diskusion Kort inden jeg påbegyndte specialearbejdet, havde man i Stine Falsig Pedersens laboratorium fundet, at ERM proteiner aktiveres af celleskrumpning i Ehrlich Lettre Ascites (ELA) celler. I dette speciale har jeg derfor ønsket, at klarlægge signaltransduktionsveje op- og nedstrøms for ERM proteiner efter celleskrumpning. Ligeledes har jeg ønsket at teste den mulige sammenhæng mellem skrumpningsinduceret NHE1 regulering af MAP-kinaser (ERK1/2, JNK1/2 og p38 MAPK) og celleoverlevelse/celledød. Mit speciale har været opdelt i to overordnede projekter; Et ezrin protein projekt A) og et MAP-kinase projekt B). Derfor er den følgende diskussion ligeledes opdelt i to dele, hvor jeg har testet følgende hypoteser: Del A 1. At aktivering af ERM proteiner, specielt ezrin, er et tidligt signal efter celleskrumpning, og fungerer opstrøms for skrumpningsinduceret aktivering af volumen-regulatoriske og celle-beskyttende mekanismer. Specifikt ønskede jeg at undersøge ezrins roller i (i) aktivering af Na + /H + exchangeren NHE1, (markeret i arbejdsmodellen med rødt) (ii) skrumpnings-induceret Rho aktivering og F-aktin reorganisering, (markeret med blå-grøn i arbejdsmodellen) og (iii) regulering af celleoverlevelse efter skrumpning via aktivering af en NHE1-Ezrin-PI3K-Akt/PKB overlevelsesvej, (markeret med grøn i arbejdsmodellen). 2. At skrumpningsinduceret aktivering af NHE1 findes nedstrøms for aktivering af Rho-ROCK kinase vejen, (markeret med blå i arbejdsmodellen). Del B 3. At skrumpnings-induceret aktivering af NHE1, kan være et opstrøms signal for regulering af MAPkinaserne ERK1/2, JNK1/2, og p38 MAPK, muligvis igennem effekter på intracellulær ph og/eller MEK1/2 eller MKK3/6 aktivitet. 4. At NHE1 og disse MAP-kinaser regulerer celleoverlevelse efter hyperosmotisk skrumpning 96
97 5.1 Del A Ud fra hypotese 1 og 2 har jeg opstillet følgende arbejdsmodel (figur 48). Jeg vil i det følgende afsnit diskutere mine data ud fra mine hypoteser og denne arbejdsmodel. Figur 61. Arbejdsmodel for hypotese 1 og 2. Jeg ønskede at undersøge om ERM proteiner, specielt ezrin, kan være et tidligt signal om celleskrumpning og således virke opstrøms for NHE1 aktivering. Alternativt kunne NHE1 være opstrøms for ezrin aktivering. Desuden har jeg undersøgt ezrins rolle i aktivering af overlevelsesvejen, NHE1, ezrin, PI3K, Akt/PKB. Ligeledes har jeg undersøgt ERMs rolle i skrumpnings-induceret F-aktin organisering. Endeligt ville jeg undersøge samspillet mellem Rho-Rho-kinase vejen og NHE ERM proteiner Lokalisering og skrumpnings-induceret translokering af ezrin og ERM proteiner i ELA celler Mine PCR analyser viste, at alle tre ERM proteiner, samt det relaterede protein merlin, er udtrykt på mrna niveau i ELA celler. Dette er i god overensstemmelse med tidligere studier, der har vist, at ERM proteiner findes co-udtrykt og co-lokaliseret i specialiserede regioner, i de fleste dyrkede epithel- og fibroblastceller (Louvet-Vallee S., 2000), hvor aktin filamenter er tæt associeret med plasmamembraner, som f.eks. i mikrovilli, i filopodier og ved celle-celle/celle-matrix adhæssionssteder (Bretscher A et al., 2002;Sato et al., 1992;Tsukita & Yonemura, 1999;Vaheri A et al., 1997). At jeg finder merlin udtrykt på mrna niveau, skyldes muligvis at ELA-celler er en epithel-deriveret tumorcellerlinie og merlin er identificeret som et tumorsupressor gen (Bretscher A et al., 2002). 97
98 I overensstemmelse med tilstedeværelse af ERM proteiner i ELA-celler har jeg vha. immunocytokemi (CLSM) fundet, at ezrin og i det hele taget ERM proteiner primært findes i cytosolen under isotone forhold og hurtigt (>1 min efter hyperton skrumpning) translokeres til den kortikale region under hyperton skrumpning. I kortex lokaliserede de fosforylerede ERM proteiner i vid udstrækning til mikrovilli-lignende F-aktin indeholdende protrussioner. Dette stemmer overens med tidligere fund i mange forskellige celletyper, hvor ERM proteiner translokeres til det kortikale cytoskelet/plasmamembranen under aktivering (Ivetic A & Ridley AJ, 2004);(Bretscher A et al., 2000);(Pedersen SF et al., 2007). I overensstemmelse med disse resultater, fandt vi ved Western blotting, at ERM proteiners fosforylering kraftigt øges ved osmotisk skrumpning i flere andre celletyper bl.a. AP1 celler, (hvilket er diskuteret i afsnit 5.1.3), og i Cos-7-, NIH3T3-, LLC-PK1-celler (Maria Rasmussen, 2006), se appendix NHE Ekspression af NHE- isoformer på mrna niveau, samt aktivering af NHE1 under hyperton skrumpning i ELA-celler Skrumpnings-induceret intracellulær alkalinisering hæmmes af EIPA, hvilket indikerer at det er NHE1 isoformen der aktiveres under hyperton skrumpning. Dette er i overenstemmelse med, at jeg fandt NHE1 isoformen udtrykt i ELA celler på mrna niveua. Ligeledes har immunofluorescens-studier vist, at NHE1 er lokaliseret i plasmamembranen i ELA-celler (Barbara Vasek Darborg, 2005). Da jeg også fandt NHE8 isoformen udtrykt i ELA celler på mrna niveau og det stadig er ukendt om denne isoform hæmmes af tilstedeværelse af EIPA, kan det ikke udelukkes at NHE8 kan bidrage til den målte aktivitet af NHE i dette speciale, for diskussion se (Wakabayashi S et al., 1992), (S.F.Pedersen C.Varming, 2002). Jeg vil i denne diskussion dog kun henvise til NHE1s aktivering. Skrumpnings-induceret aktivering af NHE1 ses indenfor 1 minut efter eksponering til hyperon ringer og dette bevirker intracellulær alkalinisering. Desuden ses et samtidigt, i hvert fald delvist RVI respons, som det også er vist i andre celletyper, bl.a. i EATC (Pedersen SF et al., 1996), human bladder carcinoma celler og Chinese hamster ovary celler (CHO-celler), (Grinstein et al., 1992), (Cala & Maldonado, 1994). Den skrumpnings-inducerede alkalinisering skyldes NHE1s transport af H + ud af cellen. Den intracellulære alkalinisering aktiverer Cl - - /HCO 3 exchangeren, der således sammen med NHE1, bidrager til cellens RVI-respons i nærvær af HCO - 3. I mine forsøg observeres der ikke et fuldendt RVI-respons efter hyperton skrumpning i den observerede tidsperiode (se figur 30), hvilket 98
99 sandsynligvis, i hvert fald delvist skyldes, at der i mine forsøg er benyttet nominelt HCO 3 - fri ringer. For yderligere diskusion mellem NHE1 og AE under RVI se (Cala & Maldonado, 1994) Den causale sammenhæng mellem NHE1 og ERM proteiner under hyperton skrumpning i ELA celler Jeg fandt i modsætning til tidligere studier (Wu et al., 2004), at ERM protein aktivering sker uafhængigt af NHE1 aktivitet. Vha. Western blotting fandt jeg at AP1 cellers (NHE-deficiente) skrumpningsinducerede fosforylering af ERM proteiner ikke er signifikant forskellig S5 cellers (+hnhe1) fosforylering (figur 35), hvilket indikerer at ERM protein aktivering ikke er afhængig af skrumpningsinduceret NHE1 aktivitet og derfor ikke findes nedstrøms for NHE1 i ELA-celler. Ligeledes har Barbera og kollegaer tidligere i ELA-celler vist, at ERM protein fosforylering sker uafhængigt af tilstedeværelse af EIPA og derfor af NHE1 aktivering (Maria Rasmussen, 2006). I ELA- og i AP1 celler ser det altså ud til, at ERM proteiner og NHE1 aktiveres som to uafhængige begivenheder, eller at ERM proteinerne findes opstrøms for NHE1 aktivering. Disse to muligheder har jeg undersøgt nærmere. Ved knock-down af ezrin fandt jeg, at ELA cellers skrumpnings-inducerede aktivering af NHE1 øges signifikant. Ligeledes var der en tendens til, at cellernes RVI-respons var øget i forhold til kontrolsituationen (ikke signifikant). Dette indikerer, at ezrin i ELA-celler har en negativ regulerende effekt på skrumpnings-induceret NHE1 aktivitet. I ELA-celler, ser det altså heller ikke ud til at ERM proteiner opstrøms aktiverer NHE1, under hyperton skrumpning. At mine data ikke stemmer overens med hvad Wu og kollegaer tidligere har fundet, kan skyldes brug af forskellige celletyper og forskellige omstændigheder. Wu s forsøg, er udført med PS120 celler (en nyre-epithel cellelinie), der har NHE1 udtrykt exogent og det er muligt at overekspressions effekter kan have påvirket deres fund. De havde ligeledes serum tilstede i deres forsøg, mens jeg har benyttet Ringere (Wu et al., 2004). 99
100 5.1.4 Aktivering af Rho-ROCK vejen efter osmotisk skrumpning og mulige causale sammenhænge med NHE1 aktivering Rho aktivering under hyperton skrumpning I overensstemmelse med tidligere studier i LLC-PK1-celler (Ciano-Oliveira et al., 2003) fandt jeg, at Rho proteiner hurtigt (>1 min) og transient aktiveres under hyperton skrumpning i ELA celler. Rho familien af GTPaser stimuleres generelt af hyperosmotisk stress (Ciano-Oliveira et al., 2003) og deres aktivering er medvirkende i den osmotisk provokerede cytoskelet re-organisering, især i forstærkning af det kortikale cytoskelet, under hyperosmotisk skrumpning (C.Di Ciano-Oliveira et al., 2006;Ciano- Oliveira et al., 2003;Pedersen SF et al., 2001), hvilket kan forklare deres hurtige aktivering under hyperosmotisk skrumpning. Ciano-Oliveira og kollegaer har tidligere vist, at Rho proteiners aktivering under hypertont stimuli, er proportionelt med cellernes stigning i ekstracellulær osmolaritet og at Rho proteinernes aktivering falder, når cellerne genopretter til isotonicitet, hvilket kan forklare hvorfor aktivering af Rho-proteiner er transient, idet cellerne over tid volumen regulerer og derved opnår isotonicitet (Di Ciano-Oliveira C, 2006) Rho-ROCK vejens rolle i skrumpnings-induceret aktivering af NHE1 Jeg fandt i overensstemmelse med andre studier (C.Di Ciano-Oliveira et al., 2006;Pedersen et al., 2002), at NHE1 aktivering under hyperosmotisk skrumpning, sker uafhængigt af Rho-ROCK kinase i ELA celler. Dette udelukker, at Rho-ROCK findes opstrøms for skrumpnings-induceret NHE1 aktivering. I modsætning hertil har andre studier vist, at p160rock og RhoA findes som en opstrøms direkte aktivatorer af NHE1 og derigennem modulerer tidlige trin i integrin-induceret cytoskeletale reorganiseringer i fibroblast celler (Tominaga T et al., 1998;Tominaga & Barber, 1998). Dette har jeg dog ikke kunne bevise Causale sammenhænge mellem ezrin og Rho aktivering Jeg fandt, at knock-down af ezrin medfører ca. 50 % lavere Rho aktivitet, efter hyperton skrumpning. Dette indikerer at ezrin findes opstrøms for skrumpnings-induceret Rho protein aktivering. Dette 100
101 stemmer overens med tidligere studier, der har vist at ERM proteiner kan displacere den GDP-bundne form af Rho proteiner fra Rho-GDI og derved aktivere Rho-proteiner (Bretscher A., 1999;Bretscher et al., 1997;Mackay et al., 1997;Takahashi et al., 1997). Vi fandt at ERM protein fosforylering øges kraftigt, når ELA celler er transfekteret med konstitutiv aktiv Rho, hvilket indikerer at Rho protein aktivering, ligeledes findes opstrøms for ERM protein aktivering i ELA celler (Maria Rasmussen, 2006). Desuden fandt vi, at hæmning af Rho-kinasen, fører til øget ERM protein fosforylering, som det også er set i mange andre studier (se afsnit 2.5.1). Disse resultater peger på, at der findes et positivt feedback loop mellem skrumpnings-induceret ERM og Rho protein aktivering, som det er diskuteret i afsnit Skrumpnings-inducerede F-aktin ændringer i ELA-celler Ezrins rolle i F-aktin re-organisering under osmotisk skrumpning I de fleste undersøgte celler er hyperosmotisk skrumpning associeret med en reorganisering af det aktinbaserede cytoskelet og i mange tilfælde ses en netto stigning i cellulært F-aktin indhold (Pedersen et al., 1999). ERM proteiner er vigtige regulatorer af cytoskelettes organisering og har vigtige funktioner i mikrovilli dannelse i mange celletyper (Bretscher A et al., 2002;Tsukita & Yonemura, 1999;Bretscher A et al., 2000;Denker SP et al., 2000;Tsukita & Yonemura, 1999), idet bl.a. ezrin associerer med F-aktin (Mackay et al., 1997). Derfor har jeg ønsket, at teste ezrins opstrøms rolle, for F-aktin mængde og reorganisering i ELA celler, under hyperton skrumpning. Mens den kortikale F-aktin fluorescens stiger under hyperton skrumpning (se figur 32 og 33), er den skrumpnings-inducerede stigning i netto mængden af cellulært F-aktin ikke signifikant forskellig fra den isotone kontrol. Der var en stigning dog en tendens til, at mængden af F-aktin stiger ved hyperosmotisk skrumpning (p-værdi på 0.14), i overensstemmelse med der tidligere er fundet i andre celletyper (Kenneth R.Hallows et al., 1995;Pedersen SF et al., 2001;Pedersen et al., 1999).. Ezrin knockdown ser ikke ud til at påvirke mængden af F-aktin under hyperton skrumpning, hvilket indikerer at ezrin ikke umiddelbart er en essentiel komponent i ELA- cellers F-aktin mængde under hyperton skrumpning. I overensstemmelse med at ERM proteiner er vigtige regulatorer af cytoskelettets organisering (Saotome I et al., 2004), (Shaw et al., 1998), (Bretscher A et al., 2002), (Takeuchi et al., 1994), har jeg fundet at fosforylerede ERM proteiner co-lokaliserer med F-aktin i skrumpnings-inducerede mikrovillus- lignende apikale protrusioner. Dannelse af disse protrusioner ser ud til at være delvist hæmmet ved ezrin sirna behandling i ELA celler, hvilket indikerer, at aktivering af ezrin er en vigtig del af dannelse og stabilitet 101
102 af disse strukturer. Dannelsen af disse strukturer blev dog kun delvist hæmmet af ezrin knock-down, hvilket betyder at andre faktorer spiller ind i denne dannelse. Disse kan bl.a. omfatte de to andre ERM proteiner, moesin og radixin, idet de også har mange kendte funktioner i cytoskelettets opretholdelse (Shaw et al., 1998), (Bretscher A et al., 2000;Mangeat P et al., 1999;Tsukita S & Yonemura S, 1997;Tsukita et al., 1994). Ligeledes kan den delvise hæmning af dannelsen af cytoskelet strukturer, skyldes at den ezrin sirna medierede knock-down kun er ca. 70 % Ezrins rolle i balancen mellem død og overlevelse efter hyperton skrumpning Tab af cellevolumen er et fundamentalt træk ved apoptose. Celler kan kompensere for deres ændringer i cellevolumen via aktivering af flere volumen regulatoriske iontransport mekanismer og cellevolumen regulering efter celleskrumpning er vist at være afgørende for at modvirke skrumpnings-induceret celledød (Bortner CD & Cidlowski JA, 1998;Okada Y & Maeno E, 2001). NHE1 er således en vigtig komponent, der beskytter celler mod apoptose efter skrumpning og andre stimuli (Matsuyama S et al., 2000;Nylandsted J et al., 2004;Wu et al., 2004). I overensstemmelse med dette fandt jeg, at hæmning af NHE1, signifikant øgede ELA-cellers dødelighed ved celleskrumpning, mens hæmning af NHE1 ikke har nogen betydning under isotonicitet (figur 32). Denker og kollegaer har tidligere fundet, at NHE1 er koblet til plasmamembranen og cytoskelettet gennem en direkte interaktion med ERM proteiner (Denker SP og Barber, 2002;Denker SP et al., 2000). Ligeledes er det foreslået, at NHE1 medieret modstand overfor apoptose, kan ske gennem dens kobling med ERM proteiner og derigennem aktivere af ezrin-pi3k-akt overlevelsesvejen (Wu et al., 2003). Mine resultater er ikke i overensstemmelse med denne foreslåede model, idet jeg som tidligere nævnt, fandt at ERM protein fosforylering sker uafhængigt af NHE1 aktivitet. Ligeledes fandt jeg, at ELA cellers skrumpnings-inducerede celledød, er upåvirket af ezrin knock-down og af PI3K hæmning. Det er desuden tidligere i vores laboratorium vist, at PKB aktivitet ikke stiger ved celleskrumpning i ELAceller (Rasmussen M et al., 2007). Ud fra disse resultater kan det konkluderes, at skrumpnings-induceret ERM protein aktivering sker uafhængigt af NHE1 og celleskrumpning ser ikke ud til at aktivere NHE1- ezrin-pi3k-akt/pkb overlevelsesvejen i ELA celler. Grunden til de observerede forskellige mellem Wu et al s forsøg i nyre epithel celler og mine forsøg i ELA celler er ikke fuldt ud forstået. En grund til forskellene kan være, at i nyre epithel celler er ion-udveksling via NHE1 krævet for NHE1-medieret beskyttelse mod skrumpnings-induceret apoptose, men at den ikke er krævet i NHE1 medieret PKB aktivering, hvilket tyder på, at PKBs rolle er forholdsvis lille (Wu et al., 2003;Wu et al., 2004). I det hele taget er PKBs rolle i skrumpnings-induceret celledød meget kontroversiel, idet netto effekten på 102
103 Akt/PKB reflekterer en balance mellem aktiverings- og hæmnings effekter af skrumpning og den ser ud til at være celletype afhængige (Pedersen SF., 2006). I relation til hypotese 1 og 2 kan det altså konkluderes, at ERM proteiner aktiveres af hyperton celleskrumpning, uafhængigt af NHE1 aktivitet, mens de negativt regulerer skrumpnings-induceret NHE1 aktivitet. Ezrin findes opstrøms for skrumpnings-induceret Rho aktivitet og ser ud til at være involveret i dannelse og opretholdelse af F-aktin indeholdende protrusioner under hyperton celleskrumpning. Ligeledes kan det konkluderes at ezrin, under hyperton celleskrumpning ikke er involveret i regulering af celleoverlevelse efter skrumpning, via aktivering af en NHE1-Ezrin-PI3K- Akt/PKB overlevelsesvej. Mht. hypotese 2, kan det konkluderes at NHE1 ikke reguleres af Rho-ROCK kinase vejen efter celleskrumpning. Jeg er kommet frem til følgende model, mht. del projekt A: Figur 62. Model for projekt A. Gennem mine resultater kommet frem til, at celleskrumpning aktiverer NHE1, Rho og ERM proteiner, samt at celleskrumpning medfører reorganisering af F-aktin, på en måde der er delvist afhængig af ezrin. De fede pile indikerer, de resultater der har bekræftet mine hypoteser, mens de tynde pile, med krydser over, indikerer de hypoteser der kunne afkræftes. indikerer at hæmning mens indikerer aktivering. 103
104 5.2 Del B Inden jeg startede på dette speciale, var det i Stine Falsig Pedersens laboratorium fundet, at skrumpnings-induceret NHE1 aktivering hæmmer ERK1/2 og aktiverer JNK1/2, mens den ingen effekt havde på p38 MAPK, efter osmotisk skrumpning. Jeg ønskede derfor at uddybe disse fund ved at undersøge følgende hypoteser: 1) At skrumpnings-induceret aktivering af NHE1, kan være et opstrøms signal for regulering af MAP-kinaserne ERK1/2, JNK1/2, og p38 MAPK, muligvis igennem effekter på intracellulær ph og/eller MEK1/2 eller MKK3/6 aktivitet. 2) At NHE1 og disse MAP-kinaser regulerer celleoverlevelse efter hyperosmotisk skrumpning. Ud fra disse hypoteser har jeg opstillet følgende model (se figur 50). Jeg vil i det følgende afsnit diskutere mine data ud fra mine hypoteser og denne arbejdsmodel. Figur 63. Arbejdsmodel for hypotese 3 og 4. Jeg ønskede at undersøge hvorledes skrumpnings-induceret aktivering af NHE1 kan være opstrøms for MAPKs. Hypoteserne var at dette kunne foregå igennem effekter på ph i og/eller MEK1/2 eller MKK3/6 aktivitet. Endelig ville jeg undersøge om disse MAPKs kan regulere cellens overlevelse efter hyperosmotisk skrumpning phis betydning for fosforylering af MAP-kinaser (ERK1/2, p38 MAPK og JNK1/2) Flere forsøg har peget på, at ændringer i ph i kan regulere ERK1/2, p38 MAPK og JNK1/2 aktivitet i flere celletyper (Haworth et al., 2003), (Shrode et al., 1997), derfor kunne det tænkes, at den intracellulære alkalinisering, der medieres gennem skrumpnings-induceret NHE1 aktivering, er det der er ansvarlig for regulering af MAPK generelt. Jeg har derfor undersøgt effekterne af cytosolisk alkalinisering på MAP-kinaserne (ERK1/2, JNK og p38 MAPK). Det skal nævnes at jeg for at ændre ph i valgte, at inkubere cellerne ved ændret ph o i mine forsøg. Dette vil ændre ph i tilsvarende om end mindre 104
105 (Rentsch M et al., 2006). Ulemperne er dog at jeg ikke kan skelne mellem effekter på ph i og ph o. Alternativt kunne jeg have valgt at inkubere eller prepulse med svage syrer/baser (f.eks. ved NH 4 Clprepulsing, som beskrevet af (Simchowitz & Roos, 1985)), men ulemper ved disse ph i ændringer er at de er transiente og således ville det være svært, at korrelere data direkte til ændret ph i. Jeg fandt, at JNK1/2 fosforylering er signifikant højere ved en ph o værdi på 8.0, mens fosforyleringsgraden af JNK1 var signifikant lavere ved ph o værdi 6.8 (JNK2 var upåvirket af lavere ph værdier). Mine data er således i overensstemmelse med den fortolkning, at den NHE1 medierede stigning i JNK aktivitet efter osmotisk skrumpning er ph i medieret (Shrode et al., 1997), (Stine Falsig Pedersen et al., 2007). Jeg fandt desuden at p38 MAPK fosforylering er signifikant lavere ved ph 6.8 og stiger en smule ved ph 8, hvilket indikerer at p38 MAPK tilsyneladende er ph i afhængig, som Shrode og kollegaer ligeledes har vist (Shrode et al., 1997). Da p38 MAPKs aktivering ikke er signifikant højere, ved højere ph i værdier må det antages, at ph i effekten på p38 MAPK ikke er nok til at afgøre dens NHE1 afhængighed. ERK1/2s fosforyleringsgrad er upåvirket af ph i ændringer, hvilket indikerer at ph i ikke modulerer ERK1/2 aktivitet i ELA celler under osmotisk skrumpning NHE1s mulige rolle i skrumpnings-induceret regulering af MEK1/2 og MKK3/6 Da ph i ændringer ikke påvirker aktivering af ERK1/2 og ikke kan forklare p38 MAPK aktiviteten, har jeg undersøgt effekten af skrumpning og NHE1 hæmning på MEK1/2 og MKK3/6 aktivering. Jeg fandt at MEK1/2 aktivitet hæmmes ved hyperosmotisk skrumpning, hvorefter dens aktivitet stiger igen til ca. udgangspunktet. At MEK1/2 hæmmes ved hyperosmotisk skumpning, stemmer overens med at vi og andre har vist, at ERK1/2, hæmmes af osmotisk skrumpning (Friis et al., 2005), (Pedersen SF et al., 2007). NHE1-hæmmeren EIPA forhindrer delvist denne skrumpnings-inducerede hæmning af MEK1/2 aktivering, hvilket indikerer, at MEK1/2 aktivering er afhængig af skrumpnings-induceret NHE1 aktivitet, i overensstemmelse med den NHE1 afhængige hæmning af ERK1/2 under celleskrumpning (Pedersen SF et al., 2007). Som det fremgår af figur 46 aktiveres MKK3/6 efter ca. 15 minutters hyperosmotisk skrumpning, hvilket stemmer overens med flere andre studier (Hoffmann EK & Pedersen SF, 1998;S.F.Pedersen C.Varming, 2002;Shrode et al., 1997). MKK3/6 fosforyleringen er i mine forsøg uafhængig af skrumpnings-induceret NHE1 aktivitet, hvilket ligeledes stemmer overens med Barbaras tidligere studier på p38 MAPK fosforylering (Barbara Vasek Darborg, 2005;Pedersen SF et al., 2007). At MKK3/6 aktiveres som respons over hyperosmotisk skrumpning i ELA-celler, stemmer ligeledes overens med tidligere studier, der har vist at hyperton skrumpning medfører aktivering af TonEBP, gennem en p38 MAPK afhængig måde (Nadkarni et al., 1999);(Ko et al., 2002;Padda et al., 2006), se 105
106 afsnit Det er foreslået at der findes et osmotisk stress relevant aktin-bundet scaffold af proteiner, der inkluderer MEKK3, MKK3 og Rac GTPase. Dette kompleks ser ud til at være krævet for den hypertone medierede p38 MAPK aktivering og derved kan dette kompleks muligvis være det mammales udgave af det kendte osmosensing, der findes i gær (Uhlik MT et al., 2003) Effekt af NHE1, samt effekten af hæmning af de tre MAPKs (ERK1/2, JNK1/2 og p38 MAPK) på celledød og celleoverlevelser, efter hyperton skrumpning For at klarlægge nogle af de signaleringsveje, der regulerer cellers overlevelse under hyperosmotisk skrumpning, har jeg undersøgt effekten af MAP-kinase hæmning (ERK1/2, JNK1/2 og p38 MAPK) på cellers viabilitet over 2 døgns hyperosmotisk skrumpning. Jeg fandt, at 48 timers hypertonicitet inducerer en signifikant celledødelighed, som forværres ved hæmning af både ERK1/2, samt af JNK1/2 (se figur 37). Dette indikerer, at ERK1/2 og JNK1/2 aktivitet, er vigtige faktorer i overlevelse, under celleskrumpning. Effekten af ERK1/2 hæmning på celledød, stemmer overens med tidligere studier, der har fundet, at ERK fremmer celleoverlevelse og vækst ved langtidsforstyrrelser af celler via osmotisk stress (Pages G et al., 1993). JNK og p38 MAPK inducerer generelt celledød og modvirker celle proliferering, under hyperosmotisk skrumpning (Else K.Hoffmann & Stine F.Pedersen, 2006;Harper SJ & LoGrasso P, 2001), men JNK1/2 inducerer også celleoverlevelse i nogle celletyper (Kennedy NJ & Davis RJ, 2003;Patricia Hess et al., 2002). Den øgede celledød ved hæmning af JNK1/2 kan muligvis forklares ved, at nogle studier har peget på, at de to forskellige isoformer af JNK, har modsatrettede funktioner. JNK1 ser ud til at være en positiv regulator af cellulær proliferering, mens JNK2 fungerer som negativ regulator af cellulær proliferering og derved udviser beskyttelse overfor apoptose (se(sheikh-hamad & Gustin, 2004;Sabapathy K et al., 2004). Ved p38 MAPK hæmning ses en signifikant lavere celledød, både i forhold til den isotone kontrol og i forhold til den hypertone kontrol (der er taget i forhold til den isotone kontrol), hvilket stemmer overens med, at p38 MAPK inducerer celledød og modvirker celle-proliferering, under langtidsforstyrrelser af cellen via osmotisk stress (Harper SJ & LoGrasso P, 2001;Miyakawa H et al., 1999;Nadkarni et al., 1999;Sheikh-Hamad & Gustin, 2004). At jeg finder at p38 MAPK er en vigtig faktor i mediering af celledød, stemmer ligeledes overens med at Friss og kollegaer i NIH3T3 celler vist, at hæmning af p38 MAPK reducerer den hypertone- inducerede aktivering af caspase-3 og p53 og derved findes opstrøms for disse signaleringsveje, under skrumpnings-induceret apoptose (Friis et al., 2005). Under aktivering trabslokeres p53 til cellekernen, hvor den stimulerer pro-apoptotiske molekyler, som f.eks. bax, hvilket 106
107 resulterer i Cyt c frigivelse, caspase-9 stimulering og derved stimulering af caspase-3 (Sanchez-Prieto et al., 2000;Kim et al., 2002;Friis et al., 2005). I relation til hypotese 3 og 4 kan det konkluderes, 1) at stigninger i phi aktiverer JNK1/2 og i mindre grad muligvis p38 MAPK, mens ERK1/2 er upåvirket. 2) at MEK1/2 aktiviteten hæmmes af celleskrumpning på en NHE1 afhængig måde, mens MKK3/6 ser ud til at blive aktiveret af celleskrumpning på en NHE1 uafhængig måde. 3) at NHE1, ERK1/2 og JNK1/2 favoriserer overlevelse, mens p38 MAPK inducerer celledød under osmotisk skrumpning. Jeg er kommet frem til følgende model, mht. del projekt B: Figur 64. Model for projekt B. Jeg er gennem mine resultater kommet frem til, at NHE1 hæmmer MEK1/2 og ERK1/2 aktivitet, mens den aktiverer MKK3/6 og p38 MAPK under hyperton skrumpning i ELA celler. phi ændringer medfører aktivering af JNK1/2 og p38 MAPK, men påvirker ikke ERK1/2 aktivitet. Ligeledes har jeg vist, at hæmning af ERK1/2 og JNK1/2 medfører signifikant højere celledød, mens p38 MAPK og medfører en signifikant lavere celledød. 107
108 6 Konklusion Ud fra de opstillede hypoteser kan følgende konkluderes: Hypotese 1. At skrumpnings-induceret aktivering af ERM proteiner, specielt ezrin, er et tidligt signal for celleskrumpning, og derved fungerer opstrøms for skrumpningsinduceret aktivering af volumenregulatoriske og celle-beskyttende mekanismer. Specifikt ønskede jeg at undersøge ezrins roller i (i) aktivering af Na + /H + exchangeren NHE1, (ii) skrumpningsinduceret F-aktin reorganisering, herunder Rho aktivering, og (iii) regulering af celleoverlevelse efter skrumpning via aktivering af en NHE1-Ezrin- PI3K-Akt/PKB overlevelsesvej. ERM proteiner aktiveres ved hyperton skrumpning, på en NHE1 uafhængig måde. Ezrin regulerer negativt skrumpnings-induceret NHE1 aktivitet. Fosforylerede ERM proteiner co-lokaliserer med F-aktin under hyperosmotisk skrumpning og ezrin er medvirkende i dannelse og opretholdelse af F-aktin indeholdende protrusioner, under hyperton skrumpning. Ezrin findes opstrøms for skrumpnings-induceret Rho aktivering. NHE1, Ezrin og PI3K ikke er involveret i regulering af celleoverlevelse efter skrumpning via aktivering af en NHE1-Ezrin-PI3K-Akt/PKB overlevelsesvej. Hypotese 2. At skrumpnings-induceret aktivering af ERM proteiner er nedstrøms for aktivering af Rho- Rho kinase vejen. ERM proteiner findes ikke nedstrøms for Rho-Rho kinasen under hyperton skrumpning. Hypotese 3. At skrumpnings-induceret aktivering af NHE1, kan være et opstrøms signal for regulering af MAP kinaserne ERK1/2, JNK1/2, og p38 MAPK, muligvis igennem effekter på ph i og/eller MEK1/2 eller MKK3/6 aktivitet. 108
109 JNK1/2 aktivering og tilsyneladende p38 MAPK er sekundær til ph i stigninger, mens ERK1/2 er upåvirket af ph i ændringer. MEK1/2 aktivering hæmmes af celleskrumpning på en NHE1 afhængig måde, mens MKK3/6 aktiveres af celleskrumpning på en NHE uafhængig måde. Hypotese 4. At disse MAP kinaser regulerer celleoverlevelse efter hyperosmotisk skrumpning. ERK1/2 og JNK1/2 favoriserer celleoverlevelse, mens p38 MAPK favoriserer celledød, efter osmotisk skrumpning. 109
110 7 Perspektivering I denne specialerapport er effekten af celleskrumpning på ERM proteiner og MAP-kinaser, samt deres aktiveringsmekanismer og fysiologiske roller undersøgt i ELA-celler. De resultater jeg har opnået har ført til en bedre forståelse af disse sammenhæng i ELA celler, men har ligeledes rejst en række af nye interessante spørgsmål. Mekanismen og de fysiologiske roller, bag den skrumpnings-inducerede aktivering af ERM proteiner, samt deres rolle i mediering af intracellulære respons induceret under osmotisk celleskrumpning, bør undersøges nærmere. Især bør mekanismerne i ezrins negativt regulerende rolle i skrumpnings-induceret NHE1 aktivering undersøges nærmere. Det kunne være relevant at undersøge om denne effekt på NHE1 aktivitet, også gælder de andre to ERM proteiner, radixin og moesin, hvilket som det var tilfældet med ezrin kan undersøges vha. sirna rettet mod radixin og moesin. ERM proteinernes funktion i dannelse og opretholdelse af F-aktin-indeholdende strukturer under osmotisk celleskrumpning, bør ligeledes undersøges ved samtidig knock-down af radixin og moesin. Andre mulige mediatorer af skrumpnings-induceret ERM protein fosforylering, burde også også undersøges nærmere, således er protein kinase C, NIK og medlemmer af den ste20-relaterede kinase familie tidligere blevet vist, som værende volumen-følsomme (Baumgartner et al., 2006;Else K.Hoffmann & Stine F.Pedersen, 2006;Zhuang et al., 2000) og derfor kan de muligvis have en opstrøms funktion i skrumpnings-induceret ERM-protein aktivering. Samspillet melllem skrumpnings-medieret NHE1 aktivering og MAP-kinase regulering, bør undersøges nærmere. I første omgang burde man vha. coimmunoprecipitering og CLSM undersøges hvorledes MAP-kianser interagerer og co-lokaliserer med NHE1, under osmotisk skrumpning. Det kunne ligeledes være relevant at undersøge MAP-kinasernes regulering af skrumpnings-induceret NHE1 aktivering, f.eks. ved at forhindre MAP-kinasernes eventuelle binding til NHE1 og derefter undersøge NHE1 aktivitet. 110
111 Reference Liste Aharonovitz O, Zaun HC, Balla T, York JD, Orlowski J, & Grinstein S (2000). Intracellular ph Regulation by Na+/H+ Exchange Requires Phosphatidylinositol 4,5-Bisphosphate. J Cell Biol 150, Alexander RT & Grinstein S. (2006). Na+/H+ exchangers and the regulation of volume. Acta Physiol (Oxf). Aronson PS, Nee J, & Suhm MA. Modifier role of internal H+ in activating the Na+-H+ exchanger in renal microvillus membrane vesicles. Nature Ref Type: Abstract Aspenstrom P. (1999). Effectors for the Rho GTPases. Curr Opin Cell Biol. Bachmeier CJ, Trickler WJ, & Miller DW (2004). Drug efflux transport properties of 2',7'-bis(2- carboxyethyl)-5(6)-carboxyfluorescein acetoxymethyl ester (BCECF-AM) and its fluorescent free acid, BCECF. J Pharm Sci. Barbara Vasek Darborg. Skrumpningsinduceret regulering af celledød og overlevelsesveje i EATC: mulige roller for NHE1 og NKCC Ref Type: Unpublished Work Barbara Vasek Darborg, Else Kay Hoffmann, & Stine Falsig Pedersen. Causal relationship between NHE1, NKCC1, MAPKs and ERM proteins after osmotic shrinkage in Ehrlich Lettre mouse ascites tumor cells. The FASEB Journal Ref Type: Abstract Barret C, Roy C, Montcourrier P, Mangeat P, & Niggli V (2000). Mutagenesis of the Phosphatidylinositol 4,5-Bisphosphate (PIP2) Binding Site in the NH2-Terminal Domain of Ezrin Correlates with Its Altered Cellular Distribution. J Cell Biol 151, Baumgartner M, Sillman AL, Blackwood EM, Srivastava J, Madson N, Schilling JW, Wright JH, & Barber DL (2006). The Nck-interacting kinase phosphorylates ERM proteins for formation of lamellipodium by growth factors. PNAS 103, Berg JM, Tymoczko JL, & and Stryer L (2002). Biochemistry fifth edition. Bertrand B, Wakabayashi S, Ikeda T, Pouyssegur J, & Shigekawa M (1994). The Na+/H+ exchanger isoform 1 (NHE1) is a novel member of the calmodulin-binding proteins. Identification and characterization of calmodulin-binding sites. J Biol Chem 269,
112 Bhattacharya M, Babwah AV, & Ferguson SS (2004). Small GTP-binding protein-coupled receptors. Biochem Soc Trans. Bianchini L, L'Allemain G, & Pouyssegur J (1997). The p42/p44 Mitogen-activated Protein Kinase Cascade Is Determinant in Mediating Activation of the Na+/H+ Exchanger (NHE1 Isoform) in Response to Growth Factors. J Biol Chem 272, Bishop AL & Hall A (2000). Rho GTPases and their effector proteins. Biochem J. Boens N, Qin W, Basaric N, Orte A, Talavera EM, & Alvarez-Pez JM (2006). Photophysics of the fluorescent ph indicator BCECF. J Phys Chem A Mol Spectrosc Kinet Environ Gen Theory. Bortner CD & Cidlowski JA (1998). A necessary role for cell shrinkage in apoptosis. Biochem Pharmacol. Boyarsky G, Ganz MB, Sterzel RB, & Boron WF (1988). ph regulation in single glomerular mesangial cells. I. Acid extrusion in absence and presence of HCO3-. Am J Physiol Cell Physiol 255, C844-C856. Bretscher A, Chambers D, Nguyen R, & Reczek D. (2000). ERM-Merlin and EBP50 protein families in plasma membrane organization and function. Annu Rev Cell Dev Biol. Bretscher A, Edwards K, & Fehon RG (2002). ERM proteins and merlin: integrators at the cell cortex. Nat Rev Mol Cell Biol. Bretscher A. (1999). Regulation of cortical structure by the ezrin-radixin-moesin protein family. Curr Opin Cell Biol. Bretscher A (1983). Purification of an 80,000-dalton protein that is a component of the isolated microvillus cytoskeleton, and its localization in nonmuscle cells. J Cell Biol 97, Bretscher A, Edwards K, & Fehon RG (2002a). ERM proteins and merlin: integrators at the cell cortex. Nat Rev Mol Cell Biol 3, Bretscher A, Edwards K, & Fehon RG (2002b). ERM proteins and merlin: integrators at the cell cortex. Nat Rev Mol Cell Biol 3, Bretscher A, Reczek D, & Berryman M (1997). Ezrin: a protein requiring conformational activation to link microfilaments to the plasma membrane in the assembly of cell surface structures. J Cell Sci 110, Brett CL, Donowitz M, & Rao R (2005). Evolutionary origins of eukaryotic sodium/proton exchangers. Am J Physiol Cell Physiol 288, C223-C
113 Brewster JL, de Valoir T, Dwyer ND, Winter E, & Gustin MC (2006). An osmosensing signal transduction pathway in yeast. Science. Burg MB, Kwon ED, & Kultz D (1997). Regulation of gene expression by hypertonicity. Annu Rev Physiol. Burg MB, Kwon ED, & Kultz D (1996). Osmotic regulation of gene expression. FASEB J 10, Burridge K & Wennerberg K (2004). Rho and Rac take center stage. Cell. Burton JD. (2005). The MTT assay to evaluate chemosensitivity. Methods Mol Med. C.Di Ciano-Oliveira, A.C.P.Thirone, & K.Szászi and A.Kapus (2006). Osmotic stress and the cytoskeleton: the R(h)ole of Rho GTPases. Acta Physiologica. Cala PM (1980). Volume regulation by Amphiuma red blood cells. The membrane potential and its implications regarding the nature of the ion-flux pathways. J Gen Physiol 76, Cala PM & Maldonado HM (1994). ph regulatory Na/H exchange by Amphiuma red blood cells. J Gen Physiol 103, Cantiello HF. (1997). Role of actin filament organization in cell volume and ion channel regulation. J Exp Zool. Cheng JC, Moore TB, & Sakamoto KM (2003). RNA interference and human disease. Mol Genet Metab. Ciano-Oliveira CD, Sirokmany G, Szaszi K, Arthur WT, Masszi A, Peterson M, Rotstein OD, & Kapus A (2003). Hyperosmotic stress activates Rho: differential involvement in Rho kinase-dependent MLC phosphorylation and NKCC activation. Am J Physiol Cell Physiol 285, C555-C566. Dahl SC, Handler JS, & Kwon HM (2001). Hypertonicity-induced phosphorylation and nuclear localization of the transcription factor TonEBP. Am J Physiol Cell Physiol 280, C248-C253. DeMali KA, Wennerberg K, & Burridge K (2003). Integrin signaling to the actin cytoskeleton. Curr Opin Cell Biol. Denker SP, Huang DC, Orlowski J, Furthmayr H, & Barber DL. (2000). Direct binding of the Na--H exchanger NHE1 to ERM proteins regulates the cortical cytoskeleton and cell shape independently of H(+) translocation. Mol Cell. 113
114 Denker SP og Barber (2002). Ion transport proteins anchor and regulate the cytoskeleton. Curr Opin Cell Biol. Di Ciano C, Nie Z, Szaszi K, Lewis A, Uruno T, Zhan X, Rotstein OD, Mak A, & Kapus A (2002). Osmotic stress-induced remodeling of the cortical cytoskeleton. Am J Physiol Cell Physiol 283, C850-C865. Di Ciano-Oliveira C TASKKA (2006). Osmotic stress and the cytoskeleton: the R(h)ole of Rho GTPases. Acta Physiol (Oxf). Dissing S and Gasbjerg PK (1993). Basic principles behind the application of flourescent dyes for the study of cellular electrolyte concentrations, membrane potential and microenviroment. Dogra C.Changotra, Wergedal JE, & Kumar A (2006). Regulation of phosphatidylinositol 3-kinase (PI3K)/Akt and nuclear factor-kappa B signaling pathways in dystrophin-deficient skeletal muscle in response to mechanical stretch. J Cell Physiol. Downward J. (2004). PI 3-kinase, Akt and cell survival. Semin Cell Dev Biol. Elbashir SM, Harborth J, Weber K, & Tuschl T (2002). Analysis of gene function in somatic mammalian cells using small interfering RNAs. Methods. Else K.Hoffmann & Stine F.Pedersen (2006). Sensors and signal transduction pathways in vertebrate cell volume regulation. Karger. Fievet BT, Gautreau A, Roy C, Del Maestro L, Mangeat P, Louvard D, & Arpin M (2004). Phosphoinositide binding and phosphorylation act sequentially in the activation mechanism of ezrin. J Cell Biol 164, Fliegel L. (2005). The Na+/H+ exchanger isoform 1. Int J Biochem Cell Biol. Friis MB, Friborg CR, Schneider L, Nielsen MB, Lambert IH, Christensen ST, & Hoffmann EK (2005). Cell shrinkage as a signal to apoptosis in NIH 3T3 fibroblasts. J Physiol (Lond) 567, Garnovskaya MN, Mukhin YV, Vlasova TM, & Raymond JR (2003). Hypertonicity Activates Na+/H+ Exchange through Janus Kinase 2 and Calmodulin. J Biol Chem 278, Gautreau A, Poullet P, Louvard D, & Arpin M (1999). Ezrin, a plasma membrane-microfilament linker, signals cell survival through the phosphatidylinositol 3-kinase/Akt pathway. Proc Natl Acad Sci U S A. Gillis D, Shrode LD, Krump E, Howard CM, Rubie EA, Tibbles LA, Woodgett J, & Grinstein S (2001). Osmotic stimulation of the Na+/H+ exchanger NHE1: relationship to the activation of three MAPK pathways. J Membr Biol. 114
115 Goss GG, Jiang L, Vandorpe DH, Kieller D, Chernova MN, Robertson M, & Alper SL (2001). Role of JNK in hypertonic activation of Cl--dependent Na+/H+ exchange in Xenopus oocytes. Am J Physiol Cell Physiol 281, C1978-C1990. Gregory RI, Chendrimada TP, Cooch N, & Shiekhattar R (2005). Human RISC couples microrna biogenesis and posttranscriptional gene silencing. Cell. Grinstein S & Foskett JK (1990). Ionic mechanisms of cell volume regulation in leukocytes. Annu Rev Physiol. Grinstein S, Rotin D, & Mason MJ (1989). Na+/H+ exchange and growth factor-induced cytosolic ph changes. Role in cellular proliferation. Biochim Biophys Acta. Grinstein S, Woodside M, Sardet C, Pouyssegur J, & Rotin D (1992). Activation of the Na+/H+ antiporter during cell volume regulation. Evidence for a phosphorylation-independent mechanism. J Biol Chem 267, Gusella JF, Ramesh V, MacCollin M, & Jacoby LB (1999). Merlin: the neurofibromatosis 2 tumor suppressor. Biochim Biophys Acta. Hall A. Small GTP-binding proteins and the regulation of the actin cytoskeleton Ref Type: Generic Han J, Lee JD, Bibbs L, & Ulevitch RJ (1994). A MAP kinase targeted by endotoxin and hyperosmolarity in mammalian cells. Science. Han J, Lee JD, Jiang Y, Li Z, Feng L, & Ulevitch RJ (1996). Characterization of the Structure and Function of a Novel MAP Kinase Kinase (MKK6). J Biol Chem 271, Hansen MB, Nielsen SE, & Berg K (1989). Re-examination and further development of a precise and rapid dye method for measuring cell growth/cell kill. J Immunol Methods. Harborth J, Elbashir SM, Vandenburgh K, Manninga H, Scaringe SA, Weber K, & Tuschl T (2003). Sequence, chemical, and structural variation of small interfering RNAs and short hairpin RNAs and the effect on mammalian gene silencing. Antisense Nucleic Acid Drug Dev. Harper SJ & LoGrasso P (2001). Signalling for survival and death in neurones: the role of stress-activated kinases, JNK and p38. Cell Signal. Haworth RS, McCann C, Snabaitis AK, Roberts NA, & Avkiran M (2003). Stimulation of the Plasma Membrane Na+/H+ Exchanger NHE1 by Sustained Intracellular Acidosis: EVIDENCE FOR A NOVEL MECHANISM MEDIATED BY THE ERK PATHWAY. J Biol Chem 278,
116 Hayashi K, Yonemura S, Matsui T, & Tsukita S (1999). Immunofluorescence detection of ezrin/radixin/moesin (ERM) proteins with their carboxyl-terminal threonine phosphorylated in cultured cells and tissues. J Cell Sci 112, Henson JH. (1999). Relationships between the actin cytoskeleton and cell volume regulation. Microsc Res Tech. Hirao M, Sato N, Kondo T, Yonemura S, Monden M, Sasaki T, Takai Y, Tsukita S, & Tsukita S (1996). Regulation mechanism of ERM (ezrin/radixin/moesin) protein/plasma membrane association: possible involvement of phosphatidylinositol turnover and Rho-dependent signaling pathway. J Cell Biol 135, Hoffmann EK & Dunham PB. Membrane mechanisms and intracellular signalling in cell volume regulation Ref Type: Generic Hoffmann EK & Pedersen SF. Sensors and signal transduction in the activation of cell volume regulatory ion transport systems Ref Type: Generic Hoffmann EK. Intracellular transmission in cell volume regulation in Ehrlich ascites tumor cells Ref Type: Generic Hughes J, Bortner CD, Purdy GD, & Cidlowski JA (1997). Intracellular K+ Suppresses the Activation of Apoptosis in Lymphocytes. J Biol Chem 272, Ivetic A & Ridley AJ (2004). Ezrin/radixin/moesin proteins and Rho GTPase signalling in leucocytes. Immunology. Jin Z & El-Deiry WS (2005). Overview of cell death signaling pathways. Cancer Biol Ther. Karin M & Gallagher E (2005). From JNK to pay dirt: jun kinases, their biochemistry, physiology and clinical importance. IUBMB Life. Kennedy NJ & Davis RJ (2003). Role of JNK in tumor development. Cell Cycle. Kenneth R.Hallows, Foon-Yee Law, Charles H.Packman, & Philip A.Knauf (1995). Changes in cytoskeletal actin content, F-actin distribution, and surface morphology during HL-60 cell volume regulation. Journal of Cellular Physiology. Kenneth R.Hallows and Philip A.Knauf (1994). Principles of Cell Volume Regulation. 116
117 Kim DH, Behlke MA, Rose SD, Chang MS, Choi S, & Rossi JJ (2005). Synthetic dsrna Dicer substrates enhance RNAi potency and efficacy. Nat Biotechnol. Kim SJ, Hwang SG, Shin DY, Kang SS, & Chun JS (2002). p38 Kinase Regulates Nitric Oxide-induced Apoptosis of Articular Chondrocytes by Accumulating p53 via NFkappa B-dependent Transcription and Stabilization by Serine 15 Phosphorylation. J Biol Chem 277, Ko BCB, Lam AKM, Kapus A, Fan L, Chung SK, & Chung SSM (2002). Fyn and p38 Signaling Are Both Required for Maximal Hypertonic Activation of the Osmotic Response Element-binding Protein/Tonicityresponsive Enhancer-binding Protein (OREBP/TonEBP). J Biol Chem 277, Kurreck J. (2006). sirna Efficiency: Structure or Sequence-That Is the Question. Biomed Biotechnol. Kyriakis JM, App H, Zhang XF, Banerjee P, Brautigan DL, Rapp UR, & Avruch J (1992). Raf-1 activates MAP kinase-kinase. Nature. Kyriakis JM & Avruch J (2001). Mammalian Mitogen-Activated Protein Kinase Signal Transduction Pathways Activated by Stress and Inflammation. Physiol Rev 81, Lang F, Ritter M, Gamper N, Huber S, Fillon S, Tanneur V, Lepple-Wienhues A, & Szabo I GE (2000). Cell volume in the regulation of cell proliferation and apoptotic cell death. Cell Physiol Biochem. LANG FLOR, BUSCH GL, RITTER MARK, VOLKL HARA, WALDEGGER SIEG, GULBINS ERIC, & HAUSSINGER DIET (1998a). Functional Significance of Cell Volume Regulatory Mechanisms. Physiological Reviews 78, LANG FLOR, BUSCH GL, RITTER MARK, VOLKL HARA, WALDEGGER SIEG, GULBINS ERIC, & HAUSSINGER DIET (1998b). Functional Significance of Cell Volume Regulatory Mechanisms. Physiol Rev 78, Lee Anne McLean. From Gliomas to Corps: A role of the Na+/H+ Exchanger in regulation of intracellular ph Ref Type: Unpublished Work Lewis A, Di Ciano C, Rotstein OD, & Kapus A (2002). Osmotic stress activates Rac and Cdc42 in neutrophils: role in hypertonicity-induced actin polymerization. Am J Physiol Cell Physiol 282, C271-C279. Li X, Alvarez B, Casey JR, Reithmeier RAF, & Fliegel L (2002). Carbonic Anhydrase II Binds to and Enhances Activity of the Na+/H+ Exchanger. J Biol Chem 277, Lin X & Barber DL (1996). A calcineurin homologous protein inhibits GTPase-stimulated Na-H exchange. Proc Natl Acad Sci U S A. 117
118 Louvet-Vallee S. (2000). ERM proteins: from cellular architecture to cell signaling. Biol Cell. Mackay DJG, Esch F, Furthmayr H, & Hall A (1997). Rho- and Rac-dependent Assembly of Focal Adhesion Complexes and Actin Filaments in Permeabilized Fibroblasts: An Essential Role for Ezrin/Radixin/Moesin Proteins. J Cell Biol 138, Mangeat P, Roy C, & Martin M (1999). ERM proteins in cell adhesion and membrane dynamics. Trends Cell Biol. Maria Rasmussen RTABVDEKHAKaSFP. Osmotic cell shrinkage activates Ezrin/Radixin/Moesin (ERM) proteins: Activation mechanisms and physiological implications Ref Type: Unpublished Work Matsuda S, Kawasaki H, Moriguchi T, Gotoh Y, & Nishida E (1995). Activation of Protein Kinase Cascades by Osmotic Shock. J Biol Chem 270, Matsui T, Yonemura S, Tsukita S, & Tsukita S (1999). Activation of ERM proteins in vivo by Rho involves phosphatidyl-inositol 4-phosphate 5-kinase and not ROCK kinases. Curr Biol. Matsuyama S, Llopis J, Deveraux QL, Tsien RY, & Reed JC (2000). Changes in intramitochondrial and cytosolic ph: early events that modulate caspase activation during apoptosis. Nat Cell Biol. McLean LA, Zia S, Gorin FA, & Cala PM (1999). Cloning and expression of the Na+/H+ exchanger from Amphiuma RBCs: resemblance to mammalian NHE1. Am J Physiol Cell Physiol 276, C1025-C1037. McManus M, Fischbarg J, Sun A, Hebert S, & Strange K (1993). Laser light-scattering system for studying cell volume regulation and membrane transport processes. Am J Physiol Cell Physiol 265, C562-C570. Meier R, Thelen M, & Hemmings BA (1998). Inactivation and dephosphorylation of protein kinase Balpha (PKBalpha) promoted by hyperosmotic stress. EMBO J. Mills JW & Mandel LJ (1994). Cytoskeletal regulation of membrane transport events. FASEB J 8, Misik AJ, Perreault K, Holmes CF, & Fliegel L (2005). Protein phosphatase regulation of Na+/H+ exchanger isoform I. Biochemistry. Miyakawa H, Woo SK, Dahl SC, Handler JS, & Kwon HM (1999). Tonicity-responsive enhancer binding protein, a rel-like protein that stimulates transcription in response to hypertonicity. Proc Natl Acad Sci U S A. 118
119 Mongin AA & Orlov SN (2001). Mechanisms of cell volume regulation and possible nature of the cell volume sensor. Pathophysiology 2001 Dec;8(2): Moor AN & Fliegel L (1999). Protein Kinase-mediated Regulation of the Na+/H+ Exchanger in the Rat Myocardium by Mitogen-activated Protein Kinase-dependent Pathways. J Biol Chem 274, Morrison DK & Davis RJ (2003). Regulation of MAP kinase signaling modules by scaffold proteins in mammals. Annu Rev Cell Dev Biol. Mosmann T. (1983). Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods. Mukhin YV, Garnovskaya MN, Ullian ME, & Raymond JR. ERK Is Regulated by Sodium-Proton Exchanger in Rat Aortic Vascular Smooth Muscle Cells. Journal of Biological Chemistry 279[3], Ref Type: Motion Picture Nadkarni V, Gabbay KH, Bohren KM, & Sheikh-Hamad D (1999). Osmotic Response Element Enhancer Activity. REGULATION THROUGH p38 KINASE AND MITOGEN-ACTIVATED EXTRACELLULAR SIGNAL-REGULATED KINASE KINASE. J Biol Chem 274, Nakamura N, Oshiro N, Fukata Y, Amano M, Fukata M, Kuroda S, Matsuura Y, Leung T, Lim L, & Kaibuchi K (2000). Phosphorylation of ERM proteins at filopodia induced by Cdc42, Genes Cells. Negulescu PA & Machen TE (1990). Intracellular ion activities and membrane transport in parietal cells measured with fluorescent dyes. Methods Enzymol. Niggli V, Andreoli C, Roy C, & Mangeat P (1995). Identification of a phosphatidylinositol-4,5- bisphosphate-binding domain in the N-terminal region of ezrin. FEBS Lett. Nylandsted J, Jaattela M, Hoffmann EK, & Pedersen SF. Heat shock protein 70 inhibits shrinkage-induced programmed cell death via mechanisms independent of effects on cell volume-regulatory membrane transport proteins Ref Type: Unpublished Work O'Neill WC (1999). Physiological significance of volume-regulatory transporters. Am J Physiol Cell Physiol 276, C Okada Y & Maeno E (2001). Apoptosis, cell volume regulation and volume-regulatory chloride channels. Comp Biochem Physiol A Mol Integr Physiol. 119
120 Okada Y. (2004). Ion channels and transporters involved in cell volume regulation and sensor mechanisms. Cell Biochem Biophys. Orlowski J & Grinstein S (2004). Diversity of the mammalian sodium/proton exchanger SLC9 gene family. Pflugers Arch. Ozkan P & Mutharasan R (2002). A rapid method for measuring intracellular ph using BCECF-AM. Biochim Biophys Acta. Padda R, Wamsley-Davis A, Gustin MC, Ross R, Yu C, & Sheikh-Hamad D (2006). MEKK3-mediated signaling to p38 kinase and TonE in hypertonically stressed kidney cells. Am J Physiol Renal Physiol 291, F874-F881. Paddock SW. (1999). Confocal laser scanning microscopy. Biotechniques. Pages G, L'Allemain G, Chambard JC, Meloche S, Pouyssegur J, & Lenormand P (1993). Mitogen-activated protein kinases p42mapk and p44mapk are required for fibroblast proliferation. Proc Natl Acad Sci U S A. Papakonstanti EA, Vardaki EA, & Stournaras C (2000). Actin cytoskeleton: a signaling sensor in cell volume regulation. Cell Physiol Biochem. Patricia Hess, German Pihan, Charles L.Sawyers, Richard A.Flavell, & Roger J.Davis (2002). Survival signaling mediated by c-jun NH2-terminal kinase in transformed B lymphoblasts. Nature. Pearson MA, Reczek D, Bretscher A, & Karplus PA (2000). Structure of the ERM protein moesin reveals the FERM domain fold masked by an extended actin binding tail domain. Cell. Pedersen SF & Cala PM (2004). Comparative biology of the ubiquitous Na+/H+ exchanger, NHE1: lessons from erythrocytes. J Exp Zoolog A Comp Exp Biol. Pedersen SF, Darborg BV, Rasmussen M, Hoffmann EK, & Nylandsted J. The Na+/H+ exchanger, NHE1, differentially regulates mitogen-activated protein kinase subfamilies after osmotic shrinkage in Ehrlich Lettre Ascites cells Ref Type: Generic Pedersen SF & Hoffmann EK. Possible interrelationship between changes in F-actin and myosin II, protein phosphorylation, and cell volume regulation in Ehrlich ascites tumor cells Ref Type: Generic Pedersen SF, Hoffmann EK, & Mills JW. The cytoskeleton and cell volume regulation Ref Type: Generic 120
121 Pedersen SF, Jorgensen NK, Damgaard I, Schousboe A, & Hoffmann EK (1998). Mechanisms of phi regulation studied in individual neurons cultured from mouse cerebral cortex. J Neurosci Res. Pedersen SF, Kramhoft B, Jorgensen NK, & Hoffmann EK (1996). Shrinkage-induced activation of the Na+/H+ exchanger in Ehrlich ascites tumor cells: mechanisms involved in the activation and a role for the exchanger in cell volume regulation. J Membr Biol. Pedersen SF. (2006). The Na(+)/H (+) exchanger NHE1 in stress-induced signal transduction: implications for cell proliferation and cell death. Pflugers Arch 2006 Jun;452(3): Epub 2006 Apr 4. Pedersen SF (2006). The Na(+)/H (+) exchanger NHE1 in stress-induced signal transduction: implications for cell proliferation and cell death. Pflugers Arch. Pedersen SF, Hoffmann EK, & Mills JW (2001). The cytoskeleton and cell volume regulation. Comp Biochem Physiol A Mol Integr Physiol 130, Pedersen SF, Mills JW, & Hoffmann EK (1999). Role of the F-actin Cytoskeleton in the RVD and RVI Processes in Ehrlich Ascites Tumor Cells. Experimental Cell Research 252, Pedersen SF, Beisner KH, Hougaard C, Willumsen BM, Lambert IH, & Hoffmann EK (2002). Rho family GTP binding proteins are involved in the regulatory volume decrease process in NIH3T3 mouse fibroblasts. J Physiol (Lond) 541, Pouyssegur J, Volmat V, & Lenormand P (2002). Fidelity and spatio-temporal control in MAP kinase (ERKs) signalling. Biochem Pharmacol. Putney LK, Denker SP, & Barber DL (2002). The changing face of the Na+/H+ exchanger, NHE1: structure, regulation, and cellular actions. Annu Rev Pharmacol Toxicol. Raingeaud J, Whitmarsh AJ, Barrett T, Derijard B, & Davis RJ (1996). MKK3- and MKK6-regulated gene expression is mediated by the p38 mitogen- activated protein kinase signal transduction pathway. Mol Cell Biol 16, Rasmussen M, Todd Alexander, Barbara V.Darborg, Else K.Hoffmann, & Andras Kapus and Stine F.Pedersen. Osmotic cell shrinkage activates Ezrin/Radixin/Moesin (ERM) proteins: Activation mechanisms and physiological implications Ref Type: Unpublished Work Reczek D & Bretscher A (1998). The Carboxyl-terminal Region of EBP50 Binds to a Site in the Aminoterminal Domain of Ezrin That Is Masked in the Dormant Molecule. J Biol Chem 273,
122 Rentsch M, Hoffmann EK, & Pedersen SF. Effects of chemical anoxia on NHE1, p38 MAPK, p53, Akt/PKB and ERM proteins in NIH3T3 mouse fibroblasts: evidence for a role of NHE1 upstream of p38 MAPK Ref Type: Generic Ridley AJ & HallA (1994). Signal transduction pathways regulating Rho-mediated stress fibre formation: requirement for a tyrosine kinase. EMBO J. Ritter M, Fuerst J, Woll E, Chwatal S, Gschwentner M, Lang F, Deetjen P, & Paulmichl M (2001). Na(+)/H(+)exchangers: linking osmotic dysequilibrium to modified cell function. Cell Physiol Biochem. Roger F, Martin PY, Rousselot M, Favre H, & Feraille E (1999). Cell Shrinkage Triggers the Activation of Mitogen-activated Protein Kinases by Hypertonicity in the Rat Kidney Medullary Thick Ascending Limb of the Henle's Loop. REQUIREMENT OF p38 KINASE FOR THE REGULATORY VOLUME INCREASE RESPONSE. J Biol Chem 274, S.F.Pedersen, M.E.O'Donnell, & S.E.Anderson and P.M.Cala (2006). Physiology and pathophysiology of Na+/H+ exchange and Na +-K+-2Cl cotransport in the heart, brain, and blood. Am J Physiol Regulatory Integrative Comp Physiol. S.F.Pedersen C.Varming STCEH2 (2002). Mechanism of activation of NHE by Cell Shrinkage and by Calyculin A in Erlich Ascites Tumor cells. J Memb biol. Sabapathy K, Hochedlinger K, Nam SY, Bauer A, Karin M, & Wagner EF (2004). Distinct roles for JNK1 and JNK2 in regulating JNK activity and c-jun-dependent cell proliferation. Mol Cell. Sanchez-Prieto R, Rojas JM, Taya Y, & Gutkind JS (2000). A Role for the p38 Mitogen-activated Protein Kinase Pathway in the Transcriptional Activation of p53 on Genotoxic Stress by Chemotherapeutic Agents. Cancer Res 60, Saotome I, Curto M, & McClatchey AI (2004). Ezrin is essential for epithelial organization and villus morphogenesis in the developing intestine. Dev Cell. Sarkadi B & Parker JC (1991). Activation of ion transport pathways by changes in cell volume. Biochim Biophys Acta. Sasaki T & Takai Y (1998). The Rho small G protein family-rho GDI system as a temporal and spatial determinant for cytoskeletal control. Biochem Biophys Res Commun. Sato N, Funayama N, Nagafuchi A, Yonemura S, Tsukita S, & Tsukita S (1992). A gene family consisting of ezrin, radixin and moesin. Its specific localization at actin filament/plasma membrane association sites. J Cell Sci 103,
123 Schmidt A & Hall MN (1998). Signaling to the actin cytoskeleton. Annu Rev Cell Dev Biol 1998;14: Segal MS & Beem E (2001). Effect of ph, ionic charge, and osmolality on cytochrome c-mediated caspase-3 activity. Am J Physiol Cell Physiol 281, C1196-C1204. Shaw RJ, Henry M, Solomon F, & Jacks T (1998). RhoA-Dependent Phosphorylation and Relocalization of ERM Proteins into Apical Membrane/Actin Protrusions in Fibroblasts. Mol Biol Cell 9, Sheikh-Hamad D & Gustin MC (2004). MAP kinases and the adaptive response to hypertonicity: functional preservation from yeast to mammals. Am J Physiol Renal Physiol 287, F1102-F1110. Shinya Inoue (1995). foundations of confocal scanned imaging in light microspopy. Shrode LD, Rubie EA, Woodgett JR, & Grinstein S (1997). Cytosolic Alkalinization Increases Stressactivated Protein Kinase/c-Jun NH2-terminal Kinase (SAPK/JNK) Activity and p38 Mitogen-activated Protein Kinase Activity by a Calcium-independent Mechanism. J Biol Chem 272, Simchowitz L & Roos A (1985). Regulation of intracellular ph in human neutrophils. J Gen Physiol 85, Stine Falsig Pedersen, Barbara Vasek Darborg, Maria Rasmussen, Jesper Nylandsted, & Else Kay Hoffmann. The Na + /H + exchanger, NHE1, differentially regulates mitogen-activated protein kinase subfamilies after osmotic shrinkage in Ehrlich Lettre Ascites cells Ref Type: Generic Stossel TP (1989). From signal to pseudopod. How cells control cytoplasmic actin assembly. J Biol Chem 264, Strange K (2004). Cellular volume homeostasis. Advan Physiol Edu 28, Takahashi K, Sasaki T, Mammoto A, Hotta I, Takaishi K, Imamura H, Nakano K, Kodama A, & Takai Y. Interaction of radixin with Rho small G protein GDP/GTP exchange protein Dbl Ref Type: Generic Takahashi E, Abe Ji, Gallis B, Aebersold R, Spring DJ, Krebs EG, & Berk BC (1999). p90rsk Is a Serumstimulated Na+/H+ Exchanger Isoform-1 Kinase. REGULATORY PHOSPHORYLATION OF SERINE 703 OF Na+/H+ EXCHANGER ISOFORM-1. J Biol Chem 274, Takahashi K, Sasaki T, Mammoto A, Takaishi K, Kameyama T, Tsukita S, Tsukita S, & Takai Y (1997). Direct Interaction of the Rho GDP Dissociation Inhibitor with Ezrin/Radixin/Moesin Initiates the Activation of the Rho Small G Protein. J Biol Chem 272,
124 Takaishi K, Matozaki T, Nakano K, & Takai Y (2000). Multiple downstream signalling pathways from ROCK, a target molecule of Rho small G protein, in reorganization of the actin cytoskeleton in Madin-Darby canine kidney cells. Genes Cells. Takeuchi K, Sato N, Kasahara H, Funayama N, Nagafuchi A, Yonemura S, Tsukita S, & Tsukita S (1994). Perturbation of cell adhesion and microvilli formation by antisense oligonucleotides to ERM family members. J Cell Biol 125, Tauer U (2002). Advantages and risks of multiphoton microscopy in physiology. Exp Physiol 87, Tilly BC, Edixhoven MJ, Tertoolen LG, Morii N, Saitoh Y, Narumiya S, & de Jonge HR (1996). Activation of the osmo-sensitive chloride conductance involves P21rho and is accompanied by a transient reorganization of the F-actin cytoskeleton. Mol Biol Cell. Tominaga T, Ishizaki T, Narumiya S, & Barber DL. p160rock mediates RhoA activation of Na-H exchange Ref Type: Generic Tominaga T & Barber DL (1998). Na-H Exchange Acts Downstream of RhoA to Regulate Integrin-induced Cell Adhesion and Spreading. Mol Biol Cell 9, Tsien RY. (1989). Fluorescent probes of cell signaling. Annu Rev Neurosci. Tsukita S & Yonemura S (1997). ERM (ezrin/radixin/moesin) family: from cytoskeleton to signal transduction. Curr Opin Cell Biol. Tsukita S, Oishi K, Sato N, Sagara J, Kawai A, & Tsukita S (1994). ERM family members as molecular linkers between the cell surface glycoprotein CD44 and actin-based cytoskeletons. J Cell Biol 126, Tsukita S & Yonemura S (1999). Cortical Actin Organization: Lessons from ERM (Ezrin/Radixin/Moesin) Proteins. J Biol Chem 274, Turunen O, Wahlstrom T, & Vaheri A (1994). Ezrin has a COOH-terminal actin-binding site that is conserved in the ezrin protein family. J Cell Biol 126, Uhlik MT, Abell AN, Johnson NL, Sun W, Cuevas BD, Lobel-Rice KE, Horne EA, Dell'Acqua ML, & Johnson GL (2003). Rac-MEKK3-MKK3 scaffolding for p38 MAPK activation during hyperosmotic shock. Nat Cell Biol. Vaheri A, Carpen O, Heiska L, Helander TS, Jaaskelainen J, Majander-Nordenswan P, Sainio M TT, & Turunen O (1997). The ezrin protein family: membrane-cytoskeleton interactions and disease associations. Curr Opin Cell Biol. 124
125 Wakabayashi S, Sardet C, Fafournoux P, Counillon L, Meloche S, & Pages G PJ (1992). Structure function of the growth factor-activatable Na+/H+ exchanger (NHE1). Rev Physiol Biochem Pharmacol. Wakabayashi S, Bertrand B, Ikeda T, Pouyssegur J, & Shigekawa M (1994). Mutation of calmodulin-binding site renders the Na+/H+ exchanger (NHE1) highly H(+)-sensitive and Ca2+ regulation-defective. J Biol Chem 269, Wakabayashi S, Shigekawa M, & Pouyssegur J (1997). Molecular physiology of vertebrate Na+/H+ exchangers. Physiol Rev 77, Wakabayashi S, Pang T, Su X, & Shigekawa M (2000). A Novel Topology Model of the Human Na+/H+ Exchanger Isoform 1. J Biol Chem 275, Werry TD, Christopoulos A, & Sexton PM (2006). Mechanisms of ERK1/2 regulation by seventransmembrane-domain receptors. Curr Pharm Des. Widmann C.H.R.I., Gibson S.P.E.N., Jarpe Mathew B, & Johnson Gary L (1999). Mitogen-Activated Protein Kinase: Conservation of a Three-Kinase Module From Yeast to Human. Physiol Rev 79, William T.Arthur, Leslie A, & Petch and Keith Burridge (2000). Integrin engagement suppresses RhoA activity via a c-src-dependent mechanism. Curr Biol. Woo SK, Lee SD, & Kwon HM (2002). TonEBP transcriptional activator in the cellular response to increased osmolality. Pflugers Arch. Wright SJ & Wright DJ (2002). Introduction to confocal microscopy. Methods Cell Biol. Wu KL, Khan S, Lakhe-Reddy S, Jarad G, Mukherjee A, Obejero-Paz CA, Konieczkowski M, Sedor JR, & Schelling JR (2004). The NHE1 Na+/H+ Exchanger Recruits Ezrin/Radixin/Moesin Proteins to Regulate Akt-dependent Cell Survival. J Biol Chem 279, Wu KL, Khan S, Lakhe-Reddy S, Wang L, Jarad G, Miller RT, Konieczkowski M, Brown AM, Sedor JR, & Schelling JR (2003). Renal tubular epithelial cell apoptosis is associated with caspase cleavage of the NHE1 Na+/H+ exchanger. Am J Physiol Renal Physiol 284, F829-F839. Yan C, Luo H, Lee JD, Abe Ji, & Berk BC (2001a). Molecular Cloning of Mouse ERK5/BMK1 Splice Variants and Characterization of ERK5 Functional Domains. J Biol Chem 276, Yan W, Nehrke K, Choi J, & Barber DL (2001b). The Nck-interacting Kinase (NIK) Phosphorylates the Na+-H+ Exchanger NHE1 and Regulates NHE1 Activation by Platelet-derived Growth Factor. J Biol Chem 276,
126 Yonemura S, Matsui T, Tsukita S, & Tsukita S (2002). Rho-dependent and -independent activation mechanisms of ezrin/radixin/moesin proteins: an essential role for polyphosphoinositides in vivo. J Cell Sci 115, Yoon S & Seger R (2006). The extracellular signal-regulated kinase: multiple substrates regulate diverse cellular functions. Growth Factors. Yoshimi Takai & Takuya Sasaki and Takashi Matozaki (2001). Small GTP-Binding Proteins. Physiol Rev. Zhu Y, Mao XO, Sun Y, Xia Z, & Greenberg DA (2002). p38 Mitogen-activated Protein Kinase Mediates Hypoxic Regulation of Mdm2 and p53 in Neurons. J Biol Chem 277, Zhuang S, Hirai SI, & Ohno S (2000). Hyperosmolality induces activation of cpkc and npkc, a requirement for ERK1/2 activation in NIH/3T3 cells. Am J Physiol Cell Physiol 278, C102-C109. Zigmond SH. (1996). Signal transduction and actin filament organization. Curr Opin Cell Biol. 126
127 9 Stjerneartikler (Denker SP et al., 2000) (Wu et al., 2004) (Pedersen SF et al., 2007) (Di Ciano et al., 2002) (Else K.Hoffmann & Stine F.Pedersen, 2006) (Gillis D et al., 2001) (Pedersen SF et al., 2001) (Sheikh-Hamad & Gustin, 2004) (Shrode et al., 1997) (Bretscher A et al., 2000) 127
128 10 Appendiks 10.1 Materialer RPMI medium (Sigma, kat. Nr. R8758) a-minimal essential medium (Invitrogen, Gibco, kat. nr ) Pen/Strep (penicillin/streptomycin) (Invitrogen, Gibco, kat. nr ) FBS (føtal bovin serum) (Invitrogen, Gibco, kat. nr ) G418-sulfat (Gibco BRL, Invitrogen, Carlsbad, CA) L-glutamin (Invitrogen, Gibco, kat. nr ) Trypsin (Invitrogen, kat. nr ) Reagent A (Biorad. Kat. nr ) Reagent S (Biorad. Kat. nr ) Reagent B, (Biorad. Kat. nr ) loadingbuffer (Invitrogen, kat. nr. LC56771) DTT (Invitrogen, kat. nr. D1532) Bis-Tris-geler (Invitrogen, kat.nr. NPO302BOX) Runningbuffer (Nupage MOPS SDS Running buffer 20XStock (Invitrogen, kat.nr. NP0001)) Transferbuffer (Invitrogen, kat.nr. NP0006) Antioxidant (Invitrogen, kat.nr. NP0005) Kb plus DNA ladder (Invitrogen, kat nr ). 2,7 -bis-(2-carboxyethyl)-5,6 Carboxyfluorescein, tetraacetoxymethylester (BCECF-AM), Molecular Probes. Katalog Nummer - B3051 MTT (3,(4,5-dimethylthiazol-2 yl)2,5-diphenyl-tetrazolium bromide) (Sigma, kat.nr. M6555) RNA oprensningskit er et Qiagen RNeasy protect mini Kit, kat. nr Rho aktiveringskit er fra Cytoskeleton, Kat. nr. BK
129 10.2 Opløsninger Stamopløsning I (stam I) 83,56 g NaCl 3,72 g KCl 2,46 g MgSO 4, 7H 2 O Tilsæt ddh 2 O til 1000 ml Stamopløsning II (stam II) 1,78 g Na 2 HPO 4, 2H 2 O Tilsæt ddh 2 O til 100 ml KCL ringer 78 ml 1 M KCL 5 ml 100 mm MgSO 4 5 ml 100 mm CaCl 2 5 ml 100 mm K 2 HPO 4 5 ml MTH Justér ph til 7.4 med KOH. Tilsæt ddh 2 O til 500 ml Stamopløsning III (stam III) 1,47 g CaCl 2 * 2H 2 O Tilsæt ddh 2 O til 100 ml Isoton ringer 600 ml H 2 O 100 ml Stam I 10 ml Stam II 10 ml Stam III 10 ml MTH Indstil ph til 7,4. Tilsæt ddh 2 O til 1000 ml Opløsninger til AP1 celler Isoton Ringer 130 mm NaCl 3 mm KCl 20 mm Hepes 1 mm MgCl mm CaCl 2 10 mm NaOH 10 mm Glucose Justér til ph 7.4 Tilsæt ddh 2 O til 2000 ml Hyperton ringer (1X) 600 ml H 2 O 100 ml Stam I 10 ml Stam II 5 ml Stam III 5 ml MTH Indstil ph til 7,4. Tilsæt ddh 2 O til 1000 ml Hyperton Ringer 275 mm NaCl 3 mm KCl 20 mm Hepes 1 mm MgCl mm CaCl 2 10 mm NaOH Justér til ph 7.4 Tilsæt ddh 2 O til 500 ml 129
130 MTH 6.9 g MOPS 7.56 g TES g HEPES Tilsæt ddh 2 O til 100 ml TBS 150 mm NaCl 1 mm MgCl 2 1 mm EGTA 10 mm Tris/HCl Justér til ph 7.3 med NaOH Tilsæt ddh 2 O til 1000 ml Lysisbuffer 1% SDS 10 mm Tris ph 7.5 ddh 2 O MTT 50 mg MTT 10 ml PBS PBS 16,000 g NaCl 0,400 g KCl 2,300 g Na 2 HPO 4 0,400 g KH 2 PO 4 Indstil ph til 7.4. Tilsæt ddh 2 O til 2000ml Monterings forsegling 0.1 g N-propyl-galleat fra Sigma 4.5 ml glycerol 500 µl 10 x PBS Tilsæt ddh 2 O til 5 ml Solubiliseringsbuffer 0.01 M HCl SDS MOPS 10 mm MOPS 5 mm EGTA 20 mm K 2 HPO 4 2 mm MgSO 4 130
131 10.3 Antistoffer De primære antistoffers data (baseret på fabrikantens oplysninger) Produkt Molekylevægt Epitop Fortyndingsforhold Producent Kat. nr. Monoklonalt kda Thr567 1:1000 Sigma E8897 anti-ezrin p-jnk 46 og 52 kda Thr183 1:100 Santa cruz Sc-6254 and Tyr185 p-p38 38 kda Thr 180 1:200 Cell 9211 Tyr 182 Signaling Technoloky, Inc. ERK1/2 og kda fosforyleret 1:100 Cell 9102 perk1/2 Thr202 / Signaling 9106 Tyr204 Technoloky, peptidsekv Inc. ens P-MEK1/ kda Ser217/221 1:200 Cell Signaling (Beverly, MA), 9121 p-mkk3/ kda Ser189/207 1:200 Cell Signaling (Beverly, MA), 9231 RhoA 20 kda 1:500 Cytoskeleton ARH01 p-nhe1 100 kda 1:1000 Gave fra Peter Cala, Uni. of California Davis Phospho- ERM kda Syntetisk fosforyleret Thr567/ Thr564 / Thr558 peptidsekv ens ERM kda Thr567/ Thr564 / Thr558 peptidsekv ens 1:1000 Cell Signaling Technoloky, Inc. 1:1000 Cell Signaling Technoloky, Inc Sekundære antistoffer Ged- anti kanin (Jackson ImmunoResearch, kat. Nr ) Ged-anti mus (Jackson ImmunoResearch, kat. Nr ) Cy3 konjugeret ged-antikanin (Jackson ImmunoResearch, kat. Nr ) FITC-konjugeret anti mus (Jackson ImmunoResearch, kat. Nr ) 131
132 10.4 Hæmmere SB Calbiochem Kat. No SP Calbiochem Kat. No PD98059 Calbiochem Kat. No Y27632 Calbiochem Kat. No Wortmannin Sigma-Aldrich W (N-ethyl-Nisopropyl)amiloride (EIPA) er fra Molecular Probes (Leiden, the Netherlands) 10.5 sirna Monoclonal anti-ezrin clone 3C12 (Lot# 054K4764) (Sigma-aldrich). MWG-Biotech AG Desalted, annealed, 21-bp sirna duplexes med 2-nt overhæng er fra Dharmacon RNA Technologies (Lafayette, CO, USA). Mål sekvensen for ezrin er 5 -CAAGAAGGCACCUGACUUU-3, hvilket svarer til position i muse ezrin. Kontrol sirna ( 5-AGG UAG UGU AAU CGC CUU GTT -3 ) (Lot# /1) MWG-Biotech AG. Et 47 % GC-matchende kontrol 21 bp oligomer, fra Dharmacon, blev brugt som kontrol Primere Primere der er blevet brugt under forsøgene er købt fra Invitrogen Inc, Burlingame, CA, USA.: Mouse radixin (fw 835- GGCCTGAATATTTATGAACA, rv AGCTCTTCCTTTTCACGTTC) mouse moesin (fw TGCTCTCCTGGAAAATGAGA, rv CGAGAAGCCTGCAGCA) ezrin mouse (fw ACAGCAGTTGGAAACCG, rv GGCCTCCAGACGTTCAG) mouse merlin (fw 603- GAGCCAGGGATGAAGCT, rv TCTTGTACGCTCGGCCT) NHE1 (fw CTGTGGTCATTATGGCC, rv TGGGTTCATAGGCCAGT) NHE2 (fw CAGCAAGCTGTCAGTGA, rv TCGGGAGGTTGAAGTGG) NHE3 (fw TTCGACCACATCCTCTC, rv TCCTGGTCCTGTTTCTC) NHE4 (fw ACTAATCGCCTTCACTA, rv GATGGAGAAGGGGAAAG) NHE8 (fw GCTGAAGGTCTAACAAGAAA, rv AGAAGTTCAGCAGGTAGGAC) 370 bp 263 bp 213 bp 460 bp ~ 500 bp ~ 500 bp ~ 500 bp ~ 500 bp ~ 500 bp 132
133 10.7 PUBLIKATIONER Abstrakt til Sandbjerg mode, Maj
134 Abstrakt til Experimental Biology konference i Washington DC, April Osmotic cell shrinkage activates ezrin/radixin/moesin (ERM) proteins: Activation mechanisms and physiological implications M. Rasmussen 1, T. Alexander 2, B. Darborg 1, A. Kapus 3, S.F. Pedersen 1,* 1 Dept. of Molecular Biology, University of Copenhagen, DK-2100 Copenhagen, Denmark, 2 Hospital for Sick Children and 3 St. Michaels Hospital Research Institute, University of Toronto, Ontario M5G 1X8, Canada Osmotic cell shrinkage elicits multiple cellular events, including rapid cytoskeletal reorganization, activation of Na + /H + exchanger isoform 1 (NHE1), and, on a longer time scale, programmed cell death. Here, we evaluated the role of ezrin/radixin/moesin (ERM) proteins in these processes. Osmotic shrinkage of Ehrlich Lettre ascites (ELA) cells elicited rapid translocation of ERM proteins to the cell cortex and long microvilli-like protrusions, and Thr 567/564/558 (ezrin/radixin/moesin) phosphorylation of cortical ERM proteins. Shrinkage-induced ERM protein activation was prevented by PtdIns(4,5)P 2 depletion, yet was unaffected by NHE1 inhibition by EIPA, and did not require the presence of NHE1 (as evaluated in AP1 cells +/- human NHE1). Constitutively active RhoA increased basal and shrinkageinduced ERM protein phosphorylation, yet the relative shrinkage-induced increase was unaffected. Ezrin knockdown by sirna increased shrinkage-induced NHE1 activity by about 25%, and appeared to partially prevent the shrinkage-induced formation/elongation of microvilli-like protrusions. In contrast, shrinkage-induced cell death was unaffected by ezrin knockdown. In conclusion, ERM proteins are activated by osmotic shrinkage in a PtdIns(4,5)P 2 -dependent, NHE1-independent manner, and this in turn negatively regulates NHE1 and may contribute to F-actin rearrangement in the shrunken cells. 134
135 Reference Liste Aharonovitz O, Zaun HC, Balla T, York JD, Orlowski J, & Grinstein S (2000). Intracellular ph Regulation by Na+/H+ Exchange Requires Phosphatidylinositol 4,5-Bisphosphate. J Cell Biol 150, Alexander RT & Grinstein S. (2006). Na+/H+ exchangers and the regulation of volume. Acta Physiol (Oxf). Aronson PS, Nee J, & Suhm MA. Modifier role of internal H+ in activating the Na+-H+ exchanger in renal microvillus membrane vesicles. Nature Ref Type: Abstract Aspenstrom P. (1999). Effectors for the Rho GTPases. Curr Opin Cell Biol. Bachmeier CJ, Trickler WJ, & Miller DW (2004). Drug efflux transport properties of 2',7'-bis(2- carboxyethyl)-5(6)-carboxyfluorescein acetoxymethyl ester (BCECF-AM) and its fluorescent free acid, BCECF. J Pharm Sci. Barbara Vasek Darborg. Skrumpningsinduceret regulering af celledød og overlevelsesveje i EATC: mulige roller for NHE1 og NKCC Ref Type: Unpublished Work Barbara Vasek Darborg, Else Kay Hoffmann, & Stine Falsig Pedersen. Causal relationship between NHE1, NKCC1, MAPKs and ERM proteins after osmotic shrinkage in Ehrlich Lettre mouse ascites tumor cells. The FASEB Journal Ref Type: Abstract Barret C, Roy C, Montcourrier P, Mangeat P, & Niggli V (2000). Mutagenesis of the Phosphatidylinositol 4,5-Bisphosphate (PIP2) Binding Site in the NH2-Terminal Domain of Ezrin Correlates with Its Altered Cellular Distribution. J Cell Biol 151, Baumgartner M, Sillman AL, Blackwood EM, Srivastava J, Madson N, Schilling JW, Wright JH, & Barber DL (2006). The Nck-interacting kinase phosphorylates ERM proteins for formation of lamellipodium by growth factors. PNAS 103, Berg JM, Tymoczko JL, & and Stryer L (2002). Biochemistry fifth edition. 135
136 Bertrand B, Wakabayashi S, Ikeda T, Pouyssegur J, & Shigekawa M (1994). The Na+/H+ exchanger isoform 1 (NHE1) is a novel member of the calmodulin-binding proteins. Identification and characterization of calmodulin-binding sites. J Biol Chem 269, Bhattacharya M, Babwah AV, & Ferguson SS (2004). Small GTP-binding protein-coupled receptors. Biochem Soc Trans. Bianchini L, L'Allemain G, & Pouyssegur J (1997). The p42/p44 Mitogen-activated Protein Kinase Cascade Is Determinant in Mediating Activation of the Na+/H+ Exchanger (NHE1 Isoform) in Response to Growth Factors. J Biol Chem 272, Bishop AL & Hall A (2000). Rho GTPases and their effector proteins. Biochem J. Boens N, Qin W, Basaric N, Orte A, Talavera EM, & Alvarez-Pez JM (2006). Photophysics of the fluorescent ph indicator BCECF. J Phys Chem A Mol Spectrosc Kinet Environ Gen Theory. Bortner CD & Cidlowski JA (1998). A necessary role for cell shrinkage in apoptosis. Biochem Pharmacol. Boyarsky G, Ganz MB, Sterzel RB, & Boron WF (1988). ph regulation in single glomerular mesangial cells. I. Acid extrusion in absence and presence of HCO3-. Am J Physiol Cell Physiol 255, C844-C856. Bretscher A, Chambers D, Nguyen R, & Reczek D. (2000). ERM-Merlin and EBP50 protein families in plasma membrane organization and function. Annu Rev Cell Dev Biol. Bretscher A, Edwards K, & Fehon RG (2002). ERM proteins and merlin: integrators at the cell cortex. Nat Rev Mol Cell Biol. Bretscher A. (1999). Regulation of cortical structure by the ezrin-radixin-moesin protein family. Curr Opin Cell Biol. Bretscher A (1983). Purification of an 80,000-dalton protein that is a component of the isolated microvillus cytoskeleton, and its localization in nonmuscle cells. J Cell Biol 97, Bretscher A, Reczek D, & Berryman M (1997). Ezrin: a protein requiring conformational activation to link microfilaments to the plasma membrane in the assembly of cell surface structures. J Cell Sci 110, Brett CL, Donowitz M, & Rao R (2005). Evolutionary origins of eukaryotic sodium/proton exchangers. Am J Physiol Cell Physiol 288, C223-C
137 Brewster JL, de Valoir T, Dwyer ND, Winter E, & Gustin MC (2006). An osmosensing signal transduction pathway in yeast. Science. Burg MB, Kwon ED, & Kultz D (1997). Regulation of gene expression by hypertonicity. Annu Rev Physiol. Burg MB, Kwon ED, & Kultz D (1996). Osmotic regulation of gene expression. FASEB J 10, Burridge K & Wennerberg K (2004). Rho and Rac take center stage. Cell. Burton JD. (2005). The MTT assay to evaluate chemosensitivity. Methods Mol Med. C.Di Ciano-Oliveira, A.C.P.Thirone, & K.Szászi and A.Kapus (2006). Osmotic stress and the cytoskeleton: the R(h)ole of Rho GTPases. Acta Physiologica. Cala PM (1980). Volume regulation by Amphiuma red blood cells. The membrane potential and its implications regarding the nature of the ion-flux pathways. J Gen Physiol 76, Cala PM & Maldonado HM (1994). ph regulatory Na/H exchange by Amphiuma red blood cells. J Gen Physiol 103, Cantiello HF. (1997). Role of actin filament organization in cell volume and ion channel regulation. J Exp Zool. Cheng JC, Moore TB, & Sakamoto KM (2003). RNA interference and human disease. Mol Genet Metab. Ciano-Oliveira CD, Sirokmany G, Szaszi K, Arthur WT, Masszi A, Peterson M, Rotstein OD, & Kapus A (2003). Hyperosmotic stress activates Rho: differential involvement in Rho kinase-dependent MLC phosphorylation and NKCC activation. Am J Physiol Cell Physiol 285, C555-C566. Dahl SC, Handler JS, & Kwon HM (2001). Hypertonicity-induced phosphorylation and nuclear localization of the transcription factor TonEBP. Am J Physiol Cell Physiol 280, C248-C253. DeMali KA, Wennerberg K, & Burridge K (2003). Integrin signaling to the actin cytoskeleton. Curr Opin Cell Biol. Denker SP, Huang DC, Orlowski J, Furthmayr H, & Barber DL. (2000). Direct binding of the Na--H exchanger NHE1 to ERM proteins regulates the cortical cytoskeleton and cell shape independently of H(+) translocation. Mol Cell. 137
138 Denker SP og Barber (2002). Ion transport proteins anchor and regulate the cytoskeleton. Curr Opin Cell Biol. Di Ciano C, Nie Z, Szaszi K, Lewis A, Uruno T, Zhan X, Rotstein OD, Mak A, & Kapus A (2002). Osmotic stress-induced remodeling of the cortical cytoskeleton. Am J Physiol Cell Physiol 283, C850- C865. Di Ciano-Oliveira C TASKKA (2006). Osmotic stress and the cytoskeleton: the R(h)ole of Rho GTPases. Acta Physiol (Oxf). Dissing S and Gasbjerg PK (1993). Basic principles behind the application of flourescent dyes for the study of cellular electrolyte concentrations, membrane potential and microenviroment. Dogra C.Changotra, Wergedal JE, & Kumar A (2006). Regulation of phosphatidylinositol 3-kinase (PI3K)/Akt and nuclear factor-kappa B signaling pathways in dystrophin-deficient skeletal muscle in response to mechanical stretch. J Cell Physiol. Downward J. (2004). PI 3-kinase, Akt and cell survival. Semin Cell Dev Biol. Elbashir SM, Harborth J, Weber K, & Tuschl T (2002). Analysis of gene function in somatic mammalian cells using small interfering RNAs. Methods. Else K.Hoffmann & Stine F.Pedersen (2006). Sensors and signal transduction pathways in vertebrate cell volume regulation. Karger. Fievet BT, Gautreau A, Roy C, Del Maestro L, Mangeat P, Louvard D, & Arpin M (2004). Phosphoinositide binding and phosphorylation act sequentially in the activation mechanism of ezrin. J Cell Biol 164, Fliegel L. (2005). The Na+/H+ exchanger isoform 1. Int J Biochem Cell Biol. Friis MB, Friborg CR, Schneider L, Nielsen MB, Lambert IH, Christensen ST, & Hoffmann EK (2005). Cell shrinkage as a signal to apoptosis in NIH 3T3 fibroblasts. J Physiol (Lond) 567, Garnovskaya MN, Mukhin YV, Vlasova TM, & Raymond JR (2003). Hypertonicity Activates Na+/H+ Exchange through Janus Kinase 2 and Calmodulin. J Biol Chem 278, Gautreau A, Poullet P, Louvard D, & Arpin M (1999). Ezrin, a plasma membrane-microfilament linker, signals cell survival through the phosphatidylinositol 3-kinase/Akt pathway. Proc Natl Acad Sci U S A. 138
139 Gillis D, Shrode LD, Krump E, Howard CM, Rubie EA, Tibbles LA, Woodgett J, & Grinstein S (2001). Osmotic stimulation of the Na+/H+ exchanger NHE1: relationship to the activation of three MAPK pathways. J Membr Biol. Goss GG, Jiang L, Vandorpe DH, Kieller D, Chernova MN, Robertson M, & Alper SL (2001). Role of JNK in hypertonic activation of Cl--dependent Na+/H+ exchange in Xenopus oocytes. Am J Physiol Cell Physiol 281, C1978-C1990. Gregory RI, Chendrimada TP, Cooch N, & Shiekhattar R (2005). Human RISC couples microrna biogenesis and posttranscriptional gene silencing. Cell. Grinstein S & Foskett JK (1990). Ionic mechanisms of cell volume regulation in leukocytes. Annu Rev Physiol. Grinstein S, Rotin D, & Mason MJ (1989). Na+/H+ exchange and growth factor-induced cytosolic ph changes. Role in cellular proliferation. Biochim Biophys Acta. Grinstein S, Woodside M, Sardet C, Pouyssegur J, & Rotin D (1992). Activation of the Na+/H+ antiporter during cell volume regulation. Evidence for a phosphorylation-independent mechanism. J Biol Chem 267, Gusella JF, Ramesh V, MacCollin M, & Jacoby LB (1999). Merlin: the neurofibromatosis 2 tumor suppressor. Biochim Biophys Acta. Hall A. Small GTP-binding proteins and the regulation of the actin cytoskeleton Han J, Lee JD, Bibbs L, & Ulevitch RJ (1994). A MAP kinase targeted by endotoxin and hyperosmolarity in mammalian cells. Science. Han J, Lee JD, Jiang Y, Li Z, Feng L, & Ulevitch RJ (1996). Characterization of the Structure and Function of a Novel MAP Kinase Kinase (MKK6). J Biol Chem 271, Hansen MB, Nielsen SE, & Berg K (1989). Re-examination and further development of a precise and rapid dye method for measuring cell growth/cell kill. J Immunol Methods. Harborth J, Elbashir SM, Vandenburgh K, Manninga H, Scaringe SA, Weber K, & Tuschl T (2003). Sequence, chemical, and structural variation of small interfering RNAs and short hairpin RNAs and the effect on mammalian gene silencing. Antisense Nucleic Acid Drug Dev. Harper SJ & LoGrasso P (2001). Signalling for survival and death in neurones: the role of stress-activated kinases, JNK and p38. Cell Signal. 139
140 Haworth RS, McCann C, Snabaitis AK, Roberts NA, & Avkiran M (2003). Stimulation of the Plasma Membrane Na+/H+ Exchanger NHE1 by Sustained Intracellular Acidosis: EVIDENCE FOR A NOVEL MECHANISM MEDIATED BY THE ERK PATHWAY. J Biol Chem 278, Hayashi K, Yonemura S, Matsui T, & Tsukita S (1999). Immunofluorescence detection of ezrin/radixin/moesin (ERM) proteins with their carboxyl-terminal threonine phosphorylated in cultured cells and tissues. J Cell Sci 112, Henson JH. (1999). Relationships between the actin cytoskeleton and cell volume regulation. Microsc Res Tech. Hirao M, Sato N, Kondo T, Yonemura S, Monden M, Sasaki T, Takai Y, Tsukita S, & Tsukita S (1996). Regulation mechanism of ERM (ezrin/radixin/moesin) protein/plasma membrane association: possible involvement of phosphatidylinositol turnover and Rho-dependent signaling pathway. J Cell Biol 135, Hoffmann EK & Dunham PB. Membrane mechanisms and intracellular signalling in cell volume regulation Hoffmann EK & Pedersen SF. Sensors and signal transduction in the activation of cell volume regulatory ion transport systems Hoffmann EK. Intracellular transmission in cell volume regulation in Ehrlich ascites tumor cells Hughes J, Bortner CD, Purdy GD, & Cidlowski JA (1997). Intracellular K+ Suppresses the Activation of Apoptosis in Lymphocytes. J Biol Chem 272, Ivetic A & Ridley AJ (2004). Ezrin/radixin/moesin proteins and Rho GTPase signalling in leucocytes. Immunology. Jin Z & El-Deiry WS (2005). Overview of cell death signaling pathways. Cancer Biol Ther. Karin M & Gallagher E (2005). From JNK to pay dirt: jun kinases, their biochemistry, physiology and clinical importance. IUBMB Life. Kennedy NJ & Davis RJ (2003). Role of JNK in tumor development. Cell Cycle. Kenneth R.Hallows, Foon-Yee Law, Charles H.Packman, & Philip A.Knauf (1995). Changes in cytoskeletal actin content, F-actin distribution, and surface morphology during HL-60 cell volume regulation. Journal of Cellular Physiology. 140
141 Kenneth R.Hallows and Philip A.Knauf (1994). Principles of Cell Volume Regulation. Kim DH, Behlke MA, Rose SD, Chang MS, Choi S, & Rossi JJ (2005). Synthetic dsrna Dicer substrates enhance RNAi potency and efficacy. Nat Biotechnol. Kim SJ, Hwang SG, Shin DY, Kang SS, & Chun JS (2002). p38 Kinase Regulates Nitric Oxide-induced Apoptosis of Articular Chondrocytes by Accumulating p53 via NFkappa B-dependent Transcription and Stabilization by Serine 15 Phosphorylation. J Biol Chem 277, Ko BCB, Lam AKM, Kapus A, Fan L, Chung SK, & Chung SSM (2002). Fyn and p38 Signaling Are Both Required for Maximal Hypertonic Activation of the Osmotic Response Element-binding Protein/Tonicity-responsive Enhancer-binding Protein (OREBP/TonEBP). J Biol Chem 277, Kurreck J. (2006). sirna Efficiency: Structure or Sequence-That Is the Question. Biomed Biotechnol. Kyriakis JM, App H, Zhang XF, Banerjee P, Brautigan DL, Rapp UR, & Avruch J (1992). Raf-1 activates MAP kinase-kinase. Nature. Kyriakis JM & Avruch J (2001). Mammalian Mitogen-Activated Protein Kinase Signal Transduction Pathways Activated by Stress and Inflammation. Physiol Rev 81, Lang F, Ritter M, Gamper N, Huber S, Fillon S, Tanneur V, Lepple-Wienhues A, & Szabo I GE (2000). Cell volume in the regulation of cell proliferation and apoptotic cell death. Cell Physiol Biochem. LANG FLOR, BUSCH GL, RITTER MARK, VOLKL HARA, WALDEGGER SIEG, GULBINS ERIC, & HAUSSINGER DIET (1998a). Functional Significance of Cell Volume Regulatory Mechanisms. Physiological Reviews 78, LANG FLOR, BUSCH GL, RITTER MARK, VOLKL HARA, WALDEGGER SIEG, GULBINS ERIC, & HAUSSINGER DIET (1998b). Functional Significance of Cell Volume Regulatory Mechanisms. Physiol Rev 78, Lee Anne McLean. From Gliomas to Corps: A role of the Na+/H+ Exchanger in regulation of intracellular ph Lewis A, Di Ciano C, Rotstein OD, & Kapus A (2002). Osmotic stress activates Rac and Cdc42 in neutrophils: role in hypertonicity-induced actin polymerization. Am J Physiol Cell Physiol 282, C271- C279. Li X, Alvarez B, Casey JR, Reithmeier RAF, & Fliegel L (2002). Carbonic Anhydrase II Binds to and Enhances Activity of the Na+/H+ Exchanger. J Biol Chem 277,
142 Lin X & Barber DL (1996). A calcineurin homologous protein inhibits GTPase-stimulated Na-H exchange. Proc Natl Acad Sci U S A. Louvet-Vallee S. (2000). ERM proteins: from cellular architecture to cell signaling. Biol Cell. Mackay DJG, Esch F, Furthmayr H, & Hall A (1997). Rho- and Rac-dependent Assembly of Focal Adhesion Complexes and Actin Filaments in Permeabilized Fibroblasts: An Essential Role for Ezrin/Radixin/Moesin Proteins. J Cell Biol 138, Mangeat P, Roy C, & Martin M (1999). ERM proteins in cell adhesion and membrane dynamics. Trends Cell Biol. Maria Rasmussen RTABVDEKHAKaSFP. Osmotic cell shrinkage activates Ezrin/Radixin/Moesin (ERM) proteins: Activation mechanisms and physiological implications Ref Type: Unpublished Work Matsuda S, Kawasaki H, Moriguchi T, Gotoh Y, & Nishida E (1995). Activation of Protein Kinase Cascades by Osmotic Shock. J Biol Chem 270, Matsui T, Yonemura S, Tsukita S, & Tsukita S (1999). Activation of ERM proteins in vivo by Rho involves phosphatidyl-inositol 4-phosphate 5-kinase and not ROCK kinases. Curr Biol. Matsuyama S, Llopis J, Deveraux QL, Tsien RY, & Reed JC (2000). Changes in intramitochondrial and cytosolic ph: early events that modulate caspase activation during apoptosis. Nat Cell Biol. McLean LA, Zia S, Gorin FA, & Cala PM (1999). Cloning and expression of the Na+/H+ exchanger from Amphiuma RBCs: resemblance to mammalian NHE1. Am J Physiol Cell Physiol 276, C1025- C1037. McManus M, Fischbarg J, Sun A, Hebert S, & Strange K (1993). Laser light-scattering system for studying cell volume regulation and membrane transport processes. Am J Physiol Cell Physiol 265, C562-C570. Meier R, Thelen M, & Hemmings BA (1998). Inactivation and dephosphorylation of protein kinase Balpha (PKBalpha) promoted by hyperosmotic stress. EMBO J. Mills JW & Mandel LJ (1994). Cytoskeletal regulation of membrane transport events. FASEB J 8, Misik AJ, Perreault K, Holmes CF, & Fliegel L (2005). Protein phosphatase regulation of Na+/H+ exchanger isoform I. Biochemistry. 142
143 Miyakawa H, Woo SK, Dahl SC, Handler JS, & Kwon HM (1999). Tonicity-responsive enhancer binding protein, a rel-like protein that stimulates transcription in response to hypertonicity. Proc Natl Acad Sci U S A. Mongin AA & Orlov SN (2001). Mechanisms of cell volume regulation and possible nature of the cell volume sensor. Pathophysiology 2001 Dec;8(2): Moor AN & Fliegel L (1999). Protein Kinase-mediated Regulation of the Na+/H+ Exchanger in the Rat Myocardium by Mitogen-activated Protein Kinase-dependent Pathways. J Biol Chem 274, Morrison DK & Davis RJ (2003). Regulation of MAP kinase signaling modules by scaffold proteins in mammals. Annu Rev Cell Dev Biol. Mosmann T. (1983). Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods. Mukhin YV, Garnovskaya MN, Ullian ME, & Raymond JR. ERK Is Regulated by Sodium-Proton Exchanger in Rat Aortic Vascular Smooth Muscle Cells. Journal of Biological Chemistry 279[3], Nadkarni V, Gabbay KH, Bohren KM, & Sheikh-Hamad D (1999). Osmotic Response Element Enhancer Activity. REGULATION THROUGH p38 KINASE AND MITOGEN-ACTIVATED EXTRACELLULAR SIGNAL-REGULATED KINASE KINASE. J Biol Chem 274, Nakamura N, Oshiro N, Fukata Y, Amano M, Fukata M, Kuroda S, Matsuura Y, Leung T, Lim L, & Kaibuchi K (2000). Phosphorylation of ERM proteins at filopodia induced by Cdc42, Genes Cells. Negulescu PA & Machen TE (1990). Intracellular ion activities and membrane transport in parietal cells measured with fluorescent dyes. Methods Enzymol. Niggli V, Andreoli C, Roy C, & Mangeat P (1995). Identification of a phosphatidylinositol-4,5- bisphosphate-binding domain in the N-terminal region of ezrin. FEBS Lett. Nylandsted J, Jaattela M, Hoffmann EK, & Pedersen SF. Heat shock protein 70 inhibits shrinkageinduced programmed cell death via mechanisms independent of effects on cell volume-regulatory membrane transport proteins O'Neill WC (1999). Physiological significance of volume-regulatory transporters. Am J Physiol Cell Physiol 276, C Okada Y & Maeno E (2001). Apoptosis, cell volume regulation and volume-regulatory chloride channels. Comp Biochem Physiol A Mol Integr Physiol. 143
144 Okada Y. (2004). Ion channels and transporters involved in cell volume regulation and sensor mechanisms. Cell Biochem Biophys. Orlowski J & Grinstein S (2004). Diversity of the mammalian sodium/proton exchanger SLC9 gene family. Pflugers Arch. Ozkan P & Mutharasan R (2002). A rapid method for measuring intracellular ph using BCECF-AM. Biochim Biophys Acta. Padda R, Wamsley-Davis A, Gustin MC, Ross R, Yu C, & Sheikh-Hamad D (2006). MEKK3-mediated signaling to p38 kinase and TonE in hypertonically stressed kidney cells. Am J Physiol Renal Physiol 291, F874-F881. Paddock SW. (1999). Confocal laser scanning microscopy. Biotechniques. Pages G, L'Allemain G, Chambard JC, Meloche S, Pouyssegur J, & Lenormand P (1993). Mitogenactivated protein kinases p42mapk and p44mapk are required for fibroblast proliferation. Proc Natl Acad Sci U S A. Papakonstanti EA, Vardaki EA, & Stournaras C (2000). Actin cytoskeleton: a signaling sensor in cell volume regulation. Cell Physiol Biochem. Patricia Hess, German Pihan, Charles L.Sawyers, Richard A.Flavell, & Roger J.Davis (2002). Survival signaling mediated by c-jun NH2-terminal kinase in transformed B lymphoblasts. Nature. Pearson MA, Reczek D, Bretscher A, & Karplus PA (2000). Structure of the ERM protein moesin reveals the FERM domain fold masked by an extended actin binding tail domain. Cell. Pedersen SF & Cala PM (2004). Comparative biology of the ubiquitous Na+/H+ exchanger, NHE1: lessons from erythrocytes. J Exp Zoolog A Comp Exp Biol. Pedersen SF & Hoffmann EK. Possible interrelationship between changes in F-actin and myosin II, protein phosphorylation, and cell volume regulation in Ehrlich ascites tumor cells Pedersen SF, Hoffmann EK, & Mills JW. The cytoskeleton and cell volume regulation Pedersen SF, Jorgensen NK, Damgaard I, Schousboe A, & Hoffmann EK (1998). Mechanisms of phi regulation studied in individual neurons cultured from mouse cerebral cortex. J Neurosci Res. 144
145 Pedersen SF, Kramhoft B, Jorgensen NK, & Hoffmann EK (1996). Shrinkage-induced activation of the Na+/H+ exchanger in Ehrlich ascites tumor cells: mechanisms involved in the activation and a role for the exchanger in cell volume regulation. J Membr Biol. Pedersen SF. (2006). The Na(+)/H (+) exchanger NHE1 in stress-induced signal transduction: implications for cell proliferation and cell death. Pflugers Arch 2006 Jun;452(3): Epub 2006 Apr 4. Pedersen SF, Mills JW, & Hoffmann EK (1999). Role of the F-actin Cytoskeleton in the RVD and RVI Processes in Ehrlich Ascites Tumor Cells. Experimental Cell Research 252, Pedersen SF, Beisner KH, Hougaard C, Willumsen BM, Lambert IH, & Hoffmann EK (2002). Rho family GTP binding proteins are involved in the regulatory volume decrease process in NIH3T3 mouse fibroblasts. J Physiol (Lond) 541, Pouyssegur J, Volmat V, & Lenormand P (2002). Fidelity and spatio-temporal control in MAP kinase (ERKs) signalling. Biochem Pharmacol. Putney LK, Denker SP, & Barber DL (2002). The changing face of the Na+/H+ exchanger, NHE1: structure, regulation, and cellular actions. Annu Rev Pharmacol Toxicol. Raingeaud J, Whitmarsh AJ, Barrett T, Derijard B, & Davis RJ (1996). MKK3- and MKK6-regulated gene expression is mediated by the p38 mitogen- activated protein kinase signal transduction pathway. Mol Cell Biol 16, Rasmussen M, Todd Alexander, Barbara V.Darborg, Else K.Hoffmann, & Andras Kapus and Stine F.Pedersen. Osmotic cell shrinkage activates Ezrin/Radixin/Moesin (ERM) proteins: Activation mechanisms and physiological implications Reczek D & Bretscher A (1998). The Carboxyl-terminal Region of EBP50 Binds to a Site in the Aminoterminal Domain of Ezrin That Is Masked in the Dormant Molecule. J Biol Chem 273, Rentsch M, Hoffmann EK, & Pedersen SF. Effects of chemical anoxia on NHE1, p38 MAPK, p53, Akt/PKB and ERM proteins in NIH3T3 mouse fibroblasts: evidence for a role of NHE1 upstream of p38 MAPK Ridley AJ & HallA (1994). Signal transduction pathways regulating Rho-mediated stress fibre formation: requirement for a tyrosine kinase. EMBO J. Ritter M, Fuerst J, Woll E, Chwatal S, Gschwentner M, Lang F, Deetjen P, & Paulmichl M (2001). Na(+)/H(+)exchangers: linking osmotic dysequilibrium to modified cell function. Cell Physiol Biochem. 145
146 Roger F, Martin PY, Rousselot M, Favre H, & Feraille E (1999). Cell Shrinkage Triggers the Activation of Mitogen-activated Protein Kinases by Hypertonicity in the Rat Kidney Medullary Thick Ascending Limb of the Henle's Loop. REQUIREMENT OF p38 KINASE FOR THE REGULATORY VOLUME INCREASE RESPONSE. J Biol Chem 274, S.F.Pedersen, M.E.O'Donnell, & S.E.Anderson and P.M.Cala (2006). Physiology and pathophysiology of Na+/H+ exchange and Na +-K+-2Cl cotransport in the heart, brain, and blood. Am J Physiol Regulatory Integrative Comp Physiol. S.F.Pedersen C.Varming STCEH2 (2002). Mechanism of activation of NHE by Cell Shrinkage and by Calyculin A in Erlich Ascites Tumor cells. J Memb biol. Sabapathy K, Hochedlinger K, Nam SY, Bauer A, Karin M, & Wagner EF (2004). Distinct roles for JNK1 and JNK2 in regulating JNK activity and c-jun-dependent cell proliferation. Mol Cell. Sanchez-Prieto R, Rojas JM, Taya Y, & Gutkind JS (2000). A Role for the p38 Mitogen-activated Protein Kinase Pathway in the Transcriptional Activation of p53 on Genotoxic Stress by Chemotherapeutic Agents. Cancer Res 60, Saotome I, Curto M, & McClatchey AI (2004). Ezrin is essential for epithelial organization and villus morphogenesis in the developing intestine. Dev Cell. Sarkadi B & Parker JC (1991). Activation of ion transport pathways by changes in cell volume. Biochim Biophys Acta. Sasaki T & Takai Y (1998). The Rho small G protein family-rho GDI system as a temporal and spatial determinant for cytoskeletal control. Biochem Biophys Res Commun. Sato N, Funayama N, Nagafuchi A, Yonemura S, Tsukita S, & Tsukita S (1992). A gene family consisting of ezrin, radixin and moesin. Its specific localization at actin filament/plasma membrane association sites. J Cell Sci 103, Schmidt A & Hall MN (1998). Signaling to the actin cytoskeleton. Annu Rev Cell Dev Biol 1998;14: Segal MS & Beem E (2001). Effect of ph, ionic charge, and osmolality on cytochrome c-mediated caspase-3 activity. Am J Physiol Cell Physiol 281, C1196-C1204. Shaw RJ, Henry M, Solomon F, & Jacks T (1998). RhoA-Dependent Phosphorylation and Relocalization of ERM Proteins into Apical Membrane/Actin Protrusions in Fibroblasts. Mol Biol Cell 9,
147 Sheikh-Hamad D & Gustin MC (2004). MAP kinases and the adaptive response to hypertonicity: functional preservation from yeast to mammals. Am J Physiol Renal Physiol 287, F1102-F1110. Shinya Inoue (1995). foundations of confocal scanned imaging in light microspopy. Shrode LD, Rubie EA, Woodgett JR, & Grinstein S (1997). Cytosolic Alkalinization Increases Stressactivated Protein Kinase/c-Jun NH2-terminal Kinase (SAPK/JNK) Activity and p38 Mitogen-activated Protein Kinase Activity by a Calcium-independent Mechanism. J Biol Chem 272, Simchowitz L & Roos A (1985). Regulation of intracellular ph in human neutrophils. J Gen Physiol 85, Stine Falsig Pedersen, Barbara Vasek Darborg, Maria Rasmussen, Jesper Nylandsted, & Else Kay Hoffmann. The Na + /H + exchanger, NHE1, differentially regulates mitogen-activated protein kinase subfamilies after osmotic shrinkage in Ehrlich Lettre Ascites cells Stossel TP (1989). From signal to pseudopod. How cells control cytoplasmic actin assembly. J Biol Chem 264, Strange K (2004). Cellular volume homeostasis. Advan Physiol Edu 28, Takahashi K, Sasaki T, Mammoto A, Hotta I, Takaishi K, Imamura H, Nakano K, Kodama A, & Takai Y. Interaction of radixin with Rho small G protein GDP/GTP exchange protein Dbl Takahashi E, Abe Ji, Gallis B, Aebersold R, Spring DJ, Krebs EG, & Berk BC (1999). p90rsk Is a Serum-stimulated Na+/H+ Exchanger Isoform-1 Kinase. REGULATORY PHOSPHORYLATION OF SERINE 703 OF Na+/H+ EXCHANGER ISOFORM-1. J Biol Chem 274, Takahashi K, Sasaki T, Mammoto A, Takaishi K, Kameyama T, Tsukita S, Tsukita S, & Takai Y (1997). Direct Interaction of the Rho GDP Dissociation Inhibitor with Ezrin/Radixin/Moesin Initiates the Activation of the Rho Small G Protein. J Biol Chem 272, Takaishi K, Matozaki T, Nakano K, & Takai Y (2000). Multiple downstream signalling pathways from ROCK, a target molecule of Rho small G protein, in reorganization of the actin cytoskeleton in Madin- Darby canine kidney cells. Genes Cells. Takeuchi K, Sato N, Kasahara H, Funayama N, Nagafuchi A, Yonemura S, Tsukita S, & Tsukita S (1994). Perturbation of cell adhesion and microvilli formation by antisense oligonucleotides to ERM family members. J Cell Biol 125, Tauer U (2002). Advantages and risks of multiphoton microscopy in physiology. Exp Physiol 87,
148 Tilly BC, Edixhoven MJ, Tertoolen LG, Morii N, Saitoh Y, Narumiya S, & de Jonge HR (1996). Activation of the osmo-sensitive chloride conductance involves P21rho and is accompanied by a transient reorganization of the F-actin cytoskeleton. Mol Biol Cell. Tominaga T, Ishizaki T, Narumiya S, & Barber DL. p160rock mediates RhoA activation of Na-H exchange Tominaga T & Barber DL (1998). Na-H Exchange Acts Downstream of RhoA to Regulate Integrininduced Cell Adhesion and Spreading. Mol Biol Cell 9, Tsien RY. (1989). Fluorescent probes of cell signaling. Annu Rev Neurosci. Tsukita S & Yonemura S (1997). ERM (ezrin/radixin/moesin) family: from cytoskeleton to signal transduction. Curr Opin Cell Biol. Tsukita S, Oishi K, Sato N, Sagara J, Kawai A, & Tsukita S (1994). ERM family members as molecular linkers between the cell surface glycoprotein CD44 and actin-based cytoskeletons. J Cell Biol 126, Tsukita S & Yonemura S (1999). Cortical Actin Organization: Lessons from ERM (Ezrin/Radixin/Moesin) Proteins. J Biol Chem 274, Turunen O, Wahlstrom T, & Vaheri A (1994). Ezrin has a COOH-terminal actin-binding site that is conserved in the ezrin protein family. J Cell Biol 126, Uhlik MT, Abell AN, Johnson NL, Sun W, Cuevas BD, Lobel-Rice KE, Horne EA, Dell'Acqua ML, & Johnson GL (2003). Rac-MEKK3-MKK3 scaffolding for p38 MAPK activation during hyperosmotic shock. Nat Cell Biol. Vaheri A, Carpen O, Heiska L, Helander TS, Jaaskelainen J, Majander-Nordenswan P, Sainio M TT, & Turunen O (1997). The ezrin protein family: membrane-cytoskeleton interactions and disease associations. Curr Opin Cell Biol. Wakabayashi S, Sardet C, Fafournoux P, Counillon L, Meloche S, & Pages G PJ (1992). Structure function of the growth factor-activatable Na+/H+ exchanger (NHE1). Rev Physiol Biochem Pharmacol. Wakabayashi S, Bertrand B, Ikeda T, Pouyssegur J, & Shigekawa M (1994). Mutation of calmodulinbinding site renders the Na+/H+ exchanger (NHE1) highly H(+)-sensitive and Ca2+ regulation-defective. J Biol Chem 269, Wakabayashi S, Shigekawa M, & Pouyssegur J (1997). Molecular physiology of vertebrate Na+/H+ exchangers. Physiol Rev 77,
149 Wakabayashi S, Pang T, Su X, & Shigekawa M (2000). A Novel Topology Model of the Human Na+/H+ Exchanger Isoform 1. J Biol Chem 275, Werry TD, Christopoulos A, & Sexton PM (2006). Mechanisms of ERK1/2 regulation by seventransmembrane-domain receptors. Curr Pharm Des. Widmann C.H.R.I., Gibson S.P.E.N., Jarpe Mathew B, & Johnson Gary L (1999). Mitogen-Activated Protein Kinase: Conservation of a Three-Kinase Module From Yeast to Human. Physiol Rev 79, William T.Arthur, Leslie A, & Petch and Keith Burridge (2000). Integrin engagement suppresses RhoA activity via a c-src-dependent mechanism. Curr Biol. Woo SK, Lee SD, & Kwon HM (2002). TonEBP transcriptional activator in the cellular response to increased osmolality. Pflugers Arch. Wright SJ & Wright DJ (2002). Introduction to confocal microscopy. Methods Cell Biol. Wu KL, Khan S, Lakhe-Reddy S, Jarad G, Mukherjee A, Obejero-Paz CA, Konieczkowski M, Sedor JR, & Schelling JR (2004). The NHE1 Na+/H+ Exchanger Recruits Ezrin/Radixin/Moesin Proteins to Regulate Akt-dependent Cell Survival. J Biol Chem 279, Wu KL, Khan S, Lakhe-Reddy S, Wang L, Jarad G, Miller RT, Konieczkowski M, Brown AM, Sedor JR, & Schelling JR (2003). Renal tubular epithelial cell apoptosis is associated with caspase cleavage of the NHE1 Na+/H+ exchanger. Am J Physiol Renal Physiol 284, F829-F839. Yan C, Luo H, Lee JD, Abe Ji, & Berk BC (2001a). Molecular Cloning of Mouse ERK5/BMK1 Splice Variants and Characterization of ERK5 Functional Domains. J Biol Chem 276, Yan W, Nehrke K, Choi J, & Barber DL (2001b). The Nck-interacting Kinase (NIK) Phosphorylates the Na+-H+ Exchanger NHE1 and Regulates NHE1 Activation by Platelet-derived Growth Factor. J Biol Chem 276, Yonemura S, Matsui T, Tsukita S, & Tsukita S (2002). Rho-dependent and -independent activation mechanisms of ezrin/radixin/moesin proteins: an essential role for polyphosphoinositides in vivo. J Cell Sci 115, Yoon S & Seger R (2006). The extracellular signal-regulated kinase: multiple substrates regulate diverse cellular functions. Growth Factors. Yoshimi Takai & Takuya Sasaki and Takashi Matozaki (2001). Small GTP-Binding Proteins. Physiol Rev. 149
150 Zhu Y, Mao XO, Sun Y, Xia Z, & Greenberg DA (2002). p38 Mitogen-activated Protein Kinase Mediates Hypoxic Regulation of Mdm2 and p53 in Neurons. J Biol Chem 277, Zhuang S, Hirai SI, & Ohno S (2000). Hyperosmolality induces activation of cpkc and npkc, a requirement for ERK1/2 activation in NIH/3T3 cells. Am J Physiol Cell Physiol 278, C102-C109. Zigmond SH. (1996). Signal transduction and actin filament organization. Curr Opin Cell Biol. 150
Syv transmembrane receptorer
 Syv transmembrane receptorer Receptoren som kommunikationscentral Cellemembranen definerer grænsen mellem en celles indre og ydre miljø, der er meget forskelligt. Det er essentielt for cellens funktion
Syv transmembrane receptorer Receptoren som kommunikationscentral Cellemembranen definerer grænsen mellem en celles indre og ydre miljø, der er meget forskelligt. Det er essentielt for cellens funktion
Eksamen i. Cellebiologi (kandidatdelen): Cellebiologi - Cellers struktur og funktion - Membranbiokemi - Cellulær signaltransduktion
 Eksamen i Cellebiologi (kandidatdelen): Cellebiologi - Cellers struktur og funktion - Membranbiokemi - Cellulær signaltransduktion Opgavesættet består af 5 sider inklusive denne forside. Sættet består
Eksamen i Cellebiologi (kandidatdelen): Cellebiologi - Cellers struktur og funktion - Membranbiokemi - Cellulær signaltransduktion Opgavesættet består af 5 sider inklusive denne forside. Sættet består
Hvilket af efterfølgende udsagn er forkert? a) Golgi-proteiner syntetiseres i ER b) mitochondriale proteiner syntetiseres i cytosol c)
 Test 3 Hvilket af efterfølgende udsagn er forkert? a) Golgi-proteiner syntetiseres i ER b) mitochondriale proteiner syntetiseres i cytosol c) plasmamembran-proteiner syntetiseres i cytosol d) lysosomale
Test 3 Hvilket af efterfølgende udsagn er forkert? a) Golgi-proteiner syntetiseres i ER b) mitochondriale proteiner syntetiseres i cytosol c) plasmamembran-proteiner syntetiseres i cytosol d) lysosomale
Almen cellebiologi Membrantransport
 Almen cellebiologi 2007 Membrantransport Kap. 12, s. 389-420 Forelæsning 1 Stine Falsig Pedersen [email protected] 35321546/room 527 1 De næste tre forelæsninger: 1. - Membranen og membran-transport
Almen cellebiologi 2007 Membrantransport Kap. 12, s. 389-420 Forelæsning 1 Stine Falsig Pedersen [email protected] 35321546/room 527 1 De næste tre forelæsninger: 1. - Membranen og membran-transport
Enzyme-linked receptors p557- p566
 Enzyme-linked receptors p557- p566 2007 Hvor sidder receptoren er agonisten lipid permeabel? 16_09_molecules_bind.jpg Peptid-ligander binder til membran associerede receptorer Receptorer A A A A B A B
Enzyme-linked receptors p557- p566 2007 Hvor sidder receptoren er agonisten lipid permeabel? 16_09_molecules_bind.jpg Peptid-ligander binder til membran associerede receptorer Receptorer A A A A B A B
Studienummer: MeDIS Exam 2015. Husk at opgive studienummer ikke navn og cpr.nr. på alle ark, der skal medtages i bedømmelsen
 MeDIS Exam 2015 Titel på kursus: Uddannelse: Semester: Videregående biokemi og medicinudvikling Bachelor i Medis 5. semester Eksamensdato: 26-01-2015 Tid: kl. 09.00-11.00 Bedømmelsesform 7-trin Vigtige
MeDIS Exam 2015 Titel på kursus: Uddannelse: Semester: Videregående biokemi og medicinudvikling Bachelor i Medis 5. semester Eksamensdato: 26-01-2015 Tid: kl. 09.00-11.00 Bedømmelsesform 7-trin Vigtige
Kapitel 19. cell division. Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526
 Kapitel 19 cell division Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526 [email protected] Vigtige MT koncepter MT tilhører gruppen af cytoskeletfilamenter, som er polære strukturer med
Kapitel 19 cell division Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526 [email protected] Vigtige MT koncepter MT tilhører gruppen af cytoskeletfilamenter, som er polære strukturer med
Glat muskulatur F16 : B: , ,
 Læringsmål Beskrive glat muskulaturs opbygning (ikke tværstribet, organisering varierer fra multi unit (ukoblede celler) til single unit" (kraftig kobling)) Beskrive det kontraktile apparats opbygning
Læringsmål Beskrive glat muskulaturs opbygning (ikke tværstribet, organisering varierer fra multi unit (ukoblede celler) til single unit" (kraftig kobling)) Beskrive det kontraktile apparats opbygning
Besvarelse af opgaverne til den Spm.A: efter TGA TCA Spm. B:
 Besvarelse af opgaverne til den 20-9-06 Spm.A: Her vil vi gerne sætte et relativt lille stykke DNA (FLAG) sammen med et relativt stort stykke (PRB1). Det lille stykke er for lille til at vi kan PCR amplificere
Besvarelse af opgaverne til den 20-9-06 Spm.A: Her vil vi gerne sætte et relativt lille stykke DNA (FLAG) sammen med et relativt stort stykke (PRB1). Det lille stykke er for lille til at vi kan PCR amplificere
CYP7A1 (0,1 nm) CYP7A1 (0nM) UBIC (0,1 nm)
 Opgave 1 Leveren spiller en central rolle i lipid metabolismen og i opretholdelse af lipid homeostasen i hele kroppen. Lipidmetabolismen er fejlreguleret hos blandt andet svært overvægtige personer samt
Opgave 1 Leveren spiller en central rolle i lipid metabolismen og i opretholdelse af lipid homeostasen i hele kroppen. Lipidmetabolismen er fejlreguleret hos blandt andet svært overvægtige personer samt
Programmed cell death. Apoptose. (betyder at falde af på græsk) Alberts. Essential Cell Biology. Kap.18, side 625
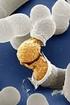 Programmed cell death. Apoptose (betyder at falde af på græsk) Alberts. Essential Cell Biology. Kap.18, side 625 Programmeret celledød eller apoptose er en central proces der styrer udviklingen af multicellulære
Programmed cell death. Apoptose (betyder at falde af på græsk) Alberts. Essential Cell Biology. Kap.18, side 625 Programmeret celledød eller apoptose er en central proces der styrer udviklingen af multicellulære
Test Canvas: Eksamen i BMB502 Januar 2012
 BMB502, Enzymer og membraner, efterår 11. f Tests, Surveys and Pools Tests Test Canvas : Eksamen i BMB502 Januar 2012 Edit Mode is: Test Canvas: Eksamen i BMB502 Januar 2012 Create Reuse Upload s Settings
BMB502, Enzymer og membraner, efterår 11. f Tests, Surveys and Pools Tests Test Canvas : Eksamen i BMB502 Januar 2012 Edit Mode is: Test Canvas: Eksamen i BMB502 Januar 2012 Create Reuse Upload s Settings
Proteiner: en introduktion. Modul 1; F13 Rolf Andersen, 18/2-2013
 Proteiner: en introduktion Modul 1; F13 Rolf Andersen, 18/2-2013 4 facts om proteiner Proteiner udgør én af de vigtigste stofgrupper i vores organisme; de varetager en lang række forskellige funktioner.
Proteiner: en introduktion Modul 1; F13 Rolf Andersen, 18/2-2013 4 facts om proteiner Proteiner udgør én af de vigtigste stofgrupper i vores organisme; de varetager en lang række forskellige funktioner.
Opgave 1 Listeria. mørkviolette bakteriekolonier, se figur 1a. og b. 1. Angiv reaktionstypen for reaktion. 1 vist i figur 1b.
 Opgave 1 Listeria Bakterien Listeria monocytogenes kan være sygdomsfremkaldende for personer, der i forvejen er svækkede. For at identificere Listeria kan man anvende indikative agarplader. Her udnyttes
Opgave 1 Listeria Bakterien Listeria monocytogenes kan være sygdomsfremkaldende for personer, der i forvejen er svækkede. For at identificere Listeria kan man anvende indikative agarplader. Her udnyttes
Forårseksamen Titel på kursus: Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin med industriel specialisering
 Studienummer: 1/10 Forårseksamen 2014 Titel på kursus: Det hæmatologiske system og immunsystemet Uddannelse: Bacheloruddannelsen i Medicin/Medicin med industriel specialisering Semester: 2. semester Eksamensdato:
Studienummer: 1/10 Forårseksamen 2014 Titel på kursus: Det hæmatologiske system og immunsystemet Uddannelse: Bacheloruddannelsen i Medicin/Medicin med industriel specialisering Semester: 2. semester Eksamensdato:
Eksamen den 7. april 2006. Cellulær og Integrativ Fysiologi
 1 Eksamen den 7. april 2006 Cellulær og Integrativ Fysiologi Sættet indeholder 5 sider. Der må ikke medbringes bøger og noter. Svarene kan være på dansk eller engelsk. Dee er 4 hovedspørgsmål i sættet.
1 Eksamen den 7. april 2006 Cellulær og Integrativ Fysiologi Sættet indeholder 5 sider. Der må ikke medbringes bøger og noter. Svarene kan være på dansk eller engelsk. Dee er 4 hovedspørgsmål i sættet.
Actin-cytoskelettet og muskelkontraktion
 Actin-cytoskelettet og muskelkontraktion Actin filamenter a er opbygget af heterodimerer bestående af 1 α- og 1 β-actin subunits b er to-strengede helices opbygget af globulære subunits c er ca 20 nm brede
Actin-cytoskelettet og muskelkontraktion Actin filamenter a er opbygget af heterodimerer bestående af 1 α- og 1 β-actin subunits b er to-strengede helices opbygget af globulære subunits c er ca 20 nm brede
Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr
 Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr Besøget retter sig primært til elever med biologi på B eller A niveau Program for besøget Hvis besøget foretages af en hel klasse,
Stofskiftets afhængighed af temperatur og aktivitet hos vekselvarme dyr Besøget retter sig primært til elever med biologi på B eller A niveau Program for besøget Hvis besøget foretages af en hel klasse,
Sommereksamen 2012 Med korte, vejledende svar
 1 Sommereksamen 2012 Med korte, vejledende svar Titel på kursus: Uddannelse: Semester: ksamensdato: Tid: Bedømmelsesform Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin
1 Sommereksamen 2012 Med korte, vejledende svar Titel på kursus: Uddannelse: Semester: ksamensdato: Tid: Bedømmelsesform Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin
Opgave 1. EPO og bloddoping
 Side 1 af 8 sider Opgave 1. EPO og bloddoping Nogle sportsfolk snyder ved at få tilført hormonet erythropoietin, EPO, eller røde blodceller (bloddoping) før en konkurrence, fordi det øger præstationsevnen.
Side 1 af 8 sider Opgave 1. EPO og bloddoping Nogle sportsfolk snyder ved at få tilført hormonet erythropoietin, EPO, eller røde blodceller (bloddoping) før en konkurrence, fordi det øger præstationsevnen.
Appendix 1: Udregning af mængde cellesuspention til udsåning. Faktor mellem total antal celler og antal celler der ønskes udsås:
 Appendix Appendix 1: Udregning af mængde cellesuspention til udsåning Fortyndingsfaktor: Efter trypsinering og centrifugering af celler fra cellestokken, opblandes cellerne i 1 ml medie. For at lave en
Appendix Appendix 1: Udregning af mængde cellesuspention til udsåning Fortyndingsfaktor: Efter trypsinering og centrifugering af celler fra cellestokken, opblandes cellerne i 1 ml medie. For at lave en
Energi, Enzymer & enzymkinetik.metabolisme
 (gruppeopgaver i databar 152 (og 052)) Energi, Enzymer & enzymkinetik.metabolisme Tirsdag den 17. september kl 13-14.15 (ca) Auditorium 53, bygning 210 Susanne Jacobsen [email protected] Enzyme and Protein
(gruppeopgaver i databar 152 (og 052)) Energi, Enzymer & enzymkinetik.metabolisme Tirsdag den 17. september kl 13-14.15 (ca) Auditorium 53, bygning 210 Susanne Jacobsen [email protected] Enzyme and Protein
[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]
![[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU] [BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]](/thumbs/39/19540330.jpg) Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
ANATOMI for tandlægestuderende. Henrik Løvschall Anatomisk Afsnit
 ANATOMI for tandlægestuderende Henrik Løvschall Anatomisk Afsnit CELLEBIOLOGI celleform kubisk celle pladeformet celle prismatisk celle kugleformet celle uregelmæssig stjerneformet celle celleform varierer
ANATOMI for tandlægestuderende Henrik Løvschall Anatomisk Afsnit CELLEBIOLOGI celleform kubisk celle pladeformet celle prismatisk celle kugleformet celle uregelmæssig stjerneformet celle celleform varierer
Nyrefysiologi: Renal ionbehandling, kap. 8 Anne Agersted, 5. sem. efterår 2013 CALCIUM HOMEOSTASEN
 CALCIUM HOMEOSTASEN 35 % af Ca +2 indholdet i en normal voksen persons kost absorberes gennem mavetarmkanalen. Den ekstracellulære Ca +2 pool indeholder ca. 25 mmol, hvorfra Ca +2 udskilles i urinen. PTH:
CALCIUM HOMEOSTASEN 35 % af Ca +2 indholdet i en normal voksen persons kost absorberes gennem mavetarmkanalen. Den ekstracellulære Ca +2 pool indeholder ca. 25 mmol, hvorfra Ca +2 udskilles i urinen. PTH:
Forsvar mod meldug i byg 8/1-07
 Forsvar mod meldug i byg 8/1-07 Meldugsvampens angreb på bygplanten aktiverer en række interessante gener der fungerer i reguleringen af plantens forsvar. Modtagelig David B. Collinge, Michael K. Jensen
Forsvar mod meldug i byg 8/1-07 Meldugsvampens angreb på bygplanten aktiverer en række interessante gener der fungerer i reguleringen af plantens forsvar. Modtagelig David B. Collinge, Michael K. Jensen
Brugsvejledning for 7827.10 dialyseslange
 Brugsvejledning for 7827.10 dialyseslange 14.06.07 Aa 7827.10 1. Præsentation Dialyseslangen er 10 m lang og skal klippes i passende stykker og blødgøres med vand for at udføre forsøgene med osmose og
Brugsvejledning for 7827.10 dialyseslange 14.06.07 Aa 7827.10 1. Præsentation Dialyseslangen er 10 m lang og skal klippes i passende stykker og blødgøres med vand for at udføre forsøgene med osmose og
Undervisningsplan FORÅR februar Introduktion til faget Hana Malá februar Hjernens opbygning og funktion Hana Malá
 Undervisningsplan FORÅR 2008 1. 5. februar Introduktion til faget Hana Malá 2. 12. februar Hjernens opbygning og funktion Hana Malá 3. 19. februar Nyt fra forskningen Hana Malá 4. 26. februar Plasticitet
Undervisningsplan FORÅR 2008 1. 5. februar Introduktion til faget Hana Malá 2. 12. februar Hjernens opbygning og funktion Hana Malá 3. 19. februar Nyt fra forskningen Hana Malá 4. 26. februar Plasticitet
Liste A 1 Na + -glucosetransportør 2 Glucosetransportør 3 Na + /H + exchanger 4 Na +,K + ATPase 5 Acetylcholinreceptoren i den neuromuskulære junction
 Liste A 1 Na + -glucosetransportør 2 Glucosetransportør 3 Na + /H + exchanger 4 Na +,K + ATPase 5 Acetylcholinreceptoren i den neuromuskulære junction Liste B A B C D E F Antiport Symport Passiv transport
Liste A 1 Na + -glucosetransportør 2 Glucosetransportør 3 Na + /H + exchanger 4 Na +,K + ATPase 5 Acetylcholinreceptoren i den neuromuskulære junction Liste B A B C D E F Antiport Symport Passiv transport
Det innate virusforsvar. TLR7, TLR8, TLR9, MDA5, RIG I og type I interferoner
 Det innate virusforsvar. TLR7, TLR8, TLR9, MDA5, RIG I og type I interferoner A kursus i teoretisk og immunologi TLR3 og LGP 2 Odense, 13. april 2015 Søren T. Lillevang Klinisk Immunologisk Afdeling Odense
Det innate virusforsvar. TLR7, TLR8, TLR9, MDA5, RIG I og type I interferoner A kursus i teoretisk og immunologi TLR3 og LGP 2 Odense, 13. april 2015 Søren T. Lillevang Klinisk Immunologisk Afdeling Odense
Basic statistics for experimental medical researchers
 Basic statistics for experimental medical researchers Sample size calculations September 15th 2016 Christian Pipper Department of public health (IFSV) Faculty of Health and Medicinal Science (SUND) E-mail:
Basic statistics for experimental medical researchers Sample size calculations September 15th 2016 Christian Pipper Department of public health (IFSV) Faculty of Health and Medicinal Science (SUND) E-mail:
B i o k e m i ø v e l s e 1 Regulatoriske mekanismer i det intermediære stoftskifte Udarbejdet af: Matilda Lantz og Elif Bayram
 Regulatoriske mekanismer i det intermediære stoftskifte Udarbejdet af: Matilda Lantz og Elif Bayram Dato: 20. November 2011 Underskrifter: Godkendt: Dato Regulatoriske mekanismer i det intermediære stofskifte
Regulatoriske mekanismer i det intermediære stoftskifte Udarbejdet af: Matilda Lantz og Elif Bayram Dato: 20. November 2011 Underskrifter: Godkendt: Dato Regulatoriske mekanismer i det intermediære stofskifte
ANATOMI for tandlægestuderende. Henrik Løvschall Anatomisk afsnit Afd. for Tandsygdomslære Odontologisk Institut Århus Universitet
 ANATOMI for tandlægestuderende Henrik Løvschall Anatomisk afsnit Afd. for Tandsygdomslære Odontologisk Institut Århus Universitet CELLEBIOLOGI celleform kubisk celle pladeformet celle prismatisk celle
ANATOMI for tandlægestuderende Henrik Løvschall Anatomisk afsnit Afd. for Tandsygdomslære Odontologisk Institut Århus Universitet CELLEBIOLOGI celleform kubisk celle pladeformet celle prismatisk celle
[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]
![[BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU] [BESØGSSERVICE INSTITUT FOR MOLEKYLÆRBIOLOGI OG GENETIK, AU]](/thumbs/72/66305306.jpg) Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
Enzymkinetik INTRODUKTION Enzymer er biologiske katalysatorer i alle levende organismer som er essentielle for liv. Selektivt og effektivt katalyserer enzymerne kemiske reaktioner som ellers ikke ville
Det lyder enkelt, men for at forstå hvilket ærinde forskerne er ude i, er det nødvendigt med et indblik i, hvordan celler udvikles og specialiseres.
 Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
Dansk resumé for begyndere
 Dansk resumé for begyndere Dansk resumé for begyndere Dette afsnit introducerer bakteriel genregulation for enhver uden forudgående kendskab til dette emne. Alle nødvendige, videnskabelige betegnelser
Dansk resumé for begyndere Dansk resumé for begyndere Dette afsnit introducerer bakteriel genregulation for enhver uden forudgående kendskab til dette emne. Alle nødvendige, videnskabelige betegnelser
4. Onkogener og tumorsuppressorer
 4. Onkogener og tumorsuppressorer Kræftcellernes svar på speeder og bremse Dette kapitel fortæller, hvorfor kræftceller deler sig ukontrolleret hvad et onkogen er hvad en tumorsuppressor er hvad denne
4. Onkogener og tumorsuppressorer Kræftcellernes svar på speeder og bremse Dette kapitel fortæller, hvorfor kræftceller deler sig ukontrolleret hvad et onkogen er hvad en tumorsuppressor er hvad denne
Imatinib til behandling af GIST
 Imatinib til behandling af GIST - et case study af targeted therapeutics Treatment of GIST with Imatinib a case study of targeted therapeutics December 2006 Molekylærbiologi Modul I Roskilde Universitetscenter
Imatinib til behandling af GIST - et case study af targeted therapeutics Treatment of GIST with Imatinib a case study of targeted therapeutics December 2006 Molekylærbiologi Modul I Roskilde Universitetscenter
Biofysik-kompendium Mark Niegsch 2003. Biofysik-Kompendium. Udarbejdet af 2.sem 2003 Stud. Med. Mark Niegsch. manan.
 Biofysik-Kompendium Udarbejdet af 2.sem 2003 Stud. Med. Mark Niegsch manan.dk Side 1 af 48 Indhold INDHOLD 2 1.TRANSPORTPROCESSER. 4 1.1 STOFTRANSPORT I ET FRIT UBEGRÆNSET MEDIUM 4 J (FLUXEN) 4 FICK S
Biofysik-Kompendium Udarbejdet af 2.sem 2003 Stud. Med. Mark Niegsch manan.dk Side 1 af 48 Indhold INDHOLD 2 1.TRANSPORTPROCESSER. 4 1.1 STOFTRANSPORT I ET FRIT UBEGRÆNSET MEDIUM 4 J (FLUXEN) 4 FICK S
Eukaryote celler arbejder
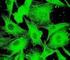 Eukaryote celler arbejder Niveau: 9. klasse Varighed: 5 lektioner Præsentation: I dette forløb skal eleverne arbejde med den eukaryote celle. I forløbet kommer vi omkring funktioner og kemiske processer
Eukaryote celler arbejder Niveau: 9. klasse Varighed: 5 lektioner Præsentation: I dette forløb skal eleverne arbejde med den eukaryote celle. I forløbet kommer vi omkring funktioner og kemiske processer
FORKOMST OG EFFEKTER AF HORMONFORSTYRRENDE KEMIKALIER I DANSKE VANDLØB
 AARHUS UNIVERSITET Den 8. December 2010 FORKOMST OG EFFEKTER AF HORMONFORSTYRRENDE KEMIKALIER I DANSKE VANDLØB Pia Lassen, Seniorforsker Danmarks Miljøundersøgelser, Aarhus Universitet FORMÅL Formålet
AARHUS UNIVERSITET Den 8. December 2010 FORKOMST OG EFFEKTER AF HORMONFORSTYRRENDE KEMIKALIER I DANSKE VANDLØB Pia Lassen, Seniorforsker Danmarks Miljøundersøgelser, Aarhus Universitet FORMÅL Formålet
Sommereksamen 2011. Titel på kursus: De endokrine organer I. Eksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 Bedømmelsesform Bestået-/ikke bestået
 Sommereksamen 2011 Titel på kursus: e endokrine organer I Uddannelse: achelor Semester: 2. semester ksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 edømmelsesform estået-/ikke bestået Vigtige oplysninger:
Sommereksamen 2011 Titel på kursus: e endokrine organer I Uddannelse: achelor Semester: 2. semester ksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 edømmelsesform estået-/ikke bestået Vigtige oplysninger:
En forsker har lavet et cdna insert vha PCR og har anvendt det følgende primer sæt, som producerer hele den åbne læseramme af cdna et:
 F2011-Opgave 1. En forsker har lavet et cdna insert vha PCR og har anvendt det følgende primer sæt, som producerer hele den åbne læseramme af cdna et: Forward primer: 5 CC ATG GGT ATG AAG CTT TGC AGC CTT
F2011-Opgave 1. En forsker har lavet et cdna insert vha PCR og har anvendt det følgende primer sæt, som producerer hele den åbne læseramme af cdna et: Forward primer: 5 CC ATG GGT ATG AAG CTT TGC AGC CTT
PCR (Polymerase Chain Reaction): Opkopiering af DNA
 PCR (Polymerase Chain Reaction): Opkopiering af DNA PCR til at opkopiere bestemte DNA-sekvenser i en prøve er nu en af genteknologiens absolut vigtigste værktøjer. Peter Rugbjerg, Biotech Academy PCR (Polymerase
PCR (Polymerase Chain Reaction): Opkopiering af DNA PCR til at opkopiere bestemte DNA-sekvenser i en prøve er nu en af genteknologiens absolut vigtigste værktøjer. Peter Rugbjerg, Biotech Academy PCR (Polymerase
EKSAMEN. ALMEN FARMAKOLOGI (Modul 1.2) Medicin og MedIS 1. semester. Mandag den 13. januar :00-11:00
 1 Aalborg University EKSAMEN ALMEN FARMAKOLOGI (Modul 1.2) Medicin og MedIS 1. semester Mandag den 13. januar 2014 09:00-11:00 2 timer skriftlig eksamen, evalueres med karakter efter 7-skalaen. Intern
1 Aalborg University EKSAMEN ALMEN FARMAKOLOGI (Modul 1.2) Medicin og MedIS 1. semester Mandag den 13. januar 2014 09:00-11:00 2 timer skriftlig eksamen, evalueres med karakter efter 7-skalaen. Intern
Menneskets væskefaser
 Menneskets væskefaser Mennesket består af ca. 60% væske (vand) Overordnet opdelt i to: Ekstracellulærvæske og intracellulærvæske Ekstracellulærvæske udgør ca. 1/3 Interstitielvæske: Væske der ligger mellem
Menneskets væskefaser Mennesket består af ca. 60% væske (vand) Overordnet opdelt i to: Ekstracellulærvæske og intracellulærvæske Ekstracellulærvæske udgør ca. 1/3 Interstitielvæske: Væske der ligger mellem
Nervesystemets celler, fysiologi & kemi
 Nervesystemets celler, fysiologi & kemi Carsten Reidies Bjarkam. Professor, specialeansvarlig overlæge, Ph.D. Neurokirurgisk Afdeling Aalborg Universitetshospital Nervesystemet er opbygget af nerveceller
Nervesystemets celler, fysiologi & kemi Carsten Reidies Bjarkam. Professor, specialeansvarlig overlæge, Ph.D. Neurokirurgisk Afdeling Aalborg Universitetshospital Nervesystemet er opbygget af nerveceller
Atomic force mikroskopi på blodceller
 1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
Det hæmostatiske system
 Det hæmostatiske system Hæmostasen omfatter alle de mekanismer, som bidrager til at standse en blødning. Blodets evne til at holde sig flydende under normale omstændigheder og evne til at størkne i et
Det hæmostatiske system Hæmostasen omfatter alle de mekanismer, som bidrager til at standse en blødning. Blodets evne til at holde sig flydende under normale omstændigheder og evne til at størkne i et
Undervisningsbeskrivelse for STX 1m Kemi B
 Undervisningsbeskrivelse for STX 1m Kemi B Termin Afslutning i juni skoleår 14/15 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi B Hasse Bonde Rasmussen 1mKe Denne undervisningsbeskrivelse
Undervisningsbeskrivelse for STX 1m Kemi B Termin Afslutning i juni skoleår 14/15 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi B Hasse Bonde Rasmussen 1mKe Denne undervisningsbeskrivelse
Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting
 Center for Undervisningsmidler, afdeling København Western blotting Øvelsesvejledning Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting Teori Proteomik er studiet af celleproteiners
Center for Undervisningsmidler, afdeling København Western blotting Øvelsesvejledning Formål At analysere for myosin i muskelvæv fra fisk ved brug af western blotting Teori Proteomik er studiet af celleproteiners
Kapitel 17. the cytoskeleton: microtubules. Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526
 Kapitel 17 the cytoskeleton: microtubules Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526 [email protected] Tre typer af protein filamenter, som danner cytoskelletet OBS: mikrovilli ikke
Kapitel 17 the cytoskeleton: microtubules Søren Tvorup Christensen, Biokemisk afdeling, AKI, rum 526 [email protected] Tre typer af protein filamenter, som danner cytoskelletet OBS: mikrovilli ikke
Undervisningsbeskrivelse for STX 2m Kemi B
 Undervisningsbeskrivelse for STX 2m Kemi B Termin Afslutning i juni skoleår 13/14 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi A valgfag Hasse Bonde Rasmussen 3gKE Denne
Undervisningsbeskrivelse for STX 2m Kemi B Termin Afslutning i juni skoleår 13/14 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi A valgfag Hasse Bonde Rasmussen 3gKE Denne
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men
 På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
På grund af reglerne for copyright er det ikke muligt at lægge figurer fra lærebøger på nettet. Derfor har jeg fjernet figurerne fra slides ne, men skrevet hvorfra de er taget. De tre bøger, hvorfra illustrationerne
- men er det farligt for mennesker?
 Center for Hormonforstyrrende Center Hormonforstyrrende Stoffer Stoffer cehos.dk Hormonforstyrrende effekter - men er det farligt for mennesker? Anna-Maria Andersson biolog, centerleder og forsker ved
Center for Hormonforstyrrende Center Hormonforstyrrende Stoffer Stoffer cehos.dk Hormonforstyrrende effekter - men er det farligt for mennesker? Anna-Maria Andersson biolog, centerleder og forsker ved
Effekt af hydrolyse af animalske biprodukter på interaktion og optag af jern
 Effekt af hydrolyse af animalske biprodukter på interaktion og optag af jern René Lametsch Trine D. Damgaard Section of DMP, department of Food science Dias 1 Animalske biprodukter Definitionen af hvad
Effekt af hydrolyse af animalske biprodukter på interaktion og optag af jern René Lametsch Trine D. Damgaard Section of DMP, department of Food science Dias 1 Animalske biprodukter Definitionen af hvad
Re- eksamen Det hæmatologiske system og immunsystemet. Bacheloruddannelsen i Medicin/Medicin med industriel specialisering
 Studienummer: 1 Re- eksamen 2012 Titel på kursus: Uddannelse: Semester: Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin med industriel specialisering 2. semester Eksamensdato:
Studienummer: 1 Re- eksamen 2012 Titel på kursus: Uddannelse: Semester: Det hæmatologiske system og immunsystemet Bacheloruddannelsen i Medicin/Medicin med industriel specialisering 2. semester Eksamensdato:
BIOTEKNOLOGI HØJT NIVEAU
 STUDENTEREKSAMEN 2007 2007-BT-1 BITEKNLGI HØJT NIVEAU Torsdag den 31. maj 2007 kl. 9.00 14.00 Sættet består af 1 stor og 2 små opgaver samt 1 bilag i 2 eksemplarer. Det ene eksemplar af bilaget afleveres
STUDENTEREKSAMEN 2007 2007-BT-1 BITEKNLGI HØJT NIVEAU Torsdag den 31. maj 2007 kl. 9.00 14.00 Sættet består af 1 stor og 2 små opgaver samt 1 bilag i 2 eksemplarer. Det ene eksemplar af bilaget afleveres
TrP Akupunktur kursus
 TrP Akupunktur kursus Hvad er jeres forventninger og erfaringer med emnet? Vores forventninger er at i bliver fortrolige med TrP aku, og at i føler jer rustet til at behandle med nåle overfor visse smertetilstande.
TrP Akupunktur kursus Hvad er jeres forventninger og erfaringer med emnet? Vores forventninger er at i bliver fortrolige med TrP aku, og at i føler jer rustet til at behandle med nåle overfor visse smertetilstande.
Ekstrakter - rammebevillinger
 Ekstrakter - rammebevillinger Professor Bente Vilsen Aarhus Universitet Biokemi 4.736.000 kr. Natrium-kalium pumpen sidder i membranen på alle celler og er livsnødvendig for at opretholde deres funktion.
Ekstrakter - rammebevillinger Professor Bente Vilsen Aarhus Universitet Biokemi 4.736.000 kr. Natrium-kalium pumpen sidder i membranen på alle celler og er livsnødvendig for at opretholde deres funktion.
X M Y. What is mediation? Mediation analysis an introduction. Definition
 What is mediation? an introduction Ulla Hvidtfeldt Section of Social Medicine - Investigate underlying mechanisms of an association Opening the black box - Strengthen/support the main effect hypothesis
What is mediation? an introduction Ulla Hvidtfeldt Section of Social Medicine - Investigate underlying mechanisms of an association Opening the black box - Strengthen/support the main effect hypothesis
14. Mandag Endokrine kirtler del 2
 14. Mandag Endokrine kirtler del 2 Midt i dette nye spændende emne om endokrine kirtler kan det være nyttigt med lidt baggrundsdiskussion omkring især glukoses (sukkerstof) forskellige veje i kroppen.
14. Mandag Endokrine kirtler del 2 Midt i dette nye spændende emne om endokrine kirtler kan det være nyttigt med lidt baggrundsdiskussion omkring især glukoses (sukkerstof) forskellige veje i kroppen.
BIOTEKNOLOGI HØJT NIVEAU
 STUDETEREKSAME 2006 2006-BT-2 BIOTEKOLOGI HØJT IVEAU Onsdag den 16. august 2006 kl. 9.00 14.00 Sættet består af 1 stor og 2 små opgaver. Alle hjælpemidler tilladt. STOR OPGAVE 1. Myoglobin A. Den røde
STUDETEREKSAME 2006 2006-BT-2 BIOTEKOLOGI HØJT IVEAU Onsdag den 16. august 2006 kl. 9.00 14.00 Sættet består af 1 stor og 2 små opgaver. Alle hjælpemidler tilladt. STOR OPGAVE 1. Myoglobin A. Den røde
[ ] =10 7,4 = 40nM )
![[ ] =10 7,4 = 40nM ) [ ] =10 7,4 = 40nM )](/thumbs/22/1453135.jpg) Syre og base homeostasen (BN kap. 9) Nyrefysiologi: Syre/base homeostase, kap. 9 Normal ph i arterielt plasma: 7,4 ( plasma H + [ ] =10 7,4 = 40nM ) o ECV indhold af H+: 40 nm (ph 7,4) x 15 l =600 nmol
Syre og base homeostasen (BN kap. 9) Nyrefysiologi: Syre/base homeostase, kap. 9 Normal ph i arterielt plasma: 7,4 ( plasma H + [ ] =10 7,4 = 40nM ) o ECV indhold af H+: 40 nm (ph 7,4) x 15 l =600 nmol
Cellen og dens funktioner
 Eksamensopgaver Biologi C, 17bic80 6. og 7. juni 2018 1 Cellen og dens funktioner 1. Redegør for hvordan eukaryote og prokaryote celler i hovedtræk er opbygget, herunder skal du gøre rede for forskelle
Eksamensopgaver Biologi C, 17bic80 6. og 7. juni 2018 1 Cellen og dens funktioner 1. Redegør for hvordan eukaryote og prokaryote celler i hovedtræk er opbygget, herunder skal du gøre rede for forskelle
Aktivering af Survey funktionalitet
 Surveys i REDCap REDCap gør det muligt at eksponere ét eller flere instrumenter som et survey (spørgeskema) som derefter kan udfyldes direkte af patienten eller forsøgspersonen over internettet. Dette
Surveys i REDCap REDCap gør det muligt at eksponere ét eller flere instrumenter som et survey (spørgeskema) som derefter kan udfyldes direkte af patienten eller forsøgspersonen over internettet. Dette
Epigenetik Arv er andet end gener
 Epigenetik Arv er andet end gener Indhold Indledning Afsnit1: Epigenetik og DNA Afsnit 2: DNA, nukleosomer og kromatin Afsnit 3: Epigenetik og celledifferentiering Afsnit 4: Genetisk ens individer kan
Epigenetik Arv er andet end gener Indhold Indledning Afsnit1: Epigenetik og DNA Afsnit 2: DNA, nukleosomer og kromatin Afsnit 3: Epigenetik og celledifferentiering Afsnit 4: Genetisk ens individer kan
Cellekernen (Nucleus) Sebastian Frische Anatomisk Institut
 Cellekernen (Nucleus) Sebastian Frische Anatomisk Institut Cellekernen Cellekernens overordnede struktur kernemembranen/nucleolemma kromatin nucleolus Cellecyklus faser i cellecyklus faser i mitosen Størrelse:
Cellekernen (Nucleus) Sebastian Frische Anatomisk Institut Cellekernen Cellekernens overordnede struktur kernemembranen/nucleolemma kromatin nucleolus Cellecyklus faser i cellecyklus faser i mitosen Størrelse:
Proteiner. Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde
 Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
Proteiner Proteiner er molekyler der er opbygget af "aminosyrer",nogle er sammensat af få aminosyrer medens andre er opbygget af mange tusinde Der findes ca. 20 aminosyrer i menneskets organisme. Nogle
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Intercellulær komponenter og transport
 Intercellulær komponenter og transport En eucaryotic celle har mange funktioner, men det kræver at alle komponenter i cellen er adskilt af endomembraner, hvor i procaryotic celle har kun en komponent,
Intercellulær komponenter og transport En eucaryotic celle har mange funktioner, men det kræver at alle komponenter i cellen er adskilt af endomembraner, hvor i procaryotic celle har kun en komponent,
EKSAMEN. ALMEN FARMAKOLOGI, modul 1.2. Medicin og MedIS 1. semester. Torsdag den 21. februar :00-11:00
 Aalborg Universitet EKSAMEN ALMEN FARMAKOLOGI, modul 1.2 Medicin og MedIS 1. semester Torsdag den 21. februar 2016 09:00-11:00 Skriftlig eksamen, evalueres med karakter efter 7-skalaen. Intern censur.
Aalborg Universitet EKSAMEN ALMEN FARMAKOLOGI, modul 1.2 Medicin og MedIS 1. semester Torsdag den 21. februar 2016 09:00-11:00 Skriftlig eksamen, evalueres med karakter efter 7-skalaen. Intern censur.
BIOLOGI HØJT NIVEAU. Mandag den 9. august 2004 kl
 STUDENTEREKSAMEN AUGUST 2004 2004-6-2 BIOLOGI HØJT NIVEAU Mandag den 9. august 2004 kl. 9.00-14.00 Af de store opgaver 1 og 2 må kun den ene besvares. Af de små opgaver 3, 4, 5 og 6 må kun to besvares.
STUDENTEREKSAMEN AUGUST 2004 2004-6-2 BIOLOGI HØJT NIVEAU Mandag den 9. august 2004 kl. 9.00-14.00 Af de store opgaver 1 og 2 må kun den ene besvares. Af de små opgaver 3, 4, 5 og 6 må kun to besvares.
Den menneskelige cochlea
 Den menneskelige cochlea Af Leise Borg Leise Borg er netop blevet cand.scient. Artiklen bygger på hendes speciale i biofysik Introduktion Hørelsen er en vigtig sans for mennesket, både for at sikre overlevelse,
Den menneskelige cochlea Af Leise Borg Leise Borg er netop blevet cand.scient. Artiklen bygger på hendes speciale i biofysik Introduktion Hørelsen er en vigtig sans for mennesket, både for at sikre overlevelse,
8. Metastasering. Kræftceller, der spreder sig
 8. Metastasering Kræftceller, der spreder sig Dette kapitel fortæller, hvordan kræftceller spreder sig i kroppen hvilke egenskaber en celle skal have for at kunne sprede sig Celle bliv på din plads Et
8. Metastasering Kræftceller, der spreder sig Dette kapitel fortæller, hvordan kræftceller spreder sig i kroppen hvilke egenskaber en celle skal have for at kunne sprede sig Celle bliv på din plads Et
Fysikken bag hverdagens materialer.
 Fysikken bag hverdagens materialer. Carsten Svaneborg, Lektor Institut for Fysik, Kemi og Farmaci Syddansk Universitetet Campusvej 55, 5320 Odense M [email protected] Http://www.zqex.dk Oversigt Intro hverdagens
Fysikken bag hverdagens materialer. Carsten Svaneborg, Lektor Institut for Fysik, Kemi og Farmaci Syddansk Universitetet Campusvej 55, 5320 Odense M [email protected] Http://www.zqex.dk Oversigt Intro hverdagens
Undervisningsbeskrivelse for STX 2t Kemi C
 Undervisningsbeskrivelse for STX 2t Kemi C Termin Afslutning i juni skoleår 14/15 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi C Hasse Bonde Rasmussen 2t ke Denne undervisningsbeskrivelse
Undervisningsbeskrivelse for STX 2t Kemi C Termin Afslutning i juni skoleår 14/15 Institution Marie Kruses Skole Uddannelse Fag og niveau Lærer(e) Hold STX Kemi C Hasse Bonde Rasmussen 2t ke Denne undervisningsbeskrivelse
Ekstra zink og kobber til grise i fravænningsperioden? Bag om de fysiologiske mekanismer. Danmarks JordbrugsForskning
 Husdyrbrug nr. 35 Juni 2003 Ekstra zink og kobber til grise i fravænningsperioden? Bag om de fysiologiske mekanismer Dorthe Carlson & Hanne Damgaard Poulsen Afd. for Husdyrernæring og Fysiologi, Forskningscenter
Husdyrbrug nr. 35 Juni 2003 Ekstra zink og kobber til grise i fravænningsperioden? Bag om de fysiologiske mekanismer Dorthe Carlson & Hanne Damgaard Poulsen Afd. for Husdyrernæring og Fysiologi, Forskningscenter
Biocide resistance in Salmonella Typhimurium
 FACULTY OF HEALTH AND MEDICAL SCIENCES UNIVERSITY OF COPENHAGEN PhD thesis Mette Rørbæk Gantzhorn Biocide resistance in Salmonella Typhimurium Academic advisor: Line Elnif Thomsen This thesis has been
FACULTY OF HEALTH AND MEDICAL SCIENCES UNIVERSITY OF COPENHAGEN PhD thesis Mette Rørbæk Gantzhorn Biocide resistance in Salmonella Typhimurium Academic advisor: Line Elnif Thomsen This thesis has been
Naturvidenskabelig metode
 Naturvidenskabelig metode Introduktion til naturvidenskab Naturvidenskab er en betegnelse for de videnskaber der studerer naturen gennem observationer. Blandt sådanne videnskaber kan nævnes astronomi,
Naturvidenskabelig metode Introduktion til naturvidenskab Naturvidenskab er en betegnelse for de videnskaber der studerer naturen gennem observationer. Blandt sådanne videnskaber kan nævnes astronomi,
Ekstraordinær re-eksamen 2015
 Ekstraordinær re-eksamen 2015 Titel på kursus: Uddannelse: Semester: Introduktion til basalfagene Bachelor i Medicin og Medicin med Industriel Specialisering 1. semester Eksamensdato: 04-08-2016 Tid: kl.
Ekstraordinær re-eksamen 2015 Titel på kursus: Uddannelse: Semester: Introduktion til basalfagene Bachelor i Medicin og Medicin med Industriel Specialisering 1. semester Eksamensdato: 04-08-2016 Tid: kl.
Komplementsystemets fysiologi og patofysiologi. Søren Hansen, Cancer og Inflammationsforskning, WP21-1, [email protected]
 Komplementsystemets fysiologi og patofysiologi C3 Søren Hansen, Cancer og Inflammationsforskning, WP21-1, [email protected] Detaljeret - aktiveringsmekanismer - opbygning - effektorfunktioner (incl.
Komplementsystemets fysiologi og patofysiologi C3 Søren Hansen, Cancer og Inflammationsforskning, WP21-1, [email protected] Detaljeret - aktiveringsmekanismer - opbygning - effektorfunktioner (incl.
Er der flere farver i sort?
 Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
Eksamensspørgsmål til BiB biologi B 2015
 Eksamensspørgsmål til BiB biologi B 2015 Med udgangspunkt i de udleverede bilag og temaet evolution skal du: 1. Redegøre for nogle forskellige teorier om evolution, herunder begrebet selektion. 2. Analysere
Eksamensspørgsmål til BiB biologi B 2015 Med udgangspunkt i de udleverede bilag og temaet evolution skal du: 1. Redegøre for nogle forskellige teorier om evolution, herunder begrebet selektion. 2. Analysere
