Osteoporose og Parathyroideahormon
|
|
|
- Søren Oscar Toft
- 9 år siden
- Visninger:
Transkript
1 Osteoporose og Parathyroideahormon En analyse af Parathyroideahormons anabolske og katabolske virkning Osteoporosis and Parathyroid hormone An Analysis of Parathyroid Hormones Anabolic and Catabolic Function Studerende: Mille Dahl Andersen Derya Aslan Lene Bjerring Gede Tine Kelleman Hansen Sara Rubek Jørgensen Vejleder: Niklas Rye Jørgensen Ekstern lektor på Natur, Systemer og Modeller / Medicinalbiologi 4. semester, forår 2008, hus 13.2 Naturvidenskabelige basisstudier
2 II Roskilde universitetscenter
3 III
4 Abstrakt Dette projekt belyser hvilke mekanismer, der ligger til grund for parathyroideahormons (PTH) s anabolske virkning på knoglerne givet ved impulsbehandling. Dette er interessant, da PTH normalt har en katabolsk virkning i kroppen, og ved forhøjede værdier kan føre til osteoporose. Projektet er et litteraturstudie, som er centreret omkring at finde hypoteser for PTH anabolske virkning. Følgende hypoteser er beskrevet og diskuteret; 1) Proteinkinase A-signalvejen er essentiel for PTH s anabolske virkning 2) PTH opregulerer c-fos-udtrykket i knogleceller, 3) IGF-I er essentiel for PTH s anabolske virkning ved blandt andet at stimulere antiapoptose og proliferation, 4) bone lining celler omdannes til osteoblaster, 5) mesenkymale stamceller klæber sig fast på knogleoverflader og danner kolonier under påvirkning af PTH, 6) PTH har en antiapoptotisk effekt på osteoblaster og 7) når impulsgivet PTH griber ind i knogleremodelleringen overkompenserer osteoblaster. PTH s netto knogleformative effekt ved impulsbehandling fremkommer igennem et komplekst netværk af signalveje der alle resulterer i det såkaldte anabole vindue, som skyldes, at PTH aktiverer osteoblaster, der pga. PTH s korte halveringstid enten ikke når at opregulere RANKL eller opregulerer denne i mindre grad. Osteoklastforstadier får hermed ikke, eller kun i mindre grad, deres signal til differentiering, hvorfor modne osteoklaster ikke dannes, mens osteoblaster overkompenserer. Dette, sammen med den omstændighed, at der findes flere knogle sites hvor der foregår formation end resorption, resulterer i en netteoknogleformativ effekt. IV
5 V
6 Abstract This project clarifies which mechanisms that underlie the anabolic effect of parathyroid hormone (PTH) on bones, given in intermittent treatment. This is interesting because PTH normally has a katabolic effect in the body, and by increased values can lead to osteoporosis. This project is a literary study which is centred on finding hypotheses about the anabolic effect of PTH. Following hypotheses are described and discussed; 1) The proteinkinase A pathway is essential for PTH s anabolic effect, 2) PTH up regulates c-fos expression in bone cells, 3) IGF-I is essential for PTH s anabolic effect because it, amongs other things, stimulates antiapoptosis and proliferation, 4) bone lining cells converts to osteoblasts, 5) mesenchymal stem cells adhere to the bone surface and form colonies under the influence of PTH, 6) PTH has an antiapoptotic effect on osteoblasts and 7) when PTH interferes with remodelling the osteoblasts over compensate. The netto formative effect of PTH given in intermittent treatment emerge through a complex network of pathways, which all results in the so called Anabolic window, caused by PTH activation of osteoblasts which, because of the short half-life of PTH, either do not up regulate RANKL, or up regulates this to a lesser degree. Hereby, the osteoklast precursors do not get their signal for differentiation, or get it to a lesser degree, and therefore mature osteoclasts will not be formed, while osteoblasts overcompensate. This, and the fact, that there are more bone sites where formation takes place than with resoption, gives the netto anabolic effect. VI
7 VII
8 Forord Projektet er udarbejdet i foråret 2008, og er et fjerde semesterprojekt på det naturvidenskabelige basisstudium på Roskilde Universitetscenter. Fjerde semesterprojekt på RUC er ikke bundet af en egentlig semesterbinding, som det er tilfældet i de foregående tre semestre. Dog skal dette semesters projektarbejde inddrage og omhandle naturvidenskabelige teorier, metoder og fænomener, hvor formålet er at kunne opnå fordybelse på baggrund af erfaringerne tildraget i de forudgående semestre [Studievejledningen 2007]. Nærværende projekt er et litterært studie, der ønsker at belyse og diskuterer hvilke mekanismer, der ligger til grund for at parathyroideahormon, indenfor knogleremodellering, virker katabolsk ved kontinuerligt forhøjede værdier og anabolsk ved impulsbehandling. I denne forbindelse arbejdes der med naturvidenskabelige teorier, metoder og hypoteser. Projektet henvender sig til forskere indenfor feltet knoglebiologi, samt personer med interesse i emnet. For personer som ikke arbejder eller har viden indenfor knoglebiologien, kræves visse læseforudsætninger for at kunne opnå forståelse for projektet. Disse kan med fordel være en grundlæggende molekylærbiologisk og biokemisk viden svarende til gennemførelsen af en molekylær- og medicinalbiologisk bachelorgrad. I forbindelse med dette projekt vil vi gerne takke vores vejleder Niklas Rye Jørgensen, ekstern lektor på Natur, System og Modeller på Roskilde Universitetscenter; 1. Reservelæge på Klinisk Biokemisk Afdeling på Roskilde Sygehus og Forskningscenter for Aldring og Osteoporose, Glostrup Hospital, for professionel og kyndig vejledning gennem hele forløbet. Roskilde Universitetscenter, den 30. maj 2008 Projektet er udarbejdet af: Mille Dahl Andersen Lene Bjerring Gede Tine Kellemann Hansen Derya Aslan Sara Rubek Jørgensen VIII
9 IX
10 Læsevejledning Nedenstående læsevejledning er udformet med ønske om, at læseren får en forståelse for projektets opbygning. Ud over de obligatoriske indledende punkter, såsom problemformulering, metode m.m., ønsker projektet først at give en kort redegørelse for sygdommen osteoporose, som danner baggrund for det udformede problemfelt. Herunder vil det kort præsenteres, hvordan sygdommen diagnosticeres og hvilke behandlingsmuligheder der eksisterer på nuværende tidspunkt. For interesserede personer med forudsætninger svarende til molekylærbiologisk og biokemisk viden på universitetsniveau, men uden indgående kendskab til knoglebiologien, medtages teoriafsnittet 2 Knoglebiologi. I dette afsnit forklares knogle - og calciummetabolismen, herunder PTH s virkning på knogleceller og relevante signalveje i forbindelse hermed. Skulle læseren i forvejen have kendskab til den grundlæggende knoglebiologi, kan pågældende teoridel undlades, og i stedet kan læseren påbegynde afsnittet 4 Osteoporosepatogenese. I dette afsnit klarlægges de patofysiologiske mekanismer, der forårsager osteoporose. I afsnittet vil centrale hormoner, vækstfaktorer og vitaminer, der er essentielle for sygdomsudviklingen, gennemgås. Hvis læseren i forvejen har kendskab til osteoporose og de bagvedliggende mekanismer, kan afsnittene 2 Knoglebiologi, 1 Osteoporose og 4 Osteporosepatogenese undlades. I afsnittet 5 Hypoteser omkring parathyroideahormons anabolske effekt præsenteres de af projektgruppen udvalgte hypoteser for PTH s anabolske virkning. Hypoteserne er valgt ud fra eksperimentelle forsøg, der underbygger disse. I denne forbindelse vil selve eksperimentet, resultater, diskussion og konklusioner præsenteres. Efterfølgende vil der være en diskussion af hypoteserne, hvor eventuelle overenstemmelser eller uoverensstemmelser blandt disse sammenholdes og diskuteres med henblik på troværdigheden af eksperimenternes resultater. Heraf vil drages en konklusion og projektrapporten sluttes af med en perspektivering. Efter læsevejledningen forefindes en forkortelsesliste. De kilder som i hypoteserne tages udgangspunkt i, kaldes hovedkilder. Alle kilder skrives i hårde klammer, medmindre det er kilder, som afsnittets hovedkilde refererer til, som ikke er blevet grundigt læst. Dette skyldes tidsmæssige årsager eller at det ikke har været muligt, at finde disse kilder. I sådanne tilfælde skrives kilderne i bløde parenteser. X
11 XI
12 Forkortelser ALP Alkaline phosphatase (Alkalisk fosfortase) AP-1 Activator Protein-1 (Aktivator Protein-1) ATF Activating Transcription Factor (Aktiverende transkription faktor) ATP Adenosine triphosphat (Adenosin trifosfat) BMD Bone mineral density (Knoglemineraldensitet) BMP Bone morphogenetic proteins (Knoglemorfogenetiske proteiner) camp Cyclic adenosine monophosphat (Cykliske adenosin monofosfat) CaSR Calcium receptors (Calcium receptorer) c-fms Receptor for M-CSF (Receptor for M-CSF) DXA Dual energy X-ray absorption (Dual energi X-ray-absorption) GDP Guanosine diphosphat (Guanosin difosfat) hpth Human Parathyroid hormone (menneske parathyroideahormon) IGF-I Insulin growth factor I (Insulin vækstfaktor-i) IL Interleukin (Interleukin) LIF Leukemia inhibitory factor (Leukemia inhibitor faktor) M-CSF Macrofag coloni stimulating factor (Makrofag koloni-stimulerende faktor) MDR Minimal daily requiertment (Det daglige minimale behov) MSC Mesenchymal stem cells (Mesenkymale stamceller) NFATc1 Nuclear factor of activated T-cells 1 (Nukleær faktor af aktiverede T- celler 1) NFkB Nuclear factor-kb (Nuclear faktor-kb) OPG Osteoprotegerin (Osteoprotegerin) OSM Oncostatin M (Oncostain M) OVX Ovariectomized (Overiektomerede) PBM Maximal bone niveau (Maksimale knogle niveau) PGE2 Prostaglandin E2 (Prostaglandin E2) PKA Protein kinase A (Protein kinase A) PKC Protein kinase C (Protein kinase C) PLC γ Phospholipase C γ (Fosforlipase C γ) PMA Phorbon 12-myristate 13-acetate (Forbon 12-myristat 13-acetat) PTH Parathyorid hormon (Parathyorideahormon) PTHrP Parathyorid hormone related protein (Parathyorideahormon- relateret protein) PTHr1 Parathyorid hormone receptor 1 (Parathyorideahormon receptor 1) RANK: Receptor nuklear factor-kb (Receptor nukleær faktor-kb) RANKL Receptor nuklear factor-kb ligand (Receptor nukleær faktor-kb ligand) RER Rough endoplasmtic reticulum (Ru endoplasmatisk retikulum) TGF-β: Transforming growth factor- beta (Transforming vækst faktor- beta) TNF Tumor necrosis factor (Tumor necrosis faktor) TNF-α Tumor necrosis factor-α (Tumor necrosis faktor-α) TRAF6 Tumor necrosis factor Receptor-Associated Factor 6 (Tumor necrosis XII
13 faktor receptor-associeret faktor 6) Vitamin D3 1,25-dihydroxyvitamin D3 (1,25-dihydroxyvitamin D3) VDR Vitamin D receptor ( Vitamin D receptor) XIII
14 Indholdsfortegnelse INDLEDNING... 1 PROBLEMFORMULERING... 3 PROBLEMFELT... 3 METODE OSTEOPOROSE DIAGNOSTICERING BEHANDLINGSMULIGHEDER KNOGLEBIOLOGI KNOGLEOPBYGNING Makroskopisk knoglestruktur Mikroskopisk knoglestruktur KNOGLECELLER Osteoblaster Osteoklaster Osteoklastogenese CALCIUMHOMØOSTASEN PARATHYORIDEAHORMON OSTEOPOROSEPATOGENESE CYTOKINER PROSTAGLANDIN VITAMIN D VÆKSTFAKTORER HYPOTESER OMKRING PARATHYROIDEAHORMONS ANABOLSKE EFFEKT PROTEINKINASE A OG -C AFHÆNGIGE SIGNLVEJE OG PARATHYROIDEAHORMONS ANABOLSKE EFFEKT PARATHYROIDEAHORMON OPREGULERER C-FOS-UDTRYKKET I KNOGLECELLER IGF-I ER ESSENTIEL FOR PARATHYROIDEAHORMONS ANABOLSKE VIRKNING PARATHYROIDEAHORMONS AKTIVERING AF BONE LINING CELLER TIL OMDANNELSE TIL OSTEOBLASTER PARATHYROIDEAHORMON STIMULERER SAMMENKLÆBNING AF MESENKYMALE STAMCELLER TIL KNOGLEOVERFLADER PARATHYROIDEAHORMONS ANTIAPOPTISKE VIRKNING PÅ KNOGLECELLER NÅR IMPULSGIVET PTH GRIBER IND I REMODELLERINGEN OVERKOMPENSERER OSTEOBLASTER DISKUSSION PROTEINKINASE A OG -C AFHÆNGIGE SIGNLVEJE OG PARATHYROIDEAHORMONS ANABOLSKE EFFEKT BONE LINING CELLER OMDANNES TIL OSTEOBLASTER OG MSC KLÆBES TIL KNOGLEOVERFLADER PARATHYROIDEAHORMONS ANTIAPOPTISKE VIRKNING PÅ KNOGLECELLER IGF-I ER ESSENTIEL FOR PARATHYROIDEAHORMONS ANABOLSKE VIRKNING PARATHYROIDEAHORMON OPREGULERER C-FOS-UDTRYKKET I KNOGLECELLER NÅR IMPULSGIVET PTH GRIBER IND I REMODELLERINGEN OVERKOMPENSERER OSTEBLASTER OPSAMLING AF HYPOTESER DET ANABOLE VINDUE KONKLUSION PERSPEKTIVERING LITTERATURLISTE XIV
15 XV
16
17 Indledning Osteoporose, som i daglig tale kaldes knogleskørhed, er en betegnelse for fremkomsten af porøse knogler. Osteoporose kan i sidste ende resultere i frakturer, hvis knoglerne udsættes for en større kraft end de kan klare, og disse kan ved denne tilstand opstå selv ved beskedne belastninger. [Osteoporosedoktor 2008]. Osteoporose er en af de oftest forekommende sygdomme. Det forudsiges, at tilfælde af osteoporose på verdensplan vil stige fra 300 millioner til 700 millioner i de næste 25 år, og at lidelsen yderligere vil opnå epidemiske proportioner [Henderson & Goltzman 2000]. Risikoen for osteoporose stiger med alderen, og det er også denne tilstand, der bevirker sammenfald i ryggen, som ofte ses hos ældre mennesker. Pga. den aldersafhængige risiko er problemet stigende, da befolkningen bliver ældre og ældre, hvorfor osteoporose udgør et væsentligt folkesundhedsproblem [Fødevaredirektoratet/sundhedsstyrelsen 2000]. Sygdommen er især et stort problem for kvinder, da tabet af østrogen i overgangsalderen bevirker en hurtigere reduktion af knoglemassen. Dette skyldes, at østrogen under normale omstændigheder er med til at bevare en balance mellem knogledannelse (formation) og nedbrydning (resorption). Det skønnes at % af alle kvinder og % af alle mænd over 50 år vil pådrage sig et osteoporotisk brud i deres resterende levetid [Abrahamsen et al. 2005]. Den største opbygning af knoglevæv sker i barndommen og ungdommen, hvilket bevirker, at knoglerne opnår den største styrke 10 år efter et individ er fuldt udvokset, hvorefter dette niveau holdes mere eller mindre stabilt, indtil knoglestyrken gradvist mindskes i 40 års alderen [Garg 2004, s. 3-21]. Tab af knoglemasse kan dog forbygges. Blandt andet har indtagelse af D-vitamin og kalk samt fysisk aktivitet en positiv indvirkning på knoglestyrken. Rygning, stort forbrug af alkohol, samt lav vægt har derimod en negativ indvirkning herpå [Andreasen et al. 2005]. Der skal skelnes mellem knoglemodellering og -remodellering. Knoglemodellering refererer til formering af knoglevæv, hvilket stoppes eller mindskes når individer er fuldt udviklet. Knogleremodellering ændrer ikke form og størrelse på knogler, men kan fjerne gammelt knoglevæv og erstatte dette med nyt [Garg 2004, s. 3-21]. Normalt er det den nøje kontrollerede balance mellem resorption og formation af knoglevævet, som opretholder et stærkt skelet [Jørgensen & Kassem 2008]. Osteoporose opstår, når der resorberes mere knoglevæv end der formeres, men der findes behandlingsmidler som standser knogleresorptionen. Dette er dog ikke en optimal behandlingsform, idet det ligeledes bevirker at opbygningen af knoglerne efterhånden også standes, da knogleresorptionen og -formationen er en 1
18 koblet proces. Når begge stopper, vil personer med osteoporose derfor ende med at have gamle knogler hvormed menes at knoglemassen ikke vil fornys, som det normalt sker, og derfor ikke tilpasser sig kroppens behov. En optimal behandlingsform ville kunne opbygge knoglevævet og ikke blot standse resorptionen, således at balancen mellem resorptionen og formationen gendannes. Dette viser sig, netop at være tilfældet med parathyorideahormon (PTH), som har en anabolsk virkning på knoglerne, når det gives som impulsbehandling [Koval & Seaton 2005; Simonelli 2002], Dette er bemærkelsesværdigt, da PTH almindeligvis indvirker på resorptionen af knoglevæv, og ved forhøjede værdier i kroppen kan det endda være skyld i udviklingen af osteoporose. De første forsøg, der viste en anabolsk effekt på knogleformering ved PTH-behandling af rotter, blev foretaget i tidsrummet mellem 1929 og 1937 [Reeve 2002], og senere er PTH blevet godkendt til behandling af osteoporose. Mekanismerne bag PTH s anabolske effekt på knoglerne er der dog endnu ikke opnået en endegyldig forklaring herpå. Forskellige hypoteser er fremkommet og udvalgte vil i dette projekt blive beskrevet og sammenholdt for at belyse PTH s anabolske virkning ved impulsbehandling. 2
19 Problemformulering PTH kan virke både anabolsk og katabolsk på knoglerne ved forskellig dosering. I denne sammenhæng er det interessant at kigge på eventuelle virkningsmekanismer, som kan give ophav til hormonets knogleformerende evne ved impulsbehandling. Vi vil derfor i dette projekt forsøge at afdække følgende problemformulering: Hvilke mekanismer ligger til grund for, at parathyroideahormon virker anabolsk på knoglerne ved impulsbehandling, når det under normale knoglemetaboliske omstændigheder virker katabolsk? Følgende hypoteser undersøges: 1) Proteinkinase A-signalvejen er essentiel for PTH s anabolske virkning. 2) PTH opregulerer c-fos-udtrykket i knogleceller. 3) IGF-I er essentiel for PTH s anabolske virkning ved blandt andet at stimulere antiapoptose og proliferation. 4) Bone lining celler omdannes til osteoblaster. 5) Mesenkymale stamceller klæber sig fast på knogleoverflader og danner kolonier under påvirkning af PTH. 6) PTH har en antiapoptotisk effekt på osteoblaster. 7) Når impulsgivet PTH griber ind i remodelleringen, overkompenserer osteoblaster. Problemfelt Knogleremodellering er et komplekst system, hvorigennem knoglernes styrke fornyes og calciumniveauet i blodet forsøges holdt stabilt indenfor et snævert normalområde. PTH spiller en afgørende rolle i denne regulering og frigives normalt når calciumniveauet i blodet falder. For at opretholde et normalt calciumniveau bliver Ca 2+ fra knoglerne nedbrudt af specifikke knogleceller. Knoglevævet skal dannes i samme tempo, som det resorberes for at undgå svage knogler og dermed brud. Ved hyperparathyroidisme, hvor PTH af forskellige grunde udskilles i en for stor mængde, er resultatet netto resorption af knoglevævet og dermed frigivelse af en større mængde calcium til blodet begge dele er uhensigtsmæssigt, da forhøjede mængder af calcium i blodet kan resulterer i svimmelhed, depression og påvirkning af hjertet [Dsgnet Helse og Bio reference 2008]. Nyere forskning har vist, at PTH givet som impulsbehandling til patienter med 3
20 osteoporose har en anabolsk virkning på knoglerne, hvilket umiddelbart er i modstrid med hormonets naturlige virkning i kroppen. Det er nærværende projekts ønske at belyse hvilke mekanismer, der gør PTH i stand til at virke både katabolsk og anabolsk på knoglerne. 4
21 Metode Nærværende projekt er udformet på baggrund af et litteraturstudie, som indbefatter en indsamling af grundviden om knoglebiologi, calciummetabolismen, osteoporose, knogleremodellering og PTH. Til dele af ovenstående emner blev der benyttet videnskabelige artikler, som blandt andet blev fundet under søgeord såsom Bone Biology, Osteoporosis og Parathyroid hormone i diverse naturvidenskabelige databaser, hvoraf kan nævnes Medline og andre websites, så som ASBMR og Springerlink. Artikler er endvidere fundet med hjælp fra projektets vejleder, Niklas Rye Jørgensen, og ud fra artikelsamlingen, Principles of Bone Biology. Herudover omfatter den litterære del anvendelse af biokemiske og molekylærbiologiske lærebøger. For besvarelse af problemformuleringen er hypoteser omkring PTH s anabolske virkning fundet på føromtalte naturvidenskabelige databaser og -websites under søgeorderne PTH, anabolic. Hypoteserne er udvalgt på baggrund af, hvorvidt flere artikler og forsøg underbyggede hver enkelt hypotese, da dette viser udbredelsen og af pågældende hypotese.. Flere uafhængige forsøg, som underbygger hinanden, repræsenterer en mere troværdig hypotese. De udvalgte hypoteser, og de forsøg disse baseres på, vil blive diskuteret i forhold til hinanden. Modsigelser mellem de forskellige hypoteser vil blive fremhævet, og til slut vil eventuelle overordnede sammenhænge tydeliggøres. Det er forsøgt at forholde sig kritisk i forbindelse med indsamling af materiale, således at der hovedsageligt er benyttet nyere artikler skrevet efter år 2000, medmindre der er tale om baggrundsviden, som er alment accepteret, eller hvis der er gjort brug af originale artikler. Med originale artikler menes artikler hvori eventuelle hypoteser er blevet efterprøvet eksperimentelt for første gang. I forbindelse med overensstemmelse af kildeudsagn blev det efterstræbt, at flere artikler skulle læses for herved at få et bredt overblik over oplysninger og teorier i forhold til projektets problemstilling. 5
22 6
23 1. Osteoporose I dette afsnit vil sygdommen osteoporose blive defineret, og herunder beskrives der, hvad der ved sygdommen fører til frakturer. Der vil yderligere kommes ind på, hvordan osteoporose diagnosticeres, samt gives en kort beskrivelse af hvilke behandlingsmuligheder, der på nuværende tidspunkt er tilgengælige. Osteoporose er latinsk og betyder "porøs knoglemasse". Sygdommen berører hele skelettet og er karakteriseret som en tilstand med reduceret knoglemasse og hermed reduceret knoglestyrke. Dette kan resultere i, at knoglers brudstyrke nedsættes i en sådan grad, at der kan opstå brud ved beskedne belastninger. Knoglebrud forårsaget af osteoporose, kaldet osteoporotiske brud, forekommer hyppigst i håndled, ryghvirvler og lårbenshalse, men generelt vil personer med osteoporose også lettere få knoglebrud andre steder i kroppen end personer, der ikke lider af osteoporose [Fødevaredirektoratet/sundhedsstyrelsen 2000]. På figur 1 ses forskellen mellem raskt og osteoporotisk knoglevæv. Figur 1: På figuren til venstre ses et billede af rask knoglevæv som er tættere forbundet, hvormed knoglestyrken er stor. Til høje ses det osteoporotiske knoglevæv, hvor det tydeligt fremgår at knoglevævet er porøst og derved svagere [Fødevaredirektoratet/sundhedsstyrelsen s ]. Der kan ikke peges på én veldefineret årsag til, at osteoporose udvikles. Knogleremodelering består af to sammenkoblede processer; knogleformation og knogleresorption, som kontinuerligt finder sted over hele skelettet. En uligevægt mellem disse, hvor knogleresorption er større end knogleformationen forårsager osteoporose. Da flere forskellige faktorer regulerer og påvirker knogleomsætningen, er osteoporose en multi-faktoriel sygdom [Rodan et al. 2002; Raisz 2005]. Knoglemængden øges op gennem barndommen og når, som sagt, sit maksimale niveau (PBM) 10 år efter et individ er fuldt udvokset. PBM varierer i almindelighed meget og er større hos mænd end hos kvinder, hvorfor tilfælde af osteoporotiske brud oftest ses hos kvinder. Knoglemængden 7
24 begynder som før nævnt at formindskes i 40-års alderen [Garg 2004] og hos kvinderne ses accelereret tab i de første 5-10 år efter overgangsalderen, efterfulgt af et langsommere og mere stabilt tab. Denne senere knoglesvindende fase ses også hos mænd efter 40 erne. Knoglemængden i en givet alder og risikoen for osteopotiske brud, er afhængig af den individuelles PBM og raten for knogletab gennem livet. Studier har vist at PBM primært er genetisk bestemt, mens calciumindtagelse, produktionen af kønshormoner, fysisk aktivitet især i barndommen og puberteten også har en indflydelse [Osteoporoseforeningen 2008]. Der er altså en række livsfaktorer som har indflydelse på udviklingen af osteoporose. Osteoporose forekommer dels som en selvstændig sygdom, hvilket betegnes primær osteoporose, og dels som følge af andre sygdomme og betegnes hermed sekundær osteoporose. Ved primær osteoporose skelnes der yderligere mellem post-menopausal osteoporose, og aldersbetinget osteoporose såkaldt senil osteoporose, som ses hos både ældre mænd og kvinder. Årsagerne til primær osteoporose er multi-faktorielle, hvor en række førnævnte livsfaktorer har betydning. Aldersbetinget- og post-menopausal osteoporose skyldes blandt andet nedsat fysisk aktivitet og aldersbetingede ændringer i kroppen såsom nedsat calciumabsorptionen fra tarmen, hvilket betyder at man ikke optager tilstrækkeligt calcium og hermed får et øget PTH-niveau i kroppen der resulterer i en øget knogleresorption [Osteoporoseforeningen 2008; Rodan et al. 2002]. 1.1 Diagnosticering Da osteoporose kan forebygges, er det ønskeligt at få stillet diagnosen så tidligt som muligt i sygdomsforløbet, men almindeligvis opdages osteoporose først ved osteoporotisk brud. Dette skyldes at overgangen mellem udviklingen af osteoporose og normal aldersbetinget knoglevævstab er glidende, og da osteoporose ikke medfører kliniske symptomer, er det usandsynligt at diagnosticeringen finder sted før knoglebrud opstår [Fødevaredirektoratet/sundhedsstyrelsen 2000]. Blandt metoder til måling af knoglemassen er den mest anvendte og mest nøjagtige DXA (dual energy X-ray absorption). Denne giver en værdi af kalkindholdet i knoglerne, altså knoglemineraltætheden (BMD). Ved brug af denne metode koncentreres målingerne som regel til de steder, hvor der erfaringsmæssigt hyppigst optræder brud, men der kan tages BMD måling af hele skelettet. Inden der opstår brud, vil det på denne måde være muligt at observere, at knoglemassen i pågældende område er lavere end normalt [Adams & Lukert 1999]. I tillæg til 8
25 DXA scanning kan man udføre røntgenundersøgelse af rygsøjlen for at detektere evt. tilstedeværelse af sammenfald af ryghvirvler. Røntgenundersøgelser er ikke velegnede til påvisning af knogletætheden, da det menes, at der skal tabes 50 % af knoglevævet, før dette kan registreres [Compston & Sørensen 2001]. Det er endnu ikke muligt at helbrede osteoporose, da det ikke er muligt at hæmme resorptionen uden også at hæmme formationen, hvilket giver behandlingsmæssige konsekvenser. Til patienter med osteoporose gives en medikamentel behandling, der styrker og bevarer den tilbageværende knoglestruktur og -masse. Af behandlingsmuligheder for osteoporose findes to overordnede; en anabolsk som opbygger knoglevævet og en antiresorptiv som kan standse knogleresorptionen. Disse to behandlingsmuligheder kan kombineres på forskellig vis [Osteoporoseforeningen 2008]. 1.2 Behandlingsmuligheder Dette afsnit ønsker at give et indblik i, hvilke behandlingsmuligheder der er tilgængelige for osteoporosepatienter, hvorunder PTH-behandling afslutningsvis kort beskrives. De mest almindelige behandlingsformer for osteoporose i Danmark er bisfosfonater, Selective Estrogen Receptor Modulators (SERM), strontiumranelater og PTH-analoger. Bifosfonater optages af knoglevævet og hæmmer resorptionen, og betegnes derfor som en antiresorptiv behandling [Frederiksberghospital 2008b]. SERM binder sig til østrogens receptorer og virker som østrogen i visse henseender, f.eks. indenfor knogleomsætning [Cosman 2006]. Strontium stimulerer knogleformationen samtidig med, at knogleresorptionen hæmmes, hvorfor dette præparat både virker anabolsk og antiresorptivt i kroppen. Behandling med PTH(1-34) viser sig ved impulsbehandling at have en anabolsk og antiresorptiv effekt på knogler [Cosman 2006]. I dag gøres der brug af denne behandling over en maksimal tidsperiode på 18 måneder i Danmark og 24 måneder i USA. Denne afgrænsede tidsperiode opstår blandt andet i kraft af, at PTHbehandling kan føre til tumorer i forsøgsdyr, hvis der behandles i længere periode end foreskrevet. Endvidere er der en risiko for knoglefortætning, som kan resultere i fortrængning af knoglemarven. Lægemidlets navn er FORSTEO, som også betegnes teriparatid og svarer til PTHanalogen PTH(1-34). FORSTEO doseres i 20 mikrogram en gang dagligt [lægemiddelstyrelsen- Forsteoproduktresume 2008]. Fremstilling af PTH er omkostningsfuld, og det er hovedsageligt patienter med svær osteoporose, hvor patienten f.eks. har vertebral sammenfald, der bliver behandlet med PTH [Vestergård et al. 2004; Hodsman et al.2002]. Se afsnit 3 Calciumhomøostase og 3.1 Parathyroideahormon. 9
26 Desuden anbefales D-vitamin- og calciumtilskud til osteoporosepatienter, hvis tilførslen gennem kosten er utilstrækkelig [Fødevaredirektoratet/sundhedsstyrelsen 2000]. 10
27 2. Knoglebiologi Skelettet er et dynamisk organ hvor knogleresorption og -formation foregår konstant ved hjælp af henholdsvis osteoklaster og osteoblaster. Processerne er tæt koblede og reguleres så de under normale forhold opretholder knoglemassen, for herved at undgå frakturer samtidig med, at calciumniveauet i kroppen holdes konstant. Dette kræver forskellige knogleceller og et netværk af signalveje, som hver især er vigtige for et balanceret forhold mellem knogleformation og - resorption [Garg 2004, s. 3-21]. Nedenstående afsnit beskriver derfor knoglestrukturen og de forskellige knogleceller samt dannelsen af de knogleresorptive osteoklaster. 2.1 Knogleopbygning Makroskopisk knoglestruktur Skelettet er opbygget af to forskellige slags knoglevæv med forskellig porøsitet; kortikal (kompakt) knoglevæv og trabekulært (svampet) knoglevæv, se figur 2. Kortikalt knoglevæv udgør omkring 85 % af den totale knoglemængde i kroppen og findes i knogleskafter på de lange rørknogler hvor de danner en skal omkring det trabekulære knoglevæv [Garg 2004, s. 3-21]. Det er denne knogletype der har størst betydning som mekanisk støttefunktion. Grundet et forholdsvist lille overfladeareal, foregår kun 20 % af den totale metaboliske aktivitet i denne knogletype [Jørgensen & Kassem 2008]. Det kortikale væv er organiseret i cylindere fordelt omkring centrale blodkar, kaldet Haversk system. Haverske kanaler, som indeholder kapillærer og nerver, er forbundet med hinanden og forbundet til ydersidens knogleoverflade ved hjælp af korte, tværgående Volkmannske kanaler, se figur 4. Gennem disse kanaler løber et vaskulært netværk, der er i kontakt med levedygtige celler og nerver. Det trabekulære knoglevæv som udgør omkring 15 % af den totale knoglemængde i kroppen er fundet i vertebrae, flade knogler og i enden på de lange knogler [Garg 2004, s. 3-21]. Selv om det trabekulære knoglevæv kun bidrager med en lille procentdel af den totale knoglemasse står de, pga. det større overfladeareal, for 80 % af den metaboliske aktivitet, hvilket gør dem mere følsomme overfor knoglevævstab [Jørgensen & Kassem 2008]. Det ikke-mineraliserede område indeni knoglen indeholder marven, som blandt andet består af blodvesikler, nerver og forskellige celletyper. Knoglemarvens hovedfunktion er at producere knogleceller, og de celler der er til stede i blodet. 11
28 Figur 2: Knogle opbygget af kortikal knoglevæv, det ydre lag, og trabekulær knoglevæv, det svampet væv inden i knoglen [Knogleforlængelse 2008] Mikroskopisk knoglestruktur Med undtagelse af ledoverfladerne er knoglers overflader dækket med knoglehinde, hvilket er en kar- og nerverig hinde af fast bindevæv. Denne hinde danner en grænse mellem hårdt og blødt knoglevæv, og det er her metabolisk, cellulær og biomekanisk aktivitet finder sted, som modulerer knoglevækst og form. Det ydre lag består hovedsaligt af kollagenfibre og fibroblaster, kaldet periost, se figur 4, hvilket tilsammen giver knoglerne deres styrke. Det indre lag indeholder funktionelle osteoblaster arrangeret i lag, og betegnes endost. Osteoklaster befinder sig både på den endosteale og periosteale side af knoglen, idet der kan foregå knogleresorption begge steder [Garg 2004, s. 3-21; Jørgensen & Kassem 2008]. Osteocytter er indlejret i lakuner, som er snævre hulrum dybt i knoglen, hvor de har udløbere rige på mikrofilamenter, der har kontraktile egenskaber, og er forbundet via gap-junctions til andre osteocytter samt osteoklaster og osteoblaster på knogleoverfladen, se figur 3. Det er disse udløbere der er beliggende i kanalikuli, hvilket penetrerer knoglevævet, se figur 4 [Jørgensen og Kassem 2008]. Figur 3: Knogleresorption. Bone lining celler dækker knogleoverfladen og osteoklaster resorberer knoglevæv ved bestemte områder. Osteocytter ligger dybt i knoglevævet og kommunikerer via dendritter [Smart skeletons, redigeret af Hansen 2008]. 12
29 Figur 4: Osteon er et haversk lamelsystem som består af adskillige lag af flere millimeter lange, koncentriske, cylindriske lameller som omslutter haverske kanaler, hvori der løber blodkar til ernæring af osteonet. Volkmann kanaler forbinder Haverske kanaler med hinanden og med ydersiden af knoglen. Det trabekulære knoglevæv findes inden i knogleskaftet, kanalikuli er fine kanaler der penetrerer knoglevævet. Lamellær knoglevæv er mest talrige i vægtbærende knogler og anses som værende en stærk knogle. Periost er den ydre knoglehinde [Answers, redigeret af Hansen 2008]. 2.2 Knogleceller Osteoblaster og osteoklaster er ansvarlige for knogleremodelleringen, som sker overalt i skelettet i centrale pakker, der er adskilt i lokalisering og kronologi. Det tyder herved på, at aktiveringen af cellulære sekvenser, ansvarlig for knogleremodelleringen, er kontrolleret lokalt og muligvis af en autoregulerende mekanisme, så som autokrine eller parakrine faktorer genereret i knoglemikromiljøet [Garg 2004, s. 3-21] Osteoblaster Osteoblaster stammer ligesom osteocytter og bone lining celler fra mesenkymale multipotente stamceller, som residerer i knoglemarven [Siegel 2006]. Mesenkymale stamceller (MSC) er selvfornyende og højproliferative, og de kan ved hjælp af særlige stimuli differentieres til celler af osteoblastlinien, fedtceller, muskelceller eller bindevævsceller. Osteoblastlinien omfatter osteoblasternes differentieringsrække, dvs. de stadier der findes mellem MSC og modne osteoblaster. Når osteoblaster er fuldt modne, har de en kubisk form og ligger lagvis[siegel 2006; Jørgensen & Kassem 2008], og det menes at osteoblaster har en levetid på ca. 150 dage [Diernæs & Nørholt 2006]. Osteoblaster producerer den lamellære knoglestruktur, se figur 4, som er mest talrig i store vægtbærende knogler og disse anses for at være stærke knogler. Den lamellære knoglestruktur produceres ved først at udskille knoglematrix, hvorefter denne mineraliseres ved 13
30 hjælp af alkalisk fosfatase [Siegel 2006; Jørgensen & Kassem 2008]. Den knogledannende proces tager omkring tre måneder. Når osteoblaster danner knoglevæv, udskiller de samtidig knogle morfogenetiske proteiner (BMP) til det minerale matrix. Dette syreruopløselige protein ligger i matrixen, indtil det bliver frigjort under osteoklastresorption. Denne syreruopløselighed bevirker at den lave ph, skabt af osteoklaster, har mulighed for at opløse knoglemineraler uden at påvirke BMP. Når BMP først er udskilt, bindes det til receptorer på udifferentierede MSC, hvilket fører til aktivering af signalveje, som fører til osteoblastdifferentiering og stimulering af ny knogleproduktion. En dysfunktion i denne proces kan blandt andet forårsage osteoporose [Garg 2004, s. 3-21]. Ud over dannelse af organisk knoglematrix er osteoblaster også ansvarlige for produktion af andre proteiner involveret i knogleformation, såsom ikke-kollagen proteiner og vækstfaktorer f.eks. osteocalcin, osteopontin, samt receptoraktivator af nuklear faktor-kb ligand (RANKL) og osteoprotegerin (OPG). RANKL og OPG har indflydelse på dannelse og regulering af osteoklaster [Huang et al. 2004], hvorfor disse vil gennemgås i afsnit Osteoklastogenese. En lang række faktorer virker via osteoblaster, der derfor spiller en vigtig rolle som hovedregulator af knogleremodelleringen. Osteoblaster hjælper gennem celle-til-celle kommunikation hæmatopoietiske stamceller til at differentiere sig til osteoklastforstadier og fusionere med andre osteoklastforstadier til multinukleære aktive osteoklaster. Denne celle-tilcelle kommunikation sker gennem membranproteinet RANKL, udskilt på overfladen af osteoblaster. RANKL sætter sig i Receptor Activator of Nuclear factor-kb (RANK), som er en receptor på osteoklastforstadiets overflade, og derefter starter en række signalveje, der aktiverer osteoklastforstadiet. Osteoblaster udskiller RANKL ved at blive stimuleret af en lang række faktorer deriblandt PTH, 1,25-dihydroxyvitamin D3 (Vitamin D3), cytokiner og prostaglandin E2 (PGE2). Dette uddybes i afsnit Osteoklastogenese [Jørgensen & Kassem 2008; Takami et al. 2000] Osteoklaster Osteoklaster nedstammer fra hæmatopoietiske stamceller, og har dermed forstadier til fælles med makrofag- og monocytfamilien, og er ansvarlig for knogleresorptionen. Deres aktivitet styres overordnet af PTH. Osteoklaster er store sammensmeltede monocytter, der kan indeholde op til 50 kerner, som er koncentrerede midt i cellen [Siegel 2006; Garg 2004, s. 3-21]. Osteoklaster er lokaliseret i snævre hulrum langs den mineraliserede knogleoverflade og er yderst mobile. Et specifikt område af osteoklasters membran dannes tæt ved knogleoverfladen så de kan 14
31 resorbere denne. Dette område, kendt som the ruffled border, er formet af tråd-lignende udhæng som osteoklaster sender ud mod knogleoverfladen, hvilket består af folder og invaginationer der tillader nærkontakt mellem cellemembranen og knogleoverfladen [Jørgensen & Kassem 2008]. Knogleresorption sker ved the ruffled border da det tråd-lignende udhæng udskiller proteolytiske enzymer, som opløser det organiske knoglematrix ved hjælp af fagocytose [Garg 2004, s. 3-21; Jørgensen & Kassem 2008]. Resorptionen tager ca. tre uger, og knogleformationen tager som før nævnt ca. tre måneder. Dette betyder, at der normalt er ca. fire gange så mange knogle sites hvor der foregår formation, som sites hvor der foregår resorption. Osteoklaster eksisterer typisk i små, men koncentrerede grupper, der nedbryder knoglemasse i omkring tre uger. Knogleresorption starter ved hjælp af signaler fra osteoblaster og lining celler som aktiverer osteoklasterne. Ved signal fra osteoblaster og efter lokal knogleresorption er færdigt, forsvinder osteoklasterne, muligvis ved nedbrydning eller migration til andre steder hvor knogleresorption skal foregå, hvorefter det dannede hulrum/kløft igen invaderes af osteoblaster og remodelleringscyklus kan starte forfra ved en anden knogle site, se figur 5 [Garg 2004, s. 3-21]. Figur 5: Her ses remodelleringscyklus. Først er knogleoverfladen dækket af bone lining celler, hvorefter disse trækker sig til side, så der gøres plads til, at osteoklasterne kan begynde at resorberer knoglevævet. Når denne resorption er færdig dækkes den nedbrudte overflade med osteoblaster som går i gang med knogleformation. Til sidst dækkes overfladen igen med lining celler og cyklussen gentages[the Science Creative Quarterly, redigeret af Hansen 2008] Osteoklastogenese Knogleresorption afhænger af om hæmatopoietiske stamceller bliver aktiveret til fuldt modne osteoklaster, hvorfor det er relevant at se nærmere på dannelse af osteoklaster. I sammenhæng med osteoporose giver det et billede af hvor mange signalveje der skal aktiveres for at 15
32 resorptionen foregår optimalt, og hvor det derfor også kan afvige fra normalen, så osteoklaster enten bliver inaktiveret eller overaktiveret. Hæmatopoietiske stamceller kan dog ikke udføre differentieringen på egen hånd, og et samarbejde mellem disse og blandt andet osteoblaster og knoglematrix er altafgørende for aktive og funktionelle osteoklaster. Dette afsnit vil derfor først beskæftige sig med de, for projektet essentielle signalstoffer og signalveje, der fører til osteoblasters aktivering af hæmatopoietiske stamceller, og derefter disses differentiering til knogleresorptive osteoklaster. Der er også andre signalstoffer og veje i osteoklastogenese end de nævnte, men da disse enten ikke har direkte relevans for projektet, eller ikke er tilstrækkeligt undersøgt, vil pågældende ikke blive gennemgået. Osteoblaster og deres rolle i osteoklastogenese Osteoblaster er en altafgørende faktor i osteoklastogenese. Osteoblaster stimulerer som sagt hæmatopoietiske stamceller, hvilket gøres igennem vækstfaktoren glycoproteinet makrofag koloni-stimulerende faktor (M-CSF) [Jimi et al. 1995]. M-CSF dannes i osteoblaster og efter osteoblasters udskillelse bindes denne til sin receptor, c-fms, på hæmatopoietiske stamceller. Cytokinerne Interleukin-1 (IL-1) og Tumor necrosis factor-α (TNF-α) udskilles af osteoklastforstadier og modne osteoklaster ved påvirkning af overlevelsessignaler gennem integrinmedieret signalering, og det er disse der aktiverer osteoblaster til at syntetisere M-CSF [Seelentag et al. 1987] og osteoklastforstadier til at udtrykke c-fms på celleoverfladen. Binding af M-CSF til c-fms forårsager at RANK bliver udtryk på osteoklastforstadiernes overflade, hvorefter disse påbegynder differentieringen [Arai et al. 1999]. RANK er yderst vigtig i osteoklastdifferentiering, da denne gør det muligt at have en tæt celle-til-celle kommunikation mellem osteoblaster og osteoklastforstadier [Jimi et al. 1996]. RANKL bliver udtrykt på osteoblasters celleoverflade og er medlem af tumor necrosis factor ligand familien (TNF), der aktiverer osteoklastforstadiedifferentiering ved at sætte sig i RANK. Dette forårsager en forandring i osteoklastforstadiet, der derefter påbegynder sin differentiering, se figur 6 og figur 8 [Yasuda et al. 1998b]. Der findes med sikkerhed tre uafhængige signalveje, der kan få osteoblaster til at udtrykke RANKL, og ved nyere forskning menes der også at kunne forefindes en fjerde. De signalstoffer der aktiverer disse signalveje kan deles op i tre grupper: i) 1,25-dihydroxyvitamin D3 ii) PGE 2 og PTH iii) cytokiner. PGE 2 og PTH sættes i samme undergruppe, da de stimulerer de samme signalveje i osteoblaster. Dog menes det at PTH også kan stimulere den fjerde signalvej iv), hvor 16
33 calciumniveauet i osteoklastforstadier øges [Takami et al. 2000]. I det følgende vil de fire signalveje, som ses illustreret på figur 6, blive gennemgået. i) Vitamin D findes i specifikke fødevaregrupper, og kan derfor indtages ved den rigtige diæt. Desuden syntetiseres vitamin D også i huden fra 7-dehydrocholesterol. I leveren hydrolyseres vitamin D, og udkommet af dette, 25-(OH) vitamin D, transporteres videre til nyrerne. Her hydrolyseres det igen, og omdannes til det hormonelt aktive 1,25-dihydroxyvitamin D3. 1,25-dihydroxyvitamin D3 syntesen bliver reguleret af calciumniveauet i blodet [Haussler & Rasmussen 1972] og PTH spiller derfor en rolle i denne syntese. Et forhøjet niveau af calcium og hermed hæmmet udskillelse af PTH, vil nedregulere 1,25-dihydroxyvitamin D3 syntesen. 1,25-dihydroxyvitamin D3 stimulerer osteoblaster ved at det bindes til vitamin D receptor (VDR) på osteoblastcelleoverfladen [Takeda et al. 1999]. Bindingen aktiverer åbning af calciumkanaler i osteoblastmembranen, og calcium diffunderer ind i cellen [Lieberherr 1987; Caffrey & Farach-Carson 1989]. Calciumniveauet i cellen øges, og dette stimulerer en opregulering af transskriptionen af RANKL, som derefter udtrykkes på osteoblasternes overflade [Takami et al. 2000]. ii) gp130 er en almindelig signal transducer i osteoblaster og bliver aktiveret ved cytokiners binding i deres respektive receptorer. Der findes mange bud på hvilke cytokiner, der virker stimulerende på gp130, men nogle af de påviste er Interleukin-11 (IL-11), Interleukin 6 (IL-6), Oncostatin M (OSM) og Leukemia inhibitory factor (LIF). Disse cytokiner binder til deres egen receptor og aktiverer gp130, der ligesom vitamin D3 opregulerer transskriptionen af RANKL [Tamura et al. 1993]. iii) PGE 2 og PTH stimulerer samme signalvej, men har hver deres receptor for aktiveringen. PGE 2 er en fedtsyre, hvis dannelse bliver stimuleret af IL-1β og TNF-α [Yucel-Lindberg et al. 1999]. PGE 2 kan binde sig til flere receptorer, men hovedsageligt foretrækkes EP4, hvor binding til EP2 kan forekomme. EP2 og EP4 er g-protein koblede receptorer, der ved hjælp af adenyl cyklase omdanner ATP til camp [Suzawa et al. 2000]. Når niveauet af camp stiger i cellen aktiveres flere signalmolekyler, og disse fremmer i sidste ende transkriptionen af RANKL. PTH 17
34 bindes til PTH-receptor 1 (PTHr1) [Liu et al. 1998] og har samme virkning som PGE 2, der aktiverer RANKL-transkription ved hjælp af et øget niveau af camp [Chase & Aurbach 1970; Ma et al. 2001]. iv) Det er desuden blevet foreslået at PTH stimulerer en fjerde signalvej, hvor PTH igennem sin receptor stimulerer protein kinase C (PKC), der ved aktivering forøger calciumniveauet i osteoblaster. Dette stimulerer igen transkriptionen af RANKL [Takami et al. 2000]. Udover de positivt stimulerende faktorer, der hjælper osteoklastforstadierne til at differentiere sig, udskiller osteoblaster også en faktor, der hæmmer celle-til-celle kommunikationen mellem osteoblaster og osteoklastforstadiet. Dette er cytokinet OPG der fungerer som en lokkeduereceptor for RANKL. OPG sidder ikke i en membran, men bliver udskilt af osteoblaster, se figur 6. Formålet med OPG er at flyde rundt i nærheden af cellerne og binde sig til RANKL, og dermed forhindre binding af denne til RANK. Herved forhindrer OPG osteoklastformation [Yasuda et al. 1998a]. Det kan populært siges at OPG ligner og udgiver sig for at være RANK og "snyder" derfor RANKL til at binde sig. OPG bliver nedreguleret af nogle af de samme faktorer, der stimulerer aktiveringen af RANKL. Dette er blandt andet PGE 2 og PTH [Lee & Lorenzo 1999; Brändström et al. 1998]. Forholdet mellem udtrykket af RANKL og OPG afgør hvor mange osteoklastforstadier, der bliver omdannet til aktive osteoklaster, og derfor er OPG en måde at regulere knogleomsætningen på. Nedenstående figur 6 giver et overblik over relevante signalvejene via osteoblaster. 18
35 Figur 6: De fire signalveje igennem osteoblaster, der aktiverer RANKL til at udtrykkes på osteoblasters celleoverflade. Dette giver mulighed for celle-til-celle kommunikation mellem osteoblaster og osteoklastforstadier ved RANKL binding til RANK [Jørgensen 2008]. 19
36 Signalvejene i osteoklastforstadier fra RANK til differentiering RANKL-RANK kommunikationen er essentiel for osteoklastdifferentiering, da aktivering af RANK som sagt igangsætter en signalvej i osteoklastforstadier, der netop resulterer i differentiering. På figur 7 ses signalvejene i osteoklastforstadier. Det gen, der i sidste ende er centralt for at osteoklasterforstadierne differentierer sig til multinukleære osteoklaster, kaldes Nuclear factor of activated T-cells 1 (NFATc1). Dette gens produkt menes at være en hovedregulator for RANK-aktiveret differentiering, hvor det som transkriptionsfaktor aktiverer den endelige differentiering til modne osteoklaster [Takayanagi et al. 2002]. Hvilke og hvor mange gener, der står for denne endelige differentiering, er endnu uvist. Det menes dog, at genet β 3 integrin, hvis genprodukt er indblandet i forbindelsen mellem osteoklaster og knogler [Crotti et al. 2006], og genet cathepsin K, hvis genprodukt er et lysosomalt enzym, der er indblandet i knogleresorption, er to af de gener, der aktiveres af NFATc1 [Matsumoto et al. 2004; Kafienah et al. 1998]. NFATc1 aktiveres af en signalvej, der starter ved RANK-RANKL interaktionen. RANK mangler dog indre enzymatisk aktivitet og må derfor bruge adaptorprotein til at bringe signalet videre. Den cytoplasmiske hale på RANK indeholder tre bindingssteder til et sådan adaptorprotein, Tumor necrosis factor Receptor-Associated Factor 6 (TRAF6), og bindes TRAF6 til RANK igangsættes en trimerisering, hvor et tredje signalmolekyle, Nuclear factor-kb (NFkB), aktiveres [Galibert et al. 1998]. NFkB er en familie af transkriptionsfaktorer, der binder sig til genet NFATc1, og efter aktiveringen af NFkB igangsættes transkriptionen af NFATc1. Dette hjælper til at igangsætte transkriptionen [Gohda et al. 2005]. Der findes andre måder hvorpå transkriptionen af NFATc1-genet kan igangsættes. RANK kan også aktivere et transkriptionsfaktor kompleks; Activator Protein-1 (AP-1). Dette kompleks består af proteindimerer fra protooncogenet, c-fos, Activating Transcription Factor (ATF) og Jun, og som før aktiverer det NFATc1 ved at igangsætte transkriptionen [Asagiri & Takayanagi 2006; (Eferl & Wagner 2003)]. Desuden kan fosfolipase C γ (PLCγ) øge niveauet af calcium i osteoklastforstadierne, og dette kan også igangsætte transkriptionen af NFATcl [Koga et al. 2004]. Når NFATc1 virker som hovedregulator for osteoklasternes endelige differentiering foregår dette ofte i samarbejde med AP-1. Når NFATc1 og AP-1 bindes til hinanden kan disse igangsætte transkriptionen af målgener som indgår i osteoklastdifferentieringen [Chen et al. 1998]. Figur 7 viser signalvejene, der aktiverer NFATc1. 20
37 Figur 7: Signalvejene fra RANK og PLCγ til aktivering af NFATc1. Denne aktivering får osteoklastforstadierne til at foretage den endelige differentiering til modne osteoklaster [Jørgensen 2008]. Udover signalvejene beskrevet ovenfor og i figur 7, bruger IL-1 også TRAF6 som en signaltransducer, der aktiverer NFkB [Cao et al. 1996], og selvom det endnu ikke vides hvad denne signaloverførsel i osteoklaster bruges til, menes det at IL-1 også er indblandet i osteoklastforstadiernes fusion til multinukleære celler, og deres evne til at danne hulrum når de resorberer [Jimi et al. 1999]. For et overblik over hvilke nøglemolekyler der har indflydelse på osteoklastdifferentiering, se figur 8. 21
38 Figur 8: Ud fra denne figur fåes et overblik over hvilke molekyler der er medvirkende i osteoklastdifferentieringen, og på hvilke stadier i udviklingen de indvirker. Det skal endnu engang påpeges at det kun er de for projektet relevante faktorer der er medtaget [Jørgensen 2008]. 22
39 3. Calciumhomøostasen Skelettet spiller, foruden en strukturel rolle, en stor rolle som calciumreservebeholdning, hvorfra plasmacalciumkoncentrationen opretholdes, og calciumindtaget bliver optimalt udnyttet. Andre mineraler som fosfat, magnesium, kalium og bikarbonat lagres ligeledes i knoglerne [Jørgensen & Kassem 2008]. Et fuldvoksent menneskes calciumindhold ligger på omkring 1000 gram. 99 % af dette eksisterer som hydroxyapatitkrystaller i knoglerne. Den sidste 1 % af kroppens totale mængde calcium findes i det bløde væv og i den ekstracellulære væske, herunder blodet. Ca 2+ er den biologisk aktive form af calciummineralet, som er afgørende for helbredet og blandt andet spiller en vigtig rolle i forbindelse med skelettet. Den primære calciumkilde kommer fra mælkeprodukter, og i mindre mængder fra grønne grøntsager [Weaver & Heaney 2006, kap 2]. Kroppens calciumbehov, kaldet minimum dagligt behov, varierer med alder og beskrives som det laveste calciumindtag, hvor knoglebevarelsen er maksimal, altså det mindste daglige behov for at opretholde et sundt skelet. Knoglestyrke er en funktion af knoglemasse, som igen afhænger af mængden af calciumreserver [Weaver & Heaney 2006, kap 2]. Der er to forhold, der gør sig gældende i forbindelse med opretholdelsen af homøostasen. Det første er de G-protein-koblede calciumfølsomme receptorer (CaSR) der blandt andet findes i parathyroideaceller som producerer PTH, knogleceller osv. Disse receptorer kan registrere den ekstracellulære væskes indhold af calcium, hvorved det sikres at små ændringer i plasmacalcium vil udløse kompensatoriske hormonale reaktioner. Det andet forhold, der har afgørende betydning for homøostasen er, at der i nyrerne og skelettet er oprettet to tærskelsystemer. Disse systemer sørger for nøjagtig regulering af calciumdeponeringen i skelettet og calciumtab til omgivelserne. Ved højt calciumindtag vil der være en initial positiv Ca 2+ -balance. Denne er betinget af en øget deponering i knoglernes mineralfase i et hurtigt mobiliserbart depot. Samtidig hermed vil calciumudskillelse fra nyren øges, hvorved en overskydende del tabes. Endvidere vil et fald i dannelsen af aktivt D-vitamin i nyrerne reducere den intestinale absorption af kalk. Hvis et højt calciumindtag fortættes over en længere periode, vil overskydende calcium deponeres dybt i skelettet [Schwarz et al. 2005]. 23
40 3.1 Parathyorideahormon Krav til calciumindtag og calciumniveau i knogler varierer med alderen, men også fra dag til dag. Homøostasesystemet er derfor konstant nødt til at tilpasses, så der leveres tilstrækkeligt calcium fra tarmen og nyrerne til den ekstracellulære væske og blod, og videre herfra til knoglerne. Nedenstående afsnit vil beskrive hormonet, PTH s regulering af calciumkoncentrationen i blodet. PTH er et hormon, som udskilles af de fire biskjoldbruskkirtler og har til opgave at hæve calciumniveauet i blodet, hvis det ligger under normalområdet. PTH er et peptidhormon bestående af 84 aminosyrer med N-terminalen 1-34, og har i kroppen en halveringstid på fem minutter [Tfelt-Hansen & Schwatz 2003; Region Sjælland Sygehus Syd 2008]. Calciumfølsomme celler i biskjoldbruskkirtlerne registrerer ved hjælp af CaSR niveauet af calcium i blodet og danner som respons enten mere eller mindre PTH. CaSR har en meget lav affinitet for liganden, som er ekstracellulær Ca 2+, og derfor bemærkes selv meget små ændringer i calcium-koncentrationen. Ved stigende calciumniveau i blodet hæmmes udskillelsen af PTH [Tfelt-Hansen & Schwatz 2003]. Ved faldende calciumniveau aktiverer CaSR en signalvej som øger niveauet af camp. Et hormon kaldet calcitonin virker modsatrettet PTH og bliver stimuleret, når serumniveauet af calcium stiger over normalværdien. Glukokortikoider menes at stimulere PTH produktionen og aktiviteten, dette kan skyldes følgende virkninger; 1) indvirkning på gentransskriptionen, hvilket er en kendt virkning af glukokortikoider, 2) øgning af knoglecellernes følsomhed overfor PTH, 3) øget ekspressionen af PTH-receptorer på osteoblaster eller 4) ændring i receptorens affinitet for PTH [Compston & Shane 2005]. PTH har de fleste målceller i nyrer og knogler, og human PTH(hPTH) binder sig til målcellerne ved hjælp af receptoren PTHr1. PTHr1 findes på adskillige celletyper såsom osteoblaster, immunceller og svagt differentierede knoglemarvsceller [Murrills 2006]. Der er ikke helt enighed omkring hvorvidt der findes PTHr1 på osteoklaster da studiers resultater omkring dette ikke er entydige. (Dempster et al. 2005) har lavet forsøg som påviser disse receptorer på osteoklaster mens forsøg af [Lee et al. 1994] viser det modsatte. Der findes et proteinhormon kaldet PTHrelated protein (PTHrP), som blandt andet kan binde sig til samme receptor som PTH [Curtis et al. 1998]. Denne vil dog ikke blive beskrevet yderligere, da denne ikke direkte er relevant i forbindelse med projektets problemformulering. Bindingen mellem PTH og PTHr1 resulterer, som før nævnt, i aktiveringen af adenyl cyklase og fosforlipaser og giver derved en øget cellulær koncentration af camp og calcium [Ann Cranney et al. 2006]. Uanset om der findes PTHr1 på 24
41 osteoklaster, stimulerer PTH differentieringen af osteoklaster gennem osteoblaster [Yasuda et al. 1998b]. Derfor kan forhøjet udskillelse af PTH over længere tid medføre osteoporose pga. øget resorption af knoglevæv uden en efterfølgende tilstrækkelig formation. Dette kan blandt andet skyldes svulster i én eller flere biskjoldbruskirtler. Udskillelsen af PTH øger mængden af Ca 2+ i blodet på tre måder. 1) Det mobiliserer calcium fra knoglerne ved at aktivere osteoklaster, 2) øger calciumabsorptionen fra tyndtarmen og 3) nedsætter udskillelsen af calcium i urinen. I nyrerne aktiverer PTH 25-hydroxyvitamin D- αhydroxylase til øget produktion af 1,25-dihydroxyvitamin D og derved fremmes den intestinale absorption af calcium [Schwarz et al. 2005]. Under normale forhold stimulerer PTH altså knogleomsætningen, hovedsagligt ved at binde sig til receptorer på osteoblasterne. Osteoblasterne stimulerer herved proliferation, differentiering, fusion og aktivitet af omkringliggende osteoklaster, som resorberer afgrænsede mængder af knoglevæv, og derved frigør calcium til blodet [Schwarz et al. 2005]. Andre resultater fra undersøgelser viser, at mobilisering og deponering af calcium til og fra skelettet sker ved hjælp af osteocytter, der kommunikerer med hinanden, med osteoblaster og med bone lining celler på knogleoverfladen. Calciumhomøostasen er som før nævnt en nøje reguleret proces, hvori mange mekanismer er involveret. PTH spiller en afgørende rolle, men andre stoffer har også en regulerende rolle for knogleomsætningen og er der en ubalance i udskillelsen af disse, kan det resultere i f.eks. osteoporose. Følgende stoffer kan nævnes; østrogen, prostaglandin, vitamin D, cytokiner og vækstfaktorer. Nogle af disses indvirkninger står beskrevet i afsnittet 4. Osteoporosepatogenese. 25
42 4. Osteoporosepatogenese I dette afsnit gennemgås de forskellige patofysiologiske mekanismer, der resulterer i udviklingen af osteoporose. Afsnittet kan siges at ligge i forlængelse af Osteoporoseafsnittet, men for at udvikle de rette kompetencer til forståelse af pågældende afsnit, har det været nødvendigt først at gennemgå dele af knoglebiologien. Nærværende afsnit vil berøre ændringer i knogleremodelleringen, og give en forklaring på hvordan blandt andet vitamin D og cytokiner indvirker på sygdomsudviklingen. Desuden vil der redegøres for andre mulige lokale og systemiske faktorer, der også har en indvirkning på osteoporosepatogenesen. Som tidligere nævnt ligger adskillige mekanismer til grund for reguleringen af knogleremodelleringen. Disse involverer ikke alene celler fra osteoblast- og osteoklastlinien, men også andre celler i knoglemarven samt samspillet af systemiske hormoner, lokale cytokiner, vækstfaktorer og transskriptionelle faktorer [Lawrence 2005]. De fleste tilfælde, der fører til osteoporose, skyldes nedsatte østrogen eller utilstrækkelig calcium og vitamin D indtagelse. Østrogen er ikke en vigtig faktor i dette projekt, og vil derfor ikke blive beskrevet nærmere. Det ligger dog klart, at formindsket østrogenniveau forårsager en forøget aktivitet af cytokiner i knogleceller, der både skyldes en øget produktion af cytokiner og ændringer i deres receptorer eller antagonister. Dette betyder som før nævnt at udviklingen af osteoporose er påvirket af mange forskellige faktorer [Lawrence 2005; Henderson & Goltzman 2000]. 4.1 Cytokiner De cytokiner som har en indflydelse på knogleomsætningen bliver klassificeret indenfor tre grupper, i) hvor IL-1 og TNF- α har størst indflydelse på knogleresorptionen og disse stimulerer resorptionen, hvilket er vist både in vivo og in vitro, mens ii) IL-4, IL-13 og interferon-gamma (INF-γ) kan hæmme resorptionen. iii) IL-6, IL-11 og relaterede cytokiner medvirker i et receptorsystem med involvering af proteinet gp130 der sandsynligvis virker som en stimulator i tidligere stadier af osteoklastformation, se figur 6. Herigennem forøges det knogleresorptive respons for andre agonister. Alle disse faktorer kan have en indflydelse på prostaglandin produktionen [Rodan et al. 2002], se afsnittet 4.2 Prostaglandin. TNF-α og IL-1 tænkes at spille en central rolle som en patogen faktor i knogleresorptionen i rotter, der har fået fjernet æggestokkene for at efterligne menopausen. Disse vil fremover bliver betegnet som, ovariektomerede (OVX) forsøgsdyr. I denne sammenhæng har det vist sig, at resorptionen kan blive hæmmet, ikke alene ved hjælp af østrogen, men ved en kombination med 26
43 IL-1 antagonist-receptor og TNF-bindingsprotein. TNF-α s rolle er yderligere understøttet af undersøgelser, der har vist at knogleresorption efter ovariektomi foregår langsommere hos transgene dyr med forøgede niveauer af TNF-bindingsproteiner. Andre undersøgelser har vist at mangel på IL-1-receptorer også blokerer knogleresorptionen efter OVX. Omtalte cytokiner menes at stamme fra marvens hæmatopoietiske stamceller [Rodan et al. 2002; Henderson & Goltzman 2000]. 4.2 Prostaglandin Prostaglandiner er komplekse multifunktionelle regulatorer af knogleomsætningen, og de produceres både af hæmatopoietiske stamceller- og modne knogleceller i talrige mængder som er nøje reguleret [Henderson & Goltzman 2000]. De fleste systematiske hormoner såsom cytokiner og vækstfaktorer, som indvirker på knogleomsætningen har også en effekt på prostaglandinproduktionen. Prostaglandinproduktionens respons til hormoner og lokale faktorer varierer meget og har dermed mange forskellige konsekvenser. Faktorer der stimulerer knogleresorptionen stimulerer også prostaglandin produktionen, mens inhibitorer såsom glukokortikoider, IL-4 og interferon-gamma, kan hæmme prostaglandin produktionen [Rodan et al. 2002; Henderson & Goltzman 2000]. 4.3 Vitamin D 1,25-dihydroxyvitamin D3 forøger absorptionen af calcium fra mavetarmkanalen. 1,25- Dihydroxyvitamin D3 hjælper på denne måde med at regulere calciumtransporten i leveren, hvilket virker regulerende i knogleremodelleringen og fungerer som en vigtig regulator for PTH. Enhver ustabilitet i vitamin D-metabolismen kan hermed ændre calciumbalancen og forårsage ændringer i remodelleringen. Flere studier har rapporteret et fald i koncentrationen af 1,25- dihydroxyvitamin D3 med alderen, hvilket tyder på, at koncentrationen af denne er aldersbetinget. En reduceret koncentration af vitamin D-metabolitter betragtes som én af årsagerne til at reducerede koncentrationer af vitamin D har en indvirkning på aldersbetinget tab af knoglevæv [Rodan et al. 2002]. 27
44 4.4 Vækstfaktorer Både TGF- β og IGF-I bliver produceret og lagret i knoglematrixen. TGF-β er lagret i inaktiv form associeret med et bindingsprotein og bliver frigivet ved knogleresorption. TGF-β fungerer både som hæmmer af knogleresorptionen og stimulator af knogleformationen. I blandt andet osteoklastkulturer stimuleres apoptose af østrogen og tamofixifen (som er et SERM), via en TGFβ medieret mekanisme. Reducerede TGF-β-niveauer er fundet i knogleekstrakter fra ovariektomerede dyreforsøg [Henderson & Goltzman 2000]. Aldersbetinget reduktion af væksthormonsekretionen menes at være ledsaget af aldersbetinget nedsat produktion af IGF-I i skelettet. Yderligere er der blevet observeret aldersrelaterede ændringer i IGF-bindingsproteiner hos mennesker med osteoporose [Henderson & Goltzman 2000]. 28
45 5. Hypoteser omkring parathyroideahormons anabolske effekt PTH er kendt som et knogleresorptivt hormon i knogleomsætningen, men det viser sig, at PTH både har en anabolsk og katabolsk effekt på knoglerne, afhængig af om det gives som impulsbehandling eller om det findes i kontinuerligt forhøjede værdier [Simonelli 2002]. PTH s anabolske egenskaber på knogler i mennesker og dyr blev reporteret første gang i 1931 (Pehue et al. 1931; Selye 1932). 45 år senere i en undersøgelse af (Reeve et al. 1976; Reeve et al. 1980), hvor en gruppe ældre mennesker med osteoporose blev behandlet med hpth(1-34), reporteredes der om tydelig forbedring i knogleomsætningen og i den trabekulære vækst [Hodsman et al. 2002]. Et lille antal kliniske forsøg som undersøgte muligheden for brug af PTH til behandling af osteoporose, viste ligeledes at PTH(1-34) havde en fordelagtig anabolisk virkning [Hodsman et al. 2002]. Efter opdagelsen af PTH s anabolske virkning på knoglerne ved impulsbehandling, er der blevet forsket i baggrunden for dennes virkning. Forskellige hypoteser for de bagvedliggende mekanismer er fremkommet, og af disse er udvalgt syv, som menes at være repræsentative for de forskellige retninger forskningen har bevæget sig i. Disse hypoteser vil blive beskrevet i de følgende afsnit med henblik på grundlæggende forsøgsstrategier og resultater. Artiklerne læst i forbindelse hermed skelner ikke mellem de forskellige knoglecellers udviklingsstadier. Dette ses især i forbindelse med osteoblastcellelinier, hvor der ikke i særlig høj grad skelnes mellem stamceller, forstadier og osteostamceller. Det er derfor forsøgt så vidt muligt at præcisere hvilket cellestadie der refereres til. Dette gøres vel vidende at alle celler befinder sig på individuelle stadier, og at det ikke er praktisk muligt kun at udtage celler som befinder sig på samme stadium. Der gøres opmærksom på, at følgende hypoteser beskæftiger sig med impulsgivet PTH, og derfor ikke med den PTH-regulering der normalt finder sted i kroppen. 5.1 Proteinkinase A og -C afhængige signalveje og parathyroideahormons anabolske effekt PTH(1-34) har i flere forsøg vist at udøve samme effekt som PTH(1-84), da de begge via PTHr1 aktiverer en række parallelle signalveje såsom camp-afhængig proteinkinase A (PKA)- signalvejen og den fosfolipase C (PLC)-afhængige samt PLC-uafhængige proteinkinase C (PKC)-signalvej [Yang et al ]. PKC-signalvejen er endnu ikke fuldt ud forstået, mens der haves en større viden om PKA-signalvejens virkning og funktion. Forsøg udført for at klarlægge 29
46 signalvejene for den anabolske virkning af PTH på knoglevævet har hidtil fundet at signalering via camp-afhængige signalveje resulterer i aktiveringen af PKA-signalvejen [Murrills et al. 2004; Yang et al. 2007]. Det har desuden vist sig at aktiveringen af PKA/PKC-signalvejene ligger i specifikke områder i PTH(1-34) s aminosyresekvens. Det vides blandt andet at de to første amino-terminal-syrer i PTH(1-34) er krævet for aktivering af adenyl cyklase, som er det enzym der omdanner ATP til camp [Yang et al. 2007]. I et studie af [Mohan et al. 2000] undersøgtes forskellige PTH-analogers påvirkning af knoglevævsformation for at eftervise, at forskellige analoger aktiverer forskellige signalveje, i dette tilfælde PKA og PKC. For at afklare hvilke af de undersøgte PTH-analoger der er involveret i PTH s anabolske effekt, indsprøjtedes PTH-analogerne (1-34), (1-31) og (2-34) i mus, og disses virkninger måltes på markører for knogleformation. Yderligere undersøgte [Mohan et al. 2000] de tre analogers effekt på BMD efter længere tid. Deres resultater viste, at når PTH(1-34) blev indsprøjtet i mus over en periode på 15 dage, sås der en dosis-afhængig forøgelse af osteocalcinniveauet i serum og i knogleekstraktens alkaline phosphatase aktivitet (ALP), som begge er markører for knogleformationen. PTH(1-31) viste den samme effekt som PTH(1-34), mens en indsprøjtning af PTH(2-34) resulterede i betydeligt lavere værdier af både ALP og osteocalcin. For yderligere at undersøge PKA s rolle i knogleformationen ved indsprøjtninger af PTH, indsprøjtede [Mohan et al. 2000] mus med to forskellige PTH-analoger henholdsvis PTH(1-34) og PTH(2-34), hvor PTH(2-34) har en reducerende virkning på campaktiviteten. PTH(2-34) stimulerede altså ikke adenyl cyklase-aktiviteten, som camp-aktiviteten og dermed PKA-signalvejen er afhængig af. Forsøget viste at indsprøjtning med PTH(1-34) resulterede i forhøjede værdier af ostecalcin og knogle-alp-niveauet i forhold til PTH(2-34) og kontrolgruppen. Disse data peger i retningen af, at aktiviteten af camp er essentiel for knogleformationen ved injektion af PTH, hvormed sagt at camp er essentiel for PTH s anabolske virkning. For at undersøge virkningen af analogerne over en længere periode, behandlede [Mohan et al. 2000] musene dagligt med PTH(1-34) og PTH(1-31) i 22 uger, og disse blev sammenlignet med kontrolvehicle. Både behandling med PTH(1-34) og PTH(1-31) viste forøgede værdier af osteocalcin i serum og værdierne opnåede et maksimumniveau indenfor to uger. Niveauet blev bevaret under hele behandlingsperioden. Der var ingen betydelige forskelle i osteocalcin-niveauet for henholdsvis PTH(1-34) og PTH(1-31). Den totale BMD for den midterste del af knoglen var forøget med 18 % og 9 % ved indsprøjtning af henholdsvis PTH(1-34) og PTH(1-31). 30
47 Knoglemineralindholdet (BMC) blev forøget med 41 % for PTH(1-34) og 26 % for PTH(1-31). Det ses heraf at PTH(1-34) havde en betydelig større virkning på både BMD og BMC i forhold til PTH(1-31) [Mohan et al. 2000]. Disse forsøgsresultater understøttes af [Murrills et al. 2004] der ligeledes analyserede forskellige PTH-analogers effekt i forhold til deres anabolske virkning både in vivo og in vitro i OVX-rotter. C-terminal trunkerede PTH-analoger viste sig at forøge den totale BMD i skinnebenet, og der blev yderligere observeret en forøgelse i trabekulære regioner i forhold til ikke behandlede OVX-rotter. Ydermere viste forsøgsresultaterne at N-terminal trunkerede- og PTH-midtregion-analoger kun havde en minimal virkning på BMD i trabekulære områder af skelettet, samt at PTH(53-84) viste sig at være inaktiv ved alle parametre [Murrills et al. 2004]. Begge studier konkluderer at N-terminalen er yderst betydelig for PTH s anabolske virkning, og at de første amino-terminal grupper er ansvarlige for aktiveringen af PKA, samt at PTH(1-34) er den mest potente PTH-analog til behandling af osteoporose. [Yang et al. 2007] undersøgte hvorvidt PTH s anabolske effekt er medieret af PLC-afhængig eller uafhængig PKC-signalering in vivo. Fra [Yang et al. 2007] s tidligere arbejde har det vist sig at mutation i PTH(1-34), hvor serin erstattes med glycin, kraftigt forringer PLC-aktiveringen uden at påvirke camp/pka-signalvejen. De analoger som besidder denne mutation er desuden i stand til at aktivere den PLC-uafhængige PKC-signalering. Dette muliggør en undersøgelse af PLC-uafhængig PKC-signalering. PTH-analoger med denne mutation betegnes med [M] foran analogen. [Yang et al. 2007] arbejdede med PTH-analogerne: [M]hPTH(1-34), [M]hPTH(1-28) og hpth(1-34). For at bedømme [M]hPTH ernes knogleanabolske effekt blev disse og hpth(1-34) indsprøjtet i mus. Resultaterne viste at både hpth(1-34) og begge [M]hPTH-analoger forøgede den totale BMD, men at [M]hPTH(1-34) havde en betydelig større virkning. Dette betyder at den PLC-uafhængige PKC-signalvej optimerer PKA s effekt på BMD. Yderligere blev der observeret at [M]hPTH(1-34) s virkning sås hurtigere end de to andres. Resultaterne fra den totale BMD blev sammenlignet med resultater fra BMD målt på yderpunkterne af lårbenet. Denne sammenligning viste også at [M]hPTH(1-34) s virkning var størst og sås hurtigere. Det skal dog nævnes at [Yang et al. 2007] også har undersøgt dette ex vivo, og her viste [M]hPTH(1-34) ikke denne effekt på BMD. [M]hPTH(1-34) og hpth(1-34) viste yderligere at forårsage en signifikant forøgelse i knoglevolumen og i mængden af trabekulær væv i skinnebenet i forhold til [M]hPTH(1-28), hvilke er vist både in vivo og ex vivo. Samlet set peger [Yang et al. 2007] s resultater på, at camp/pka-signalvejen stimuleret via PTHr1 er den dominerende respons i forhold til den knogleanabolske virkning. PLC-uafhængig 31
48 PKC-signalveje bliver stimuleret af PTH-peptider, der indeholder sekvensen PTH(29-34). PTHpeptider med denne sekvens viser sig at optimere PKA-signalering ved at forøge hastigheden af knogleformationen i det trabekulære knoglevæv, og antallet af aktive knogle sites. For at få et overblik over signalvejene, se figur 9. Figur 9: PTH(1-34) bindes til PTHr1 på osteoblaster for herigennem at aktivere camp/pkasignalvejen og PKC-afhængig og -uafhængig signalering. Disse signalveje stimulerer knogleformation, men camp/pkasignalvejen har den største effekt [Jørgensen 2008]. 5.2 Parathyroideahormon opregulerer c-fos-udtrykket i knogleceller Studier med mus viser, at disse i deres tidlige udviklingsstadium primært udtrykker c-fos i vækstregionerne hvor brusk og knogler udvikles [Grigoriadis et al. 1995], hvilket indikerer at c- fos er involveret i knoglevækst og derfor er interessant i forhold til knogleformation. Andre undersøgelser viser, at c-fos knock out mus udvikler osteoporose og mangel på osteoklaster (Johnson et al.1992). Transgene mus som overudtrykker c-fos udvikler ossøs hyperplasia, som er en unormal cellevækst i knogler, ikke at forveksle med kræft, samt kondroblastisk osteosarkomer, som er en kræftform, der forekommer i knoglevæv [Grigoriadis et al. 1995]. c-fos udtrykkes under osteoblastisk differentiering [McCabe et al. 1995], og der ses et stort udtryk under proliferationen og under syntetisering af matrix [Grigoriadis et al. 1995; McCauley et al ]. c-fos proto-oncogenet er et tidligt respons gen og en transkriptionsfaktor, som under 32
49 påvirkning af mitogener og vækstfaktorer undergår hurtigt transskriptionsaktivering. Som tidligere nævnt i afsnittet Osteoklastogenese danner c-fos-proteinet heterodimere med medlemmer af c-jun-familien, og disse danner sammen med ATF transskriptionskomplekset AP- 1, og regulerer herved transkriptionen af en række målgener i osteoklaster. Det viser sig desuden at generne for osteocalcin og kollagenase i osteoblaster muligvis er mål for PTH-stimuleret c-fospåvirkning i knoglemæssige sammenhænge, idet de har vist sig at have AP-1 sites i deres promoter [Rajakumar & Quinn 1996]. Dette midlertidige c-fos-respons forårsaget af PTH(1-34) koblet med den udbredte tilstedeværelse af AP-1 sites på gener, med en vigtig knogleregulatorisk egenskab, gør c-fos til en mulig kandidat i forhold til mediering af PTH s effekter i knogler [McCauley et al. 1997]. Forskning tyder på at PTH(1-34) har indvirkning på c-fos-niveauet i osteoblastiske celler, og det menes at PTH(1-34), medieret gennem camp, transskriptionelt regulerer c-fos-niveauet [Karaplis & Goltzman 2000]. I en in vitro-undersøgelse af [McCauley et al. 1997], blev det forsøgt at klarlægge PTH s virkning på steady state udtrykket af c-fos i osteoblaster, samt den transskriptionelle regulering af c-fos genet, og dets afhængighed af camp i den aktive matrixproduktion af osteoblastiske celler. Til dette blev brugt cellelinier som blev udsat for forskellig dosis af PTH(1-34), hvilket viste at behandling med PTH(1-34) over et tidsinterval på en time, dosisafhængigt stimulerede udtrykket af steady state c-fos mrna i cellerne. Desuden viste det sig at inkubering med PTH(1-34) gav et hurtigt c-fos mrna respons i osteoblaster efter 20 minutter og nåede sit maksimum efter min, hvorefter det igen aftog til et ikke-målbart niveau. Undersøgelsen understøttede ydermere hypotesen om, at den transkriptionelle regulering af c-fos forårsaget af PTH(1-34) var medieret gennem camp. Dette blev klarlagt ved at måle c-fos-udtrykket i henhold til forskellige stoffer, som enten havde en stimulerende eller inhiberede effekt på camp-signalvejen. Blandt andet blev Forskolin, som er en kraftig camp-stimulator, undersøgt i forhold til c-fos, hvor det viste sig at denne aktiverede c-fos på sammen måde som PTH. En analog af Forskolin, 1,9-dideoxyforskolin, stimulerede ikke c-fos. Forskolinanalogen havde samme egenskaber som Forskolin bortset fra at den manglede evnen til at stimulerer camp. Dette viser at det kun er den camp-stimulerende effekt af Forskolin, som har indvirkning på c-fos-udtrykket. Ydermere blev forbol 12-myristat 13-acetat (PMA), en PKC-aktivator, undersøgt. I denne forbindelse blev der ikke registreret en stigning i c-fos-udtrykket, hvilket indikerer at c-fos ikke stimuleres gennem PKC-signalvejen. In vitro-undersøgelsen af [McCauley et al. 1997], inddragede også et in vivo-forsøg af [Lee et al. 1994] til at underbygge, samt udbygge egne resultater. I dette forsøg blev PTH givet in vivo til normale fire uger gamle han-rotter. De opnåede resultater stemmer overens med [McCauley et al. 1997] s resultater, som viste et c-fos-udtryk i osteoblaster i tidsintervallet minutter. [Lee et 33
50 al. 1994] undersøgte PTH(1-84) s påvirkning af c-fos-udtrykket ved in vivo-forsøg med rotter. De registrerede c-fos mrna-udtryk efter 15 minutter i osteoblaster, og efter 30 minutter måltes der maksimalt c-fos-udtryk både i osteoblaster og kondrocytter. Efter en time sås der intet udtryk i osteoblaster, hvor knodrocytternes opregulering af c-fos-udtryk først forsvandt efter to timer. Derudover blev målt c-fos-udtryk i et lille antal stromaceller efter 30 minutter, og efter en time var udtrykket opreguleret i størstedelen af stromacellerne. Efter to timer kunne der ikke registreres c-fos-udtryk i stromaceller, men derimod var udtrykket højt i næsten alle osteoklaster. Osteoklasternes opregulering af c-fos faldt efter fire timer. Der sås en c-fos-opregulering allerede ved en dosis PTH på 1 pm. Desuden måltes PTHr1-udtrykket i osteoblaster, kondrocytter, stromaceller og osteoblaster. Der sås udtryk i kondrocytter, osteoblaster og en lille del af stromacellerne men ikke i osteoklasterne og størstedelen af stromacellerne. Dette tyder på at c-fos-opregulering i størstedelen af stromacellerne og osteoklasterne skyldes indirekte påvirkning af PTH gennem osteoblasterne. Opreguleringen i få af stromacellerne skriver [Lee et al. 1994] sandsynligvis skyldes næsten færdigdifferentierede stromaceller som besidder PTHr1. Det faktum at intervalbehandling med PTH opregulerer c-fos in vivo og in vitro, samt stimulerer knogleformation, indikerer at PTH s anaboliske effekt blandt andet kommer til udtryk gennem c- fos [McCauley et al. 1997]. På baggrund af undersøgelsens egne resultater og nævnte studiers resultater, konkluderes det at disse tyder på, at PTH(1-34) binder sig til receptorer på osteoblastiske celler for herigennem at aktivere camp, som efterfølgende stimulerer c-fostransskriptionen. [McCauley et al. 1997] skriver at de osteoblastiske celler muligvis responderer herpå, ved udskillelse af en eller flere faktorer som stimulerer differentieringen af omgivende stromaceller til aktive osteoblaster, hvilket resulterer i øget knogleformation hvilket støttes af [Lee et al. 1994] s resultater. [Lee et al. 1994] skriver desuden, at aktiveringen af osteoklaster sker gennem osteoblaster. Dette kan forklare det før omtalte c-fos-udtryk i stromaceller og osteoklaster, på trods af at disse mangler PTHr1. For at få et overblik over c-fos-udtryk og dennes virkning på knoglecellerne ved PTH-stimulering, se figur
51 Figur 10: PTH bindes til PTHr1 på de modne ostoeoblaster, samt nogle differentierede stromaceller, som derefter udtrykker c-fos. Efter c-fos-opregulering, udskiller osteoblasterne faktorer, som får stromaceller til at proliferer og differentiere sig. Derudover igangsættes produktionen af knoglematrix. Osteoblasterne opregulerer RANKL for herved at igangsætte osteoklastdifferentieringen til modne osteoklaster, som opregulerer udtrykket af c-fos [Jørgensen 2008]. 5.3 IGF-I er essentiel for parathyroideahormons anabolske virkning Det har vist sig at impulsbehandling med PTH øger produktionen af IGF-I in vivo i osteoblastiske celler i både mus og rotter (McCathy et al.1989; Linkhart & Mohan 1989), samt in vitro i osteoblastiske celler udtaget fra rotter (Watson et al.1995). Studiet [Miyakoshi et al. 2001] benyttede fem uger gamle voksende mus, som over et tidsinterval på 10 dage daglig fik injektion med PTH(1-34). I denne forbindelse blev det fundet at PTH ikke havde en signifikant effekt på knogleformationsparametrene ALP og osteocalcin i IGF-I knock out mus. Derimod viste der sig signifikant øgning af ALP og osteocalcin i vildtype mus under behandling med PTH(1-34). I overensstemmelse med disse resultater gav den samme behandling med PTH(1-34) et øget BMD i vildtype-mus i modsætning til knock out mus. Ydermere viste undersøgelsen at behandling med 35
52 PTH øgede antallet af osteoblaster i IGF-I knock out mus, som fik tilført IGF-I, hvorimod det modsatte viste sig i knock out mus, der ikke fik tilført IGF-I. Samlet indikerer disse resultater at PTH s anabolske effekt på knoglevæv afhænger af tilstedeværelsen af IGF-I i voksende mus. I samme studie af [Miyakoshi et al. 2001] blev der fremstillet forskellige hypoteser for PTH s manglende effekt på knogleformationen i IGF-I knock out mus, hvor en af disse hypoteser var at knock out mus havde færre osteoblaster end vildtype-mus. Denne hypotese blev fremstillet på baggrund af, at knock out mus udviste underudviklet knoglevækst og var størrelsesmæssigt mindre end vildtype-mus. Mangelen på osteoblaster blev modbevist, idet der blev påvist et signifikant osteocalcinniveau, som er et produkt udskilt af modne osteoblaster. Derudover ses, som tidligere nævnt, at behandling med IGF-I og PTH signifikant øger knogleformationsparametre i IGF-I knock out mus, hvilket antyder at den manglende PTH effekt, ikke er grundet en manglende evne hos osteoblaster (f.eks. grundet et lille antal eller nedsat funktion) til at reagerer på anabolske agenter som PTH. En anden hypotese [Miyakoshi et al. 2001] fremstillede for PTH s manglende effekt i knock out mus var, at den manglende IGF-I-signalvej i disse mus resulterer i, at PTH ikke kan stimulere vigtige målgener til at påvirke osteoblaster til knogleformation. Denne hypotese underbygges af, at PTH in vitro øgede antallet af osteoblaster fra knock out mus, som fik tilført IGF-I, hvorimod knock out mus som ikke fik tilført IGF-I, ikke fik et øget antal osteoblaster. In vitro-studier af (Ernst & Froesch 1988; Gray 1998) indikerer desuden at mange systemiske hormoner medierer deres knogleformative effekt ved rekruttering af IGF-I. [Miyakoshi et al. 2001] konkluderer at PTH s anabolske effekt kræver tilstedeværelsen af IGF-I i voksende mus, samt på baggrund af egne og andre studiers resultater, at IGF-I spiller en vigtig rolle i den anabolske virkning af PTH via mediering af knogleregulerende systemiske hormoner. Det er dog stadig ikke klart om tilstedeværelsen af IGF-I til mediering af PTH s anabolske effekt kun er krævet hos voksende mus, eller om det også gælder for fuldvoksne mus. IGF-I er desuden blevet sat i forbindelse med blandt andet mediering af antiapoptose hos osteoblaster. Dette undersøgtes in vitro i [Hill et al. 1997], som benyttede primære osteoblaster udtaget fra mus. Osteoblasterne blev forhindret i at proliferer ved at udsætte disse for thyminin. På denne måde kan det udelukkes at en evt. stigning i osteoblastantallet skyldes proliferation, men i stedet skyldes antiapoptose. Efter 48 timer blev der ved hjælp af MTT, som er et stof der ændrer farve når det optages i mitrokondrier hos levende celler, undersøgt antallet af overlevende osteoblaster. I denne forbindelse blev der fundet frem til, at IGF-I gennem IGF-I-receptor stimulerede antiapoptose, og at osteoblastoverlevelsen havde en dosisafhængig stigning med en maksimal overlevelsesprocent på ca. 67 % efter 24 timer og ca. 28 % efter 48 timer. Ydermere 36
53 viser en in vitro-undersøgelse af [Canalis 1980] at IGF-I også øger proliferation af osteoblastiske celler. Dette blev undersøgt ved hjælp af [3H]thymidin, hvor der sås en dosisafhængig inkorporering af [3H]thymidin i de osteoblastiske cellers DNA. Der blev dog først registreret en effekt efter 6 timer, og effekten opnåede et maksimalt niveau efter 12 timer, som blev bevaret i 96 timer. På baggrund af [Hill et al. 1997] og [Canalis 1980] s studier undersøger [Grey et al. 2003] de signalveje, der medierer IGF-I s proliferative og antiapoptotiske virkning. Resultaterne af undersøgelsen viser at IGF-I stimulerede proliferation og hæmmede apoptose, hvilket stemmer overens med de to ovenstående undersøgelser, og at denne virkning medieres gennem parallelle signalveje som involverer PI-3 kinase og MAPK-signalvejene. Derudover har både PTH og IGF-I vist sig at være involveret i udtrykket af c-fos [Lee et al. 1994; Harold et al. 1990]. I studiet af [Harold et al. 1990] blev IGF-I s effekt på c-fos undersøgt in vitro både på osteoblastiske cellelinier og på primære osteoblaster udtaget fra mus. IGF-I s effekt på c- fos mrna blev målt i både cellelinier og primære osteoblaster efter 15, 30, 60 og 240 minutter. I cellelinien blev målt et maksimalt IGF-induceret c-fos-udtryk efter 15 minutter hvorefter niveauet faldt. Efter 30 minutter var udtrykket stadig højt og efter 60 minutter kunne stadig observeres et lavt c-fos-niveau, hvorimod der ved 0 og 120 minutter ikke blev målt c-fos-udtryk. I primære osteoblaster blev det maksimale c-fos niveau målt efter 30 minutter og var efter 60 minutter næsten forsvundet. Studiet målte også at IGF-I stimulerede proliferation i osteoblastiske cellelinier, se figur 11. Det at både PTH og IGF-I indvirker på c-fos-udtrykket indikerer, at PTHsignalvejen interagerer med IGF-I-signalvejen på ét eller flere punkter. På denne måde kan fjernelse af IGF-I, og herved fjernelse af signalvejen i knock out mus forhindre PTH i at stimulerer vigtige målgener, som er nødvendige for osteoblastisk proliferation og/eller matrixsyntese [Miyakoshi et al. 2001]. Figur 11: PTH opregulerer IGF-I, som via parallelle signalveje stimulerer proliferering og antiapoptose [Jørgensen 2008]. 37
54 5.4 Parathyroideahormons aktivering af bone lining celler til omdannelse til osteoblaster Det oprindelige formål med studiet [Dobnig & Turner 1995] var at undersøge hypotesen, om at osteoblaster rekrutteres fra osteoblastforstadier ved PTH-behandling. Det vides at preosteoblaster prolifererer før de differentierer sig til osteoblaster. For at påvise de osteoblaster der er fremkommet på denne måde, tilførtes mus [3H]thymidin gennem behandlingsperioden. [3H]thymidin, som er et radioaktivt stof, inkorporeres i nydannet DNA under S-fasen i cellecyklus. Det er på denne måde muligt, at se om en celle har undergået mitose. Forsøgene blev foretaget på måneder gamle hun-rotter som blev indsprøjtet én gang dagligt med hpth(1-34) eller brugt som kontrolrotter. Igennem én uges behandling med hpth(1-34) blev der kontinuerligt tilført [3H]thymidin for at bestemme den procentdel af de nyproducerede osteoblaster som stammede fra osteoblastforstadier. Fra seks osteoblaster per mm knogleomkreds inden PTH-behandling, øgede PTH osteoblastantallet til 42 per mm knogleomkreds der opstod i behandlingsforløbet. Altså tydede det på, at i gennemsnit, 36 osteoblaster opstod i behandlingsperioden. Hvis de nye osteoblaster stammede fra osteoblastforstadier ville 86 % af osteoblasterne være mærket med [3H]thymidin. Dette var dog ikke tilfældet, da det mærkede antal var drastisk mindre end forventet (4 %) og ikke var signifikant forskellig fra kontrolrotter, se figur 12. Figur 12: Her vises antallet af [3H]thymidinmærkede osteoblaster hos PTH-behandlede og vehiclebehandlede mus, samt det forventede antal ud fra viden om antal af nydannede osteoblaster [Dobnig & Turner 1995]. 38
55 Der konkluderes derfor at det øgede antal osteoblaster ved PTH-behandling ikke rekrutteres fra celler, som gennemgår cellecyklus såsom osteoblastforstadier. Pågældende studie foreslår, at de i stedet stammer fra bone lining celler, som aktiveres og gendannes til osteoblaster, se figur 13. Dog er det ikke endegyldigt påvist, at PTH-receptorer findes på bone lining celler. [Dobnig & Turner 1995] skriver endvidere, at vækstfaktorer som IGF-I og -II produceret af osteoblaster muligvis kan ændre bone lining cellers aktivitet ved parakrin signalering. Hvis dette er tilfældet er bone lining celler inaktive osteoblaster. Det kan ikke udelukkes at osteoblasterne stammer fra nogle celler som allerede havde gennemgået cellecyklus og kun manglede yderligere differentiering selvom [Dobnig & Turner 1995] selv skriver at dette virker usandsynligt da det ville kræve en hurtig koordineret fjernelse, og erstatning af bone lining celler. Pågældende studies konklusion omkring bone lining cellers omdannelse til osteoblaster understøttes af [Leaffer et al.1995], hvor in vivo forsøg på rotter viste, at PTH-behandling resulterede i hurtige forandringer i antallet af osteoblaster og bone lining celler, som stemmer overens med omdannelse af bone lining celler til osteoblaster og omvendt ved afslutning af behandling. I forsøget blev rotterne behandlet med en syntetisk hpthrp-analog(1-34), bovinepth(1-34) eller kontrolvehicle. Herefter undersøgtes de celler, som fandtes på den vertebrale knogleoverflade både antallet af cellekerner i alt og antallet af osteoblaster og bone lining celler. Man fandt, at antallet af bone lining celler faldt, mens antallet af osteoblaster steg indenfor fem dage efter behandlingens start. Der sås en lille stigning af antallet af cellekerner på knogleoverfladen på dag 5 og 19, men denne stigning var ikke stor nok til at forklare stigningen i antallet af osteoblaster, og derfor foreslås det, at stigningen af osteoblaster skyldtes at bone lining celler omdannes til osteoblaster. Efter behandlingen sås den modsatte udvikling hvilket antyder at bone lining cellerne beholder den osteoblastiske fænotype. [Leaffer et al.1995] skriver som [Dobnig & Turner 1995], at det er usandsynligt, at det stigende antal osteoblaster skyldes osteoblastforstadier som kun mangler den endelige differentiering. Dette menes da deres forsøg viste, at antallet af cellekerner holdes nogenlunde konstant, og at dette derfor ville kræve en ligelig migrering af celler fra knogleoverfladen som til. En anden in vivo-undersøgelse (Qi et al. 1995) lavet på rotter støtter, at PTH s anabolske virkning er begrænset af knogleoverflade, hvilket netop vil være tilfældet hvis det er bone lining cellers omdannelse til osteoblaster som forårsager den anabolske virkning. 39
56 Figur 13: Her vises at bone lining celler gendannes til osteoblaster via IGF-I under påvirkning af PTH [Jørgensen 2008] 5.5 Parathyroideahormon stimulerer sammenklæbning af mesenkymale stamceller til knogleoverflader Osteoblaster dannes som før nævnt ud fra MSC. En af de første hændelser, som blev rapporteret ved in vivo-forsøg med impulsgivet PTH var c-fos-udtryk i celler på, og i nærheden af, knogleoverflader [Lee et al. 1994]. Dette kunne indikere, at MSC fra knoglemarven klæber sig fast på overfladen af det trabekulære knoglevæv og danner kolonier efter PTH-stimulering som en del af den anabolske effekt, hvilket blev nærmere undersøgt in vivo og in vitro af [Davies & Chambers 2004]. For at undersøge hypotesen, målte [Davies & Chambers 2004] mængden af MSC, som kunne ekstraheres fra knoglemarven af mus, efter en impulsgivet PTH-behandling. Tanken var, at PTH ville sænke antallet af MSC som kunne udtages fra knoglemarven, da disse ville have sat sig fast på den trabekulære knogleoverflade. Undersøgelsen blev gjort ved at indsprøjte mus med enten PTH eller kontrolvehicle. Derefter blev musenes knoglemarvsceller høstet og inkuberet i 14 dage, og kolonier blev talt. I denne in vivo-undersøgelse sås der en stor undertrykkende virkning af PTH på antallet af MSC. Antallet af MSC som blev fundet i knoglemarven efter indsprøjtning med PTH faldt i mindst seks timer, men var delvist genopbygget efter 24 timer. Andre undersøgelser af PTH s påvirkning af MSC antallet i knoglemarven modsiger dette resultat; [Jilka et al.1999] og (Sakai et al. 1999) rapporterede ingen ændring under in vivo forsøg med mus, mens (Nishida et al. 1994) rapporterede en stigning i antallet i in vivo forsøg med rotter. 40
57 Det blev desuden undersøgt om PTH kunne stimulere MSC til at klæbe sig fast på en knogleoverflade in vitro. Til dette blev knoglemarvsceller fra ubehandlede mus inkuberet med PTH i varierende tidsperioder. Ikke-adhærerede celler, altså de som ikke havde klæbet sig fast til en overflade blev fjernet, og de adhærerede celler blev inkuberet i PTH-frit medie i 14 dage for at undersøge antallet af MSC som adhærerede. Undersøgelsen viste at inkubation med PTH markant hævede antallet af MSC som klæbede sig fast på knogleoverfladen i forhold til ikke behandlede MSC. Hvis det også er tilfældet at PTH stimulerer MSC til at klæbe sig fast på knoglerne og dele sig in vivo kan det forklare ovenstående fald af MSC i knoglemarven efter PTH-behandling samt PTH s anabolske virkning. Når knoglemarvsceller in vitro blev inkuberet med PTH i en tidsperiode på 7-14 dage havde det ingen effekt på antallet af MSC celler som adhærerede. [Davies & Chambers 2004] skriver at dette indikerer at PTH muligvis påvirker MSC in vivo på en måde som ikke ses in vitro. [Davies & Chambers 2004] viste, at PTH-indsprøjtninger hurtigt resulterede i et fald i mængden af MSC, som kan fjernes fra knoglemarven. Desuden viste det sig, at inkubation med PTH øgede antallet af MSC som klæbede sig fast til en overflade indenfor 24 timer in vitro. Dette støttes af tidligere forsøg af (Friedenstein et al. 1968) som opdagede at dyrkning af uoprenset knoglemarv kunne give ophav til en gruppe celler som var i stand til at klæbe sig sammen på en overflade og danne kolonier. Dette var dog ikke tilfældet i [Davies & Chambers 2004] ved inkubering med PTH i 7-14 dage, hvilket som før nævnt tyder på at visse mekanismer som sker in vivo ikke ses in vitro. [Davies & Chambers 2004] fremkommer med hypotesen at PTH s anabolske effekt skyldes påvirkning af MSC til at sætte sig på den trabekulære knogleoverflade og danne kolonier, hvilket vil resultere i proliferering og i sidste ende et øget antal osteoblaster på knogleoverfladen, se figur
58 Figur 14: Her vises at PTH påvirker MSC til at danne kolonier på den trabekulære knogleoverflade, hvorefter disse prolifererer [Jørgensen 2008]. 5.6 Parathyroideahormons antiapoptiske virkning på knogleceller Stigningen i antallet af osteoblaster som ses ved PTH-behandling kan muligvis skyldes, at osteoblaster undgår apoptose, hvilket ville resultere i flere modne matrix-dannende osteoblaster. I denne forbindelse refereres til to artikler som begge fokuserer på PTH s indvirkning på levetiden af osteoblaster. Celleapoptose er svær at måle, da hændelsen forløber hurtigt, og ikke efterlader spor efter processen. Under apoptose udskiller celler dog kortvarigt unikke histologiske kendetegn, som kan registreres ved hjælp af deoxynucleotidyl transferase biotin-dutp nick (TUNEL)-mærkning [Jilka 2007]. I in vivo-forsøg foretaget af [Jilka 2007] blev PTH s virkning på osteoblastapoptose og knogleformation undersøgt. Her blev voksne mus dagligt indsprøjtet med PTH(1-34) i 28 dage, og der observeredes en dosisafhængig stigning i BMD, grundet reduktion i den registrerede osteoblastapoptose. I denne sammenhæng viste målinger fra det sekundære trabekulære knoglevæv i lårknoglen, at samme dosis PTH som hæmmede osteoblastapoptose, også øgede antallet af osteoblaster, hastigheden af knogleformation og mængden af trabekulæret knoglevæv. Reduceringen i osteoblastapoptose sås allerede efter to indsprøjtninger, og efter fire PTHindsprøjtninger var osteoblastapoptose reduceret med 50 %, og antallet af osteoblaster var steget til det dobbelte. Dette indikerer, at stigningen i osteoblaster direkte ses som resultat af antiapoptose. Det bekræftes af [Jilka et al.1999], som undersøgte, hvorvidt stigningen i osteoblastantal skyldes større rekruttering af osteoblaster fra MSC eller osteoblasters forlængede 42
59 levetid. [Jilka et al.1999] fandt, at MSC i mus ikke prolifererer mere ved PTH-behandling end ved indsprøjtning med kontrolvehicle, men at der tydeligt ses et fald i osteoblastapoptose. [Jilka 2007] refererer endvidere til andre studier hvor PTH s antiapoptitiske effekt har været demonstreret. I [Bellido et al. 2003] og (Krishnan et al. 2003), hvor der blev benyttet osteoblastcellekulturer sås, at PTH hurtigt aktiverede en antiapoptotisk signalvej, som involverede camp-medieret aktivering af PKA og i sidste ende fosforylering og inaktivering af et apoptotisk protein, kaldet Bad. Endvidere viste forsøgene, at PTH øgede transskription af overlevelsesgener såsom Bcl-2. Det sås desuden, at PTH påvirkede syntesen af visse osteogene vækstfaktorer og cytokiner, hvilke udøver en prolifererende og pro-overlevelseseffekt på osteoblaster [Grey et al. 2003]; (Conover 2000), se afsnit 5.3 IGF-I er essentiel for parathyroideahormons anabolske virkning [Jilka 2007] konkluderer, at PTH-behandling hæmmer osteoblastisk apoptose og, at stigningen af osteoblastoverlevelse i høj grad bidrager til stigningen i antallet af osteoblaster, og hermed knogleformation. Resultaterne af in vitro-undersøgelser udført i omtalte studie og i [Bellido et al. 2003] samt (Krishnan et al. 2003), støtter endvidere teorien om, at impulsbehandling med PTH aktiverer korte udbrud af overlevelsessignaler, som resulterer i gentagne forsinkelser af apoptose. Kontinuerligt givet PTH har ikke denne effekt fordi det resulterer i langvarig nedsættelse af transskriptionsfaktoren, Runx2, som er specifik for celler af osteoblastlinien, under den grænseværdi som anses for værende nødvendig for overlevelsessignalering [Jilka 2007]. Et andet studie, [Stanislaus et al. 2000], rapporterer i modsætning til [Jilka 2007], at der ved 7 til 21 dages PTH behandling af rotter, sås en 50 % stigning i osteoblastapoptose i det primære trabekulære knoglevæv fra lårknoglen, i prolifereringszonen, se figur 15. Figur 15: 1. Her ses den proliferende zone hvor osteoblastapoptose er målt. Dette betegnes det primære trabekulære knoglevæv. 2. Det sekundære trabekulære knoglevæv. Til venstre på figuren opdeles knoglen i epifysen, enden af knoglen hvor knoglens vækstzone ses, i metafysen som er knogleskaftets overgang til epifysen og sidst diafysen, som er selve knogleskaftet [Stanislaus et al. 2000, redigeret af Hansen]. 43
60 Denne stigning i apoptose sås dog ikke efter behandlingens 28. dag hvor forsøget endte. Formålet med pågældende undersøgelse var at efterforske PTH s regulering af apoptose i knoglecellers prolifererende zone, da proliferering og apoptose bestemmer størrelsen af en cellepopulation. Studiet foretog udelukkende in vivo-undersøgelser af PTH s virkning, hvor fire til fem uger gamle han-rotter blev indsprøjtet med enten hpth(1-34) eller kontrolvehicle én gang dagligt. Alle rotterne blev slået ihjel, da de var lige gamle og med samme tidsinterval efter PTHindsprøjtning. [Stanislaus et al. 2000] undersøgte knogleformationen ved at lægge pulveriseret knoglevæv på en vækstplade, hvor celler blev mærket med TUNEL for at lokalisere apoptose. Endvidere måltes enzymaktiviteten for caspase, da caspase er en række proteiner, som er hovedfaktorerne bag den apoptotiske proces [sgul.ac.uk]. De celler, hvis apoptose steg pga. PTH-behandling var, ifølge pågældende studie, MSC, osteoblaster, osteocytter der udtrykker PTHr1 og andre celleoverfladereceptorer for væksthormoner der står i forbindelse med proliferering, differentiering og modning af MSC in vitro (Pfeilschifter, J. et al. 1990; Margolis et al. 1996). Da knogleomsætningen sker i løbet af fem til ti dage i unge rotter [Kimmel & Jee 1980], og da apoptosen måltes til at være størst mellem tre til syv dages behandling, foreslås det, at den PTH-igangsættende stimulering af apoptose kun finder sted i de nyligt dannede MSC, osteoblaster og osteocytter. Det vides endvidere at PTH fører til stigning i antallet af aktiveringssteder for knogleformation, og hermed en stigning i knogleomsætningen [Kotowicz et al. 1990]; [Delmas et al. 1995]. Denne stigning i knogleformation er i modstrid med den korte stigning der sås i knoglecelleapoptose. [Stanislaus et al. 2000] fremstiller følgende hypotese herfor; Den korte stigning i apoptose i det primære trabekulære knoglevæv ses måske som resultat af PTH-induceret matrixnedbrydning som indledning til knogleomsætning, da matrixnedbrydning går forud for formation. Denne hypotese underbygges med, at PTH viser sig at føre til stigning i specifikke matrixmetalloproteinase i osteoblaster og osteocytter (McClelland et al. 1998; Peeters-Joris et al. 1998). Matrixmetalloproteinase er i stand til at nedbryde ekstracellulær knoglematrix, og denne nedbrydning har vist sig at stimulere apoptose i matrix-tilknyttede celler [Frisch & Ruoslahti 1997], såsom osteoblaster og osteocytter, hvorfor ovenstående kan være en forklaring på den korte stigning i apoptose. Endelig underbygges hypotesen med, at der er en sammenhæng mellem stigende aktiveringsfrekvens, som er udtryk for hvor mange steder remodelleringsprocessen foregår, og stigende osteoblastapoptose (Weinstein et al. 1999). Når der kommer flere aktive remodellerings sites, sker der ligeledes en øgning af apoptosen, netop fordi hele omsætningshastigeden sættes i vejret. Jo flere celler der bliver aktive, jo flere må også dø. 44
61 Paradoksalt nok måltes caspaseproteinekstrakt fra PTH-behandlede rotter i forsøget til at være faldende sammenlignet med vehiclebehandlede kontrolrotter. Dette tyder på at PTH inhiberer caspase og derved apoptose, se figur 16. [Stanislaus et al. 2000] påviser derved, at den kortvarige stigning i apoptose ikke var reflekteret i caspaseenzymaktiviteten som måltes i ekstrakt fra lårmetafysen. En mulig forklaring på dette nævner [Stanislaus et al. 2000] kan være, at undersøgelsesmetoden i forsøget ikke var følsom nok til at opfange stigningen i caspaseenzymaktiviteten i de lokaliserede områder, hvor apoptose var observeret. En anden grund kan være, at inhiberingen af caspaseaktiviteten, tyder på, at PTH hovedsageligt fører til fald i caspaseenzymaktivitet. Dette fald kan have maskeret den lokaliserede stigning i caspaseenzymaktiviteten, der må have fundet sted pga. den kortvarige stigning i apoptose, hvilket muligvis forklarer hvorfor en stigning i caspaseenzymaktiviteten ikke kunne registreres. [Stanislaus et al. 2000] konkluderer, at PTH kan føre til et øget antal osteoblaster, sandsynligvis fordi PTH kan forlænge cellernes levetid via inhibering af apoptose. Det blev endvidere fundet, at impulsbehandling med PTH førte til celleapoptose i den prolifererende zone. Den korte og lokale stigning i apoptose, tænkes at ses som resultat af PTH-induceret matrixnedbrydning, som opfølges af knogleformationen og større aktiveringsfrekvens. Denne stigning i apoptose ses altså som en optakt til et stigende antal steder for aktivering og knogleomsætning [Stanislaus et al. 2000]. Begge studier påpeger, at PTH overordnet fører til antiapoptose i osteoblastiske celler. Hos [Stanislaus et al. 2000] ses dog en kortvarig stigning i apoptose som ikke observeres hos [Jilka 2007]. En grund til denne uoverensstemmelse kan være, at PTH s overordnede inhiberingen af caspase muligvis maskerer den stigning i apoptose der ses hos [Stanislaus et al. 2000] som ikke ses i [Jilka 2007]. Figur 16: Impulsbehandling med PTH fører til caspaseinhibering i osteoblaster, hvormed disse undgår apoptose og kan øge knogleformationen [Jørgensen 2008]. 45
62 5.7 Når impulsgivet PTH griber ind i remodelleringen overkompenserer osteoblaster I et forsøg af [Komarova 2005] blev der ved hjælp af en simpel matematisk model, undersøgt hvordan PTH generelt påvirker mekanismerne omkring knogleresorption og -formation. Forsøget fokuserer på ét parameter af gangen, og undersøger disse ved flere forskellige doser PTH. Denne model kan derfor give et indblik i hvordan PTH s anabolske effekt kan være en del af hormonets normale signalvej. [Komarova 2005] bygger udelukkende resultaterne på den matematisk model, og der er derfor hverken foretaget in vivo- eller in vitro-forsøg for at eftervise modellens resultater. Forsøgets udgangspunkt var oprindeligt, at PTH måtte øge mængden af osteoblaster direkte, men tidligere undersøgelser af [Black et al. 2003] har fundet ud af, at antiresorptive midler forringer PTH s anabolske virkning. Dette viser, at det må være koblingen mellem osteoklaster og osteoblaster, der er skyld i virkningen, og den matematiske model opbygges omkring denne overbevisning. Selve modellen bygger på et system af differentialeligninger, som alle er udledt gennem viden fra tidligere forsøg omhandlende den normale knogleremodelleringsproces, hvor PTH stimulerer osteoblaster til at udskille RANKL og OPG, som henholdsvis kan resultere i aktivering eller hæmning af osteoklastdifferentiering, se afsnittet Osteoklastogenese, samt andre lidt forsimplede antagelser. Disse antagelser omhandler at lokale faktorer kun kan regulere processen ved osteoblast- og osteoklastformation, hvorimod systemiske faktorer kan regulere både celleformation og død. Desuden antages det at en øgning i antallet af osteoklaster og osteoblaster over steady state niveau skyldes proliferering og differentiering af forstadier til modne celler. Modellen bygger på ovenstående, og dette giver slutteligt differentialeligninger, hvor ændringen i antallet af celler er afhængig af produktionsraten i form af differentiering af forstadier og rekruttering, og bortskaffelsesraten i form af celleapopotse og migrering for hver cellepopulation. Ved brug af ligningerne er der benyttet forskellige parameterværdier, og dette resulterer i et stort antal resultater, afhængig af antallet af benyttede værdier, såsom osteoblast- og osteoklastantal. Ved tolkning af resultaterne, fremkommet af den matematiske model, er [Komarova 2005] kommet frem til en forklaring på PTH s anabolske effekt. PTH stimulerer resorption ved, gennem RANKL, at aktivere osteoklaster til at genoprette calciumniveauet i serum. Osteoblaster er lokalt koblet til osteoklaster gennem parakrine og 46
63 autokrine faktorer, derfor resulterer anvendelse af PTH i aktivering af begge celletyper. Kontinuerlig givet PTH, hermed ikke ment det PTH der naturligt bliver udskilt i kroppen, medfører knoglevævstab fordi resorption som tidligere nævnt altid går forud for knogleformation, men når PTH nedbrydes, fjerner resorptive osteoklaster sig hurtigt igen. [Komarova 2005] nævner endvidere i forbindelse med impulsbehandling, at PTH aktiverer den allerede eksisterende resorption, som er et resultat af den knogleremodellering, der normalt findes i kroppen, fulgt af osteoblasters overkompensering. Den matematiske model fokuserer på et enkelt remodellerings site, og ved PTH-anvendelse vil der umiddelbart efter, forekomme et begyndende knoglevævstab, hvorefter en øgning i knogleformationen ses. [Komarova 2005] påpeger at in vivo-undersøgelser ikke har mulighed for at se isoleret på et enkelt remodellerings site, så det lokale begyndende knoglevævstab ses ikke her, da PTH påvirke mange sites som undergår remodellering asynkront. Derfor ser in vivo-forsøg kun den nettoanabolske virkning. I den matematiske model ses også en nettoformation, da osteoklasterne hurtigt stopper resorptionen og osteoblasterne, som sagt overkompenserer, se figur 17. Det må altså betyde, at det er en del af PTH s sædvanlige signalvej, der kan resultere i en knogleanabolsk effekt. Figur 17: Gives PTH ved bestemte doser bliver resorptive osteoklaster stimuleret til forsat resorption, og osteoblastcellelinier stimuleres til proliferering og differentiering. Dog nedbrydes PTH kortvarigt efter injektion, og den manglende PTH-stimulering af resorptive osteoklaster får disse til at forlade knogle sitet. Herved vil de nyligt modnede osteoblaster overkompensere og dette vil resultere i øget knogleformation [Jørgensen 2008]. 47
64 48
65 6. Diskussion 6.1 Proteinkinase A og -C afhængige signlveje og parathyroideahormons anabolske effekt [Yang et al. 2007] konkluderer både i overensstemmelse med deres tidligere forsøg og i overensstemmende med [Mohan et al. 2000] og [Murrills et al. 2004] at camp/pka signalvejen er den dominerende mekanisme for den anabolske virkning af PTH i trabekulært knoglevæv. Yderligere konkluderes det at PLC-uafhængig PKC-signalering, accelererer den trabekulær respons og forøger BMD ved nogle knogle sites. Disse resultater underbygges af studiet [McCauley et al. 1997], som fandt at c-fos medieres gennem camp/pka-signalvejen, samt af studier af [Bellido et a.l 2003] og (Krishnan et al. 2003), som viste at PTH gennem camp-medieret aktivering af PKA, inaktiverede det apoptotiske protein Bad. Da en del studier kommer frem til, at camp/pka-signalvejen er essentiel for medieringen af PTH s anabolske effekt på knoglevæv, og ingen læste artikler har modsagt dette, kan der siges at herske bred overensstemmelse omkring denne mekanisme. 6.2 Bone lining celler omdannes til osteoblaster og MSC klæbes til knogleoverflader [Dobnig & Turner 1995] s forsøg viste, at en stigning i osteoblaster ved PTH-behandling ikke stammede fra delende celler. Dette stemmer ikke overens med forsøgsresultaterne fra [Davies & Chambers 2004] som viste at knogleformationen stammede fra MSC som klæber sig fast til den trabekulære knogleoverflade og danner kolonier. MSC er stærkt proliferative og nogle af disse vil derfor have været mærket med [3H]thymidin i [Dobnig & Turner 1995] s forsøg, og ville herved kunne ses på knogleoverfladen, hvilket ikke var tilfældet. De to studiers forsøgsresultater er derfor modstridende. [Dobnig & Turner 1995] påpeger, at det ikke kan udelukkes at knogleformationen skyldes nogle celler som har gennemgået cellecyklus og kun mangler den sidste differentiering til osteoblaster, hvormed disse ikke vil blive mærket af [3H]thymidin. Dette ville dog ikke forklare PTH s undertrykkende virkning på antallet af MSC der ses i [Davies & Chambers 2004]. [Dobnig & Turner 1995] påpeger selv, at dette er usandsynligt fordi det ville kræve en hurtig koordineret fjernelse, og erstatning af bone lining celler. Det samme mener [Leaffer et al. 1995] som fandt, at antallet af cellekerner ved knogleoverfladen var nogenlunde konstant, og derfor fandt det usandsynligt, at lige så mange celler migrerede væk fra knogleoverfladen, som nydifferentierede osteoblaster migrerede til. Da bone lining celler skal 49
66 flyttes fra det sted på knogleoverfladen hvor knogleformation skal finde sted, er det dog en mulighed, at disse migrerer væk fra knogleoverfladen, og at dette tab i cellekerner opvejes af de nydifferentierede osteoblaster. Dette virker ikke særligt troværdigt, da de må antages, at bone lining cellerne kun flyttes og ikke forlader knogleoverfladen. Andre in vivo-undersøgelser af PTH s påvirkning af MSC-antallet har modsagt [Davies & Chambers 2004]. [Jilka et al. 1999] og (Sakai et al. 1999) rapporterede ingen ændring mens (Nishida et al. 1994) rapporterede en stigning i antallet. Dette kan dog skyldes, at de undersøgte antallet af MSC i knoglemarven for lang tid efter PTH-injektion, hvormed antallet af MSC vil kunne være blevet regenereret. Forsøg som viser øget c-fos-udtryk i celler i nærheden af knogleoverflader efter PTH-behandling, [McCauley et al. 1997], støtter hypotesen om at PTH s anabolske virkning skyldes øget replikation af MSC eller osteoblastforstadier, da c-fos især udtrykkes ved celledeling. Studiet [Leaffer et al. 1995] støtter som før nævnt hypotesen om bone lining celler omdannes til osteoblaster ved in vivo forsøg med rotter som undersøger hvor hurtigt antallet af osteoblaster og bone lining celler ændrer sig ved begyndelsen og afslutningen af PTH-behandling. De konkluderer ligesom [Dobnig & Turner 1995], at bone lining celler omdannes til osteoblaster ved PTH-behandling og tilbage til bone lining celler ved afslutningen af behandlingen. [Dobnig & Turner 1995] foreslår at det er IGF-I som omdanner bone lining celler til osteoblaster hvilket ikke kan afvises, da denne vækstfaktor i [Miyakosih et al. 2001] viser sig at være essentiel for PTH s anabolske virkning. [Dobnig & Turner 1995] s forsøg viste at det øgede antal af osteoblaster der sås ved impulsbehandling ikke skyldtes øget replikation af osteoblastforstadier. Ud fra dette konkluderer de, at det er bone lining celler der gendannes til osteoblaster. Det er dog ikke en holdbar konklusion, da en anden forklaring på dette kunne være at PTH stimulerer antiapoptose hos osteoblaster. Denne mulighed undersøges ikke nærmere af [Dobnig & Turner 1995]. Da der i stedet henvises til studiet [Leaffer et al. 1995], hvis forsøg underbygger hypotesen om at lining celler omdannes til osteoblaster, er det dog ikke udelukket at mekanismen finder sted. Pågældende forsøg virker velunderbygget i kraft af, at de direkte undersøger antallet af osteoblaster og bone lining celler i forhold til hinanden, hvorimod [Dobnig & Turner 1995] kun undersøger en eventuel proliferering af MSC. [Davies & Chambers 2004] bygger deres hypotese på, at PTH bevirker at antallet af MSC som kan udtages fra knoglemarven nedsættes, idet de sætter sig fast på knogleoverfladen, hvilket modstrides af andre nævnte studier. Det er derfor svært at slutte hvilken hypotese der er bedst underbygget. 50
67 6.3 Parathyroideahormons antiapoptiske virkning på knogleceller Både [Jilka 2007] og [Stanislaus et al. 2000] påpeger, at PTH overordnet fører til overlevelse i osteoblaster. Hos [Stanislaus et al. 2000] ses dog en kortvarig stigning i blandt andet osteoblastapoptose, som ikke afspejledes i caspaseaktiviteten, der tværtimod sås at være inhiberet af PTH. Dette påpeger [Stanislaus et al. 2000] kan skyldes, at PTH s overordnede inhiberingen af caspaseaktiviteten, som sås i proteinekstrakt fra metafysen, muligvis maskerede den stigning der på grund af apoptose må have været i caspaseenzymaktiviteten i de prolifererende zoner. Endvidere er det muligt, at metoderne til måling af aktiviteten ikke har været følsomme nok. Ifølge [Jilka 2007] kan en anden forklaring være, at caspaseenzymaktiviteten blev målt i ekstrakt fra lårbensmetafysen, se figur 15, som inkluderer både det primære og sekundære trabekulære væv. Da [Stanislaus et al. 2000] kun påviste apoptose af MSC, osteoblaster og osteocytter, i det primære trabekulære væv fra lårknoglen, kan det tænkes, at der i det sekundære væv ikke har været apoptose, eller ligefrem celleoverlevelse, hvorfor det ikke har været muligt at måle en stigning i caspaseaktiviteten. Denne forklaring lyder sandsynlig da [Jilka 2007] selv påviser antiapoptose i det sekundære trabekulære væv. Endelig næver [Stanislaus et al. 2000] at den øgede celleapoptose kan skyldes flere aktive remodellerings sites, hvorved flere celler vil bliver aktiveret og ligeledes dø. Det kan undre, at der hos [Jilka 2007] blev påvist et fald i osteoblastapoptose allerede efter to PTH-indsprøjtninger, hvorimod det hos [Stanislaus et al. 2000] blev påvist, at PTH s apoptotiske effekt på MSC, osteoblaster og osteocytter kunne måles indtil behandlingens 21. dag. Det skal dog igen påpeges, at [Stanislaus et al. 2000] påviste apoptose i det primære trabekulære væv i lårknoglen, hvorimod [Jilka 2007] målte antiapoptose i det sekundære væv, så det vides ikke om de to studier ville have fremkommet med samme resultater, hvis målinger af apoptose var foretaget i samme vævzone. Dette kunne være ønskeligt at undersøge for at se, om forskellige vævszoner udviser enten apoptose eller overlevelse af osteoblaster, eller om forskellen mellem de to studiers målinger opstår på grund af brug af forskellige forsøgsdyr. Det skal påpeges, at apoptose langt fra berører alle osteoblastiske celler, hvormed der stadig vil være aktive osteoblaster. Da det endvidere tyder på, at apoptose ikke finder sted i alle vævszoner, vil hovedparten af osteoblasterne ikke påvirkes. Endvidere sker celledelingen i voksne mus som [Jilka 2007] brugte i forsøget, ikke i samme grad som celledelingen i fire til fem uger gamle rotter som [Stanislaus et al. 2000] benytter. Derfor er det muligt at de modne osteoblaster har en længere levetid i [Jilka 2007], hvormed det er sandsynligt at en eventuel kort stigning i apoptose ikke vil påvirke knogleformationen, som steg umiddelbart efter indsprøjtning med PTH. Det kan 51
68 endvidere tænkes, at apoptose målt i de prolifererende zoner, kan opvejes af PTH s prolifererende og differentierende virkning på stromaceller, som det blandt andet ses i studier af [McCauley et al. 1997; Glenda et al. 2008], hvorved knogleformationen kan være stigende, på trods af en eventuel apoptose i nogle osteoblaster. [Jilka et al. 1999] lavede in vivo-forsøg hvor det blev undersøgt hvorvidt det øgede osteoblastantal efter PTH-behandling skyldtes en øget replikation af MSC eller overlevelse af osteoblaster. Her sås ingen påvirkning af PTH på MSC-replikationen, i forhold til mus behandlet med kontrolvehicle. Dette stemmer overens med resultaterne i [Dobnig & Turner 1995] selvom pågældende foreslog, at de nydannede osteoblaster stammede fra bone lining celler. Derimod modsiger resultatet direkte [Davies & Chambers 2004] s hypotese, om MSC der klæber sig fast til knogleoverfladen og danner kolonier. [Davies & Chambers 2004] undersøgte dog ikke antiapoptosehypotesen, hvilket ville have styrket deres argument. Den antiapoptotiske effekt af PTH er bredt undersøgt og mange studier er nået frem til denne konklusion [Bellido et al. 2003]; (Machwate et al. 1998; Parfitt 1990; Chen et al. 2002) om end med indbyrdes uenigheder omkring en opstartende stigning af apoptose i de prolifererende zoner som efterfølgende erstattes af overlevelse [Stanislaus et al. 2000]. PTH s antiapoptotiske virkning på osteoblaster kan under normale omstændigheder have til opgave at sørge for et øget antal osteoblaster til rådighed til at formerer knoglematrix, samt at stimulere osteoklastdifferentiering. Osteoklastdifferentieringen kan derfor ved impulsbehandling tænkes ikke at finde sted eller kun finde sted i mindre grad, da PTH hurtigt når at blive nedbrudt. Resultatet er overlevelse hos osteoblaster og dermed en øget knogleformation. 6.4 IGF-I er essentiel for parathyroideahormons anabolske virkning I studiet af [Miyakoshi et al. 2001] vises det in vitro og in vivo at IGF-I er vigtig i forhold til mediering af PTH s anabolske effekt. Dette blev blandt andet vist ud fra, at IGF-I knock out mus ikke øgede antallet af osteoblaster under behandling med PTH, hvorimod dette var tilfældet hos IGF-I knock out mus, som fik tilført IGF-I. Det at IGF-I skulle føre til et øget osteoblastantal underbygges af [Grey et al. 2003] og [Hill et al. 1997] samt [Canalis 1980], som viser at IGF-I stimulerer osteoblastproliferation og -antiapoptose. Det at IGF-I stimulerer antiapoptose stemmer overens med hypotesen om, at PTH s anabolske effekt skyldes osteoblastoverlevelse [Jilka 2007]. Undersøgelsen af [Dobning & Turner 1995] konkluderer at den knogleformation der ses efter PTH-behandling, ikke skyldes osteoblaster der stammer fra delende celler, men derimod at bone lining celler omdannes til osteoblaster. Dette er i modstrid med [Grey et al. 2003; Canalis 1980], 52
69 der konkluderer at IGF-I stimulerer proliferation. Dog forslår [Dobning & Turner 1995], at det er IGF-I der er med til at omdanne bone lining celler til osteoblaster, hvilket ikke kan udelukkes, da det ikke er modbevist, og da resultaterne af [Miyakoshi et al. 2001] viser et øget osteoblastantal ved påvirkning med IGF-I. [Davies & Chambers 2004] fremkommer med hypotesen at PTH s anabolske effekt skyldes MSC, der sætter sig på knogleoverfladen og danne kolonier, hvilket vil resultere i et øget antal osteoblaster. Dette stemmer overens med IGF-I s prolifererende effekt. Derudover ses der overensstemmelse i forhold til hypotesen om at c-fos bliver opreguleret af PTH, idet der i studiet af [Harold et al. 1990] konkluderes at IGF-I opregulerer udtrykket af c-fos i osteoblaster. Ydermere stemmer tiden for registeret c-fos-udtryk også godt overens i de tre studier af [Harold et al. 1990], [Lee et al.1994] og [McCauley et al. 1997], da der i disse sås et højt c-fos-niveau i osteoblaster ca minutter efter PTH-påvirkning og at udtrykket var næsten fuldstændig nedreguleret efter én time. Ud fra dette ses det, at tidsintervallerne for opregulering af c-fos, stemmer overens ved stimulering af PTH og IGF-I. Derfor tyder det på, at PTH stimulerer IGF-I, hvorefter c-fos bliver opreguleret. [Grigoriadis et al. 1995] skriver, at c- fos-udtrykket er størst under proliferering, og [Lee et al.1994] påviser, at c-fos registreres i stromaceller efter en halv til én hel time. Det kan derfor virke påfaldende at [Harold et al. 1990] måler, at IGF-I s stimulering af proliferationen først ses efter seks timer. Dette kan eventuelt skyldes, at IGF-I virker gennem flere signalveje. Studiet af [Miyakoshi et al. 2001] er udført med ikke fuldvoksne mus, og det pointeres på denne baggrund, at det ikke er klart om tilstedeværelsen af IGF-I til mediering af PTH s anabolske effekt, kun er krævet hos voksende mus, eller om det både gælder for voksende og fuldvoksne mus. Samlet set er IGF-I s rolle som en vigtig mediator for PTH s anabolske effekt godt underbygget, idet flere studier uafhængige af hinanden foreslår IGF-I som stimulator af en antiapoptotisk- eller prolifererende effekt. Der er endvidere studier, som ikke underbygger at IGF-I stimulerer disse effekter, men derimod foreslår at IGF-I s anabolske rolle ligger i at omdanne bone lining celler til osteoblaster. Dvs. at studierne der nævner IGF-I ikke er uenige i, at denne har en rolle i den anabolske effekt, men er uenige om hvilken rolle den spiller. Det kan ikke afvises at IGF-I kan indvirke på flere måder, for herved at påvirke både omdannelsen af bone lining celler, stimuleringen af antiapoptose og udøve en prolifererende effekt. Dog virker hypotesen om at IGF-I skulle indvirke på omdannelsen af bone lining celler til osteoblaseter mindre underbygget, da disse ikke direkte undersøger at IGF-I udøver denne effekt. 53
70 6.5 Parathyroideahormon opregulerer c-fos-udtrykket i knogleceller c-fos opreguleres i prolifererende og proteindannende celler. PTH s stimulering af c-fos i osteoblaster og stromaceller er derfor et udtryk for en øget matrixdannelse og en øget replikation af stromacellerne hvorfra osteoblasterne stammer. [McCauley et al. 1997] viste foruden c-fosopregulering i osteoblaster også, at denne opregulering var afhængig af camp, hvilket støtter at PKA-signalvejen er essentiel i PTH s anabolske virkning. I [Lee et al. 1994] som bruges til at underbygge samt udbygge [McCauley et al. 1997] s resultater, ses c-fos mrna-udtryk i osteoblaster efter 15 minutter, samt i mindre grad i stromaceller efter en halv time. Efter én time sås udtrykket i størstedelen af stromaceller og efter to timer i osteoklasterne. [Lee et al. 1994] fandt desuden ikke noget PTHr1-udtryk hos størstedelen af stromacellerne. Dette må betyde, at osteoblasterne efter c-fos-udtryk starter en produktion af knoglematrix, samt udskiller faktorer som stimulerer videre differentiering af omgivende stromaceller, hvilket kan være årsagen til den senere opregulering af c-fos i stromaceller. Det, at der allerede efter en halv time ses et c-fosudtryk i stromaceller, kan muligvis forklares ved, at de faktorer osteoblasterne udskiller for at aktivere differentieringen af stromacellerne sker lidt hurtigere end aktiveringen af osteoklastdifferentieringen gennem RANKL. Mere sandsynligt er det dog, som [Lee et al. 1994] selv påpeger, at opreguleringen skyldes næsten færdigdifferentierede celler som udtrykker PTHr1, og herved kan cellerne stimuleres direkte af PTH til at differentierer færdig og starte matrixdannelse. c-fos-udtrykket ses, som tidligere nævnt, først opreguleret efter to timer hos osteoklaster.. Osteoklasternes opregulering af c-fos skyldes derfor sandsynligvis indirekte påvirkning af PTH gennem osteoblasterne. Dette støttes desuden af det faktum, at der ikke sås noget PTHr1-udtryk på hverken osteoklasterne, hvilket [Schwarz 2005] også understøtter. Osteoblasterne aktiveres og udtrykker efterfølgende RANKL som fører til differentiering af osteoklastforstadierne via RANK. De aktive osteoklaster opregulerer herefter c-fos, som afspejler produktionen af proteolytiske enzymer, der resorberer knoglevæv. Det er derfor muligt, at ingen, eller ikke alle osteoblaster når at udtrykke RANKL ved PTH-impulsbehandling, da dennes halveringstid i kroppen er kort, hvorved PTH hurtigt vil blive nedbrudt. Da [Lee et al. 1994] s forsøg viste, at c- fos-opreguleringen skete tidligt i både osteoblaster og stromaceller, er det sandsynligt at disse når at påvirkes til henholdsvis matrixproduktion, proliferering og differentiering inden PTH nedbrydes. Hvis PTH ved impulsbehandling når at aktivere differentieringen af en del af 54
71 osteoklasterne, og disse påbegynder resorptionen, vil denne ikke kunne fortsætte efter nedbrydningen af PTH, da denne kræver en konstant tilstedeværelse og aktivering fra PTH. Herved vil der være en nettoformation, da osteoklasternes nedbrydning ikke varer ved. Dette fænomen forudsiges af [Komarova 2005] som udarbejdede den omtalte matematiske model, se afsnit 5.7 Når impulsgivet parathyriodeahormon griber ind i remodelleringen overkompenserer osteoblaster. Det at c-fos er vigtig for PTH s anabolske virkning ved impulsbehandling, støttes af, at c-fos knock out mus udvikler både osteoporose og mangel på osteoklaster. Denne mangel på osteoklaster kan skyldes den relative mangel på osteoblaster til at stimulere osteoklastdifferentiering. Det skal dog nævnes, at den naturlige udskillelse af PTH naturligvis stadig vil resultere i osteoblaster som kan udføre dette, og derfor vil osteoklastdannelse altid forekomme. [McCauley et al.1997] viser, at den øgede knogleformation efter PTH-behandling til dels skyldes øget replikation af stromaceller. Dette modsiger forsøget lavet af [Dobnig & Turner 1995] som viste at de nydannede osteoblaster efter behandling med PTH, ikke skyldtes celler som havde undergået mitose. Dette kan eventuelt forklares med, at den første knogleformation der sker efter PTH-behandling ifølge [Lee et al. 1994] skyldes c-fos-opregulering i modne osteoblaster, som efterfølgende starter med at danne matrix. Det stigende antal osteoblaster der sås i [Dobnig & Turner 1995] kunne desuden skyldes de få stromaceller, der er næsten færdigdifferentierede og besidder PTHr1 som aktiveres efter en halv time. Derfor er disse to studier ikke nødvendigvis modstridende selvom [Dobnig & Turner 1995] fremkommer med en anden, ikke efterprøvet hypotese, om at lining celler under PTH-behandling omdannes til osteoblaster. 6.6 Når impulsgivet PTH griber ind i remodelleringen overkompenserer osteblaster I forsøget udført af [Komarova 2005] benyttes en matematisk model til at beskrive PTH s generelle mekanismer omkring knogleresorption og -formation. Dog kan det være et problem at forsøget kun bygger på en matematisk model, og at den fremstillede hypotese ikke eftervises ved in vitro eller in vivo-forsøg. Denne type forsøg ville kunne bevise, at den matematiske model afspejler, hvad der sker i organismer, selvom den er simplificeret. Det kan nemlig diskuteres om 55
72 en sådan simplificeret model alene vil være i stand til at forklarer den komplekse proces som knogleremodellering er. [Komarova 2005] udtrykker selv, at det har været nødvendigt at foretage en række antagelser som har forsimplet modellen. Blandt andet er der kun taget højde for to celletyper osteoblaster og osteoklaster, men i remodelleringen findes også celletyper såsom osteocytter og bone lining celler, og når modellen skal efterligne kroppens egne processer, er det muligvis nødvendigt at inddrage alle de bidragende mekanismer. [Komarova 2005] s model er opbygget efter populationsøkologiske differentialeligninger, hvor der er taget højde for det, som [Komarova 2005] har set som hovedpointerne: Remodelleringen er en koblet proces mellem resorption og formation, der sker ved hjælp af henholdsvis osteoklaster og osteoblaster, og disse påvirkes yderligere af lokale faktorer. Dette er i overensstemmelse med teoriafsnit Osteoklastogenese, som viser det samme billede, så det kan tænkes, at modellen er så grundlæggende, at den kan give et overordnet billede af virkeligheden, og herigennem forklarer PTH s generelle mekanismer. Modellen viser et tydeligt billede af, at det er en del af PTH s sædvanlige signalvej, der kan resultere i knogleanabolisme ved impulsbehandling. Dette stemmer derfor fint overens med hvorledes PTH må fungere normalt som regulator for kroppens calciumbalance. Osteoklaster må nødvendigvis nedsætte knogleresorptionen når calciumniveauet er i balance og PTH-udskillelsen sættes ned. Dette kan ske ved reducering af osteoklastantal og disses aktive sites. Derfor igangsættes PTH s normale signalvej ved impulsbehandling hvor det kan tænkes at enten ingen, eller få osteoklaster stimuleres til resorption, og osteoblastcellelinier stimuleres til proliferering og differentiering. Da PTH nedbrydes kortvarigt efter injektion, påpeger [Komarova 2005] at den reducerede PTH-stimulering af de resorptive osteoklaster får disse til at fjerne sig. På denne måde resulterer impulsbehandlingen i både osteoklastresorption og en hurtig fjernelse af disse. [Komarova 2005] forklarer dog ikke grunden til at osteoklasterne skulle fjerne sig efter nedbrydning af PTH, men det kunne tænkes at osteoblasterne eller den frigjorte matrix udskiller faktorer, som stimulerer osteoklasterne til apoptose eller fjernelse til et andet aktivt site. Det kunne desuden tænkes at hvis PTHr1 findes på osteoklaster, hvilket der hersker tvivl om, påvirkes disse direkte af PTH, og undergår dermed apoptose eller fjerne sig til et andet site, når PTH nedbrydes. Det kan dog også tænkes at [Komarova 2005] ikke mener reel fjernelse af osteoklaster, men at det ekstra PTH-stimuli, som impulsbehandlingen giver, vil forsvinde ved nedbrydning. Den oprindelige virkning af det normale PTH-niveau vil derefter være det eneste stimuli til osteoklasterne, og disse vil derfor sætte deres aktivitetsniveau ned til det normale. Da osteoblasterne allerede er blevet fuldt stimuleret, vil de fortsætte deres opgave og dermed overkompensere. 56
73 Ifølge [Lee et al. 1994] opreguleres c-fos i stromaceller efter en halv til én time og derfor kan det tænkes, at en del af stromacellerne desuden når at blive stimuleret til proliferering og differentiering. Dette kunne også bidrage til en øgning af knogleformationen. Proliferering inddrages ikke i [Komarova 2005] s konklusionen, hvilket umiddelbart kan virke påfaldende, da dette medtages som en faktor for stigning i antallet af osteoblaster og osteoklaster i den matematiske model. Endvidere er det sandsynligt at PTH stimulerer antiapoptose i osteoblaster som det blandt andet foreslås af [Jilka 2007] og [Stanislaus et al. 2000]. [Komarova 2005] antager at det er allerede aktive osteoklaster, der bliver stimuleret til yderligere resorption, og ikke at det er nydannede osteoklaster, fremkommet af PTH-impulsbehandling. I kraft af at resorption går forud for formation, og at [Komarova 2005] ser resorption umiddelbart efter en PTH-behandlings start, skal der ske en hurtig stimulering af osteoklaster. Det ville være en tidsmæssigt krævende proces hvis PTH s stimulering skulle nå igennem osteoblasterne for herved at aktivere osteoklastforstadierne til differentiering, modning og hermed resorption. Det kunne altså tyde på, at osteoklaster stimuleres direkte af PTH. Dette kunne f.eks. være i kraft af PTHr1, men da der som før nævnt hersker tvivl om hvorvidt disse eksisterer på osteoklaster, kunne det også tænkes at stimuleringen foregår indirekte igennem osteoblaster. Disse kunne f.eks. udskille faktorer, der stimulerede modne osteoklaster til yderligere resorption. Den direkte osteoklaststimuleringen kan ifølge [Lee et al. 1994] ikke forekomme, da studiet ikke påviser PTHr1 på osteoklaster. Ydermere blev et opreguleret c-fos-udtryk i både aktive og nydifferentierede osteoklaster efter to timer fundet. Derfor kan direkte PTH aktivering ikke forekomme, da c-fos i dette tilfælde burde være opreguleret i de allerede resorptive osteoklaster umiddelbart efter PTH injektion, hvilket ikke sås. Der vil på alle tidspunkter være flere aktive remodellerings sites for knogleformation end for knogleresorption, da knogleresorption tager tre uger og -formationen tager tre måneder. Impulsbehandling med PTH vil aktivere flere osteoblaster end osteoklaster, og remodellerings sites for knogleformation er som sagt i overtal, derfor vil nettoresultatet være mere knoglevæv. På denne måde viser det sig altså, at PTH har et kort tidsrum mellem injektion og nedbrydning, hvor det igangsætter anabolske signalveje. 57
74 6.7 Opsamling af hypoteser Forskning i PTH s anabolske virkning har resulteret i mange vidt forskellige hypoteser, men ingen virker til at kunne forklare det fulde billede af PTH s anabolske effekt. Dog er det relevant for forståelsen af PTH som behandling at samle udvalgte hypoteser og finde de punkter, hvor disse understøtter hinanden eller viser det samme overordnede billede. [Komarova 2005] har vist, at PTH s anabolske effekt opstår som en del af remodellering, men at kroppen under normale betingelser opretholder balancen mellem knogleformation og resorption, så skelettet bevares. Gives PTH som impulsbehandling, kan det tænkes, at alle de normale mekanismer i PTH s signalvej til remodellering, ikke når at blive aktiveret, grundet PTH s korte halveringstid. Derfor er det sandsynligt, at der opstår et tidsrum, hvor osteoblaster kan overkompensere for osteoklaster, hvilket betegnes det anabole vindue. Hovedparten af de hypoteser, der hidtil er opstillet om PTH s anabolske effekt, kan siges at bygge på den betingelse, at PTH igangsætter signalveje som forårsager en knogleanabolsk virkning indenfor den tid, hvor det anabole vindue finder sted. Undersøgelser af hypotesen omhandlende c-fos-opregulering, udført af blandt andet [Lee et al. 1994] viser, at PTH opregulerer c-fos i modne osteoblaster efter minutter, som herved igangsætter matrixproduktion. Desuden er det sandsynligt at PTH når at opregulere c-fos i stromaceller, da denne opregulering sker efter 30 minutter. Dette kan rimeligvis resultere i øget proliferering og/eller differentiering af disse og derved nydannede osteoblaster. Først efter to timer opreguleres c-fos i osteoklaster. Da PTH s halveringstid som sagt er fem minutter, og derfor må nedbrydes hurtigt i kroppen, når størstedelen af osteoklaster muligvis ikke at opregulere c-fos, når PTH gives som impulsbehandling. Dette giver et afgrænset tidsinterval, hvor PTH s stimulerende effekt på osteoblaster resulterer i knogleformation, hvilket stemmer godt overens med forestillingen om det anabole vindue. Hypotesen omhandlende bone lining cellers omdannelse til osteoblaster under påvirkning af PTH, kan også siges at give en anabolsk virkning indenfor et kort tidsinterval. Ved kontinuerligt tilført PTH vil hormonet være til stede i kroppen i tilstrækkelig lang tid til, at aktiverede osteoblaster vil nå at færdiggøre osteoklastdifferentiering. Herved har PTH ikke den ønskede nettoanabolske effekt. Hvis dette sidste trin ikke når at ske ved impulsbehandling med PTH, kan nævnte hypotese støtte forestillingen om det anabole vindue. Hypotesen om, at MSC danner kolonier på knogleoverflader under påvirkning af PTH, kan på samme måde tænkes at resultere i knogleformation. Dette sker når kolonien vil begynde at 58
75 differentieres til modne osteoblaster på knogleoverfladen, hvorved knogleformation kan påbegynde. Også i dette tilfælde kan det tænkes, at disse osteoblaster ikke når at opregulere RANKL og derved differentiere osteoklaster, hvilket også understøtter forestillingen om det anabole vindue. Det samme gør sig gældende for antiapoptosehypotesen, hvor en forlængelse af osteoblasters levetid vil føre til flere matrix-dannende osteoblaster og dermed til yderligere knogleformation ved impulsbehandling med PTH. Ved kontinuerlig påvirkning af PTH, som det sker naturligt i kroppen, vil disse osteoblaster endvidere stimulere osteoklastdifferentiering, hvorved PTH ikke vil have den ønskede nettoknogleformative effekt. I hypotesen der tager udgangspunkt i en matematisk model, blev det fundet, at PTH ved impulsbehandling stimulerer osteoblaster til at overkompensere for osteoklasternes resorption. Dette sker fordi osteoklastaktiviteten kræver en konstant tilstedeværelsen af PTH. Det er denne mekanisme, som gør hormonet til en effektiv regulator for serum calciumniveauet. Når PTH nedbrydes kort efter injektion, trækker en del af osteoklasternes sig tilbage, hvorefter de allerede stimulerede osteoblaster kan tage over og danne mere knoglevæv, end der resorberes af osteoklasterne. Dette giver en nettoknogleformativ effekt i det tidsrum, hvor PTH virker og igangsætter anabolske signalveje, hvilket kan ses som det anabole vindue. Hypoteserne omkring IGF-I og PKA-signalvejen som centrale faktorer for PTH s anabolske virkning, kan ikke på samme måde sættes i forbindelse med det anabole vindue. Dette skyldes, at der i disse hypoteser ikke nævnes en decideret mekanisme, som kan forklare hvordan PTH kan virke anabolsk ved impulsbehandling. IGF-I er dog blevet sat i forbindelse med både proliferering og antiapoptose af osteoblastiske celler som ovenstående er forklaret i forhold til det anabole vindue. Dog viser det sig at IGF-I først stimulerer proliferering efter 6 timer, hvilket ikke helt passer ind i det tidsrum hvor PTH virker anabolsk. Det er dog sandsynligt, at dette kan være et forsinket respons igangsat af PTH, hvorfor dette alligevel kan passe ind i det anabole vindue. Desuden er det blevet forslået, at IGF-I spiller en rolle i omdannelsen af bone lining celler til osteoblaster, og at vækstfaktoren ligeledes opregulerer c-fos-udtrykket i osteoblastiske celler. IGF-I er altså ikke en mekanisme i sig selv, men kan virke som et led i de allerede omtalte hypoteser. Det samme gælder for PKA-signalvejen, som er vist at mediere c-fos-udtrykket i osteoblaster og herigennem kan indgå i det anabole vindue. At camp/pka-signalvejen er nødvendig for PTH s anabolske virkning, er veletableret. Dog ligger ikke alle signalveje tilknyttet PKA fuldstændig fast, i forhold til den anabolske virkning af PTH ved impulsbehandling. Figur 18 viser en oversigt over de forskellige hypoteser for PTH s knogleanabolske virkning 59
76 Figur 18: Viser en oversigt over de forskellige hypoteser for PTH s anabolske virkning på knoglerne. Figuren indeholder 1) PKA-signalvejen, 2) c-fos-opregulering, 3) osteoklaster trækker sig tilbage og osteoblaster overkompenserer, 4) bone lining celler omdannes til osteoblaster, 5) MSC danner kolonier på knogleoverfladen, 6) osteoblastantiapoptose, 7) IGF-I er essentiel for PTH s anabolske virkning. Se figur under de respektive hypoteseafsnit [Jørgensen 2008]. 6.8 Det anabole vindue I nedenstående afsnit vil PTH s anabole vindue beskrives som en generel hypotese, hvor de grundlæggende mekanismer for PTH s anabolske virkning forklares. Dette gøres for at give et overordnet og samlet billede af de undersøgte hypoteser. I forklaringen på PTH s effekt har forsøg ofte vist, at der ved impulsbehandling sker en hurtig stimulering af osteoblaster. Da osteoblasternes opgave, udover knogleformation, er at aktivere osteoklastforstadier, så disse kan udvikles til modne osteoklaster, vil det forventes at osteoklasterdifferentieringen ligeledes bliver stimuleret af PTH. Dog resulterer impulsbehandling med PTH i, at nedbrydningen sker før osteoblasterne når at opregulere RANKL eller, at 60
77 osteoblasterne kun når at aktivere osteoklasterne i mindre grad. Herved når differentiering af osteoklastforstadier ikke at ske, eller kun at ske i mindre grad. Der er nogle uoverensstemmelser omkring, hvorvidt osteoklaster udtrykker PTH-receptorer, og herved om det er muligt, at der kan ske en direkte PTH-aktivering af modne osteoklaster til at resorbere knoglevæv eller om denne aktivering udelukkende sker gennem osteoblaster. Aktiveringen gennem osteoblaster kan både ske gennem RANKL eller ved at osteoblaster udskiller faktorer der direkte stimulerer modne osteoklaster til resorption. Hvis osteoklasterne stimuleres direkte, vil dette sandsynligvis ske umilddelbart efter PTH-injektion. Da PTH hurtigt bliver nedbrudt i kroppen, og når hormonet fås i bestemte daglige doser, viser det sig, at lige så snart PTH nedbrydes, nedsætter antallet af resorptive osteoklaster. Denne mekanisme er essentiel for kroppen, da PTH som før nævnt regulerer calciumniveauet i blodet. Hvis ikke osteoklaster hurtigt reagerer, når PTH bliver nedbrudt, vil PTH være ubrugelig som reguleringsfaktor. Da der, som før nævnt, er ca. fire gange flere aktive sites hvor der sker formation end resorption, og da nogle af osteoklasterne nedsætter eller stopper resorptionen efter PTH nedbrydes, fremkommer en nettoknogleformation. PTH påvirker MSC og stromaceller til proliferering og differentiering, hvorefter knogleformationen påbegyndes, umiddelbart efter osteoklaster stopper med at resorbere og fjerner sig. Det tidsrum hvor PTH virker anabolsk, kaldes som sagt PTH s anabole vindue og den nettoknogleanabolske effekt skal ses som en proces der finder sted mange steder på skelettet og ikke kun ved ét site. Figur 19 viser koncentrationen af PTH som funktion af tiden efter injektion, hvor PTH når sin maksimale koncentration og hermed sit maksimale anabolske respons. Det kan derfor siges at det anabole vindue ligger indenfor et tidsinterval på ca. to timer, hvor PTH både når sin makimale koncentration og stort set nedbrydes, hvorefter PTH-koncentrationen igen når kroppens normale niveau. Figur 19: Koncentrationen af PTH som funktion af tid efter injektion [Schwarz 2005, redigeret af Jørgensen 2008]. 61
78 62
79 7. Konklusion Nærværende projekt fandt, at PTH s anabolske effekt ikke entydigt kan forklares ud fra enkelte hypoteser, men opstår på baggrund af et netværk af signalveje og mekanismer, hvoraf størstedelen kan sættes direkte i forbindelse med det anabole vindue. Nogle hypoteser virker dog bedre underbygget end andre, hvoraf kan nævnes PTH s stimulerende effekt på forlænget levetiden af osteoblaster. Desuden virker det veldokumenteret, at c-fos-opregulering er essentiel for PTH s anabolske virkning, og at denne opregulering resulterer i øget dannelse af knoglematrix samt differentiering og proliferering af stromaceller. Impulsgivet PTH virker i et kort tidsinterval, da PTH s halveringstid i kroppen er kort. Hermed kan det tænkes, at osteoblaster ikke når at opregulere RANKL eller udtrykker denne i mindre grad. Dette bevirker, at osteoklastforstadier enten ikke når at modtage stimuli til differentiering eller, at dette sker i mindre grad, hvorfor knogleresorption ikke aktiveres yderligere eller vil være nedsat i forhold til -formation. PTH påvirker til knogleformation og -resorption af henholdsvis modne osteoblaster og osteoklaster. Da der er flere aktive sites hvor der foregår formation end hvor der sker resorption og da osteoblasterne, som ovenover beskrevet, overkompenserer, vil impulsgivet PTH have en nettoknogleformativ effekt. De præcise mekanismer bag PTH s anabolske virkning mangler dog stadig at blive fuldstændigt klarlagt. 63
80 8. Perspektivering Forskning omkring PTH s anabolske virkning er stadig et nyt og interessant forskningsområde, hvor der endnu mangles at klarlægge de præcise mekanismer, der ligger til grund for denne virkning. Det er vigtigt at forstår mekanismerne bag knogleremodellering og PTH for at fremkomme med en optimal behandlingsform for osteoporosepatienter. Forskere har på nuværende tidspunkt forskellige hypoteser for PTH s anabolske effekt, alle fremkommet ud fra forsøg. Nogle af resultater stemmer overens, mens andre direkte modsiger hinanden, som det f.eks. er tilfældet med bone lining celler som skulle omdannes til osteoblaster, og MSC som skulle klæbes til knogleoverfladen og prolifererer. Det er ønskeligt at videre forskning inden for feltet undersøger flere hypoteser samtidig, så der kan drages konklusioner, der ikke er fremkommet på baggrund af, hvad forskningsresultaterne udelukker eller henvisninger til andre undersøgelsers resultater, men på baggrund af direkte påvisninger. Med hensyn til hypotesen om bone lining cellers omdannelse til aktive osteoblaster, fremkom denne netop på baggrund af, at PTH s anabolske effekt vises ikke at skyldes delende celler. Det vil sige at pågældende studie ikke selv påviser at lining celler omdannes til osteoblaster, hvorfor de konklusioner der er draget ud fra dette studie kan betvivles. Det kunne f.eks. være væsentligt at undersøge både antiapoptose og proliferering i samme forsøg. Hvis det metodisk er muligt kunne begge hypoteser undersøges in vivo, hvormed det ville kunne påvises hvorvidt knogleformationen skyldes antiapoptose, proliferering af celler eller begge dele. Studier hvor flere faktorer medtages i samme undersøgelse, vil hermed kunne komme tættere på en klarlægning af mekanismerne bag PTH s anabolske virkning. Da PTH stimulerer en bred vifte af signalveje, og da alle mekanismer bag disse signalveje endnu ikke er fastlagt, er PTH højst sandsynligt i stand til at regulere flere signalveje end de i projektet omtalte. Det har netop vist sig at PTH udfører en knogleanabolsk virkning i samarbejde med mekanisk stress, hvor der med mekanisk stress menes fysisk aktivitet. Denne opdagelse har gjort PTH til en endnu mere vidtrækkende regulator end det var forventet. Et studie af (Frost 1987) viste at der ved mekanisk stimulering fandtes et form for tærskelsystem. Dette tærskelsystem betød at lave niveauer af mekanisk stress ikke kunne opretholde knogleformationen, og at voldsomt høje niveauer skadede knoglevæv. Dog fandtes der et mellemniveau af mekanisk stress, der kunne opretholde knogleformation [Ryder & Duncan 2000; (Frost 1987)]. (Frost 1987) mente desuden at der måtte findes faktorer, som hormoner vækstfaktorer og cytokiner, der kunne ændre disse tærskelsystemer [Ma et al. 1999; (Frost 1987)]. Ved hjælp af flere studier, hvoraf kan nævnes [Ma et al. 1999] og [Chow et al. 1998], blev PTH fastslået som en af de faktorer, der kan 64
81 sænke niveauet af påkrævet mekanisk stress for at opnå en anabolsk effekt på knoglevævet. Forholdet og mekanismer bag PTH og mekanisk stress er endnu ikke fastlagt. Flere teorier er fremkommet, men dette samspil kræver endnu yderligere forskning, så også denne viden kan udnyttes i behandlingen af osteoporose. I forbindelse med behandling af osteoporose findes der andre behandlingstyper end PTH, som er interessante at udforske nærmere. Det monoklonale antistof, denosumab, er under udvikling i kliniske forsøg. Antistoffet binder sig til RANKL med stor specificitet og affinitet og forhindrer derved differentieringen af osteoklaster [Westenfeld et al. 2006], og på denne måde efterlignes OPG [International Osteoporosis Foundation 2008]. Midlet tages som indsprøjtning, ikke i form af impulsbehandling, men med flere måneders mellemrum [Osteopenia 2008]. Netop af denne årsag er det et enklere alternativ til PTH, hvis midlet er så effektivt som det antages at være [Loprinzi 2007]. Langtidseffekten af denosumab kræver dog nærmere undersøgelser, da RANKL også er involveret i immunforsvaret [Medical News 2008]. Som ovenstående beskriver, sker der stadig en udvikling i behandlingen af osteoporose, både i forbindelse med forståelse af PTH s mekanismer og andre behandlingsformer, da osteoporosebehandlingen, både praktisk og økonomisk, stadig kan optimeres. 65
82 9. Litteraturliste Abrahamsen, B., H. A. Sørensen, B. Rud, A. P. Hermann, J. E. B. Jensen, C. Mølgaard, O. H. Sørensen (2005): Normalområder og kvalitetskontrol for dual energy X-ray absorptiometryskanning. Ugeskr. Læger 167(08): 878 Adam J. S., & B. P. Lukert (1999): Osteoporosis: genetics, prevention and Treatment. Academic publishers, Boston. Andreasen J., L. Christensen, R. Siggaard, P. T. Sørensen, D. Halkjær, A.Weimar (2005): Knogleskørhed fakta og forebyggelse. Sundhedsstyrelsen, Center for Forebyggelse, København. Answers (2008): Haversian system. (på internettet den ). Arai F., T. Miyamoto, O. Ohneda, T. Inada, T. Sudo, K. Brasel, T. Miyata, D. M. Anderson og T. Suda (1999): Commitment and Differentiation of Osteoclast Precursor Cells by the Sequential Expression of c-fms and Receptor Activator of Nuclear FactorkB (RANK) Receptors. J Exp. Med. 190(12): Bellido, T., A. A. Ali, L. I. Plotkin, Q. Fu, I. Gubrij, P. K. Roberson, R. S. Weinstein, C. A. O Brien, S. C. Manolagas og R. L Jilka (2003): Proteasomal degradation of Runx2 shortens parathyroid hormone-induced anti-apoptotic signaling in osteoblasts: a putative explanation for why intermittent administration is needed for bone anabolism. J Biol Chem 278: Brändström, H., K. B. Jonsson, C. Ohlsson, O. Vidal, S. Ljunghall og O. Ljunggren (1998): Regulation of osteoprotegerin mrna levels by prostaglandin E2 in human bone marrow stroma cells. Biochem. Biophys. Res. Commun. 247(2): Caffrey, J. M. and M. C. Farach-Carson (1989): Vitamin D3 Metabolites Modulate Dihydropyridine-sensitive Calcium Currents in Clonal Rat Osteosarcoma Cells. J Biol. Chem. 264(34):
83 Canalis, E. (1980): Effect of Insulinlike Growth Factor I on DNA and Protein Synthesis in Cultured Rat Calvaria. J. Clin. Invest. 66: Cao, Z., J. Xiong, M. Takeuchi, T. Kurama og D. V. Goeddel (1996): TRAF6 is a signal transducer for interleukin-1. Nature 383(6599): Chase, L. R. & G. D. Aurbach (1970): The Effect of Parathyroid Hormone on the Concentration of Adenosine 3, 5 -Monophosphate in Skeletal Tissue in Vitro. J. Biol. Chem. 245(7): Chen, L., J. N. Glover, P. G. Hogan, A. Rao og S. C. Harrison (1998): Structure of the DNAbinding domains from NFAT, Fos and Jun bound specifically to DNA. Nature 392(6671): 42-8 Chow, J. W. M., S. Fox, C. J. Jagger og T. J. Chambers (1998): Role for parathyroid hormone in mechanical responsiveness of rat bone. Am. J Physiol Endocrinol Metab. 274: Compston, J. & E. Shane, (red.) (2005): Bone Disease of Organ Transplantation (1. udgave) Elsevier Academic Press, San Diego, California. Conover, CA (2000): Insulin-like growth factors and the skeleton. In: Canalis E, editor. Skeletal growth factors. Philadelphia: Lippincott Williams & Wilkins: side Cosman, F., (2006): PTH Treatment for Osteoporosis. American Society for Bone and Mineral Research Cranney, A., A. Papaioannou, N. Zytaruk, D. Hanley, J. Adachi, D. Goltzman, T. Murray, A. Hodsman (2006): Parathyroid hormone for the treatment of osteoporosis: a systematic review CMAJ. 175(1): Crotti, T. N., M. Flannery, N. C. Walsh, J. D. Fleming, S. R. Goldring og K. P. Mc Hugh (2006): NFATc1 regulation of the human beta3 integrin promoter in osteoclast differentiation. Gene. 372:
84 Curtis, N. E., R. J. Thomas, M. T. Gillespie, R. G. King, G. E Rice, M. E. Wlodek (1998): Parathyroid hormone-related protein (PTHrP) mrna splicing and parathyroid hormone/pthrp receptor mrna expression in human placenta and fetal membranes. J. Molecular Endocrinology. 21(2): Davies, J., T. J. Chambers (2004): Parathyroid hormone activates adhesion in marrow stromal precurser cells. J. Endocrinology. 180(3): Delmas, P. D., P.Vergnaud, M.E. Arlot, P. Pastoureau, P.J. Meunier og M.H. Nilssen (1995): The anabolic effect of human PTH(1-34) on bone formation is blunted when bone resorption is inhibited by the bisphosphonate tiludronate is activated resorption a prerequisite for the in vivo effect of PTH on formation in a remodeling system? Bone. 16: Diernæs, M. & S. E. Nørholt (2006): Bisphosphonatassocieret osteonekrose: et nyt fænomen. Tandlægebladet 12: Dobnig, H. & R. T. Turner (1995): Evidence that intermittent treatment with parathyroid hormone increases bone formation in adult rats by activation of bone lining celler. Endocrinology. 136: Dempster, D. W, C. E. Hughes-Begos, K. Plavetic-Chee, A. Brandao-Burch, F. Cosman, J. Nieves, S. Neubort, S. S. Lu, A. Iida-Klein,. Arnett, og R. Lindsay (2005): Normal Human Osteoclasts Formed From Peripheral Blood Monocytes Express PTH Type 1 Receptors and Are Stimulated by PTH in the Absence of Osteoblasts. Journal of Cellular Biochemistry. 95: Dsgnet helse i Bio Referencer (2008): Biskjoldbruskkirtelhormon. (på internettet den ). Eferl R & E. F. Wagner (2003): AP-1: a double-edged sword in tumorigenesis. Nat Rev Cancer 3(11): Bowler, W. B., K. A. Buckley, A. Gartland, R. A. Hipskind, G. Bilbe og J. A. Gallagher (2001): Extracellular Nucleotide Signaling: A Mechanism for Integrating Local and Systemic Responses 68
85 in the Activation of Bone Remodeling. Bone, 28: Ernst, M., E. R. Froesch (1988): Growth hormone dependent stimulation of osteoblast- like cells in serum-free cultures via local synthesis of insulin-like growth factor I. Biochem Biophys Res Commun. 151: Frederiksberghospital (2008b): Osteoporose diagnostik og behandling. [ på internettet den ). Friedenstein, A. J., K. V. Petrakova, A. I. Kurolesova og G. P. Frolova (1968): Heterotopic transplants of bone marrow. Analysis of precurser cells for osteogenic and hematopoietic tissues. Transplantation. 6: Frost, H. M. (1987): The machanostat: a proposed pathogenic mechanism of osteoporoses and the bone mass effect of mechanical and non-mechanical agents. Bone Miner. 2(2): Frisch, S. M. & E. Ruoslahti (1997): Integrins and anoikis. Curr Opin Cell Biol. 9: Galibert L., M. E. Tometsko, D. M. Anderson, D. Cosman og W. C. Dougall (1998): The Involvement of Multiple Tumor Necrosis Factor Receptor (TNFR)-associated Factors in the Signaling Mechanisms of Receptor Activator of NF-kB, a Member of the TNFR Superfamily. J Biol Chem. 273(51): Garg, K. A. (2004): BONE biology, Harvesting, Grafting for Dental Implants Rationale and Clinical Applications (1. udgave). Quintessence Publishing Co, Inc, Kimberly Drive, Carol Stream. Gohda, J., T. Akiyama, T. Koga, H. Takayanagi, S. Tanaka og J. Inoue (2005): RANK-mediated amplification of TRAF6 signaling leads to NFATc1 induction during osteoclastogenesis. EMBO J. 24(4):
86 Gray, T. K., S. Mohan, T. A. Linkhart og D. J. Baylink (1989): Estradiol stimulates in vitro the secretion of insulin-like growth factors by the clonal osteoblastic cell line, UMR106. Biochem Biophys Res Commun 158: Grey, A, Q. Chen, X. Xu, K. Callon og J. Cornish (2003): Parallel Phosphatidylinositol-3 Kinase and p42/44 Mitogen-Activated Protein Kinase Signaling Pathways Subserve the Mitogenic and Antiapoptotic Actions of Insulin-Like Growth Factor I in Osteoblastic Cells. Endocrinology. 144(11): Glenda, J. P., J. A. Meganck, A. J. Koh, E. T. Keller, S. A. Goldstein og L. K McCauley (2008): Parathyroid hormone mediates bone growht through the regulation of osteoblast proliferation and differentiation. Bone. 42: Grigoriadis, A. E., Z. Wang og E. F. Wagner (1995): Fos and bone cell development: lessons from a nuclear oncogene. Elsevier Science Ltd: 11(11): Haussler, M. R & H. Rasmussen (1972): The Metabolism of Vitamin D3 in the Chick. J Biol Chem. 247(8): Henderson, J. E. & D. Goltzman (red.) (2000): The osteoporosis primer (1. udgave). Cambridge University Press, United Kingdom. Hill, P. A., A. Tumbler og M. C. Meikle (1997): Multiple Extracellular Signals Promote Osteoblast Survival and Apoptosis. Endocrinology. 138(9): Hodsman, A. B., D. A. Hanley, P. H. Watson og L. J. Fraher (2002): Parathyroid Hormone, side I Principles of Bone Biology, Bilezikian, J.P., L. G. Raisz og G.A. Rodan (red.), Academic Press. Huang, J. C., T. Sukata, L. L. Pfleger, M. Bencsik, B. P. Halloran, D. D. Bikle og R. A. Nissenson (2004): PTH Differentially Regulates Expression of RANKL and OPG. J Bone Miner Res 19(2):
87 International Osteoporosis Foundation (2008): Denosumab. (på internettet den ). Jilka, L. R. (2007): Molecular and Cellular Mechanisms of the Anabolic Effekt of Intermittent PTH. Bone. 40(6): Jilka, R. L., R. S. Weinstein, T. Bellido, P. Roberson, A. M. Parfitt og S. C. Manolagas (1999): Increased bone formation by prevention of osteoblast apoptosis with parathyroid hormone. The Journal of clinical investigation, 104(4): Jimi, E., I. Nakamura, H. Amano, Y. Taguchi, T. Tsurukai, M. Tamura, N. Takahashi og T. Suda (1996): Osteoclast function is activated by osteoblastic cells through a mechanism involving cellto-cell contact. Endocrinology 137(8): Jimi, E., I. Nakamura, L. T. Duong, T. Ikebe, N. Takahashi, G. A. Rodan og T. Suda (1999): Interleukin 1 Induces Multinucleation and Bone-Resorbing Activity of Osteoclasts in the Absence of Osteoblasts/Stromal Cells. Exp Cell Res. 247(1): Jimi, E., T. Shuto & T. Koga (1995): Macrophage Colony-Stimulating Factor and Interleukin-1α maintain the survival of osteoclast-like cells. Endocrinology 136(2): Johnson, R.S., V. M. Spiegelman, og V. Papaioannou (1992): Pleiotropic effects of a null mutation in the c-fos proto-oncogene. Cell. 71: Jørgensen, N. R. & M. Kassem (2008): Knoglevævets opbygning og funktion. Kaf lan, A. D., W. J. Reimert, R. D. Feldmans, og S. J. Dixons (1995): Extracellular Nucleotides Potentiate the Cytosolic Ca 2+, but Not Cyclic Adenosine 3, 5-Monophosphate Response to Parathyroid Hormone in Rat Osteoblastic Cells. 136:
88 Kafienah W., D. Brömme, D. J. Buttle, L. J. Croucher og A. P. Hollander (1998): Human cathepsin K cleaves native type I and II collagens at the N-terminal end of the triple helix. Biochem J. 331: Karaplis, A. C. & D. Goltzman (2000): PTH and PTHrP Effects on the Skeleton. Endocrine & Metabolic Disorders. 1: Kimmel, D. B. & Jee, W. S. (1980): Bone cell kinetics during longitudinal bone growth in the rat. Calcif Tissue Int. 32: Koga T., M. Inui, K. Inoue, S. Kim, A. Suematsu, E. Kobayashi, T. Iwata, H. Ohnishi, T. Matozaki, T. Kodama, T. Taniguchi, H. Takayanagi og T. Takai (2004): Costimulatory signals mediated by the ITAMmotif cooperate with RANKL for bone homeostasis. Nature 428: Knogleforlængelse (2008): Knogler. (på internettet den ). Komarova, S. V. (2005): Mathematical model of paracrine interactions between osteoclasts and osteoblasts predicts anabolic action of parathyroid hormone on bone. Endocrinology 146(8): Kotowicz, M. A., G. G. Klee, P. C. Kao, W. H. O Fallon, S. F. Hodgson, S. L. Cedel, E. F. Eriksen, D. G. Gonchoroff, H. L. Judd, og B. L. Riggs (1990): Relationship between serum intact parathyroid hormone concentrations and: bone remodeling in type I osteoporosis: Evidence that skeletal sensitivity is increased. Osteopor Int. 1: Koval, P. & T. L. Seaton (2005): Parathyroid Hormone. Clinical Reviews in Bone and Mineral Metabolism. 3(1): Krishnan, V, T. L. Moore, Y. L. Ma, L. M. Helvering, C. A. Frolik, K. M. Valasek, P. Ducy, A. G. Geiser (2003): Parathyroid hormone bone anabolic action requires Cbfa1/Runx2-dependent signaling. Mol Endocrinology. 17:
89 Lawrence, G. R., (2005): Pathogenesis of osteoporosis: concepts, conflicts, and prospects. J. Clin Invest. 115: Leaffer, D., M. Sweeney, L. A. Kellerman, Z. Avnur, J. L. Krstenansky, B. H. Vickery og J. P. Caulfield. (1995): Modulation of osteogenic cell ultrastructure by RS-23581, an analog of human parathyroid hormone (PTH)-related peptide-(1-34), and bovine PTH- (1-34). Endocrinology. 136(8): Lee, K., A., J. D. Deeds, S. Chiba, M. Un-no, A. T. Bond og G. V. Segre (1994): Parathyroid hormone induces sequential c-fos expression in bone cells in vivo: in situ localization of its receptor and c-fos messenger ribonucleic acids. Endocrinology. 134(1): Lee, S. & J. A. Lorenzo (1999): Parathyroid hormone stimulates TRANCE and inhibits osteoprotegerin messenger ribonucleic acid expression in murine bone marrow cultures: correlation with osteoclast-like cell formation. Endocrinology 140(8): Lieberherr, M. (1987): Effects of Vitamin D, Metabolites on CytosolicF ree Calcium in Confluent Mouse Osteoblast. J Biol Chem. 262(27): Linkhart, T. A.og S. Mohan (1989): Parathyroid hormone stimulates release of insulin-like growth factor-i (IGF-I) and IGF-II from neonatal mouse calvaria in organ culture. Endocrinology. 125: Liu, B.-Y., J. Guo, B. Lanske, P. Divieti, H. M. Kronenberg og F. R. Bringhurst (1998): Conditionally Immortalized Murine Bone Marrow Stromal Cells Mediate Parathyroid Hormone- Dependent Osteoclastogenesis in Vitro. Endocrinology. 139(4): Loprinzi, C. L. (2007): Denosumab in postmenopausal women with low bone mineral. Current Oncology Reports. 8(4): Ma, Y. L., R. L. Cain, D. L. Halladay, X. Yang, Q. Zeng, R. R. Miles, S. Chandrasekhar, T. J. Martin og J. E. Onyia (2001): Catabolic Effects of Continuous Human PTH(1 38) in Vivo Is Associated with Sustained Stimulation of RANKL and Inhibition of Osteoprotegerin and Gene- Associated Bone Formation. Endocrinology 142(9):
90 Ma, Y., W. S. S. Jee, Z- Yuan, W. Wei, H. Chen, S. Pun, H. Liang og C. Lin (1999): Parathyroid hormone and mechanical usage have a synergistic effect in rat tibial diaphyseal cortical bone. J Bone Miner Res 14(3): Margolis, R. N., E. Canalis, og N. C. Partridge (1996): Invited review of a workshop: Anabolic hormones in bone: Basic research and therapeutic potential. J Clin Endocrinol Metab. 81: Matsumoto, M., M. Kogawa, S. Wada, H. Takayanagi, M. Tsujimoto, S. Katayama, K. Hisatake og Y. Nogi (2004): Essential Role of p38 Mitogen-activated Protein Kinase in Cathepsin K Gene Expression during Osteoclastogenesis through Association of NFATc1 and PU.1. J Biol Chem. 279(44): Merfiman, H. L., D. L. Tour, T. A. Linkhart, S. Mohan, D. J. Baylink og D. D. Strong (1990): Insulin-like Growth Factor-I and Insulin-like Growth Factor-II Induce c-fos in Mouse Osteoblastic Cells. Calcif Tissue Int. 46: McCabe, L. R., M. Kockx, J. Lian, J. Stein og G. Stein (1995): Selective Expression of fos and jun- Related genes during Osteoblast Proliferation and Differentiation. Experimental Cell Research. 218: McCarthy, T. L., M. Centrella, E. Canalis (1989): Parathyroid hormone enhances the transcript and polypeptide levels of insulin-like growth factor I in osteoblastenriched cultures from fetal rat bone. Endocrinology 124: McCauley, L. K., A. J. Koh, C. A. Beecher og T. J. Rosol (1997): Proto-Oncogene c-fos Is Transcriptionally Regulated by Parathyroid Hormone (PTH) and PTH-Related Protein in a Cyclic Adenosine Monophosphate-Dependent Manner in Osteoblastic Cells. Endocrinology. 138(12):
91 McClelland, P., Onyia, J. E., Miles, R. R., Tu, Y., Liang, J., Harvey, A. K., Chandrasekhar, S., Hock, J. M., og Bidwell, J. P. (1998): Intermittent administration of parathyroid hormone (1-34) stimulates matrix metalloproteinase-9 (MMP-9) expression in rat long bone. J Cell Biochem. 70: Medical News (2008): Early findings suggest denosumab boosts bone-mineral density. (på internettet den ). Miyakoshi, N., Y. Kasukawa, T. S. Linkhart, D. J. Baylink og B. Mohan. (2001): Evidence That Anabolic Effects of PTH on Bone Require IGF-I in Growing Mice. Endocrinology. 142(10): Mohan, S., S. Kutilek, C. Zhang, H. G. Shen, Y. Kodama, A. K. Srivastava, J. E. Wergedal, W. G. Beamer, og D. J. Baylinik (2000): Comparison of Bone Formation Responses to Parathyroid Hormone(1-34), (1-31), and (2-34) in Mice. Bone. 27: Murrills, R. J., J.J. Matteo, R. L. Samuel, J. L. Andrews, B. M. Bhat, V. E. Coleburn, Y. P. Kharode og F. J. Bex (2004): In vitro and in vivo activites of C-terminally truncated PTH peptides reveal a disconnect between camp signaling and functional activity. Bone. 35: Murrills, R. (2006): Parathyroid Hormone and Bone Cells. Clinical Reviews in Bone and Mineral Metabolism. 4(4): Nishida, S., A.Yamaguchi, T. Tanizawa, N. Endo, T. Mashiba, Y Uchiyama, T. Suda, S. Yoshiki, H. E. Takahashi (1994): Increased Bone Formation by Intermittent Parathyroid Hormone Administration is Due to the Stimulation of Proliferation and Differentiation of Osteoprogenitor Cells in Bone Marrow. Bone 15(6): Osteoporosedoktor (2008): Osteoporose. (på internettet den ). 75
92 Pedersen K. K. & J. H. Jensen (red.) (2007): Det naturvidenskabelige basisstudium, studievejledning (18. udgave). Roskilde universitetscenter, Roskilde. Peeters-Joris, C., Hammani, K., og Singer, C. F. (1998): Differential regulation of MMP-13 (collagenase-3) and MMP-3 (stromelysin-1) in mouse calvariae. Biochim Biophys Acta 1405: Pehue, M., A. Policard og A. Dufort (1931): L Osteoporose ou maladie des os marmoreens. Press Med. 53 :999 Pfeilschifter, J., M. Oechsner, A. Naumann, R. G. Gronwald, H. W. Minne og Ziegler, R. (1990): Stimulation of bone matrix apposition in vitro by local growth factors: A comparison between insulin-like growth factor I, platelet-derived growth factor, and transforming growth factor beta. Endocrinology. 127: Qi, H., M. Li og T. J. Wronski (1994): A comparison of the anabolic effects of parathyroid hormone at skeletal sites with moderate and severe osteopenia in aged, ovariectomized rats. J Bone Miner Res. Raisz, L. G. (2005): Pathogenesis of osteoporosis: concepts, conflicts, and prospects. J. Clin. Invest. 115: Rajakumar, R. A. og C. O. Quinn (1996): Parathyroid Hormone Induction of Rat Interstitial Collagenase mrna in Osteosarcoma Cells Is Mediated through an AP-I -Binding Site. Molecular Endocrinology. 10(7): Reeve, J. (2002): Recombinant human parathyroid hormone. BMJ 324: Reeve, J, M. Arlot, M. Bernat, C. Edoard og R. Hesp (1980a): Treatment of osteoporosis with human parathyroid fragment 1-34: A positive final tissue balance in trabecular bone. Matab Bone Dis Relat. Res. 2:
93 Reeve, J, P. J. Meunier, J. A. Parsons, M. Bernat, O. L. M. Bijoet, P. Courpron, C. Edouard, C. Klenerman, R. M. Neer, J. C. Renier, D. Slovik, F. J. F. E. Vismans, og J. T. Jr. Potts (1980b): Anabolic effekt of human parathyroid hormon 1-34 peptide on trabecular bone in involutional osteoporosis: A multicentre trial. Br. Med. J Reeve, J, R. Hesp, D. Williams, L. Klenerman, J. M. Zanelli, A. J. Parby, G. W. Treager, J. A. Parsons og R. Hume (1976a): Anabolic efffect of low doses of human parathyroid hormone on the skeleton in postmenopausal osteoporosis. Lancet. 1: Reeve, J., G. W. Treager og J. A. Parsons (1976b): Preliminary trial of low doses of human parathyroid hormone 1-34 peptide in treatment of osteoporosis. Clin Endocrinology. 21: Region Sjælland Sygehus Syd (2008): (på internettet d ) Reproductive and cardiovaskular disease research group (2008): caspase activation. (på internettet den ). Rodan, G. A., L. G. Raisz og J. P. Bilezikian (2002): Pathophysiology of osteoporosis, side I Principles of bone biology, Bilezikian, J. P., L. G. Raisz og G. A. Rodan, Academic Press, London Ryder K. D., R. L. Duncan (2000): Parathyroid Hormone Modulates the Response of Osteoblast- Like Cells to Mechanical Stimulation. Calcif Tissue Int. 67: Sakai, A., T. Sakata, S. Ikeda, S. Uchida, R. Okazaki, T. Norimura, M. Hori og T. Nakamura (1999): Intermittent administration of human parathyroid hormone prevents immobilizationrealated bone loss by regulating bone marrow capacity for bone cells inn ddγ mice. Journal of Bone and Mineral research. 14(10): Schwarz, P., K. (2005): Personlig kommunikation. 77
94 Schwarz, P., K. T. Brixen & L. Mosekilde (2005): Calciumhomøostasen og den normale knogleremodellering. Ugeskrift for læger 167(8): Seelentag, W. K., J.-J. Mermod, R. Montesano og P. Vassalli (1987): Additive effects of interleukin 1 and tumour necrosis factor-a on the accumulation of the three granulocyte and macrophage colonystimulating factor mrnas in human endothelial cells. EMBO J 6(8): Selye, H. (1932): On the stimulation of new bone formation with parathyroid extract and irradiated ergosterol. Endocrinology. 16: Siegel, I. M. (2006): Bone Biology and the Clinical Implications for Osteoporosis. Physical Ther. 86(1): Simonelli, C. (2002): Parathyroid Hormone: A New Treatment Option for Osteoporosis. P & T. 27(8): Smart skeletons (2008): Mechanotransduction. (på internettet den ). Stanislaus, D., X. Yang, J. D. Liang, J. Wolfe, R. L. Cain, J. E. Onyia, N. Falla, P. Marder, J. P. Bidwell, S. W. Queener og J. M. Hock (2000): In Vivo Regulation of Apoptosis in Metaphyseal Trabecular Bone of Young Rats by Synthetic Human Parathyroid Hormone (1-34) Fragment. Bone. 27(2): Sundhedsstyrelsen/Fødevarederektoratet (2000): Osteoporose Forebyggelse, diagnostic og behandling (1. udgave). København Suzawa, T., C. Miyaura, M. Inada, T. Maruyama, Y. Sugimoto, F. Ushikubi, A. Ichikawa, S. Narumiya og T. Suda (2000): The role of prostaglandin E receptor subtypes (EP1, EP2, EP3, and EP4) in bone resorption: an analysis using specific agonists for the respective EPs. Endocrinology 141(4):
95 Swarthout, J. T., D. R. Tyson., S. C. J, Jefcoat JR. og N. C. Partridge (2002): Induction of transcriptional activity of the cyclic adenosine monophosphate response element binding protein by parathyroid hormone and epidermal growth factor on osteoblastic cells. Journal of Bone and Mineral Research. 17: Takami, M., N. Takahashi, N. Udagawa, C. Miyaura, K. Suda, J.-T. Woo, T. J. Martin, K. Nagai og T. Suda (2000): Intracellular Calcium and Protein Kinase C Mediate Expression of Receptor Activator of Nuclear Factor-kB Ligand and Osteoprotegerin in Osteoblasts. Endocronology 141(12): Takayanagi, H., S. Kim, T. Koga, H. Nishina, M. Isshiki, H. Yoshida, a. Saiura, M. Isobe, T. Yokochi, J.-I. Inoue, E. F. Wagner, T. W. Mak, T. Kodama og T. Taniguchi (2002): Induction and activation of the transcription factor NFATc1 (NFAT2) integrate RANKL signaling in terminal differentiation of osteoclasts. Dev Cell. 3(6): Takeda, S., T. Yoshizawa, Y Nagai, H. Yamato, S. Fukumoto, K. Sekine, S. Kato, T. Matsumoto og T. Fujita (1999):Stimulation of osteoclast formation by 1,25-dihydroxyvitamin D requires its binding to vitamin D receptor (VDR) in osteoblastic cells: studies using VDR knockout mice. Endocrinology. 140(2): Tamura, T., N. Udagawa, N. Takahashi, C. Miyaura, S. Tanaka, Y. Yamada, Y. Koishihara, Y. Ohsugi, K. Kumaki, T. Taga, T. Kishimoto og T. Suda (1993): Soluble interleukin-6 receptor triggers osteoclast formation by interleukin 6. Proc Natl Acad Sci U S A. 90(24): Tfelt-Hansen, J. & Schwatz P. (2003): Den humane calciumfølsomme receptor og dens rolle i sygdom og mål for terapi. Ugeskr Læger. 165: The Science Creative Quarterly (2008): Image (bank). (på internettet den ). Vestergaard, P., L. R. Nielsen og L. Mosekilde (2004): Teriparatid (humant aminoterminalt 1-34 parathyroideahormon) et nyt behandlingsprincip til svær osteoporose. Ugeskr. Læger. 166(32):
96 Weaver, M. C., & R. P. Heaney (red.) (2006): Calcium in Human Health (1. udgave). Humana Press Inc, Totowa, New Jersey Westenfeld, R., M. Ketteler og V. M. Brandenburg (2006): Anti-RANKL therapy -implications for the bone-vascular-axis in CKD? Denosumab in post-menopausal women with low bone mineral density. Translational Nephrology. 21(8): Watson, P., Lazowski D., Han V., Fraher L., Steer B., Hodsman A. (1995): Parathyroid hormone restores bone mass and enhances osteoblast insulin-like growth factor I gene expression in ovariectomized rats. Bone. 16: Weinstein, R. S., T. M. Chambers, J. A. Crawford, F. A. Swain, A. M. Parfitt, R. L. Jilka og S. C. Manolagas (1999): A strong positive correlation between the prevalence of osteoblast apoptosis and the activation frequency across a wide range of bone remodeling rates. J Bone Miner Res. Yang, D., R. Singh, P. Divieti, J. Guo, M.L. Bouxsin og F.R. Bringhurst (2007): Contributions of Parathyroid hormone (PTH)/PTH-related peptide receptor signaling pathways to the anabolic effect of PTH on bone. Bone. 40: Yasuda, H., N. Shima, N. Nakagawa, K. Yamaguchi, M. Kinosaki, S.-I. Mochizuku, A. Tomoyasu, K. Yano, M. Goto, A. Murakami, E. Tsuda, T. Morinaga, K. Higashio, N. Udagawa, N. Takahashi og T. Suda (1998a): Osteoclast differentiation factor is a ligand for osteoprotegerin/osteoclastogenesis-inhibitory factor and is identical totrance/rankl. Proc Natl Acad Sci U.S.A. 95(7): Yasuda, H., N. Shima, N. Nakagawa, S.-I. Mochizuku, K. Yano, N. Fujise, Y. Sato, M. Goto, K. Yamaguchi, M. Kuriyama, T. Kanno, A. Murakami, E. Tsuda, T. Morinaga og K. Higashio (1998b): Identity of Osteoclastogenesis Inhibitory Factor (OCIF) and Osteoprotegerin (OPG): A Mechanism by which OPG/OCIF Inhibits Osteoclastogenesis in Vitro. Endocrinology. 139(3):
97 Yucel-Lindberg, T., S. Nilsson & T. Modéer (1999): Signal Transduction Pathways Involved in the Synergistic Stimulation of Prostaglandin Production by Interleukin-1β and Tumor Necrosis Factor α in Human Gingival Fibroblasts. J Dent Res 78(1):
Syv transmembrane receptorer
 Syv transmembrane receptorer Receptoren som kommunikationscentral Cellemembranen definerer grænsen mellem en celles indre og ydre miljø, der er meget forskelligt. Det er essentielt for cellens funktion
Syv transmembrane receptorer Receptoren som kommunikationscentral Cellemembranen definerer grænsen mellem en celles indre og ydre miljø, der er meget forskelligt. Det er essentielt for cellens funktion
INDBERETTEDE BIVIRKNINGER I FORBINDELSE MED MEDICINSK BEHANDLING AF OSTEOPOROSE
 INDBERETTEDE BIVIRKNINGER I FORBINDELSE MED MEDICINSK BEHANDLING AF OSTEOPOROSE 2013 Titel Indberettede bivirkninger i forbindelse med medicinsk behandling af osteoporose Sundhedsstyrelsen, 2013. Publikationen
INDBERETTEDE BIVIRKNINGER I FORBINDELSE MED MEDICINSK BEHANDLING AF OSTEOPOROSE 2013 Titel Indberettede bivirkninger i forbindelse med medicinsk behandling af osteoporose Sundhedsstyrelsen, 2013. Publikationen
Knoglevævets opbygning og funktion
 Knoglevævets opbygning og funktion v/ Niklas Rye Jørgensen 1,2 og Moustapha Kassem 3 1 Klinisk Biokemisk Afdeling, Glostrup Hospital, Glostrup, Danmark 2 Forskningscenter for Aldring og Osteoporose, Glostrup
Knoglevævets opbygning og funktion v/ Niklas Rye Jørgensen 1,2 og Moustapha Kassem 3 1 Klinisk Biokemisk Afdeling, Glostrup Hospital, Glostrup, Danmark 2 Forskningscenter for Aldring og Osteoporose, Glostrup
STØTTEVÆV. amorf. BINDEVÆV fibrillært kollagent løst. organiseret: elastisk. fedtvæv. cellulært bindevæv: (fx tarmkrøs)
 STØTTEVÆV få celler meget grundsubstans spredt beliggende formet (fibriller) amorf bindevæv amorf grundsubstans er blød + fibriller bruskvæv amorf grundsubstans er relativt fast + fibriller benvæv (knoglevæv)
STØTTEVÆV få celler meget grundsubstans spredt beliggende formet (fibriller) amorf bindevæv amorf grundsubstans er blød + fibriller bruskvæv amorf grundsubstans er relativt fast + fibriller benvæv (knoglevæv)
Tips og vejledning vedrørende den tredelte prøve i AT, Nakskov Gymnasium og HF
 Tips og vejledning vedrørende den tredelte prøve i AT, Nakskov Gymnasium og HF Den afsluttende prøve i AT består af tre dele, synopsen, det mundtlige elevoplæg og dialogen med eksaminator og censor. De
Tips og vejledning vedrørende den tredelte prøve i AT, Nakskov Gymnasium og HF Den afsluttende prøve i AT består af tre dele, synopsen, det mundtlige elevoplæg og dialogen med eksaminator og censor. De
Det hæmostatiske system
 Det hæmostatiske system Hæmostasen omfatter alle de mekanismer, som bidrager til at standse en blødning. Blodets evne til at holde sig flydende under normale omstændigheder og evne til at størkne i et
Det hæmostatiske system Hæmostasen omfatter alle de mekanismer, som bidrager til at standse en blødning. Blodets evne til at holde sig flydende under normale omstændigheder og evne til at størkne i et
Knogleskørhed (osteoporose)
 Information til patienten Knogleskørhed (osteoporose) Regionshospitalet Viborg Klinik for Diabetes og Hormonsygdomme Hvad er knogleskørhed Knogleskørhed - også kaldet osteoporose - rammer hver 3. kvinde
Information til patienten Knogleskørhed (osteoporose) Regionshospitalet Viborg Klinik for Diabetes og Hormonsygdomme Hvad er knogleskørhed Knogleskørhed - også kaldet osteoporose - rammer hver 3. kvinde
Kræft. Alex Hansen Euc-Syd Sønderborg HTX 10/1/2010. news/possible-cancer-vaccines/. 29.09.2010. (Billede)
 2010 Kræft Alex Hansen Euc-Syd Sønderborg HTX 1 Cancer cells. Densley, Ross. Set: http://www.ngpharma.com/ news/possible-cancer-vaccines/. 29.09.2010. (Billede) 10/1/2010 Titelblad Skolens navn: Euc-Syd
2010 Kræft Alex Hansen Euc-Syd Sønderborg HTX 1 Cancer cells. Densley, Ross. Set: http://www.ngpharma.com/ news/possible-cancer-vaccines/. 29.09.2010. (Billede) 10/1/2010 Titelblad Skolens navn: Euc-Syd
Mette Friberg Hitz. speciallæge i endokrinologi overlæge, ph.d osteoporose enheden hvidovre hospital
 OSTEOPOROSE WORK-SHOP KØGE 20.05.2014 Nyt om osteoporose... Mette Friberg Hitz speciallæge i endokrinologi overlæge, ph.d osteoporose enheden hvidovre hospital HVAD ER OSTEOPOROSE HVAD SKER DER I KNOGLERNE,
OSTEOPOROSE WORK-SHOP KØGE 20.05.2014 Nyt om osteoporose... Mette Friberg Hitz speciallæge i endokrinologi overlæge, ph.d osteoporose enheden hvidovre hospital HVAD ER OSTEOPOROSE HVAD SKER DER I KNOGLERNE,
PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE)
 PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE) Navn: CPR nummer: Dato: Vejledning i at udfylde spørgeskemaet Spørgeskemaet om knogleskørhed indeholder spørgsmål angående generel viden, symptomer, risikofaktorer,
PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE) Navn: CPR nummer: Dato: Vejledning i at udfylde spørgeskemaet Spørgeskemaet om knogleskørhed indeholder spørgsmål angående generel viden, symptomer, risikofaktorer,
Støttevævene. Anne Mette Friis MT.
 Støttevævene. 1 Støttevæv. Mennesket har en forholdsvis konstant legemsform, dette opretholdes af støttevævene. Der findes tre overordnede typer af støttevæv: Bindevæv Bruskvæv Knoglevæv. 2 Typer af støtte
Støttevævene. 1 Støttevæv. Mennesket har en forholdsvis konstant legemsform, dette opretholdes af støttevævene. Der findes tre overordnede typer af støttevæv: Bindevæv Bruskvæv Knoglevæv. 2 Typer af støtte
Opgave 1 Listeria. mørkviolette bakteriekolonier, se figur 1a. og b. 1. Angiv reaktionstypen for reaktion. 1 vist i figur 1b.
 Opgave 1 Listeria Bakterien Listeria monocytogenes kan være sygdomsfremkaldende for personer, der i forvejen er svækkede. For at identificere Listeria kan man anvende indikative agarplader. Her udnyttes
Opgave 1 Listeria Bakterien Listeria monocytogenes kan være sygdomsfremkaldende for personer, der i forvejen er svækkede. For at identificere Listeria kan man anvende indikative agarplader. Her udnyttes
EKSAMEN. NEUROBIOLOGI OG BEVÆGEAPPARATET I (Blok 5) MedIS 3. semester. Fredag den 6. januar 2012
 AALBORG UNIVERSITET EKSAMEN NEUROBIOLOGI OG BEVÆGEAPPARATET I (Blok 5) MedIS 3. semester Fredag den 6. januar 2012 4 timer skriftlig eksamen Evalueres efter 7-skalen. Ekstern censur Vægtning af eksamenssættets
AALBORG UNIVERSITET EKSAMEN NEUROBIOLOGI OG BEVÆGEAPPARATET I (Blok 5) MedIS 3. semester Fredag den 6. januar 2012 4 timer skriftlig eksamen Evalueres efter 7-skalen. Ekstern censur Vægtning af eksamenssættets
Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010
 MedIS, AAU. Det hæmatologiske system og immunforsvaret, 7. Juni 2010 1 Navn: Studienummer: Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010 Dette eksamenssæt
MedIS, AAU. Det hæmatologiske system og immunforsvaret, 7. Juni 2010 1 Navn: Studienummer: Eksamen i Modul 2.2, Det hæmatologiske system og immunforsvaret MEDIS, AAU, 2. semester, juni 2010 Dette eksamenssæt
www.printo.it/pediatric-rheumatology/dk/intro
 www.printo.it/pediatric-rheumatology/dk/intro PAPA syndromet Version af 2016 1. HVAD ER PAPA 1.1 Hvad er det? PAPA er en forkortelse for Pyogen Artritis, Pyoderma gangrenosum og Akne. Det er en genetisk
www.printo.it/pediatric-rheumatology/dk/intro PAPA syndromet Version af 2016 1. HVAD ER PAPA 1.1 Hvad er det? PAPA er en forkortelse for Pyogen Artritis, Pyoderma gangrenosum og Akne. Det er en genetisk
STØTTEVÆV - almen histologi
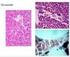 STØTTEVÆV - almen histologi Meddelelser onsdag 25.sep 2013 Kranieorientering kl 8.00 for første hold - jvf kalender 'Diagnostisk prøve' afholdes 2. oktober i Aud. 1 Nervevæv 2013.pdf med link til youtube
STØTTEVÆV - almen histologi Meddelelser onsdag 25.sep 2013 Kranieorientering kl 8.00 for første hold - jvf kalender 'Diagnostisk prøve' afholdes 2. oktober i Aud. 1 Nervevæv 2013.pdf med link til youtube
PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE)
 PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE) Navn: CPR nummer: Dato: Vejledning i at udfylde spørgeskemaet Spørgeskemaet om knogleskørhed indeholder spørgsmål angående generel viden, symptomer, risikofaktorer,
PATIENTERS VIDEN OM KNOGLESKØRHED (OSTEOPOROSE) Navn: CPR nummer: Dato: Vejledning i at udfylde spørgeskemaet Spørgeskemaet om knogleskørhed indeholder spørgsmål angående generel viden, symptomer, risikofaktorer,
En af de metoder som fremmer sundheden, og giver rigtig gode resultater, er teorien om ikke at blande protein og stivelse i samme måltid.
 Nyhedsbrev 4 I de første 3 nyhedsbreve lærte vi, at kroppen skal have vand, ilt og strøm (gennem maden), og at kroppen skal tilføres flere baseholdige fødevarer så den ikke bliver for sur. I dette nummer
Nyhedsbrev 4 I de første 3 nyhedsbreve lærte vi, at kroppen skal have vand, ilt og strøm (gennem maden), og at kroppen skal tilføres flere baseholdige fødevarer så den ikke bliver for sur. I dette nummer
Atomic force mikroskopi på blodceller
 1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
1 Atomic force mikroskopi på blodceller Problemstilling: Problemstillingen eleven bliver sat overfor er: Hvad er atomic force mikroskopi, og hvordan kan det bruges til at studere blodceller på nanometerskala?
www.printo.it/pediatric-rheumatology/dk/intro
 www.printo.it/pediatric-rheumatology/dk/intro Blau syndrom Version af 2016 1. HVAD ER BLAU SYNDROM/JUVENIL SARKOIDOSE 1.1 Hvad er det? Blau syndrom er en genetisk sygdom. Som patient lider man af en kombination
www.printo.it/pediatric-rheumatology/dk/intro Blau syndrom Version af 2016 1. HVAD ER BLAU SYNDROM/JUVENIL SARKOIDOSE 1.1 Hvad er det? Blau syndrom er en genetisk sygdom. Som patient lider man af en kombination
Det Rene Videnregnskab
 Det Rene Videnregnskab Visualize your knowledge Det rene videnregnskab er et værktøj der gør det muligt at redegøre for virksomheders viden. Modellen gør det muligt at illustrere hvordan viden bliver skabt,
Det Rene Videnregnskab Visualize your knowledge Det rene videnregnskab er et værktøj der gør det muligt at redegøre for virksomheders viden. Modellen gør det muligt at illustrere hvordan viden bliver skabt,
Nyrefysiologi: Renal ionbehandling, kap. 8 Anne Agersted, 5. sem. efterår 2013 CALCIUM HOMEOSTASEN
 CALCIUM HOMEOSTASEN 35 % af Ca +2 indholdet i en normal voksen persons kost absorberes gennem mavetarmkanalen. Den ekstracellulære Ca +2 pool indeholder ca. 25 mmol, hvorfra Ca +2 udskilles i urinen. PTH:
CALCIUM HOMEOSTASEN 35 % af Ca +2 indholdet i en normal voksen persons kost absorberes gennem mavetarmkanalen. Den ekstracellulære Ca +2 pool indeholder ca. 25 mmol, hvorfra Ca +2 udskilles i urinen. PTH:
Fedme, hvad kan vi gøre
 Fedme, hvad kan vi gøre Hvorfor overvægtige efter vægttab tager på igen. Af Svend Lindenberg. Copenhagen Fertility Center. Et af de store problemer ved vægttab er, at de fleste overvægtige efter en periode
Fedme, hvad kan vi gøre Hvorfor overvægtige efter vægttab tager på igen. Af Svend Lindenberg. Copenhagen Fertility Center. Et af de store problemer ved vægttab er, at de fleste overvægtige efter en periode
14. Mandag Endokrine kirtler del 2
 14. Mandag Endokrine kirtler del 2 Midt i dette nye spændende emne om endokrine kirtler kan det være nyttigt med lidt baggrundsdiskussion omkring især glukoses (sukkerstof) forskellige veje i kroppen.
14. Mandag Endokrine kirtler del 2 Midt i dette nye spændende emne om endokrine kirtler kan det være nyttigt med lidt baggrundsdiskussion omkring især glukoses (sukkerstof) forskellige veje i kroppen.
Underviser cand.scient Karen Hulgaard
 Velkommen til en præsentation i anatomi og fysiologi i forplantningssystemet, med vægt på mandens forplantningssystem. Præsentationen bruges i forbindelse med undervisningen på femte semester. 1 Start
Velkommen til en præsentation i anatomi og fysiologi i forplantningssystemet, med vægt på mandens forplantningssystem. Præsentationen bruges i forbindelse med undervisningen på femte semester. 1 Start
TIP EN 12 ER OM KRÆFT HOS BØRN
 TIP EN 12 ER OM KRÆFT HOS BØRN 1 X 2 1. Hvor mange børn under 18 år får kræft i Danmark om året? 750 200 85 SVAR: 200 børn (X) 2. Hvor mange børn om året er i behandling for kræft? 900-1000 500-600 300-400
TIP EN 12 ER OM KRÆFT HOS BØRN 1 X 2 1. Hvor mange børn under 18 år får kræft i Danmark om året? 750 200 85 SVAR: 200 børn (X) 2. Hvor mange børn om året er i behandling for kræft? 900-1000 500-600 300-400
Lærervejledning til power point: Småtspisende ældre vidste du at småt er godt
 Lærervejledning til power point: Småtspisende ældre vidste du at småt er godt 1. Småtspisende ældre Med alderen sker der en række ændringer i menneskets anatomiske, fysiologiske og psykiske for hold, ændringer
Lærervejledning til power point: Småtspisende ældre vidste du at småt er godt 1. Småtspisende ældre Med alderen sker der en række ændringer i menneskets anatomiske, fysiologiske og psykiske for hold, ændringer
Modul 09a F902a-2. Dysregulering og analyser af Calcium-Fosfat Stofskiftet
 Modul 09a F902a-2 Dysregulering og analyser af Calcium-Fosfat Stofskiftet Søren Frank Jørgensen Lektor Navn Navnesen Titel Side 1 Afdelning 10 august 2009 Ændringer til næste gang. FO i dysreg er nu lidt
Modul 09a F902a-2 Dysregulering og analyser af Calcium-Fosfat Stofskiftet Søren Frank Jørgensen Lektor Navn Navnesen Titel Side 1 Afdelning 10 august 2009 Ændringer til næste gang. FO i dysreg er nu lidt
1. Afrikansk plante med mulig gavnlig virkning på diabetes type II. 2. Bestemmelse af genomer hos forskellige arter organismer
 Eksamensspørgsmål til biobu maj 2013 1. Afrikansk plante med mulig gavnlig virkning på diabetes type II Forklar hvordan insulin er opbygget, dets dannelse og virkemåde. Hvad er årsagen til diabetes type
Eksamensspørgsmål til biobu maj 2013 1. Afrikansk plante med mulig gavnlig virkning på diabetes type II Forklar hvordan insulin er opbygget, dets dannelse og virkemåde. Hvad er årsagen til diabetes type
Magnetfelter og børnekræft - er der en sammenhæng?
 NOTAT NP92-961b JKJ/BT-DGR 4. december 1997 Magnetfelter og børnekræft - er der en sammenhæng? Revideret januar 1993 NOTAT NP92-961b 2 1. Om børnekræft I perioden fra 1945 og frem til i dag har udviklingen
NOTAT NP92-961b JKJ/BT-DGR 4. december 1997 Magnetfelter og børnekræft - er der en sammenhæng? Revideret januar 1993 NOTAT NP92-961b 2 1. Om børnekræft I perioden fra 1945 og frem til i dag har udviklingen
Svarark, eksamen modul 2.3 Juni 2011. Spørgsmål Svar Spørgsmål Svar 1 c 7 a 2 a 8 a 3 b 9 a 4 d 10 e 5.1 a 11 d 5.2 c 12 d 5.
 Svarark, eksamen modul 2.3 Juni 2011 Spørgsmål Svar Spørgsmål Svar 1 c 7 a 2 a 8 a 3 b 9 a 4 d 10 e 5.1 a 11 d 5.2 c 12 d 5.3 e 13 b 6 d 14 d Opgave 15 En 50-årig kvinde har haft gestationel DM under to
Svarark, eksamen modul 2.3 Juni 2011 Spørgsmål Svar Spørgsmål Svar 1 c 7 a 2 a 8 a 3 b 9 a 4 d 10 e 5.1 a 11 d 5.2 c 12 d 5.3 e 13 b 6 d 14 d Opgave 15 En 50-årig kvinde har haft gestationel DM under to
Knogleskørhed og prostatakræft
 Mads Hvid Poulsen, Læge, Ph.d. Knogleskørhed og prostatakræft Urinvejskirurgisk forskningsenhed, Urologisk Afdeling, Odense Universitets Hospital Folderen er udarbejdet på baggrund af eksisterende litteratur
Mads Hvid Poulsen, Læge, Ph.d. Knogleskørhed og prostatakræft Urinvejskirurgisk forskningsenhed, Urologisk Afdeling, Odense Universitets Hospital Folderen er udarbejdet på baggrund af eksisterende litteratur
AT MED INNOVATION ELEVMANUAL
 AT MED INNOVATION ELEVMANUAL Rammer og faser i arbejdet med AT med innovation Rammerne for AT og innovationsopgaven: I AT- opgaven med innovation kan kravene være, at du skal: - Tilegne dig viden om en
AT MED INNOVATION ELEVMANUAL Rammer og faser i arbejdet med AT med innovation Rammerne for AT og innovationsopgaven: I AT- opgaven med innovation kan kravene være, at du skal: - Tilegne dig viden om en
Dig og dine knogler. Gør det selv-råd om knogleskørhed (osteoporose) en folkesygdom, du kan forebygge
 Dig og dine knogler Gør det selv-råd om knogleskørhed (osteoporose) en folkesygdom, du kan forebygge Udarbejdet af Mejeriforeningen i samarbejde med Osteoporoseforeningen og overlæge, dr.med. Bente Langdahl
Dig og dine knogler Gør det selv-råd om knogleskørhed (osteoporose) en folkesygdom, du kan forebygge Udarbejdet af Mejeriforeningen i samarbejde med Osteoporoseforeningen og overlæge, dr.med. Bente Langdahl
Deltager information
 READ, Bilag 10 Fortroligt Side 1 af 7 Deltager information Protokol DBCG 07-READ, dateret 15. oktober 2009. Et videnskabeligt forsøg med to forskellige kombinationer af kemoterapi til patienter med brystkræft.
READ, Bilag 10 Fortroligt Side 1 af 7 Deltager information Protokol DBCG 07-READ, dateret 15. oktober 2009. Et videnskabeligt forsøg med to forskellige kombinationer af kemoterapi til patienter med brystkræft.
Tinnitus. Hvad er tinnitus?
 Tinnitus Hvad er tinnitus? Tinnitus er en oplevelse af indre lyd lokaliseret til ørerne eller mere diffust inde i hovedet. Lyden høres kun af personen selv og er ikke forårsaget af kilder fra omgivelserne
Tinnitus Hvad er tinnitus? Tinnitus er en oplevelse af indre lyd lokaliseret til ørerne eller mere diffust inde i hovedet. Lyden høres kun af personen selv og er ikke forårsaget af kilder fra omgivelserne
Biologi A. Studentereksamen. Af opgaverne 1, 2, 3 og 4 skal tre og kun tre af opgaverne besvares
 Biologi A Studentereksamen Af opgaverne 1, 2, 3 og 4 skal tre og kun tre af opgaverne besvares 2stx101-BIO/A-28052010 Fredag den 28. maj 2010 kl. 9.00-14.00 Side 1 af 9 sider Opgave 1. Hormonforstyrrende
Biologi A Studentereksamen Af opgaverne 1, 2, 3 og 4 skal tre og kun tre af opgaverne besvares 2stx101-BIO/A-28052010 Fredag den 28. maj 2010 kl. 9.00-14.00 Side 1 af 9 sider Opgave 1. Hormonforstyrrende
Rundt om knoglerne. Klinisk diætist Kirsten Bønløkke - Osteoporoseforeningen
 Rundt om knoglerne Hvad er op og ned om knoglesundhed Myter om mælk og knogler Er det kun børn der har brug for mælk til knoglerne? Giver mælk knogleskørhed? Hvorfor er knogleskørhed så udbredt i de nordiske
Rundt om knoglerne Hvad er op og ned om knoglesundhed Myter om mælk og knogler Er det kun børn der har brug for mælk til knoglerne? Giver mælk knogleskørhed? Hvorfor er knogleskørhed så udbredt i de nordiske
bedre end sit rygte Den naturlige overgangsalder
 Vi kommer alle ud for spørgsmål omkring overgangsalderen, som har mange facetter. Når den sniger sig ind på kvinderne, føler nogle at der er noget unormalt ved deres krop, hvilket giver anledning til uro
Vi kommer alle ud for spørgsmål omkring overgangsalderen, som har mange facetter. Når den sniger sig ind på kvinderne, føler nogle at der er noget unormalt ved deres krop, hvilket giver anledning til uro
Alterne.dk - dit naturlige liv
 Irriteret tyktarm Tilføjet af Jette Plesner onsdag 07. maj 2008 Sidst opdateret torsdag 03. september 2009 Irriteret tyktarm er efterhånden blevet en folkesygdom. Maven bliver oppustet og gør ondt. Man
Irriteret tyktarm Tilføjet af Jette Plesner onsdag 07. maj 2008 Sidst opdateret torsdag 03. september 2009 Irriteret tyktarm er efterhånden blevet en folkesygdom. Maven bliver oppustet og gør ondt. Man
Hvorfor har vi brug for salt?
 Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Højeffekts-hjerneskanninger afslører natriumændringer ved HS En ny hjerneskanningsteknik afslører
Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Højeffekts-hjerneskanninger afslører natriumændringer ved HS En ny hjerneskanningsteknik afslører
Stresshormonet kortisol
 Stresshormonet kortisol Tilføjet af Kiirsten Pedersen søndag 25. maj 2008 Sidst opdateret torsdag 12. november 2009 Kortisol kaldes også hydrocortison og er et glucocorticoid - et af ca. 40 hormoner, der
Stresshormonet kortisol Tilføjet af Kiirsten Pedersen søndag 25. maj 2008 Sidst opdateret torsdag 12. november 2009 Kortisol kaldes også hydrocortison og er et glucocorticoid - et af ca. 40 hormoner, der
Eksamen den 7. april 2006. Cellulær og Integrativ Fysiologi
 1 Eksamen den 7. april 2006 Cellulær og Integrativ Fysiologi Sættet indeholder 5 sider. Der må ikke medbringes bøger og noter. Svarene kan være på dansk eller engelsk. Dee er 4 hovedspørgsmål i sættet.
1 Eksamen den 7. april 2006 Cellulær og Integrativ Fysiologi Sættet indeholder 5 sider. Der må ikke medbringes bøger og noter. Svarene kan være på dansk eller engelsk. Dee er 4 hovedspørgsmål i sættet.
Spørgsmål til fordøjelse og stofskifte
 Spørgsmål til fordøjelse og stofskifte 1. Hvad er dentes decidui og dentes permanentes og hvor mange har vi af hver? 2. Beskriv smagsløgenes placering og funktion. Hvilken anden sans spiller en vigtig
Spørgsmål til fordøjelse og stofskifte 1. Hvad er dentes decidui og dentes permanentes og hvor mange har vi af hver? 2. Beskriv smagsløgenes placering og funktion. Hvilken anden sans spiller en vigtig
Del 3: Statistisk bosætningsanalyse
 BOSÆTNING 2012 Bosætningsmønstre og boligpræferencer i Aalborg Kommune Del 3: Statistisk bosætningsanalyse -Typificeringer Indholdsfortegnelse 1. Befolkningen generelt... 2 2. 18-29 årige... 2 3. 30-49
BOSÆTNING 2012 Bosætningsmønstre og boligpræferencer i Aalborg Kommune Del 3: Statistisk bosætningsanalyse -Typificeringer Indholdsfortegnelse 1. Befolkningen generelt... 2 2. 18-29 årige... 2 3. 30-49
Betydningen af at være deltager på en Osteoporose skole
 Betydningen af at være deltager på en Osteoporose skole Odense Universitets Hospital Dorthe Nielsen Sygeplejerske, Ph.d. Gruppe baserede programmer Meget få studier (kvalitative såvel som kvantitative)
Betydningen af at være deltager på en Osteoporose skole Odense Universitets Hospital Dorthe Nielsen Sygeplejerske, Ph.d. Gruppe baserede programmer Meget få studier (kvalitative såvel som kvantitative)
Anne Illemann Christensen
 7. Sociale relationer Anne Illemann Christensen Kapitel 7 Sociale relationer 7. Sociale relationer Tilknytning til andre mennesker - de sociale relationer - har fået en central placering inden for folkesundhedsvidenskaben.
7. Sociale relationer Anne Illemann Christensen Kapitel 7 Sociale relationer 7. Sociale relationer Tilknytning til andre mennesker - de sociale relationer - har fået en central placering inden for folkesundhedsvidenskaben.
OSMOSE. Formålet med disse øvelser er altså at forstå: Hvad er osmose og hvorfor er det en meget vigtig biologisk proces.
 OSMOSE I de følgende tre øvelser og efterfølgende opsamlingsspørgsmål skal I arbejde med princippet osmose, altså transport af vand mellem to forskellige koncentrationer af vand, som beskrevet i artikel
OSMOSE I de følgende tre øvelser og efterfølgende opsamlingsspørgsmål skal I arbejde med princippet osmose, altså transport af vand mellem to forskellige koncentrationer af vand, som beskrevet i artikel
Den forebyggende undersøgelse for livmoderhalskræft
 Den forebyggende undersøgelse for livmoderhalskræft Alle danske kvinder mellem 23 og 65 år bliver tilbudt at deltage i forebyggende folkeundersøgelse (screening) for livmoderhalskræft. Man bliver automatisk
Den forebyggende undersøgelse for livmoderhalskræft Alle danske kvinder mellem 23 og 65 år bliver tilbudt at deltage i forebyggende folkeundersøgelse (screening) for livmoderhalskræft. Man bliver automatisk
Selective Estrogen Receptor Modulatorer er farmaka, der kan binde sig til østrogen
 SERMs v/bente L Langdahl Selective Estrogen Receptor Modulatorer er farmaka, der kan binde sig til østrogen receptor og/eller. Det er forskellen i affinitet for de to typer østrogen receptorer, der giver
SERMs v/bente L Langdahl Selective Estrogen Receptor Modulatorer er farmaka, der kan binde sig til østrogen receptor og/eller. Det er forskellen i affinitet for de to typer østrogen receptorer, der giver
[Område] RISIKO FOR FALD - OG HVAD SÅ? For dig, der har været faldet og er over 65 år. For dig, der har været faldet og er over 65 år
![[Område] RISIKO FOR FALD - OG HVAD SÅ? For dig, der har været faldet og er over 65 år. For dig, der har været faldet og er over 65 år [Område] RISIKO FOR FALD - OG HVAD SÅ? For dig, der har været faldet og er over 65 år. For dig, der har været faldet og er over 65 år](/thumbs/39/18354157.jpg) [Område] RISIKO FOR FALD - OG HVAD SÅ? For dig, der har været faldet og er over 65 år For dig, der har været faldet og er over 65 år FAKTA OM FALD HVERT ÅR: falder 300.000 mennesker over 65 år i Danmark
[Område] RISIKO FOR FALD - OG HVAD SÅ? For dig, der har været faldet og er over 65 år For dig, der har været faldet og er over 65 år FAKTA OM FALD HVERT ÅR: falder 300.000 mennesker over 65 år i Danmark
Bioteknologi A. Gymnasiale uddannelser. Vejledende opgavesæt 1. Mandag den 31. maj 2010 kl. 9.40-14.40. 5 timers skriftlig prøve
 Vejledende opgavesæt 1 Bioteknologi A Gymnasiale uddannelser 5 timers skriftlig prøve Vejledende opgavesæt 1 Mandag den 31. maj 2010 kl. 9.40-14.40 Side 1 af 8 sider pgave 1. Genmodificeret ris Vitamin
Vejledende opgavesæt 1 Bioteknologi A Gymnasiale uddannelser 5 timers skriftlig prøve Vejledende opgavesæt 1 Mandag den 31. maj 2010 kl. 9.40-14.40 Side 1 af 8 sider pgave 1. Genmodificeret ris Vitamin
Diabetesmedicin. selv gøre, og hvad skal du være opmærksom på?
 Diabetesmedicin Denne brochure handler om medicin til type 2-diabetes. Hvordan får du den bedste effekt af din medicin? Hvilke bivirkninger kan den have? Hvad kan du selv gøre, og hvad skal du være opmærksom
Diabetesmedicin Denne brochure handler om medicin til type 2-diabetes. Hvordan får du den bedste effekt af din medicin? Hvilke bivirkninger kan den have? Hvad kan du selv gøre, og hvad skal du være opmærksom
Foredrag om hovsundhed ved barfodssmed Lioba Jung 28. marts 2009
 Hesteklubben Equus April 2009 Foredrag om hovsundhed ved barfodssmed Lioba Jung 28. marts 2009 Lioba bor sammen med sin mand og fem heste på en gård i Slesvig-Holsten. Hun har redet, siden hun var seks
Hesteklubben Equus April 2009 Foredrag om hovsundhed ved barfodssmed Lioba Jung 28. marts 2009 Lioba bor sammen med sin mand og fem heste på en gård i Slesvig-Holsten. Hun har redet, siden hun var seks
BIOLOGI A. Torsdag den 14. maj 2009. Kl. 09.00 14.00 STX091-BIA STUDENTEREKSAMEN MAJ 2009
 STUDENTEREKSAMEN MAJ 2009 BILGI A Torsdag den 14. maj 2009 Kl. 09.00 14.00 Af opgaverne 1, 2, 3 og 4 skal tre og kun tre af opgaverne besvares STX091-BIA Undervisningsministeriet Side 1 af 8 sider pgave
STUDENTEREKSAMEN MAJ 2009 BILGI A Torsdag den 14. maj 2009 Kl. 09.00 14.00 Af opgaverne 1, 2, 3 og 4 skal tre og kun tre af opgaverne besvares STX091-BIA Undervisningsministeriet Side 1 af 8 sider pgave
HS og tabet af hjerneceller
 Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Stamcelle-neuroner danner de rigtige forbindelser Erstatning af neuroner med stamceller hos mus
Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Stamcelle-neuroner danner de rigtige forbindelser Erstatning af neuroner med stamceller hos mus
LEVENDE KNOGLER, STÆRKE KNOGLER
 Mission X aktivitet Træn som en astronaut LEVENDE KNOGLER, STÆRKE KNOGLER Elevens Navn Denne undervisningstime vil lære dig metoder til at holde dine knogler sunde på, og hvordan du observerer effekten
Mission X aktivitet Træn som en astronaut LEVENDE KNOGLER, STÆRKE KNOGLER Elevens Navn Denne undervisningstime vil lære dig metoder til at holde dine knogler sunde på, og hvordan du observerer effekten
Nyt studie kaster lys over hvorfor nogle hjerneområder nedbrydes før andre i HS Styr på foldningen
 Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Nyt studie kaster lys over hvorfor nogle hjerneområder nedbrydes før andre i HS Hvorfor dør kun
Forskningsnyheder om Huntingtons Sygdom På hverdagssprog Skrevet af forskere. Til det globale HS-fællesskab Nyt studie kaster lys over hvorfor nogle hjerneområder nedbrydes før andre i HS Hvorfor dør kun
Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA)
 www.printo.it/pediatric-rheumatology/dk/intro Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA) Version af 2016 2. DIAGNOSE OG BEHANDLING 2.1 Hvordan stilles diagnosen? Lægen kalder sygdommen
www.printo.it/pediatric-rheumatology/dk/intro Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA) Version af 2016 2. DIAGNOSE OG BEHANDLING 2.1 Hvordan stilles diagnosen? Lægen kalder sygdommen
Ekstern teoretisk prøve. Modul 3. S12Vy. Dato: 25.01.2013. Kl. 9.00-12.00
 Ekstern teoretisk prøve - Modul 3 Somatisk sygdom og lidelse Fagområder: Sygepleje, Anatomi og fysiologi herunder genetik, Sygdomslære herunder patologi og Ernæringslære og diætetik. Professionshøjskolen
Ekstern teoretisk prøve - Modul 3 Somatisk sygdom og lidelse Fagområder: Sygepleje, Anatomi og fysiologi herunder genetik, Sygdomslære herunder patologi og Ernæringslære og diætetik. Professionshøjskolen
Grundbegreber om naturens økologi
 Grundbegreber om naturens økologi Om videnskab og erfaringer Hold en sten i hånden og giv slip på den stenen falder til jorden. Det er et eksperiment, vi alle kan gentage som led i en naturvidenskabelig
Grundbegreber om naturens økologi Om videnskab og erfaringer Hold en sten i hånden og giv slip på den stenen falder til jorden. Det er et eksperiment, vi alle kan gentage som led i en naturvidenskabelig
Vejrtrækning pust nyt liv og livskraft ind i din krop
 Vejrtrækning pust nyt liv og livskraft ind i din krop Der er et ordsprog, der lyder: Åndedræt er liv, og det kan ikke siges bedre. Du trækker vejret for at leve, og din livskvalitet bliver påvirket af,
Vejrtrækning pust nyt liv og livskraft ind i din krop Der er et ordsprog, der lyder: Åndedræt er liv, og det kan ikke siges bedre. Du trækker vejret for at leve, og din livskvalitet bliver påvirket af,
Endometriose og mave-tarmproblemer
 Endometriose og mave-tarmproblemer Mange kvinder med endometriose oplever mave-tarmproblemer af den ene eller den anden slags, herunder udfordringer omkring toiletbesøg. Årsagerne til disse problemer kan
Endometriose og mave-tarmproblemer Mange kvinder med endometriose oplever mave-tarmproblemer af den ene eller den anden slags, herunder udfordringer omkring toiletbesøg. Årsagerne til disse problemer kan
BIOLOGI HØJT NIVEAU. Onsdag den 10. maj 2000 kl. 9.00-14.00
 STUDENTEREKSAMEN MAJ 2000 2000-6-1 BIOLOGI HØJT NIVEAU Onsdag den 10. maj 2000 kl. 9.00-14.00 Af de store opgaver 1 og 2 må kun den ene besvares. Af de små opgaver 3, 4, 5, 6 og 7 må kun to besvares. STORE
STUDENTEREKSAMEN MAJ 2000 2000-6-1 BIOLOGI HØJT NIVEAU Onsdag den 10. maj 2000 kl. 9.00-14.00 Af de store opgaver 1 og 2 må kun den ene besvares. Af de små opgaver 3, 4, 5, 6 og 7 må kun to besvares. STORE
DER ER IKKE PENGE I RASKE DYR OG MENNESKER!
 TØR DU FODRE DIN HUND MED RÅ KOST? ELLER TØR DU VIRKELIG LADE VÆRE? DET HANDLER IKKE OM AT HELBREDE SYGDOMME, MEN OM AT SKABE SUNDHED LIVSSTIL OG IKKE LIVSSTILSSYGDOMME! DER ER IKKE PENGE I RASKE DYR OG
TØR DU FODRE DIN HUND MED RÅ KOST? ELLER TØR DU VIRKELIG LADE VÆRE? DET HANDLER IKKE OM AT HELBREDE SYGDOMME, MEN OM AT SKABE SUNDHED LIVSSTIL OG IKKE LIVSSTILSSYGDOMME! DER ER IKKE PENGE I RASKE DYR OG
07-06-2013. Calcium. (passiv)/aktiv (Vitamin D) Syre. Fedt. Hvis intag. < 200 mg/dag Ca ++ PTH + Vita.D osteoclast aktivering.
 1-2 kg i kroppen (99% in skelet) Tre former: ionizeret, frit calcium (45%) protein bundet (45%) Opløselige komplekser; bundet til mindre organiske ioner, f.eks. citrat. Meget lav intra-celluært frit calcium
1-2 kg i kroppen (99% in skelet) Tre former: ionizeret, frit calcium (45%) protein bundet (45%) Opløselige komplekser; bundet til mindre organiske ioner, f.eks. citrat. Meget lav intra-celluært frit calcium
Fremstillingsformer i historie
 Fremstillingsformer i historie DET BESKRIVENDE NIVEAU Et referat er en kortfattet, neutral og loyal gengivelse af tekstens væsentligste indhold. Du skal vise, at du kan skelne væsentligt fra uvæsentligt
Fremstillingsformer i historie DET BESKRIVENDE NIVEAU Et referat er en kortfattet, neutral og loyal gengivelse af tekstens væsentligste indhold. Du skal vise, at du kan skelne væsentligt fra uvæsentligt
Sundheds CVU Nordjylland INTERN PRØVE ANATOMI, FYSIOLOGI OG BIOKEMI S06V D. 15. JUNI 2006 KL. 09.00 13.00
 INTERN PRØVE ANATOMI, FYSIOLOGI OG BIOKEMI S06V D. 15. JUNI 2006 KL. 09.00 13.00 ANATOMI OG FYSIOLOGI Opgave 1 Den menneskelige organisme er opbygget af celler. a. Beskriv cellens opbygning, heri skal
INTERN PRØVE ANATOMI, FYSIOLOGI OG BIOKEMI S06V D. 15. JUNI 2006 KL. 09.00 13.00 ANATOMI OG FYSIOLOGI Opgave 1 Den menneskelige organisme er opbygget af celler. a. Beskriv cellens opbygning, heri skal
Er der flere farver i sort?
 Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
Er der flere farver i sort? Hvad er kromatografi? Kromatografi benyttes inden for mange forskellige felter og forskningsområder og er en anvendelig og meget benyttet analytisk teknik. Kromatografi bruges
hornhinde En lidelse, som fratager mange ældre synet og som tilmed er smertefuld
 Hanne Olsen Julian Overlæge, ph.d. Øjenafdelingen, team cornea, Glostrup Hospital Illustrationer: Mediafarm Uklar hornhinde En lidelse, som fratager mange ældre synet og som tilmed er smertefuld Den optimale
Hanne Olsen Julian Overlæge, ph.d. Øjenafdelingen, team cornea, Glostrup Hospital Illustrationer: Mediafarm Uklar hornhinde En lidelse, som fratager mange ældre synet og som tilmed er smertefuld Den optimale
Opgave 1. EPO og bloddoping
 Side 1 af 8 sider Opgave 1. EPO og bloddoping Nogle sportsfolk snyder ved at få tilført hormonet erythropoietin, EPO, eller røde blodceller (bloddoping) før en konkurrence, fordi det øger præstationsevnen.
Side 1 af 8 sider Opgave 1. EPO og bloddoping Nogle sportsfolk snyder ved at få tilført hormonet erythropoietin, EPO, eller røde blodceller (bloddoping) før en konkurrence, fordi det øger præstationsevnen.
BLIV KLOGERE PÅ HØRETAB
 BLIV KLOGERE PÅ HØRETAB Hvordan ved du, om du har et høretab? Sandsynligvis vil du være den sidste, der opdager det. De fleste høretab sker gradvist over et så langt tidsrum, at man ikke nødvendigvis opdager
BLIV KLOGERE PÅ HØRETAB Hvordan ved du, om du har et høretab? Sandsynligvis vil du være den sidste, der opdager det. De fleste høretab sker gradvist over et så langt tidsrum, at man ikke nødvendigvis opdager
Standard brugervejledning Blodtryksmåler
 Standard brugervejledning Blodtryksmåler Tak fordi du har valgt at købe din blodtryksmåler hos os Kære kunde Ca. 1 mio. danskere har forhøjet blodtryk - betyder det noget? Ca. 50% af befolkningen kender
Standard brugervejledning Blodtryksmåler Tak fordi du har valgt at købe din blodtryksmåler hos os Kære kunde Ca. 1 mio. danskere har forhøjet blodtryk - betyder det noget? Ca. 50% af befolkningen kender
Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA)
 www.printo.it/pediatric-rheumatology/dk/intro Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA) Version af 2016 1. HVAD ER JUVENIL SPONDYLARTRIT/ENTHESITIS-RELATERET ARTRIT (GIGT) (SPA-ERA)?
www.printo.it/pediatric-rheumatology/dk/intro Juvenil Spondylartrit/Enthesitis-relateret artrit (GIGT) (SPA-ERA) Version af 2016 1. HVAD ER JUVENIL SPONDYLARTRIT/ENTHESITIS-RELATERET ARTRIT (GIGT) (SPA-ERA)?
Fra skoleåret 2016/17 indføres en praktisk-mundtlig fælles prøve i fysik/kemi, biologi og geografi.
 Indhold Vejledning til den fælles prøve i fysik/kemi, biologi og geografi Guide til hvordan Alineas fællesfaglige forløb forbereder dine elever til prøven Gode dokumenter til brug før og under prøven Vejledning
Indhold Vejledning til den fælles prøve i fysik/kemi, biologi og geografi Guide til hvordan Alineas fællesfaglige forløb forbereder dine elever til prøven Gode dokumenter til brug før og under prøven Vejledning
Patientinformation. Depression. - en vejledning til patienter og pårørende. Psykiatrisk Afdeling, Odense - universitetsfunktion
 Patientinformation Depression - en vejledning til patienter og pårørende Psykiatrisk Afdeling, Odense - universitetsfunktion Depression er en folkesygdom Ca. 150.000 danskere har til hver en tid en depression.
Patientinformation Depression - en vejledning til patienter og pårørende Psykiatrisk Afdeling, Odense - universitetsfunktion Depression er en folkesygdom Ca. 150.000 danskere har til hver en tid en depression.
Lyme Artrit (Borrelia Gigt)
 www.printo.it/pediatric-rheumatology/dk/intro Lyme Artrit (Borrelia Gigt) Version af 2016 1. HVAD ER LYME ARTRIT (BORRELIA GIGT) 1.1 Hvad er det? Borrelia gigt (Lyme borreliosis) er en af de sygdomme,
www.printo.it/pediatric-rheumatology/dk/intro Lyme Artrit (Borrelia Gigt) Version af 2016 1. HVAD ER LYME ARTRIT (BORRELIA GIGT) 1.1 Hvad er det? Borrelia gigt (Lyme borreliosis) er en af de sygdomme,
Adrenogenitalt syndrom AGS
 Adrenogenitalt syndrom AGS Information til børn/voksne med adrenogenitalt syndrom og deres pårørende August 2014 Vækst og Reproduktion Afsnit 5064 Opgang 5, 6. sal Rigshospitalet Juliane Marie Centret
Adrenogenitalt syndrom AGS Information til børn/voksne med adrenogenitalt syndrom og deres pårørende August 2014 Vækst og Reproduktion Afsnit 5064 Opgang 5, 6. sal Rigshospitalet Juliane Marie Centret
Fysiologi Louise Andersen 1.3, RTG 29/10 2007
 Fysiologi Louise Andersen 1.3, RTG 29/10 2007 Indholdsfortegnelse Introduktion Metode... 3 Teori Steptesten... 4 Hvorfor stiger pulsen?... 4 Hvordan optager vi ilten?... 4 Respiration... 4 Hvad er et enzym?...
Fysiologi Louise Andersen 1.3, RTG 29/10 2007 Indholdsfortegnelse Introduktion Metode... 3 Teori Steptesten... 4 Hvorfor stiger pulsen?... 4 Hvordan optager vi ilten?... 4 Respiration... 4 Hvad er et enzym?...
LP-HÆFTE 2010 - SOCIAL ARV
 LP-HÆFTE 2010 - SOCIAL ARV Indhold Indledning... 1 Forståelsen af social arv som begreb... 1 Social arv som nedarvede sociale afvigelser... 2 Arv af relativt uddannelsesniveau eller chanceulighed er en
LP-HÆFTE 2010 - SOCIAL ARV Indhold Indledning... 1 Forståelsen af social arv som begreb... 1 Social arv som nedarvede sociale afvigelser... 2 Arv af relativt uddannelsesniveau eller chanceulighed er en
Hvad hjernen ser. Kan man tro sine egne øjne? Er det vi ser, altid det hele?
 1 Akson Terminal Synapse Dendrit Skitse af en gren (dendrit) fra nervecelle, som det kan ses i et mikroskop. Der er mange synapser. Hvad hjernen ser Kan man tro sine egne øjne? Er det vi ser, altid det
1 Akson Terminal Synapse Dendrit Skitse af en gren (dendrit) fra nervecelle, som det kan ses i et mikroskop. Der er mange synapser. Hvad hjernen ser Kan man tro sine egne øjne? Er det vi ser, altid det
Kapitel 9. Selvvurderet helbred, trivsel og sociale relationer
 Kapitel 9 Selvvurderet helbred, t r i v s e l o g s o c i a l e relationer Kapitel 9. Selvvurderet helbred, trivsel og sociale relationer 85 Andelen, der vurderer deres helbred som virkelig godt eller
Kapitel 9 Selvvurderet helbred, t r i v s e l o g s o c i a l e relationer Kapitel 9. Selvvurderet helbred, trivsel og sociale relationer 85 Andelen, der vurderer deres helbred som virkelig godt eller
Daglig motion og normalvægt Begræns madmængde
 Spis mindst fra toppen Toppen består af kød, fisk og æg mad, som er rig på proteiner. Flyttet til toppen de "hurtige" kulhydrater - ris, pasta, kartofler, hvidt brød & mælkeprodukter Spis noget fra midten
Spis mindst fra toppen Toppen består af kød, fisk og æg mad, som er rig på proteiner. Flyttet til toppen de "hurtige" kulhydrater - ris, pasta, kartofler, hvidt brød & mælkeprodukter Spis noget fra midten
Sommereksamen 2011. Titel på kursus: De endokrine organer I. Eksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 Bedømmelsesform Bestået-/ikke bestået
 Sommereksamen 2011 Titel på kursus: e endokrine organer I Uddannelse: achelor Semester: 2. semester ksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 edømmelsesform estået-/ikke bestået Vigtige oplysninger:
Sommereksamen 2011 Titel på kursus: e endokrine organer I Uddannelse: achelor Semester: 2. semester ksamensdato: 21.06.2011 Tid: kl. 12.00-14.00 edømmelsesform estået-/ikke bestået Vigtige oplysninger:
Morsø Kommunes Sundhedspolitik
 Morsø Kommunes Sundhedspolitik Vedtaget i kommunalbestyrelsen 28. januar 2008 2008 Morsø Kommunes sundhedspolitik vedtaget i kommunalbestyrelsen 28. januar Indhold Forord side 1 Sundheden i Morsø Kommune
Morsø Kommunes Sundhedspolitik Vedtaget i kommunalbestyrelsen 28. januar 2008 2008 Morsø Kommunes sundhedspolitik vedtaget i kommunalbestyrelsen 28. januar Indhold Forord side 1 Sundheden i Morsø Kommune
Henoch-Schönlein s Purpura
 www.printo.it/pediatric-rheumatology/dk/intro Henoch-Schönlein s Purpura Version af 2016 1. HVAD ER HENOCH- SCHÖNLEIN S PURPURA? 1.1. Hvad er det? Henoch-Schönleins purpura (HSP) er en tilstand med inflammation
www.printo.it/pediatric-rheumatology/dk/intro Henoch-Schönlein s Purpura Version af 2016 1. HVAD ER HENOCH- SCHÖNLEIN S PURPURA? 1.1. Hvad er det? Henoch-Schönleins purpura (HSP) er en tilstand med inflammation
Natarbejde og brystkræft
 Natarbejde og brystkræft Fyraftensmøde, SVS, Torsdag den 30. maj SØREN DAHL OVERLÆGE ARBEJDSMEDICINSK AFDELING Plan Den forskningsmæssige baggrund mistanken om døgnrytmeforstyrrelser og kræft Hvor farligt
Natarbejde og brystkræft Fyraftensmøde, SVS, Torsdag den 30. maj SØREN DAHL OVERLÆGE ARBEJDSMEDICINSK AFDELING Plan Den forskningsmæssige baggrund mistanken om døgnrytmeforstyrrelser og kræft Hvor farligt
CASEMETODEN. Knut Aspegren 02.12.2003
 1 CASEMETODEN Knut Aspegren 02.12.2003 Casemetoden er en form af probleminitieret analyse og læring. Den stammer oprindeligt fra Harvard Business School, hvor man allerede i 1920-erne begyndte at bruge
1 CASEMETODEN Knut Aspegren 02.12.2003 Casemetoden er en form af probleminitieret analyse og læring. Den stammer oprindeligt fra Harvard Business School, hvor man allerede i 1920-erne begyndte at bruge
Folderen kan frit citeres med kildeangivelse.
 Naturmedicin 1 Udgivet af ÆldreForum, februar 2008 Design: DanChristensenDesign Foto: Niels Nyholm Tegninger: Flora Danica, Det Kongelige Bibliotek Tryk: Tryk Team, Svendborg Folderen kan frit citeres
Naturmedicin 1 Udgivet af ÆldreForum, februar 2008 Design: DanChristensenDesign Foto: Niels Nyholm Tegninger: Flora Danica, Det Kongelige Bibliotek Tryk: Tryk Team, Svendborg Folderen kan frit citeres
Behandling af forfangenhed Skrevet af dyrlæge Nanna Luthersson, Hestedoktoren
 Behandling af forfangenhed Skrevet af dyrlæge Nanna Luthersson, Hestedoktoren Behandling af forfangenhed er et meget omdiskuteret område. Hesteejere oplever ofte forskellige meldinger, afhængig af hvem
Behandling af forfangenhed Skrevet af dyrlæge Nanna Luthersson, Hestedoktoren Behandling af forfangenhed er et meget omdiskuteret område. Hesteejere oplever ofte forskellige meldinger, afhængig af hvem
Det lyder enkelt, men for at forstå hvilket ærinde forskerne er ude i, er det nødvendigt med et indblik i, hvordan celler udvikles og specialiseres.
 Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
Epigenetik Men hvad er så epigenetik? Ordet epi er af græsk oprindelse og betyder egentlig ved siden af. Genetik handler om arvelighed, og hvordan vores gener videreføres fra generation til generation.
BMD Bone mineral density. Farmakologisk behandling af osteoporose. Diagnostik. Ryg & hofte
 Definition af osteoporose Farmakologisk behandling af osteoporose Lars Rejnmark Bente Langdahl Medicinsk Endokrinologisk Afdeling (MEA), THG Aarhus Universitetshospital Osteoporose (jf WHO): en systemisk
Definition af osteoporose Farmakologisk behandling af osteoporose Lars Rejnmark Bente Langdahl Medicinsk Endokrinologisk Afdeling (MEA), THG Aarhus Universitetshospital Osteoporose (jf WHO): en systemisk
INDSÆTTELSE AF KUNSTIGT KNÆLED
 INDSÆTTELSE AF KUNSTIGT KNÆLED Knæleddet er et meget kompliceret led. Det er ikke et kugleled som skulder og hofte, det er heller ikke et hængselled som albue eller fingerled. Et knæled kan bedst sammenlignes
INDSÆTTELSE AF KUNSTIGT KNÆLED Knæleddet er et meget kompliceret led. Det er ikke et kugleled som skulder og hofte, det er heller ikke et hængselled som albue eller fingerled. Et knæled kan bedst sammenlignes
Grøn Viden. Teknik til jordløsning Analyse af grubberens arbejde i jorden. Martin Heide Jørgensen, Holger Lund og Peter Storgaard Nielsen
 Grøn Viden Teknik til jordløsning Analyse af grubberens arbejde i jorden Martin Heide Jørgensen, Holger Lund og Peter Storgaard Nielsen 2 Mekanisk løsning af kompakt jord er en kompleks opgave, både hvad
Grøn Viden Teknik til jordløsning Analyse af grubberens arbejde i jorden Martin Heide Jørgensen, Holger Lund og Peter Storgaard Nielsen 2 Mekanisk løsning af kompakt jord er en kompleks opgave, både hvad
Hold styr på dit stamtræ også når det gælder prostatakræft Arv og øvrige dispositioner for prostatakræft
 Hold styr på dit stamtræ også når det gælder prostatakræft Arv og øvrige dispositioner for prostatakræft www.propa.dk Fejl i DNA molekylet er årsag til alle former for kræft også prostatakræft. Arvelighed
Hold styr på dit stamtræ også når det gælder prostatakræft Arv og øvrige dispositioner for prostatakræft www.propa.dk Fejl i DNA molekylet er årsag til alle former for kræft også prostatakræft. Arvelighed
